文摘
肺癌患者的住院重症监护与postprocedural /术后护理和医疗并发症由于癌症及其治疗,但也与急性器官衰竭不直接相关的癌症。
尽管仔细的术前风险管理和现代手术和麻醉技术的使用,胸外科仍然与高发病率相关,与切除的程度和具体的并发症有关。快速流程及时识别和治疗并发症的积极影响病人的结果。术后预防和治疗管理必须精心策划,以减少术后发病率和死亡率。
严重的并发症,患者重症监护室(ICU)死亡率从13%到47%不等,和医院的死亡率从24%到65%不等。常见的住院死亡率预测严重程度得分,没有器官的数量,一般情况、呼吸窘迫和机械通风或升压的必要性。当考虑放电后长期生存,癌症相关的参数保留他们的预后价值。
重症胸的外科医生,麻醉师,pneumologists等和肿瘤学家需要开发和自信的伙伴关系旨在实施循证病人护理,确保病人临床路径管理,同时促进教育、研究和创新。最后决定承认ICU的肺癌患者应采取密切伙伴关系这个医疗小组和病人和他或她的亲戚。
文摘
ICU应提出后肺癌患者耐心和多学科小组之间的讨论http://ow.ly/TWZ3308SB4g
介绍
在西方国家,肺癌是癌症死亡的主要原因1),8 - 15%的癌症患者承认重症监护病房(ICU)肺癌(2,3]。承认与postprocedural /术后护理,并发症由于癌症及其治疗和器官衰竭与癌症无关。ICU癌症患者的预后是由急性生理干扰导致重症监护,而不是潜在肿瘤疾病(4- - - - - -6),而复苏后存活率与潜在的肿瘤疾病有关。
肺癌患者管理的变化,医疗费用和预算约束诱导实质性修改ICU使用。传统上,肺癌手术患者经常承认眼前的术后ICU的时期,但目前我们面临的发展高度依赖(二)和post-anaesthesia护理单元(pacu)。承认晚期肺癌患者在ICU仍然是一个具有挑战性的问题,因为新的治疗发展非常活跃的靶向治疗必须考虑。
叙述评论复位当前角色的肺癌患者ICU管理,关注三大终端:选择重大手术后病人的风险;肺癌患者的预后承认ICU;和特定的并发症导致入住ICU。
选择入住ICU病人在手术后的风险
术后死亡率后胸大手术范围在2%和5%之间,和心肺发病率在20%和40%之间,导致延长住院时间,增加了医疗费用(7]。
术后ICU承认,二胺或PACU的预测是基于临床医生的判断“可以避免的”主要并发症调制的可用资源。结合病人和手术风险接近总体风险(图1)。
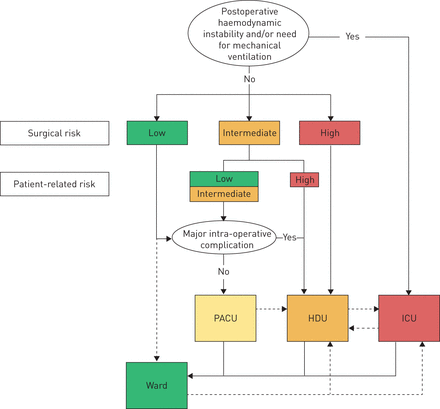
Post-thoracotomy病人分流。PACU: post-anaesthesia病房;二:高度依赖单位;ICU:重症监护室。从[复制和修改7]。
手术并发症的风险因素和风险分层
归纳了风险因素表1、2和3。
发生的风险因素
一般风险评分
美国麻醉医师协会分类身体健康(ASA)普遍应用评估术后病人的发病率和死亡率的风险要求任何外科手术,治疗或诊断程序。然而,高风险(ASA > 2)与大型interobserver可变性和可怜的特异性,为个别病人(排除准确估计11]。
Charlson发病率指数(CCI),由19个加权医疗诊断,是一个有效的医疗患者的1年死亡率的预测;得分> 5与1年死亡率> 50% (12]。肺癌患者接受治疗切除,CCI分数≥3与主要并发症的发病率10倍大(13]。手术死亡概率模型(14)是用来预测全因术后死亡率在30天15(表2和图3)。
三个进一步的分数,更专门为胸外科,必须考虑。心肺风险指数是心脏和肺的组合风险因素(16]。EVAD分数利用肺功能测试数据(在1 s (FEV用力呼气量1)和肺一氧化碳(的扩散能力DLCO))和患者年龄预测主要肺切除术后并发症的可能性(17]。“thoracoscore”,源自法国国家胸外科数据库EPITHOR包含九个独立的危险因素预测住院死亡率(18]。
心血管风险评分
修改后的心脏风险指数(RCRI)是主要的心脏并发症的预测非紧急开发非心脏手术(19)(表2和3)。RCRI指数≥3与主要术后心脏并发症(+ 11%)。胸肺切除术RCRI是来自原始RCRI [20.)(表2和3)。这两个分数的预测能力接受肺切除术的患者是有争议的。最近,心肌梗死和心脏骤停的风险计算器(21)已经确定了五个预测围手术期风险的30天,并提供更准确的心脏比RCRI风险预测,尽管没有胸外科的数据是可用的。
肺风险评分
术后肺部并发症(ppc)发病率和死亡率的主要原因,可能占死亡率超过心血管并发症。
风险评估呼吸外科患者在加泰罗尼亚(ARISCAT)发展的研究建立了一个风险评分ppc的手术患者根据七个独立的危险因素(22)(表2和3)。比分是前瞻性和外部验证在许多欧洲国家,有一个令人满意的预测能力,特别是西欧国家(23]。
肺功能测试
呼吸困难是与术后死亡率的风险24]。标准化symptom-limited爬上三层楼梯没有中断是一个简单的成本效益测试客观地确定心肺储备,可能有优越的预测能力比传统的肺量测定法值(7]。未能执行这个测试需要进一步肺功能测试,而病人能够爬≥22 m(五到六层楼梯)术后并发症的风险很低,无论肺功能测试结果(25]。
一个术前FEV1< 70%,预测术后(ppo)DLCO是否能可靠预测在胸外科围手术期并发症26]。188bet官网地址欧洲呼吸学会使用ppo-FEV /欧洲胸外科学会指导方针1< 30%,ppo -DLCO< 30%正常和高危人群之间的歧视7]。然而,ppo-FEV计算1可能高估了FEV1第一天术后∼30% (27)和一个中度到重度阻塞性肺综合症患者可能改善他们的肺切除术后呼吸动力学。
峰值摄氧量在围手术期风险预测的精确性,标准化工作可以与值> 20毫升·公斤−1·敏−1允许切除肺切除术,而值< 10毫升·公斤−1·敏−1预测高风险的任何类型的肺切除术(28)的死亡率可能超过20%29日]。
年龄和脆弱
与衰老器官功能下降和生理储备是围手术期的发病率和死亡率的主要危险因素。Sarcopenia影响四肢的肌肉、呼吸肌肉和那些控制上呼吸道。阻塞性睡眠呼吸暂停和神秘的愿望更频繁地发生在底层神经障碍(如。前中风、老年痴呆症和帕金森症)[30.]。术后低氧和高碳酸血症的风险增加,因为改变了化学敏感性,呼吸肌肉无力和增加肺分流。生热作用有利于受损的发生伤口感染,出血和心脏缺血,导致延长术后恢复(27]。术后认知障碍的风险增加,尤其是苯二氮术前用药法(31日]。
弱点是老年的复合测量的条件可能是一个宝贵的援助在确定可操作性和规划的术后护理。多维脆弱分数包括九项改编自老年综合评估的最大价值15已经阐述了预测术后1年死亡率(32]。截止5分允许从业者区分高死亡率(> 10%)和低风险人群。虽然优于ASA得分1年死亡率的预测,计算耗时的,必须由一个顾问熟悉得分。
手术的危险因素
肺切除术
胸手术风险评估主要集中于肺切除术,尤其在癌症手术。广泛,更广泛的肺切除,术后并发症的风险就越大(表4)。
最大的风险是与扩展肺切除术(表5)。总体而言,右侧肺切除携带比半球切除术并发症的风险更高,由于bronchopleural瘘形成更大的倾向,更增加右心室后负荷和潜在改变心脏sympathicovagal平衡(33,34]。
其他胸手术干预
干预措施要求单或单通风和开胸暴露患者心血管并发症、肺不张、肺炎和ventilator-induced肺损伤,导致急性呼吸窘迫综合征(ARDS)。
一诺模图验证预测术后并发症的发生和严重程度后oesophagectomy [35)和风险预测被证明是有用的在大医院(37]。独立危险因素年龄、脑血管或短暂性缺血性发作史,心肌梗死史,FEV减少1,心电图变化和广泛的手术。
肺或胸膜活检和简单bullectomy肋膜或不使用电视胸外科(大桶)要求短期进入PACU监测麻醉复苏,肺再次向,扩张滴定剩余的止痛剂和检测空气泄漏和肺不张。纵隔镜检查通常可以被监控在PACU特别注意神秘术后出血的风险。
额外的手术风险因素
几乎没有证据支持使用muscle-sparing胸廓切开术作为开胸后外侧的反对,但切口长度可能比例post-thoracotomy相关并发症(38]。鉴于有限的组织创伤和随之减少神经内分泌和炎症反应,大桶的围手术期死亡率较低有关,发病率(如。肺炎和心房心律失常)和住院时间34]。在缺乏其他术后并发症的主要危险因素,一个大桶的肺切除患者通常在pacu的监测和管理从麻醉复苏。
手术死亡率可能会降低如果胸外科医生执照有最小的情况下加载的过程39]。术后死亡率差异医院也可以解释为术后患者管理质量的变化(40]。
紧急的手术基础不断伴随着糟糕的术后结果。各种预处理和术后分数这个因素融入风险分层。
最后,主要的术中并发症的发生可能需要更高层次的术后监测和治疗比最初计划。心肌缺血,haemodynamically严重心律失常,耐火低血压和低氧血,支气管愿望和主要出血被认为是主要的并发症,证明二胺或ICU的承认。
麻醉管理
改善患者的结果可以通过实施围手术期风险最小化策略(8- - - - - -10):1)麻醉药物的滴定,根据监测大脑活动;2)采用lung-protective通气设置;3)控制血液动力学和实现最优氧运输与代谢需求(由近红外光谱学脑氧饱和度);4)控制正常体温和止血;和5)有效控制疼痛。
术后疼痛控制的类型和质量影响术后分流,因为它影响的风险,术后心肺并发症和住院时间(41]。胸硬膜外镇痛是开胸手术后疼痛治疗的黄金标准,因为它已经降低术后肺炎的发生率,缩短机械通气时间与系统性镇痛(42]。经皮胸脊椎旁,执行由外科医生,麻醉师或直接可以提供类似的镇痛,在较低的风险,低血压和尿潴留43]。在一些机构,耐火低血压引起的胸硬膜外治疗要求转移到二胺或ICU。在最近几十年,术后并发症的发生率明显减少由于在系统硬膜外镇痛(额外的好处42]。
术后ICU的患者,选择二胺或PACU的承认
对大多数患者来说,术后分流可以被考虑到病人的术前计划和手术风险因素尽管术中并发症的发生可能修改初步评估。
分数和指导方针
手术阿普加分数(SAS)包括三个术中参数:失血,最低最低平均动脉压和心率,证明是有用的在预测术后主要并发症或非心脏手术后30天死亡率(44]。到目前为止,胸手术病人没有被包括在这个探索人口样本。的SAS已成功验证单中心和在八医院在8个国家的一项国际研究(45]。得分≥5月6日信号高术后并发症的风险,提示临床医生将病人转移到二胺或ICU。
生理和手术严重程度评分枚举的死亡率和发病率(负鼠)是用于审计。它是基于12生理和六个操作参数和允许住院死亡率和发病率的预测。它被证明有用的预测lung-resected患者的术后并发症(46]。随后,负鼠分数提高和命名Portsmouth-POSSUM (P-POSSUM) [47]。
危重病医学的美国大学发出指导方针选择标准的病人承认二胺(48]和icu [49]。进入二应该考虑“重大手术后,病人血液流动稳定,但可能需要液体复苏和输血由于主要流体转变”和“谁需要护士密切监测在第一个24小时”。进入ICU对少数病人限制要求“血流动力学监测/通气支持或广泛的护理”(图1)。改变胸手术病人的临床路径从ICU PACU和二胺已被证明是安全的和具有成本效益的50]。
地方特色
术后的谱单元从日托和外科病房pacu,二胺和icu。每个医院都有一个独一无二的结合术后单位、人员、专业知识和技术设备,这将大大影响术后治疗的决定。指导原则要求必须适应这些特征,并由当地多学科小组由外科医生,麻醉师,重症pneumologists和等。
在一些机构,所有手术后的患者首先转移到PACU之前转移到病房或二胺。这提供了更多的临床信息最终分类的时候,因为第一次术后时间是一段时间的主要生理变化可能出现的早期病理过程。
转到病房需要大幅减少的质量和频率监测。提供医疗应急小组由麻醉师重症和/或等,减弱的风险(可能是一个方法51),可能影响术后分流决策。
肺癌患者的预后ICU
系列主要包括阶段iii iv肺癌已经表明,肺癌患者的预后承认ICU时间大大改善。2005年以前,ICU死亡率很高(46 - 85%)都报道;目前,这些有13 - 47%下降52]。医院死亡率遵循了类似的下降在75 - 91% [24 - 65%52]。然而,我们不得不考虑一个可能的选择性偏差,作为参数从位肺脏和肿瘤学家承认ICU患者,以及重症先进的等拒绝他们,可以改变并行期间引入新的、更积极的抗癌治疗和改善重症监护管理。
研究异构和有限的规模评估预后因素。13个研究中,只有7个国家包括> 100例(52]。最常报道ICU停留期间的独立预后因素似乎性能状况、急性呼吸衰竭、失败的器官和升压或机械通风的必要性。此外,肿瘤气道梗阻、急性呼吸衰竭、癌症状态、并发症、严重程度得分,败血症和肾功能衰竭患者住院死亡率的预测。长期死亡率评估时,癌症特征(转移和癌症恶化)保留他们的预后价值。
Roques等。(53)显示,105年肺癌患者需要ICU停留6个月死亡率为73%;三分之二的幸存者接受抗癌治疗。Toffart等。(54)表明,3个月和1年生存率分别为37%和12%,分别。器官功能障碍的恶化72 h后入住ICU与高死亡率(45%与如果改善器官功能障碍)的8%。三个月生存无关的非侵入式通风(NIV)需求(40%与47%没有NIV),但明显减少需要气管插管的病人(22%)。从ICU病人出院活着,放电后平均存活104天,估计存活率是54%和18%,1年90天。
SEER(监测、流行病学、最终结果)寄存器分析49 373名肺癌患者承认ICU的原因除了手术切除(55]。其中,76%在住院出院后6个月,35%的人还活着。医院死亡率增加机械通风时,6个月生存率只有15%。第二项研究上执行相同的数据库集中在> 65岁的1134名患者与第四阶段希望和nonsmall细胞性肺癌(NSCLC) (56]。在90天,1年死亡率分别为71%和90%,分别,住院死亡率为33%。患者出院活着,42%回家而其他人被转移到康复服务或姑息治疗机构。只有19%的病人出院后接受癌症治疗。
特定的并发症和ICU管理
手术并发症
即使最优手术和麻醉技术,发病率仍大幅升高。主要是心脏、肺和胸膜的并发症可能出现高达83%的患者与心包和膈胸膜外的肺切除后重建(57]。尽管微创程序可以执行在高危患者并发症率较低,现有的临床因素可能负责严重术后并发症,为重症密切互动等,麻醉师,pneumologists,心脏病学家、心胸外科、医疗肿瘤学家和物理治疗师在术后时期。
心律失常
室上比心室节奏快速性心律失常更常见干扰非心脏胸腔手术后(58]。心房纤维性颤动通常发生在第四术后第二天叶切除术后10 - 20%的患者,但在肺切除术后40% (59]。重大风险因素是右全肺切除术,intrapericardial解剖,先进的年龄和液体摄入量减少。足够的监控几天建议和广泛的指导方针可从美国胸外科协会(60]。
呼吸系统并发症
肺部水肿报道在肺切除术后9%的病人和较小的切除术后1 - 5%,具有高死亡率(61年,62年]。noncardiogenic,非传染性的肺部水肿,被认为是一种postresectional ARDS的特点是渗透率水肿和弥漫性肺泡损伤。病人治疗遵循的古训“保持干燥”;reintubate或应用无创通气在呼吸衰竭的情况下随着变力/ vasopressive药物的管理,同时限制液体摄入量(63年]。
Postpneumonectomy综合症是由极端纵隔转移引起的。病人抱怨由于压缩气管和血管进行性呼吸困难。在严重的情况下组织扩张器是用来定位纵隔向中线(64年]。
Orthodeoxia-platypnoea坐姿综合征的特点是呼吸困难,当病人躺下不明显。它与卵圆孔未闭的重新开放一个心脏内的分流。关闭设备可以用来消除分流(65年]。
血栓栓塞疾病(深静脉血栓形成或并发肺栓塞)是青睐的凝固性过高状态引起的癌症。其发病率高达15%的肺癌患者(66年和手术患者的1 - 5%67年]。通过使用低分子量肝素预防,弹性长袜和早期的移动是至关重要的。在高危患者建议使用气动压缩设备。管理是没有不同于其他血栓栓塞疾病,除了它必须追求只要风险因素依然存在。治疗方法有随着时间的推移,转向低分子量肝素(67年,68年];最近,在病人,直接口服抗凝血剂被证明是同样有效(69年),但还没有标准的做法。严重患者血液动力学的妥协,溶栓疗法或肺动脉栓子切除术可能应用。
延长空气泄漏是肺气肿患者的一个常见问题,据报道在50%的情况下,使其最常见的术后并发症。漏气时被认为是异常后持续5天(70年]。进步皮下和纵隔气肿可能发展,最终导致肿胀的脸和眼睛,所谓的“米其林综合症”。风险因素包括严重的大疱的肺气肿,肺减容手术和长期通气支持引起气压性创伤。围手术期控制支气管树桩和主要线路推荐,如果有必要通过应用纤维蛋白胶或其他密封剂,通过钢筋条或创建一个通过分离胸膜壁层胸膜帐篷。在Cochrane系统回顾、外科密封剂术后减少空气泄漏和时间胸管切除;然而,显著减少住院时间不能证明(71年]。术后,病人应行气管尽快减少肺内的压力。注入的滑石,其他硬化性代理或自体血液可能有助于密切坚持实质空气泄漏。插入一个猪尾导管海姆利希阀允许门诊。提出了在困难的情况下,intrabronchial阀门关闭肺泡胸膜瘘管(72年]。
叶的扭力(< 0.5%),是一种罕见但戏剧性的并发症(73年,74年]。它发生的扭曲剩下叶围绕其bronchovascular椎弓根,主要在右侧中部叶(但不仅限于75年),出血性梗死和肺坏死。诊断是通过支气管镜检查(76年),而且在大多数情况下需要完成肺切除术。预防由固定的叶/ s周围组织在最初的过程表示(75年]。
特定的胸膜并发症
持续的胸膜或剩余空间,称为“持久化气胸”胸放射科医生,观察到主要的肺切除术后不到肺切除术后。所谓的“复杂的剩余空间”存在时坚持漏气或者当殖民与细菌或真菌发生,引起胸膜积脓症。排水的胸膜腔是表示77年]。肌肉皮瓣可以用来填满剩余空间,以防止复发性感染。叶切除术后胸腔积脓症是一种罕见的事件,但发生在2 - 12%的肺切除术,并常与bronchopleural瘘(73年]。风险因素包括心血管和肺部并发症,年长的年龄、营养不良、新辅助或诱导治疗,糖尿病,类固醇,右全肺切除术和扩大切除术,术后ARDS、肺炎和长期机械通气。胸膜液体文化开始前需要抗生素检测细菌和/或真菌负责,,必要时调整抗菌或抗真菌治疗。胸膜的初始疗法包括完整的排水空间结合抗生素或抗真菌的。灌溉胸膜空间消毒的解决方案可能是必要的(78年),有时可能需要临时或最终胸廓造口术控制严重感染(79年]。
Bronchopleural瘘意味着剩余的支气管树桩和胸膜之间的直接通信空间(80年]。临床症状非常类似于积脓症和通常预示进行性炎症综合征和呼吸窘迫。大量咳痰深棕色液体可能发生在大型瘘。早期病例观察7天内的程序,通常由不充分或不完整的闭合支气管树桩。晚期病例的失败相关治疗支气管的树桩,复发性支气管或气管内感染疾病或进步。非常类似于积脓症危险因素。围手术期预防措施bronchopleural瘘与可行的组织(包括支气管树桩的覆盖81年]。支气管镜检查显示检查支气管缝合或短纤维线。小瘘管可能检测到亚甲蓝注射的树桩。管理类似于积脓症和多学科协作需要充分的治疗(82年]。在突然咳痰的情况下大量的液体,这个病人应该定位头上升和运营方面。小瘘管有时可能会被注入胶水闭塞的诊断或硬化剂。较大bronchopleural瘘的手术结束后应试图解决胸膜感染,切除坏死组织和涵盖的支气管残与可行的组织肌肉皮瓣,心包或网膜73年]。术后胸腔的灌溉是预防复发性积脓症或fistulisation表示。
胸部肿瘤特定干预措施的重症监护(除了手术并发症)
呼吸系统疾病是第二个最常见的肺癌患者入住ICU(原因83年]。以下事件通常报道:发热性中性粒细胞减少和poststenotic感染(retro-obstructive肺炎)(这里未讨论),呼吸困难和急性呼吸衰竭,一般伴有气胸或咯血。
气胸
期间癌症分期,大多数ICU招生相关不良事件后肿瘤采样。气胸经胸廓的针活检是复杂的高达60%的情况下,但只有少数人(15%)需要胸腔引流或进入重症监护84年]。Transbronchial活检并发症的发生率较低(85年]。气胸术后会出现几个小时虽然正常postprocedural摄影,必须重复。自发气胸可能发生由于化疗后的肿瘤侵犯或坏死。严重呼吸衰竭是罕见的在没有其他并发症和胸膜排水是快速有效的。延长空气泄漏管理类似于术后设置。
Intrabronchial出血
内镜活检很少导致严重出血如果采取标准预防措施:扣缴抗凝血剂和血小板antiaggregants,除了低剂量的阿司匹林。大量咯血poststenotic后可以导致肿瘤浸润或实质坏死感染,但很少从血栓栓塞。咯血的肿瘤生长通常是温和的,但大量出血的介入会发生肺动脉等大型船只。进入ICU建议当出血显著(> 200毫升每24小时或每集> 50毫升)或负责呼吸窘迫(> 4 - 5 L·分钟需要补充氧气−1或动脉氧饱和度测量脉搏血氧仪< 88%)或血液动力学的不稳定性。接受抗凝治疗的患者和那些有广泛的组织坏死,但可能适合手术也应该承认。诊断由胸部电脑断层扫描和支气管镜检查,如果出血的确切起源是未知的。管理和治疗方法是氧气选择性插管的大量出血。支气管镜检查,最好是硬支气管镜检查在全身麻醉下,可用于凝结intrabronchial病变或以确保适当的选择性插管。支气管动脉embolisation有时是有限的价值或有短暂的影响。手术有时是可行的,但死亡率高。纤溶是有限的,如果有的话,使用。如果没有禁忌症(主要是心脏缺血和不受控制的高血压),抗利尿激素类似物显示了一些有效性在等待介入支气管镜检查,embolisation或手术。
急性呼吸道梗阻
急性梗阻的主要航空公司中部出现肿瘤,由于管腔内的肿瘤生长,extraluminal压缩或混合机制。除了少数例外(严重功能受损的病人),只有气管或两国近端障碍物产生显著的呼吸窘迫。呼吸困难通常是进步的,但有时是急性,喘鸣或喘息取决于梗阻的程度。消融的管腔内的tumoural组件可以通过各种技术(激光、电凝法或机械去除)如果可见管腔持续下去,其次是内腔支架的植入。远端专利支气管和肺正常需要保险受益。硬质支气管镜检查下程序执行和全身麻醉86年,87年]。
主要的心包和胸腔积液
经常胸内的恶性肿瘤转移至胸膜和/或心包,导致呼吸/心脏损伤(88年]。除了少数例外,与大量的腔内出血症状是进步的和被直接穿刺(胸膜/心包)或排水。重复穿刺应避免,因为它提出了一个重要的肋膜感染风险,和/或心包引流应该尽快执行。
一些主要的目的:呼吸困难
很少,呼吸困难可以造成声门的水肿的上腔静脉综合症。治疗依赖于血管内支架和抗凝防止血栓形成的延伸上腔静脉侵犯。糖皮质激素和利尿剂无效(89年]。放射治疗是不紧急治疗,尽管其潜在的有效性。
进行性呼吸困难常与弥漫性肺参与通过淋巴或当地的传播。没有特定的治疗(包括皮质类固醇)显示活动以外的抗癌治疗,和ICU管理只依赖政府的氧气。患者只能承认ICU如果可以提供一个活跃的抗癌治疗(90年]。间质性肺炎可能与副作用的酪氨酸激酶抑制剂(TKIs)。有时,呼吸窘迫的原因很难精确和不止一个机制。随着这些病人频繁的心脏并发症,N终端pro-brain利钠肽剂量可以要求排除心脏病因学(91年]。
先进的肺癌和系统性抗癌治疗ICU期间
晚期肺癌的预后已经改变随着时间的推移,通过引入新的积极的化疗药物,靶向制剂和小亚种群,非常活跃。然而,面临着持续疾病预后差,几个医院死亡率的预测因素,包括预先存在的表现不佳状态和减肥,之前要考虑入住ICU (54,92年]。其他因素需要考虑之前入住ICU的可逆性急性并发症,如desobstruction近端气道,肺癌的治疗选项后交付解决急性并发症,肿瘤进展的缺失(54和病人的意愿。在最近的一次前瞻性研究,Toffart等。(83年)表明,缺乏从病人或其家属拒绝加护病房转诊的一个独立因素。
兴趣管理抗癌治疗ICU仍然是有争议的,除了高风险治疗(大剂量甲氨蝶呤,严重的过敏反应的风险,等。)。水平的证据对ICU(紧急)化疗的作用很低,和大多数系列处理混合人口,主要与血液学的恶性肿瘤(93年]。所有证明管理常规化疗的可行性的研究,尽管减少固体肿瘤的预后(93年,94年]。预后因素反映器官功能障碍(需要升压、机械通风、肝衰竭和顺序器官衰竭评估分数(93年- - - - - -95年]。
肺癌是非常有限的具体数据。在一系列的20小细胞肺癌(SCLC)病人,五在ICU停留接受化疗96年]。> 200天只有两个活了下来。然而,引入靶向治疗与快速和高反应率改变了我们悲观的看法,与案例报告(97年,98年]建议的主要活动TKIs致癌司机突变和呼吸衰竭,患者也在机械通气。最大的回顾性病例对照研究(90年)包括14名患者表皮生长因子受体突变或间变性淋巴瘤激酶或ROS-1重组。尽管医院死亡率的50%,这些激活突变患者接受TKIs降低了30天死亡率(p = 0.07)和更好的生存(风险比0.12,p = 0.002)比历史上的控制。
由于最近引进医疗设备,没有足够的免疫疗法和重症监护数据。然而,通过刺激免疫系统,这些代理应该小心使用与修改病人的免疫系统(全身炎症反应综合征、嗜中性白血球减少症等。)。
一些迹象表明放射治疗ICU期间造成小系列表明辐照对气管插管病人可能是有益的。在一系列的26例(21 NSCLC,四个SCLC), 7例气管切开和六人活着从医院出院99年]。
管理的抗癌治疗ICU证明intensivist之间的广泛讨论,肿瘤学家和病人或其家属,考虑收益和风险之间的平衡。具体的激活突变的数量应该有更多的在这个设置非常活跃的靶向治疗中获益。
结论
肺癌患者将面临重症监护管理,主要有两个原因:或急性并发症,术后设置相关癌症及其治疗。
仔细的术前评估是强制性的,以减少术后发病率和死亡率。麻醉师的过程中起着重要作用减少术后风险,减少高层术后监测的必要性。趋势移动胸手术术后ICU的护理对二胺或pacu取决于病人,手术风险因素和当地的特异性。
严重的心脏和呼吸系统并发症是最常见的并发症导致入住ICU。预防和早期识别,以及跨学科合作获得最好的结果[至关重要79年]。紧急的抗癌治疗的病人患有呼吸衰竭由于tumoural渗透取得了一些成功,主要在激活突变/重组的情况下,应该在个案基础上讨论。
虽然预后可能贫穷,进入ICU应提出后肺癌患者患者和多学科小组之间的讨论,考虑到反转的可能性的急性并发症和抗癌治疗期间或之后选择交付ICU停留。
脚注
本系列之前的文章:没有。1:Malhotra J, Malvezzi M, Negri E,等。肺癌的危险因素。欧元和J2016;48:889 - 902。2号:麦当劳F, De Waele M•爆炸下限,等。管理阶段I和II nonsmall细胞肺癌。欧元和J2017;49:1600764。3号:Leduc C,安东尼D, Charloux,等。肺癌患者的并发症的管理。欧元和J2017;49:1601721。4号:Zugazagoitia J, Molina-Pinelo年代,Lopez-Rios F,et al。在nonsmall细胞肺癌生物治疗。欧元和J2017;49:1601520。5号:Calvayrac O, Pradines,脑桥E,et al。肺腺癌的分子生物标志物。欧元和J2017;49:1601734。
利益冲突:没有宣布。
- 收到了2016年的11月9日。
- 接受2017年2月6日。
- 版权©2017人队















