摘要
COPD吸烟者呼出冷凝物中氧化还原活性铁的减少可能表明排泄失败http://ow.ly/VA4vM
致编辑:
最近的观察和遗传学研究强调了铁稳态破坏在稳定和加重慢性阻塞性肺疾病(COPD)中的潜在作用。因此,不限于贫血的铁缺乏症[1]和铁调节蛋白-2基因的单核苷酸多态性[2],一种参与细胞铁周转和控制的关键调节因素,已在该人群中被确定。由于对组织储存的影响大于对动员和限制从肠道摄取的影响,破坏了系统铁稳态可能会限制代谢目的铁的可用性。在呼气冷凝物(EBC)中可测量特定的促氧化铁池(自由或松散结合的离子,具有氧化还原活性/催化破坏性氧化剂的产生)[3.].虽然铁是生命所必需的,特别是对需氧生物而言,但铁处理不良或改变会导致与氧化剂产生、微生物毒性、氧化还原信号事件改变和细胞命运改变(包括重塑)相关的不利影响。因此,开展这项研究是为了深入了解肺和气道中的铁处理,以及这些过程在COPD中可能发生改变的程度。通过博莱霉素方法进行了测量这一特定铁池的研究[4]利用上文所述收集的EBC样本[3.]并从正常健康个体、健康吸烟者和COPD患者(现在和曾经的吸烟者)中获得。血清hepcidin和白细胞介素(IL)-6水平,已知的铁稳态调节器,也被测量。
年龄匹配的健康对照组、健康吸烟者和COPD受试者(分为当前吸烟者和戒烟者)EBC中氧化还原活性铁含量的比较显示各组之间存在显著差异(图1一个).健康吸烟者EBC中氧化还原活性铁的水平如预期的那样大幅升高,因为已知香烟烟雾中含有铁和其他金属成分[5].然而,无论当前或过去有吸烟史,COPD EBC中没有明显的这种反应,两组的值与健康对照组的样本中发现的值相同。COPD严重程度对呼出的氧化还原活性铁没有显著影响,尽管趋势很明显(数据未显示)。在之前的一项研究中,研究了不同受试者(哮喘、心脏手术和吸烟者)和环境下EBC中的氧化还原活性铁含量,得到的结果使我们有理由推测,EBC中这种特异性的活性铁池的存在可能代表了一种排泄功能,该功能可能因肺损伤或疾病而受损[3.].在这方面,所提供的数据图1一个特别是健康吸烟者体内氧化还原活性铁含量的显著差异与慢性阻塞性肺病吸烟者,似乎表明在慢性阻塞性肺病人群中无法排出铁。气道和肺部铁潴留可能导致氧化应激和损伤、微生物毒性和细胞命运改变等表现,所有这些都与COPD有关。
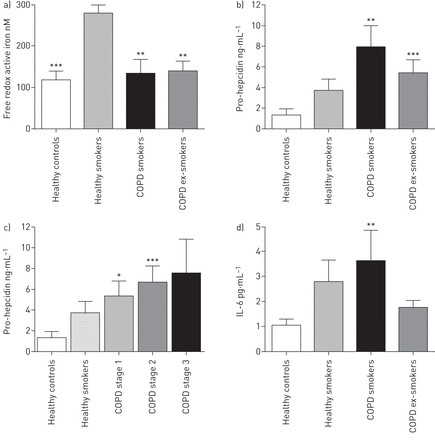
a)健康对照(n=15)、健康吸烟者(n=17)和慢性阻塞性肺疾病(COPD)受试者(目前吸烟者,n=12)呼出冷凝物(EBC)中氧化还原活性铁含量;抽过烟,n = 18)。* * *: p < 0.001;**:与健康吸烟者相比p<0.01。b)健康对照组(n=24)、健康吸烟者(n=22)和COPD患者(吸烟者,n=19)血清hepcidin前水平;抽过烟,n = 28)。c)健康对照组(n=24)、健康吸烟者(n=22)和慢性阻塞性肺疾病全球倡议(GOLD)分期(1期,n=9) COPD患者血清hepcidin前水平;阶段2,n=31;第三阶段,n=6)。d)健康对照组(n=24)、健康吸烟者(n=22)和COPD患者(吸烟者,n=19)血清白介素-6水平; ex-smokers, n=28). b–d) ***: p<0.001; **: p<0.01; and *: p<0.05 when compared with healthy controls. Data were analysed using the Kruskal–Wallis test with Dunn's multiple comparisons post-test.
人体每日所需的铁远远超过肠道从饮食中吸收铁的能力,因此这种有限而重要的资源大部分在体内被重新加工以弥补这种不足。从全球范围来看,体内铁的损失仅限于出血和粘膜细胞的损失,包括肠道和皮肤细胞的脱落。因此,特定的身体铁排泄机制通常不被很好地建立。然而,有先例表明运动员在运动过程中会在汗液中排出氧化还原活性铁[6],这可能代表了一种保护策略,以限制铁催化氧化剂生产在这些情况下的影响。呼吸道和肺部经常暴露在大气中的含铁成分中,因此天生容易受到与铁积累有关的不良后果的影响。因此,一种机制,即铁和含铁颗粒可以被细胞处理,以解毒和溶解这种过渡金属作为自由离子,并在呼吸中排出体外,似乎是合理的和可取的。巨噬细胞是一种常见于肺部和呼吸道的炎症细胞类型,是已知的铁代谢细胞中心,并以各种形式控制铁摄取的处理机制。事实上,肺泡巨噬细胞在慢性阻塞性肺病患者中隔离铁是已知的[7].重要的是,巨噬细胞还表达细胞铁输出蛋白铁转运蛋白[8,9],以及根尖表面的气道上皮细胞[10],表明这些细胞在这种情况下可能会排出铁。转运铁蛋白的表达主要由小肽激素hepcidin控制,当与转运铁蛋白结合时,hepcidin会引起内吞作用,从而阻止细胞铁的输出。Hepcidin以前激素、原激素和成熟的25个氨基酸肽的形式存在。在肝细胞中,hepcidin的成熟主要由原激素转化酶furin [8,9].hepcidin是无生物活性的[8,9而它在血清中的作用仍然是难以捉摸的。Hepcidin的表达受铁可用性和铁可用性的控制通过BMP/ smad依赖的信号通路和炎症刺激,最显著的是IL-6信号通过JAK/STAT通路[8,9].
此前的一项研究报道血浆hepcidin原与COPD严重程度呈负相关[11].我们自己的发现与该报告不一致,因为我们的数据清楚地表明,与正常健康对照组相比,吸烟者和前吸烟者COPD人群中hepcidin前水平显著升高(图1 b), hepcidin原水平有随疾病严重程度增加的趋势(图1 c).此外,COPD患者急性加重期血清hepcidin升高是其频繁加重表型的特征[12].此外,在频繁恶化组中,阳性患者的hepcidin明显高于阴性患者。
升高的hepcidin会限制转运铁蛋白的表达和活性以及细胞铁的释放,如果在肺和气道中起作用,将有利于细胞铁的保留而不是排泄,但后果不确定。重要的是,最近的另一项研究描述了由炎症驱动的COPD队列中铁缺乏的患病率[13].我们自己的研究表明,COPD患者的IL-6水平显著升高,目前有吸烟习惯(图1 d).鉴于IL-6在控制铁代谢和周转中的作用,在这些情况下,由hepcidin水平升高导致的IL-6释放和铁稳态中断之间的联系并非不合理。事实上,血清hepcidin和IL-6之间的关联在COPD加重期和稳定期均有描述[14].
以前的研究已经确定了从慢性阻塞性肺病和哮喘患者人群中获得的EBC中的总铁含量[15],这表明与对照组相比,总铁含量较低;这里提出的研究与这些不同,因为测量仅限于特定的氧化还原活性铁池。虽然在本质上是观察性的,但我们的数据表明,与正常健康和健康吸烟者对照相比,COPD患者的铁处理和排泄存在差异。考虑到铁在失去稳态时可能导致损伤、功能障碍和疾病,我们建议对慢性阻塞性肺病中的铁处理进行更深入的系统和区域分析是有必要的。
脚注
支持声明:本研究由皇家布朗普顿和海尔菲尔德NHS基金会信托基金和伦敦帝国理工学院的NIHR呼吸疾病生物医学研究部门以及皇家布朗普顿医院慈善基金支持。本文的资助信息已存入FundRef.
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2015年10月15日
- 接受2015年11月24日。
- 版权所有©ERS 2016