摘要
人气道基础干细胞有助于宿主-微生物相互作用和肺的先天免疫http://ow.ly/Q2UAF
气道上皮,覆盖气管支气管树的管腔表面,是保护肺部免受病原体、刺激物、有毒物质和其他压力源的主要屏障,这些压力源存在于每天流经气道的约10000升的空气中。这种屏障功能通常是由分化的纤毛和分泌细胞介导的,它们战略性地位于根尖层,与管腔内容物相互作用。通过这些细胞产生黏液和抗菌物质,并不断拍打纤毛以清除呼吸道中黏液滞留的细菌和其他空气微粒,保护肺部免受呼吸道损伤和感染[1].此外,紧密连接(相邻分化细胞的顶端膜域之间的多蛋白复合物)控制管腔内容物穿过上皮细胞的扩散,防止基底外侧隔室或上皮下富集的众多受体和炎症细胞的激活[2,3.].
然而,由于与环境接近,腔室细胞群,特别是纤毛细胞,最容易受到损伤,作为终末分化细胞,它们不能通过自我更新来应对损伤[4].因此,气道上皮屏障的维持和再生需要位于基膜正上方基底层的基底细胞(BCs),它们牢固地附着在基膜上通过半脂质体,这一特征使上皮细胞群更能抵抗损伤。与气道修复尤其相关的是,bc作为干细胞/祖细胞,能够自我更新并分化为气道上皮细胞的整个特化细胞群,包括纤毛细胞和分泌细胞[5].
在稳定状态下,由于组织学完整的气道上皮细胞周转缓慢,bc相对静止。然而,在对损伤的反应中,气道bc被激活,获得一组损伤相关的表型,需要快速恢复和正常分化的上皮屏障的后续再生。这一过程涉及到细胞骨架组织的改变,因此除了这些细胞组成性表达的角蛋白(KRT)5外,bc还获得间充质细胞相关的vimentin、各种基质金属蛋白酶,以在剥离的基底膜之上迁移,以及形成临时屏障所需的鳞状细胞相关的KRT6、KRT13和KRT14 [6].然而,要实现完全修复,需要气道bc的干/祖细胞功能,这涉及到bc衍生的“早期祖细胞”的自我更新和扩张,也称为中间细胞,在特定的利基衍生信号(包括Notch通路相关信号)的控制下,分化为纤毛细胞和分泌细胞[5].
当正常提供宿主防御功能的分化细胞被破坏,而在介导宿主-病原体相互作用方面“缺乏经验”的bc直接暴露在充满微生物的外部环境中时,气道是如何在损伤过程中免受病原体的伤害的?这个问题的答案在amatngalimet al。[7的论文中,作者证明了气道bc,除了作为已知的干细胞/祖细胞的作用外,还可以作为宿主防御因子的独特来源。在这项研究中,人气道的BCs,而不是分化的气道上皮细胞,对刺激有反应流感嗜血杆菌,一种常见的呼吸道病原体,RNase 7表达上调[7],是一种抗菌蛋白,最初从皮肤角质形成细胞中纯化[8].此外,许多其他先天免疫介质在气道bc中被上调,包括抗菌肽人β-防御素(hBD)-2、脂钙素2、促炎细胞因子白细胞介素(IL)-6和IL-8以及趋化因子CCL20 [7].尽管上皮细胞在介导先天免疫反应中的作用已被证实[1,3.],上皮干细胞除了在组织维护和修复中的作用外,还可以促进先天免疫防御的观察是新颖的,并对更好地理解宿主-微生物相互作用和上皮再生具有重要意义。
一些早期的研究已经将气道bc描述为呼吸道病原体的目标。机会致病菌,铜绿假单胞菌在修复的气道上皮细胞中,它与表达krt13的bc强烈结合[9].这种结合是由α5β1整合素介导的,该整合素在迁移到伤口区域的气道bc中上调[9].一旦紧密连接屏障被破坏,许多病毒可以访问bc,包括鼻病毒,它在增殖的表达krt14的bc上结合细胞间粘附分子(ICAM)-1 [10].有趣的是,鼻病毒感染BC会上调神经生长因子及其受体的表达,神经生长因子及其受体是气道BC干细胞的标记物[11],这可能与调节BC存活和进一步促进病毒进入有关[12].在气道上皮细胞损伤后,气道BC可被呼吸道合胞病毒感染,这使BC的命运偏向产生粘液的细胞系,并抑制向纤毛细胞的分化[13],导致在包括哮喘和慢性阻塞性肺疾病(COPD)在内的人类肺部疾病中常见的粘液增生。挑战这一传统观点,气道bc仅仅是病原体的目标,后者利用病原体促进微生物发病和感染性组织损伤,amatngalimet al。[7]提供的证据表明,气道BCs可以感知病原体的存在,并通过产生抗菌因子和细胞因子来激活免疫反应的各个方面,这表明BCs可以作为先天免疫细胞参与宿主-微生物的相互作用。
细胞通过感知普通微生物模式而非特定抗原的受体来识别“非我”的能力,这是先天免疫的一个关键特征[14],当这个细胞是组织干细胞时,可能有相当独特的意义。这可能是一种策略,可以让干细胞在修复过程中进行多任务处理,这样一个单一事件,即。感知微生物的危险,将允许两种保护性反应,组织再生和抗菌防御,同时发生,当这两种反应同等重要的情况下。虽然matngalimet al。[7]并没有评估先天免疫激活气道bc对其杀死细菌或介导组织修复能力的影响,已知气道上皮细胞对微生物模式的识别通过toll样受体(TLRs)可刺激增殖和组织修复[15].与这一概念一致的是,用细菌肽聚糖(胞质固有免疫传感器Nod2识别的一种常见细菌基元)刺激Lgr5肠干细胞,可保护该干细胞群体免受氧化应激介导的死亡,并增强上皮再生[16].最近,研究表明,肠道和乳腺上皮干细胞中的TLR2信号通路可促进这些细胞的自我更新和再生能力[17].
另一个有趣的观察是Amatngalimet al。[7的研究结果表明,即使在没有病原体的情况下,香烟烟雾引起的短暂上皮损伤也会增加气道bc中RNase 7的表达。这种反应依赖于信号通过表皮生长因子受体(EGFR),它在气道bc中高度表达[18],并介导微生物模式和香烟烟雾诱导的气道上皮组织修复和炎症细胞因子的产生[15,19,20.],并促进气道BCs对吸烟的反应的病理编程[21].因此,BC抗菌潜力的增强通过EGFR信号的激活可能代表着BCs对损伤的防御反应,使干细胞/祖细胞群准备好应对可能的微生物攻击,组织损伤的常见“伴侣”。类似的策略已经被描述在人类表皮上,无菌损伤促进抗菌肽的表达,包括hBD-3,它可以防止常见的皮肤病原体金黄色葡萄球菌[22].这种反应依赖于皮肤损伤后角质形成细胞释放的肝素结合表皮生长因子激活的EGFR [22].进一步与EGFR在增强上皮宿主防御以应对损伤的作用一致,EGFR抑制剂,通常用于治疗肺癌,显著降低表皮屏障的完整性,RNase 7的表达和人类角质形成细胞的抗菌活性[23].不仅微生物模式和损伤,而且响应这些刺激诱导的抗菌肽也利用egfr依赖的机制促进组织修复和先天免疫细胞因子的产生[24,25].鉴于除EGFR外,气道bc还表达大量EGFR配体[26],该干细胞/祖细胞群可能通过激活自身/旁分泌EGFR信号,同时参与组织修复和先天免疫反应(图1).
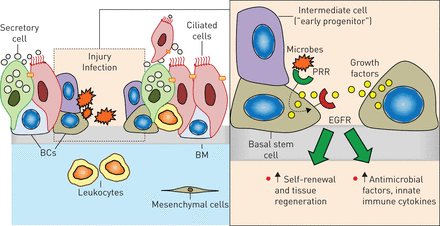
气道基础干细胞(BCs)有助于气道上皮组织再生和先天免疫。人类气道上皮由分化的纤毛细胞和分泌细胞组成,在正常情况下,纤毛细胞和分泌细胞共同在气道上皮表面提供宿主防御,而BCs是位于基底膜(BM)之上的干/祖细胞群。损伤会导致分化细胞,特别是纤毛细胞的损伤,因此BCs迁移到裸露的BM区域,产生中间细胞,或“早期祖细胞”,分化为纤毛和分泌细胞。这一过程受到生态位信号的调控,包括在损伤反应中上调的生长因子,激活了bc上的表皮生长因子受体(EGFR)。此外,bc还能感知经常伴随受伤的微生物通过模式识别受体(PRRs),它与EGFR信号合作,诱导抗菌肽/蛋白和先天免疫细胞因子的表达,并进一步促进组织再生。
气道BC干细胞的新颖的先天免疫功能可能与疾病的发病机制有关。紧密连接屏障的破坏是哮喘和吸烟引起的气道疾病的一个共同特征,通常由EGFR信号的改变介导[21,27,28],可使气道bc接近病原体。通过这种机制,气道bc中固有免疫反应的持续激活可能有助于这些疾病的慢性炎症特征。慢性阻塞性肺疾病(COPD)患者气道中常见由气道bc在损伤反应中产生的鳞状化生和上皮-间质过渡样重塑,并与IL-1β、IL-8和IL-33等炎性细胞因子的上调有关[21,29,30.].干细胞/祖细胞中夸大的先天免疫信号转导可能导致自我更新增强,可能导致致癌[17],这与吸烟诱发的肺癌尤其相关,气道bc被认为是肺癌的候选细胞来源[31].
进一步了解bc如何在人类气道中参与宿主防御和修复,以及这两个过程是如何协调的,将为人类肺部疾病的机制提供重要的见解,并确定新的治疗方法的靶点,以恢复这些疾病的正常气道上皮屏障通过气道bc干细胞和先天免疫功能的正常化。
脚注
支持声明:R. Shaykhiev部分由美国国家卫生研究院(国家心脏、肺和血液研究所)支持,授予R01 HL107882、R01 HL1189541和HL123544。本文的资助信息已存入FundRef.
利益冲突:没有声明。
- 收到了2015年3月31日。
- 接受2015年5月3日。
- 版权所有©ERS 2015