文摘
通气不稳定,反映在增强急性缺氧(AHVR)和hypercapnic (AHCVR)通气反应是一个基本组件的阻塞性睡眠呼吸暂停(OSA)的发病机理。间歇性低氧诱导炎症是提出促进AHVR增强在阻塞性睡眠呼吸暂停综合症,虽然在间歇低氧诱导呼吸系统炎症的作用变化,人类还没有检查。因此,本研究评估间歇性低氧诱导的炎症的作用在健康人体内呼吸可塑性。
一项双盲、安慰剂对照、随机交叉研究设计,12男性受到6 h间歇性缺氧三次。间歇性低氧暴露之前,参与者摄取(4天)安慰剂或非甾体类抗炎药吲哚美辛(非选择性环氧合酶(COX)抑制剂)和塞来昔布(选择性COX - 2抑制剂)。预处理和post-intermittent缺氧休息通风、AHVR AHCVR和血清浓度的促炎细胞因子肿瘤坏死因子(TNF) -α评估。
Pre-intermittent缺氧休息通风、AHVR AHCVR和TNF-α浓度在所有三个条件相似(p≥0.093)。间歇性低氧增加休息通风和AHVR同样在所有条件(p = 0.827),尽管AHCVR增加(p = 0.003)和TNF-α减少(p = 0.006)只有选择性的cox - 2抑制。
这些发现表明,炎症不导致人类间歇性低氧诱导呼吸可塑性。此外,选择性cox - 2抑制增强AHCVR间歇性低氧暴露后,表明选择性抑制cox - 2可能会加剧阻塞性睡眠呼吸暂停综合症严重程度增加通气不稳定。
文摘
非甾体类抗炎药不会阻止间歇性低氧诱导的人体呼吸系统可塑性http://ow.ly/MDiCk
介绍
阻塞性睡眠呼吸暂停(OSA)是一种慢性医学障碍与心血管和脑血管发病率和死亡率增加有关1,2]。阻塞性睡眠呼吸暂停综合症的特点是重复在睡眠中呼吸暂停由于咽的崩溃导致间歇性低氧暴露(IH)和血碳酸过多症。通气不稳定,部分反映了加强急性通气对缺氧的反应(AHVR) [3)和血碳酸过多症(AHCVR) [4),与阻塞性睡眠呼吸暂停综合症(严重性呈正相关5),导致阻塞性睡眠呼吸暂停综合症发病机理(6]。
IH接触被认为有助于增加通气不稳定在阻塞性睡眠呼吸暂停综合症急性(分钟小时)和慢性(天年)暴露增加AHVR [7- - - - - -11)和AHCVR (11- - - - - -14),虽然这些不一致的结果8,15]。逐步增加AHVR和AHCVR IH可能被认为是形式的呼吸可塑性(定义为持续改变的神经系统控制呼吸基于经验(16])。与增加通气反应缺氧后短暂IH曝光,这种形式的呼吸可塑性被贴上“渐进增强”(17]。,IH背后的分子机制增强通风的化学敏感性知之甚少,但涉及增加氧化应激(3,8,18- - - - - -24)和炎症(18,25]。在老鼠、预防IH-induced系统性和颈动脉体氧化应激也取消了增强颈动脉体化学感应的缺氧反应(20.)和AHVR (26]。此外,使用一个实验IH的人体模型,我们之前报道的增加与IH AHVR与IH-induced氧化应激(8]。是否氧化应激增强颈动脉体化学感应增强了AHVR直接仍在争论,直接应用活性氧(ROS)的颈动脉体不会产生激励和修改颈动脉体ROS生产不修改含有儿茶酚胺的分泌对缺氧的反应(18,22,27]。此外,抑制促炎细胞因子下游氧化应激与非甾体类抗炎药(非甾体抗炎药)布洛芬(非选择性环氧合酶(COX)抑制剂)废除了IH-induced AHVR增强[18]。这种废除AHVR增强结合最小化颈动脉体肿瘤坏死因子(TNF) -α和白介素(IL) 1β水平,和c-fos阳性神经元的数量在尾核束solitarii (nt)。
阻塞性睡眠呼吸暂停综合症是与升高的炎症标记物(28),这些发现表明,非甾体抗炎药可能提供减少严重阻塞性睡眠呼吸暂停综合症的治疗途径通过减少通气不稳定(18,25),但炎症的作用IH-induced通气化学敏感性的增加缺氧和高碳酸血症在人类还没有检查。因此,使用我们的人类实验模型的显示增加氧化应激和AHVR [8,29日),本研究评估IH-induced呼吸道的炎症可塑性的作用在健康人类广泛使用两个规定的非甾体抗炎药:消炎痛(非选择性COX抑制剂)和塞来昔布(选择性COX - 2抑制剂)。提出,炎症参与IH-induced人类呼吸的变化,非甾体抗炎药的使用将防止这些呼吸的变化。
方法
批准
本研究联合卫生研究伦理委员会批准的卡尔加里大学(加拿大卡尔加里AB)和执行根据《赫尔辛基宣言》。在最初接触之后,志愿者使熟悉试验装置,仪表和提供知情同意的形式。
参与者
这个双盲(15名健康男性志愿者即。实验者和参与者)、安慰剂对照、随机交叉研究2010年9月至2011年10月。招聘结束后实现所需的样本大小(在线补充材料)。两个志愿者拒绝参与和13提供书面知情同意(在线补充和无花果。S1)。随后,一位与会者没有完成这项研究由于第一个分配药物不良反应(30.]。因此,12个参与者完成了先前发表的实验协议及其特点(30.]。简单地说,参与者特征如下(意味着±sem):25.8±1.5岁,身体质量指数24.9±0.7公斤·m−2,血压正常的动脉血压(平均83.0±0.7毫米汞柱),没有睡眠呼吸紊乱(呼吸紊乱指数(RDI) 1.8±0.1事件·h−1和平均动脉oxyhaemoglobin饱和度(年代aO2)94.8±0.1%)。额外的细节呈现在网上补充材料。
试验协议
参与者暴露在实验室实验IH的人类脑血管生理学(卡尔加里大学)三次管理在一个双盲,安慰剂对照、随机交叉时尚。4天前每个IH曝光,参与者摄入安慰剂(订单。每天三次在喂饲h, h和夏令时间20:00 h),吲哚美辛(50毫克订单。每天三次在喂饲h, h和夏令时间20:00 h)或塞来昔布(200毫克订单。一家乳制品喂饲h和20:00 h)的两倍。维护的双盲研究中,安慰剂药丸是包含在第二药丸塞来昔布条件。实验天(5天),给药方案是保持到年底生理测试。因此,只有最后的药物剂量(定于20:00 h)省略在所有条件。每次IH曝光后,有一个最低为期4天,洗脱期(30.]。更多细节关于药物剂量在网上提供的补充材料。
在实验的日子里,参与者到达∼喂饲h和毛细血管和静脉血样不久。接下来,使用的技术动态end-tidal迫使[31日)的参与者进行了急性试验来评估通气反应isocapnic缺氧和hypercapnic氧过多。接下来,参与者接触到6 h (IH)。Post-IH,毛细血管和静脉血液样本收集和通气反应isocapnic缺氧和hypercapnic氧过多被重新评估。6小时IH曝光被选中,是因为我们之前发现使用为期4天IH协议AHVR显示最大的增加和氧化应激发生第一次6小时后IH接触(8]。
间歇isocapnic缺氧
利用定制,normobaric缺氧的房间,IH由自行车参与者end-tidal氧张力(P采访时表示288托(之间)年代aO2≈96 - 97%)和45托(年代aO2≈80 - 85%)每60年代6 h,因此复制的RDI 30事件·h−1是严重阻塞性睡眠呼吸暂停综合症患者的观察。End-tidal二氧化碳张力(PETCO2在IH曝光)是维持在正常水平,如前所述[31日]。从鼻插管气息奄奄的气体连续采样150毫升·分钟−1和分析有限公司2和O2分数由双气体分析器(Normocap氧;Datex-Ohmeda,路易斯维尔,美国),允许breath-by-breath的决心P采访时表示2和PETCO2在IH曝光。此外,年代aO2监视着一个耳垂脉搏血氧计(3900 p;Datex-Ohmeda,麦迪逊,美国WI)。参与者在IH曝光不允许睡觉。更多细节在网上提供的补充材料。
预处理和post-IH评估休息通风,AHVR AHCVR
主要的研究结果是抗炎药物的效果AHVR IH后增加。pre-IH测试开始10分钟的空气呼吸决定休息PETCO2和P采访时表示2。接下来,PETCO2+ 1托高于静止水平和提高P采访时表示2维持在euoxic(88托)5分钟(isocapnic euoxia基线)。随后,PETCO2保持在+ 1托P采访时表示2是骑车45至88托每90年代直到六缺氧发作。第六缺氧发作后,PETCO2保持在+ 1托P采访时表示25分钟增加到300托(isocapnic氧过多休息),之后呢PETCO2增加额外+ 9托休息水平以上5分钟(hypercapnic氧过多),紧随其后的是回归isocapnic euoxia 5分钟恢复。图1展示了一个示意性的急性测试;技术细节和数据分析提供了在线补充材料。
示意图的急性试验前后经历了由参与者接触6 h isocapnic间歇性缺氧。实线:end-tidal氧张力;虚线:end-tidal二氧化碳张力。
炎症标记物
血清TNF-α和IL-1β浓度测定通过ELISA (Ready-SET-Go !;美国圣地亚哥eBioscience CA)后,制造商的指示。TNF-α和IL-1β工具包的敏感性4 pg·毫升−1和范围的4 - 500 pg·毫升−1。
统计分析
因变量都为正常使用Shapiro-Wilk测试评估。随后,三-(药物:安慰剂,消炎痛或塞来昔布)由两个(IH: pre -和post)因素重复测量方差分析是用来比较依赖变量。TNF-α数据不是正态分布,分析了使用一个对齐的秩变换和重复测量方差分析32]。如果主要的影响是重要的,事后比较进行合并Bonferonni修正多重比较。α是先天的使用SPSS 0.05和统计分析(版本21;IBM公司,美国纽约阿蒙克)。结果意味着±扫描电镜。一位与会者Post-IH血液抽样是不成功的。因此,参与者被撤TNF-α和IL-1β浓度的分析。
结果
Isocapnic euoxia基线
有一个显著的影响(p = 0.020)的摄入的药物4天休息,吸气式的PETCO2(安慰剂37.7±0.6托;托非选择性COX抑制36.6±0.6,p = 0.026与安慰剂;和选择性cox - 2抑制37.1±0.7托,p = 0.298与安慰剂,p = 0.721与非选择性COX抑制),通过设计,翻译成isocapnic euoxia基线(表1)。
通过设计,IH没有影响PETCO2在isocapnic euoxia基线(p = 0.819)。相比之下,P采访时表示2所有药物在isocapnic euoxia基线相似条件(p = 0.502)和预处理和post-IH条件(p = 0.949)。同样,每分通气量的药物主要作用不显著(V′E)(p = 0.383),潮汐卷(VT)(p = 0.985)和呼吸频率(fR)(p = 0.428),尽管IH有显著的影响V′E(p = 0.003)fR(p = 0.004),但不是VT(p = 0.120)。pre-IH值相比,post-IHV′E在安慰剂更高(p < 0.001)和COX - 2抑制条件(p = 0.003),和显示趋势更大的非选择性COX抑制条件(p = 0.072)。fR增加在所有三个药物条件IH (p≤0.049)。
通气对缺氧的反应
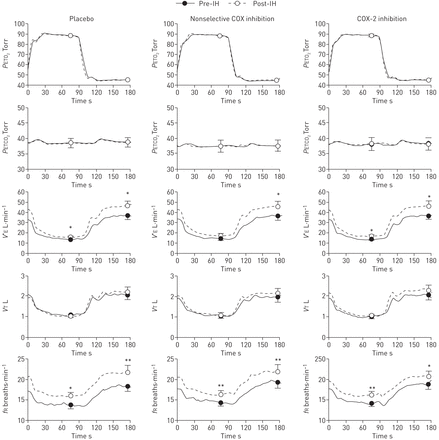
图2显示了覆盖的预处理和post-IH组平均测试期间急性缺氧周期。对所有药物条件,预处理和post-IHPETCO2(p≥0.569),P采访时表示2(p≥0.158)VT(p≥0.087)没有不同。相比之下,V′E(p < 0.001)fR后(p < 0.001),升高IH在所有条件。为V′E,有一个明显的缺氧试验的两个阶段之间的相互作用(0 - 90年代:isocapnic euoxia;91 - 180年代:isocapnic缺氧)和IH暴露在所有药物(p≤0.023)条件,更大V′E在IH后缺氧暴露(p≤0.023)。
组平均isocapnic通气反应在急性缺氧评估测试执行之前和之后6小时间歇缺氧(IH)曝光的安慰剂,非选择性COX抑制和选择性COX - 2抑制条件。为每个6周期在急性缺氧执行测试,所有的变量都是内插在1 s,覆盖和平均,从而创建一个组的意思是180年代响应(0 - 90年代:isocapnic-euoxia;91 - 180年代:isocapnic缺氧)。预处理和±post-IH数据作为手段扫描电镜最后两个阶段的30年代的挑战(isocapnic euoxia: 0 - 90年代和isocapnic缺氧:91 - 180年)。P采访时表示2:end-tidal氧张力;PETCO2:end-tidal二氧化碳张力;V′E:肺每分通气量;VT:潮汐卷;fR:呼吸频率。*:p < 0.05与pre-IH价值;* *:p < 0.01与pre-IH价值。
图3显示了预处理和post-IH AHVR所有条件。无论IH暴露(药物主要作用),AHVR相似在所有三个条件(p = 0.642)。IH的主要效应是显著(p = 0.005),与post-IH AHVR被更大的在所有条件(p≤0.026)。最后,drug-by-IH交互作用不显著(p = 0.827),表明IH-induced AHVR增加之间相似的安慰剂(图3)、非选择性COX抑制(图3 b)和选择性抑制cox - 2 (图3c)条件。
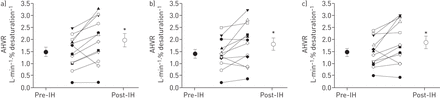
个人和均值±扫描电镜急性低氧通气反应(AHVR)之前(符号)和之后(明确的符号)接触6 h间歇性缺氧(IH)安慰剂,b)非选择性环氧合酶(COX)抑制和c)选择性COX - 2抑制条件。*:p < 0.05与pre-IH价值。
Isocapnic氧过多休息
预处理和post-IH意味着通气期间数据的最后一分钟5分钟isocapnic氧过多休息所示表1。通过设计的差异PETCO2这三个药物之间条件在isocapnic euoxia基准维护(药物主要作用p = 0.013),而前和post-IHPETCO2是相同的(IH主要影响p = 0.751)。此外,P采访时表示2所有三个药物相似条件(p = 0.275)和预处理和post-IH (p = 0.567)。类似于isocapnic euoxia基线,药物主要作用不显著V′E(p = 0.253),VT(p = 0.317)fR(p = 0.212), IH主要作用是很有意义的V′E(p = 0.012)fR(p = 0.003),但不是VT(p = 0.266)。Post-IH,V′E大于安慰剂(p = 0.025)和COX - 2抑制条件(p = 0.031),和显示趋势更大的非选择性COX抑制条件(p = 0.059)。fR在无选择性的增加(p = 0.015)和选择性cox - 2抑制(p = 0.002)条件下,增加的趋势在安慰剂条件(p = 0.068)。
通气反应血碳酸过多症
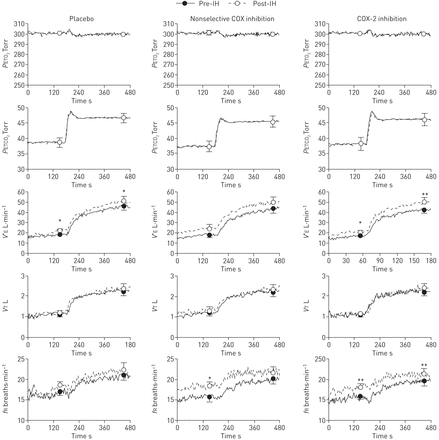
预处理和post-IH组平均hypercapnic组件的急性测试所示图4。在所有药物条件,预处理和post-IHPETCO2(p≥0.533),P采访时表示2(p≥0.142)VT(p≥0.181)没有不同。相比之下,V′E(p≤0.050)fRIH后(p≤0.034)增加。与缺氧,阶段之间的交互hypercapnic氧过多测试(0 - 180年代isocapnic氧过多;181 - 480年代:isocapnic缺氧)和IH显著的选择性cox - 2抑制条件(p = 0.007),和一个更大的提高V′E期间血碳酸过多症之后IH曝光(p = 0.007)。这是反映在一个更大的AHCVR IH曝光后(图5度),尽管在所有三个条件比较AHCVR药物主要作用不显著(p = 0.093)。此外,drug-by-IH交互作用也不显著(p = 0.086)。当比较AHCVR穿过三个条件使用一个3×2重复测量方差分析,无论是药物主要作用的结果,也不是drug-by-IH交互是很有意义的可能的后果的增加AHCVR选择性cox - 2抑制,虽然重要,相对较小。
组平均hypercapnic通气反应氧过多评估急性测试之前执行,期间和之后,6小时间歇缺氧(IH)曝光的安慰剂,非选择性环氧合酶(COX)抑制和选择性COX - 2抑制条件。对所有变量,数据的最后3分钟isocapnic氧过多的全部5分钟休息和hypercapnic氧过多在1 s允许插值计算的意思。预处理和±post-IH数据点是手段扫描电镜60年代的最后两个阶段的挑战(isocapnic氧过多0 - 180年代和isocapnic缺氧181 - 480年代)。P采访时表示2:end-tidal氧张力;PETCO2:end-tidal二氧化碳张力;V′E:肺每分通气量;VT:潮汐卷;fR:呼吸频率。*:p < 0.05与pre-IH价值;* *:p < 0.01与pre-IH价值。

个人和均值±扫描电镜急性hypercanic通气反应(AHCVR)之前(符号)和之后(明确的符号)接触6 h间歇性缺氧(IH)安慰剂,b)非选择性环氧合酶(COX)抑制和c)选择性COX - 2抑制条件。*:p < 0.05与pre-IH价值。
炎症标记物
TNF-α浓度低于检测极限(4 pg·毫升−1一位与会者。因此,TNF-α浓度为10参与者所示图6。没有药物(p = 0.394)或IH效果(p = 0.292),但drug-by-IH交互显著(p = 0.046),减少驱动后TNF-αIH内选择性cox - 2抑制条件(p = 0.009;图6c)。血清IL-1β浓度低于检测极限(4 pg·毫升−1)八个参与者(在线补充表S2)。因此,没有进行统计分析。
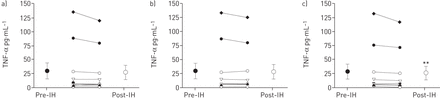
个人和均值±扫描电镜(n = 10)血清肿瘤坏死因子(TNF)之前(符号)和之后-α浓度(明确的符号)接触6 h间歇性缺氧(IH)安慰剂,b)非选择性环氧合酶(COX)抑制和c)选择性COX - 2抑制条件。* *:p < 0.01与pre-IH价值。
预处理和post-IH毛细管血液样本收集的结果是包含在网上补充(表S2)。
讨论
这是第一个研究评估机械作用在健康人体内IH-induced呼吸道炎症的可塑性。主要的发现是,非选择性和选择性cox - 2非甾体抗炎药(分别吲哚美辛和塞来昔布)阻止了海拔isocapnic euoxia休息通风或后AHVR IH的增加(即。量化使用急性测试之前执行,之后,6小时IH暴露)。此外,选择性cox - 2抑制促进一个小,但意义重大,增强AHCVR IH。这些发现表明IH-induced炎症并不导致呼吸道可塑性发生急性IH暴露于人类健康。此外,选择性cox - 2抑制可以促进通气IH后不稳定通过增加AHCVR。
休息通风
与安慰剂相比,pre-IH吸气式的休息PETCO2低1∼托考克斯在非选择性抑制状态,但类似在选择性COX - 2抑制条件PETCO2选择性和非选择性的cox - 2抑制之间的相似条件。较低的原因PETCO2后4天摄入的非选择性COX抑制剂吲哚美辛尚不清楚。据我们所知,长期抑制COX在休息通风的影响没有被调查。相比之下,90分钟后一个100毫克剂量的非选择性COX抑制剂吲哚美辛,通风已经报道有更大的变化(即。更大程度的起伏)[33]。这是否增加变异性维护,增强或减少经过4天的摄入是未知的,但如果维持或增强,这也许可以解释下PETCO2观察到。
通气长期便利(vLTF),特点是持续增加休息通风几分钟到几小时完成后的短暂接触,是一种呼吸道可塑性(17,34从高架呼吸运动输出)和结果35]。在最近的研究中,post-IH休息isocapnic euoxic通风在安慰剂,高选择性的COX - 2抑制条件下,具有较强的趋势增加通风在非选择性COX抑制状态。作为post-IH isocapnic euoxia通风评估∼20分钟后参与者退出低氧室(在血液采样和急性测试仪器),提高通风可能代表vLTF的感应。有趣的是,大post-IH通风造成增加fR作为VT没有不同于pre-IH水平(表1)。曝露这种呼吸模式不同于观察老鼠的LTF呼吸运动输出通常被作为破裂振幅增加呼吸道相关神经(如。膈),神经相当于潮汐卷(36]。相比之下,研究unanaesthetised老鼠通常报告LTF造成的呼吸运动输出增加呼吸频率(36]。此外,研究报告vLTF人类在短暂hypercapnic IH协议(八4分时间的缺氧(吸入氧气分数(FIO28%),normoxia相隔5分钟(FIO221%)描述潮汐卷和呼吸频率的增加(37,38]。因此,研究结果的通气模式IH-induced LTF是模棱两可的,和可能的结果不同IH协议。基于动物研究显示LTF呼吸运动输出短暂IH曝光后,有人提议,对于睡眠呼吸暂停患者,暴露在IH在一个晚上的睡眠也可能导致vLTF [39,40]。据我们所知,目前的研究是第一个报道的增加休息通风IH曝光后在健康人类模仿适度睡眠呼吸暂停和类似的持续时间的睡眠。
类似于休息isocapnic euoxic通风,isocapnic氧通风也是大post-IH急性试验期间,再次呼吸频率增加的结果。当氧过多平静颈动脉体活动(41期间,增加通风isocapnic氧过多IH支持在体外证据表明,继续呼吸运动输出增强是一个适应中央呼吸控制中心(42]。
最后,对休息isocapnic euoxia和isocapnic氧过多通风,无论是消炎药预防IH-induced frequency-based vLTF。因此,抑制炎性标志物通过非选择性COX抑制剂吲哚美辛和选择性COX - 2抑制剂塞来昔布(如。核因子(NF) -κB和COX通路)不出现为观察frequency-based vLTF。
AHVR和AHCVR
增加AHVR (通过增加呼吸频率)安慰剂条件类似于先前的报道(7- - - - - -12]。虽然机制不完全理解,提出了氧化应激的主要中介,作为抗氧化剂治疗前(20.]在[18]IH暴露预防颈动脉体感觉长期的便利化和增强的化学感应的缺氧反应(20.)以及增加AHVR (3,18]。此外,在健康的人类,我们报道,IH-induced增加AHVR呈正相关(r = 0.88)氧化应激的系统性措施(8]。直接应用ROS的颈动脉体不会导致激发,也没有改变颈动脉体ROS生产修改含有儿茶酚胺的分泌对缺氧的反应(18,22,27),仍然有争论关于是否IH-induced AHVR增强氧化应激增加的直接结果。最近,IH-induced炎症(造成氧化应激增加)和促炎细胞因子的生产(如。TNF-α和IL-1β)提出了有助于增强AHVR IH后(25]。支持这一假说,D埃尔Rioet al。(18)报道,政府非选择性COX抑制抗炎药布洛芬的老鼠暴露在IH阻止AHVR增强。从力学上看,尽管布洛芬最小化的增加颈动脉体TNF-αIL-1β,这并没有阻止强颈动脉体化学感觉的对缺氧的反应。相反,布洛芬的c-fos阳性神经元数量减少尾核束solitarii(衡量核束solitarii激活),表明IH-induced炎症可能会采取行动通过中央,而不是外围通路在AHVR增加。在这两种情况下,当前在健康人体内发现的一个增广AHVR IH后在选择性和非选择性的cox - 2抑制条件与这些观察。
除了物种差异,两个可以解释这些对立的结果不同。首先,当前的研究利用急性(6小时)IH暴露而D埃尔Rioet al。(18)暴露大鼠慢性IH (8 h·天−121天)。IH范例,这个概要文件的炎症反应可能不同,持续时间较长的IH曝光被要求刺激炎症(26,43]。因此,IH-induced炎症可能从力学上看更重要的是在慢性IH后通气改变,而IH-induced氧化应激(8)和/或改变气体介质内的低氧传感颈动脉体(如。一氧化碳和硫化氢)[44),可以调节呼吸变化后急性婴幼儿血管瘤,但后者仍然需要调查(45]。第二,不同的两项研究中使用的非甾体抗炎药是:非选择性COX抑制剂吲哚美辛和选择性COX - 2抑制剂塞来昔布与非选择性COX抑制剂布洛芬。尽管这些药物都是可逆的上游COX抑制剂,抑制促炎转录因子NF-κB,他们都有不同的药理属性(如。布洛芬是proprionic酸衍生物,而indometacin吲哚乙酸衍生物),药物动力学(如。抑制浓度中位数COX-1和cox - 2) (46)和非目标药效学(如。微分影响激酶与颈动脉体氧传感(45,47),可能导致这些对比的结果。
颈动脉体和呼吸中枢TNF-α浓度和IL-1β不易评估在人类中,预处理和post-IH血清浓度促炎细胞因子的量化。IL-1β是可量化的只有三个参与者,解释这些数据是有限的,但是这些发现表明IL-1β很小的作用,如果有的话,在观察IH-induced呼吸的变化。当我们观察到显著增加AHVR IH (即。研究的主要结果),没有额外的参与者招募了进一步探索IH后IL-1β和呼吸的变化之间的关系。因此,讨论仅限于TNF-α。维护后的血清浓度TNF-αIH在安慰剂条件与结果报告增加TNF-α在老鼠只有3 h (IH曝光,但类似于以前的人类研究使用那么严重IH接触(48]。这个维修后的血清浓度TNF-αIH暴露在安慰剂条件并不一定表明炎症没有参与增加AHVR,系统性TNF-α可能不能反映颈动脉体浓度(25)和中央炎症。相反,作为非选择性COX抑制剂剂量方案和选择性COX - 2抑制剂塞来昔布被用来产生系统性的抗炎作用,并抑制促炎转录因子NF-κB除了各自的考克斯同功酶,类似于休息通风,增加类似AHVR所有条件表明炎症标记物通过NF-κB和COX通路没有参与急性IH-induced AHVR增大。或者,这些结果可以表明药物剂量不足,虽然剂量足以减少尿前列腺素类含量(环前列腺素,前列腺素(PG) E2、血栓素A2和PGF2α以预期的方式(30.])。此外,IH没有改变前列腺素类含量,除了铂族元素的增加2浓度在安慰剂条件(30.]。因此,选择性和非选择性的cox - 2抑制阻止了铂族元素的增加2IH的曝光,但没有废除的增加休息isocapnic euoxia和isocapnic氧过多通风,增强AHVR,前列腺素类似乎没有一个角色在观察呼吸的变化。
后增加AHCVR IH报道之前(11- - - - - -13),但不是一个一致的观察,用较短的时间IH研究报告没有变化(8,15]。因此,在安慰剂组和非选择性COX抑制条件不变AHCVR后6小时IH暴露与先前的研究一致使用更多的急性IH曝光(8,15]。相比之下,增强AHCVR内选择性cox - 2抑制条件可能与脑血流(CBF)的变化。通常情况下,急性IH后,CBF维持或略高(31日]。以前,我们在CBF报道明显降低吸气式的休息在同一12参与者IH曝光后在选择性cox - 2抑制条件(30.]。作为CBF逆相关通风通过调节二氧化碳去除,因此,中央化学感受器细胞外的pH值(49),观察到的减少post-IH CBF可能导致观察到的增强AHCVR。
临床意义
更大的通气不稳定与提高阻塞性睡眠呼吸暂停综合症严重程度(5)和IH接触后发生在人类身上通过增强通气对缺氧的反应(7- - - - - -12和血碳酸过多症11- - - - - -14]。动物模型表明增加炎症在促进IH-induced AHVR增大,表明抗炎药物可能提供治疗途径减少通气不稳定,因此,阻塞性睡眠呼吸暂停综合症严重程度(18,25]。目前发现在人类不支持这种潜在的治疗用途,至少对于急性IH曝光。此外,选择性cox - 2抑制药物的使用可提高通气不稳定(通过一个增强AHCVR)和阻塞性睡眠呼吸暂停综合症的严重程度。未来的研究需要确定的影响不再IH暴露在健康人体内炎症和抗炎药物对IH-induced呼吸道可塑性的影响。此外,抗炎药物的影响在未经治疗的阻塞性睡眠呼吸暂停综合症AHVR和AHCVR需要调查。
必须承认,这项研究的局限性。首先,尽管使用的IH模型复制的血氧饱和度下降剖面特征是严重阻塞性睡眠呼吸暂停综合症,它不是一个完美的复制,因为它缺乏胸内压增加的负面,血碳酸过多症和睡眠破碎与阻塞性呼吸暂停(28]。第二,研究参与者的健康男性自由常常伴随阻塞性睡眠呼吸暂停综合症的并发症。虽然这些限制可能减少外推我们的发现阻塞性睡眠呼吸暂停综合症,IH模型和研究人口提供机会评估IH-induced呼吸道的炎症可塑性的作用没有混杂因素(8,30.]。
结论
这项研究表明IH-induced炎症没有参与急性IH-induced AHVR增强人类健康。此外,使用选择性cox - 2抑制治疗阻塞性睡眠呼吸暂停综合症患者或健康个体经历IH接触(如。高原训练)可能保证谨慎由于潜在的通气不稳定性增强通过提高AHCVR。最后,尽管这些发现扩展的程度阻塞性睡眠呼吸暂停综合症或健康的人类暴露于慢性IH仍需探索,这些结果值得关注和进一步研究。
确认
作者感谢参与者自愿地参与这项研究。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:披露可以找到与本文的在线版本www.qdcxjkg.com
这项研究是在注册www.clinicaltrials.gov标识号NCT01280006。
支持支持声明:A.E. Beaudin艾伯塔创新——健康解决方案(AI-HS)博士奖学金和加拿大卫生研究院研究加拿大(CIHR)——心脏及中风基金会关注中风博士奖学金。支持x华尔兹哈雷n·霍奇博士后奖学金(霍奇大脑研究所,卡尔加里大学)。支持m .双关威廉·h·戴维斯医学研究奖学金(卡尔加里大学);动向Wynne-Edwards是杰克曼比较内分泌学教授(卡尔加里大学兽医学院);S.B. Ahmed AI-HS支持CIHR和阿尔伯塔省卫生和健康之间的联合倡议和阿尔伯塔大学和卡尔加里。CIHR提供的赞助研究(首席研究员:M.J. Poulin co-applicant: P.J.汉族)和加拿大自然科学和工程研究理事会(首席研究员:M.J.保林)。M.J.保林布伦达斯特拉福德基金会主席在阿尔茨海默研究。为这篇文章一直存放在资助信息FundRef。
- 收到了2015年1月16日。
- 接受2015年4月19日。
- 版权©2015人队