文摘
与基于癌基因依赖的治疗方法提供重要的抗癌的好处,识别间变性淋巴瘤激酶(碱性)重组的一个关键方面是肺癌的管理。的针对有eml4 - alk检测到基因融合在4 - 8%的肺癌,主要对轻度吸烟者和非吸烟者。Crizotinib第一代理人批准在这个指示,与10.9个月的中位无进展生存作为一线治疗,化疗后7.7个月时管理。总体中位数生存与crizotinib二线设置为20.3个月。第二代筛选抑制剂目前正在评估,早期研究提供令人印象深刻的结果,尤其是在患者抗crizotinib或脑转移。在化疗,培美曲塞在这个人口似乎特别活跃。尽管这一进步,几个问题仍未得到解答。检测策略应该喜欢什么?的机制是什么阻力,什么选项可用来克服它们呢?进展患者的最佳方法是什么?本文概述了当前文献中的数据和解决这些问题。
文摘
碱性定义了患者受益于筛选抑制剂所以先进nonsquamous NSCLC应该系统地测试http://ow.ly/KQ2oS
介绍
肺癌是世界范围的一个主要死亡原因,每年160万新病例和140万例死亡记录(1]。转移性疾病很少治愈患者,化疗导致显著的进步在过去的几年里,不幸的是,这已经不是翻译成一个改善这些患者的预后。
致癌因素的识别是在癌症研究中最重要的发现之一。在nonsmall细胞性肺癌(NSCLC),重组的间变性淋巴瘤激酶(碱性)代表第二个主要致癌司机在表皮生长因子受体(表皮生长因子受体)突变。就像表皮生长因子受体,治疗方法针对碱性基因异常有令人印象深刻的结果的响应率和响应时间。
分别,碱性改变只出现在总人口的一小部分;然而,专门针对这个群体是至关重要的,同时具有一个有效的策略,筛选和确认诊断。病人的治疗管理窝藏这致癌基因成瘾应该个性化,考虑病人和肿瘤的生物特异性。
筛选功能和基因异常
碱是胰岛素受体酪氨酸激酶受体属于总科。它是由一个细胞外跨膜域和胞内酪氨酸激酶结构域。主要表达在中枢神经系统(2),碱的生理作用在人类和哺乳动物仍不清楚。对斑马鱼的研究表明它在神经嵴的发展过程中发挥作用3]。细胞外的域的定义特征包括glycine-rich部分,以及一个LDLa(低密度脂蛋白类a)域和老妈(meprin、A5蛋白和受体蛋白酪氨酸磷酸酶μ)段(4]。配体包括pleiotrophin [5]和midkine [6),两者都是在神经系统发育中发挥作用,以及细胞生存和肿瘤发生[7,8]。
第一个筛选异常参与癌症的证据可以追溯到二十多年前,当M鸢尾草et al。(9]报道涉及nucleophosmin基因重排(NPM1)(5 q35)碱性在非霍奇金淋巴瘤(2 p23)。可以由于易位激活筛选(异常的两个基因导致融合蛋白),放大(的表达增加碱性成绩单)或突变。的碱性轨迹是一个易位热点,超过22融合识别。在激酶结构域突变是最常见的。异常暗示alaska airlines在肿瘤发生在不同的组织,已报告的激活机制(补充图S1)。
体细胞碱性重组与支气管肺的癌症于2007年首次报道(10]。多个基因可能是融合的碱性基因,产生不同的碱性变体。基因在非小细胞肺癌的情况下,合作伙伴包括棘皮动物microtubule-associated蛋白质像4 (EML4),驱动蛋白家族成员(KIF5B)[11),TRK-fused基因(过渡政府)[121),驱动蛋白轻链(KLC1)[133)、蛋白酪氨酸磷酸酶non-receptor类型(PTPN3)和striatin calmodulin-binding蛋白(STRN)[4]。有趣的是,alaska airlines熔点是相同的在所有情况下(14]。在肺癌中,重组碱性激活的主要来源。此外,放大和突变已报告,通常情况下的耐碱性酪氨酸激酶抑制剂(TKIs)。碱性重组是筛选+在整个复习。
信号通路的下游碱性是复杂的,根据不同的激活机制。途径涉及包括RAS /增殖蛋白激酶(MAPK),磷酸肌醇3-kinase (PI3K) /哺乳动物雷帕霉素靶(mTOR),磷脂酶Cγ,RAS-related蛋白质(RAP) 1、Janus激酶(激酶),小君和信号传感器和转录激活(统计)。碱调节多个基因在转录水平,包括MYCN JUNB, b细胞淋巴瘤(BCL) 2、BIM和BCL24]。激活细胞生长和分化的筛选结果,同时限制细胞凋亡。
针对有eml4 - alk融合蛋白在肿瘤发展的作用已被广泛报道在体外以及在活的有机体内在小鼠模型15]。临床前研究表明,ALK-driven肿瘤体内碱性TKIs高度敏感在体外在人类肿瘤细胞系的面板包括非小细胞肺癌,和这些细胞是依赖于碱性的生长和存活(16]。
碱激活预测和预后的影响
的预测价值碱性易位的碱剂(乙醇)crizotinib已经明确。碱性似乎也发挥独立预后的作用。在最近的一次欧洲研究包括1281例切除舞台》肺腺癌,筛选患者+肿瘤(根据荧光原位杂交(鱼)和/或免疫组织化学(包含IHC))和碱性配对−患者(17]。在80包含IHC+病人(占总数的6.2%),无进展生存(PFS)和总生存期长而包含IHC−病人,风险比(人力资源)为0.61 (95% CI 0.41 - -0.90;p = 0.012)总生存期为0.65 (95% CI 0.46 - -0.93;PFS p = 0.018)。当只考虑鱼(2.2%的人口),与总体存活率显著差异仅仅是见过。
数据仅在晚期患者更确凿,回顾性研究。在一项研究山楂et al。(18]在crizotinib-naive患者中,无显著差异,而在生存36筛选+(鱼)患者crizotinib相比253年野生型患者没有收到crizotinib的控制。然而,矛盾的数据已发表在亚洲人群中,碱性重组与不利的预后有关的总生存期(19,20.]。
碱的特点+人口
针对有eml4 - alk易位代表non-epidermal肺癌的4 - 8%,相当于全球大约50 000名患者(21,22),代表一个主要流行病学问题。组织学检查筛选+肿瘤通常是最细粒状的腺癌,经常表达甲状腺转录因子- 1 (TTF-1) [23]。他们也可能存在特定的形态特征如印戒细胞(SRC)组件。在肿瘤窝藏SRC,一些基因异常出现在高频率,高达26%,碱为6%,ROS1 [24]。
许多临床特点的系统中发现的一些研究在世界范围内,包括美国(25),欧洲(26)和中国(27)的人口。大部分患者从不/轻度吸烟者(≤10久)碱性易位在不吸烟患者的15%与只有2%的吸烟者25]。患者也往往是年轻和表达野生型tumoral EGFR。男性的高频率不一致的报告。相比表皮生长因子受体突变、民族起源似乎没有任何影响。的主要临床特殊性与碱有关+在诊断脑转移的频率更高(40%)(26]。
美国病理学学院建议测试所有与非小细胞肺癌患者的肿瘤呈现一个腺癌组件或者当这种组织学不能完全排除由于有限的组织样本。临床特点不应该是一个限制因素,探索性分析和测试应该特别鼓励在从未/轻度吸烟者[28]。碱性异常表皮样肺癌是极其罕见的(523)(0.2%)中的一个28),一些研究报告发病率不高,在这个阶段,改变上述建议筛查(29日]。
的检测方法
鱼是目前参考检测方法筛选融合(25]。这项技术使用两个特定DNA探针,荧光标记每个耦合,一个绿色,一个红色,涵盖2 p23碱性地区。在野生型的场景中,红色的信号(3′alaska airlines)和绿色信号(5′alaska airlines)相邻。当这两个信号之间的距离信号直径的两倍多,他们被认为是分离的,反映出两个DNA区域的物理分离,因此易位。
鱼被认为是积极的,如果> 15%的肿瘤细胞数在4个字段显示绿色和红色之间的分离信号或一个红色信号损失相关的绿色信号。这15%的阈值允许错误由于背景噪音,阅读或异常的杂交(30.]。至少50细胞必须计算,第二个50细胞计数之间的第二个读者如果有10%和50%的阳性细胞。
鱼的优势在于其检测的能力碱性重组无论变体或融合蛋白,以及其与临床疗效的相关性。它已通过美国食品和药物管理局(FDA)的crizotinib (Vysis碱分解鱼探测设备;雅培分子公司、德斯普兰斯IL,美国)。
包含IHC检测是另一个方法碱性重组在肺癌。最初,它是与敏感性问题[31日- - - - - -34)和偶尔的假阳性结果;然而,新的超灵敏包含IHC技术似乎提供了一个更可靠的和敏感的筛查方法35]。积极性阈值通常是视觉,强烈要求适度染色在5 - 10%的细胞(36]。包含IHC的优势主要是它的低成本方面的时间和人力,但标准化测试是困难的。的摘要包含IHC和鱼在肺癌患者可以表现在几项研究中发现补充表S1。
同时包含IHC是一个可靠的筛查工具,鱼需要确认的事件正包含IHC甚至在某些情况下负包含IHC患者呈现预测重排标记,包括年轻时代,轻度吸烟者(≤10久)和测试为阴性其他突变,特别是表皮生长因子受体和喀斯特(34,37]。
最后,逆转录酶聚合酶链反应可能成为常规的快速诊断技术碱性易位。这种非常具体的技术提供了一个额外的好处,即识别相关的融合基因碱性。有限的使用日期是由于质量的要求从新鲜的或冷冻肿瘤组织DNA样本。然而,新平台允许使用常规的组织样本,包括石蜡包埋标本,已报告(38,39]。
目前治疗药物
有针对性的筛选抑制剂
从研究中获得的知识与表皮生长因子受体体内碱性TKIs TKIs加速了发展。在肺癌患者迄今发表的主要研究总结表1和正在进行的研究是在补充表S2。在肺癌,乙醇是目前只用于管理转移性癌症的患者,和辅助设置中没有数据或与放疗相结合。从研究结果的主要乙醇目前正在开发介绍如下。
Crizotinib
Crizotinib TKI倍数,是第一个可用碱治疗+病人。原本是为了阻止c-MET,后来发现也目标筛选,ROS1和“recepteur d’origine Nantais”(罗恩)[44]。在第一阶段我研究使用crizotinib (pf - 02341066), 37例晚期癌症患者治疗,包括十NSCLC患者筛选+肿瘤。其中,一个病人有一个完整的响应,两个反应部分和4名患者报告疾病稳定(45]。这导致了一个扩展研究的专用膨胀的149患者高级筛选+肺癌,143人可评价的46]。的推荐剂量250毫克每日两次,成立于剂量升级阶段我学习的一部分,是使用。客观反应报告了87名患者在这个扩展组(60.8%,95%置信区间52.3% - -68.9%),其中包括三个完整的响应和84年部分反应,预期的改进率< 10%,典型的细胞毒性药物。PFS是9.7个月,预计6 - 12个月总体存活率为87.9%和74.8%,分别为(47]。这些结果导致快速FDA批准于2011年8月为碱性+患者,无论前处理线的数量。副作用主要是年级1 - 2(72%)和包括恶心/呕吐、消化系统毒性(尤其是腹泻或便秘)和外周水肿。嗜中性白血球减少症和转氨酶海拔也报道,最常见的3 - 4级毒性(24%)。这个肝毒性也被报道与其他抑制剂和因此可能与抑制剂的活性crizotinib会面。crizotinib的安全性是确认在随后的III期研究(表2)[40,48]。
第三阶段概要1007年的研究表现,比较crizotinib与培美曲塞或多烯紫杉醇联合铂在碱性二线治疗+患者(40]。共有347名患者被包括,研究主要目标是积极的,PFS的7.7个月与3.0个月相比,实验臂控制杆(HR 0.49;p < 0.001)。响应率为65%与20% (p < 0.001)。一个临时生存分析所需的241事件(96)没有(20.3演示一种生存优势与分别为22.8个月);然而,这一结果是难以解释的可能接触患者在控制臂crizotinib随访。本研究形成的基础营销批准crizotinib二线设置在欧洲。
在碱性crizotinib的影响+患者一线设置是评估在1014年的第三阶段概要研究[41]。共有343名未经治疗的患者接受要么crizotinib (n = 172)或培美曲塞铂(顺铂75 mg·m−²或卡铂,目标曲线下的面积的5 - 6 mg·毫升−1·分钟每3周,长达6周期;n = 171)。PFS的主要目标是达到了,10.9个月的实验与7.0个月的化疗控制臂(HR 0.45, 95% CI 0.35−0.60;p < 0.0001)。响应率与crizotinib更高(74%与45%;p < 0.0001)。再一次,在总体存活率无显著差异被认为中期分析(HR 0.82, 95% CI 0.54−1.26;p = 0.18),可能由于交叉crizotinib为概要文件提到1007年的研究。这最近的概要1014研究的结果将导致欧洲市场的迅速扩展批准包括一线设置。
Crizotinib要么被规定为一线或二线治疗自2011年以来在美国。在欧洲,并于2012年获得了授权仅供二线治疗(49]。处方是无论检测的方法。几个研究crizotinib正在进行一系列的设置,其中包括早期辅助设置(NCT02201992),结合化疗(NCT02134912与radio-chemotherapy), (NCT01822496)或与其他靶向治疗(补充表S2)。
Ceritinib
crizotinib早期成功后的第二代乙醇已经发展提高的结果,其中一个是ceritinib (LDK378)。我第一阶段临床试验发表的与该代理进行筛选+患者(42]。以前治疗crizotinib是允许的,但在这种情况下需要re-biopsy ceritinib治疗之前,对耐药性的机制的研究。共有59包括患者,推荐剂量确定为750 mg·−1。毒性包括腹泻、呕吐、脱水、hypophosphoraemia和转氨酶海拔,3 - 4级毒性的57% (表2)。
本研究随后扩展到包括crizotinib-naive病人,和结果近日报道50]。在246名患者中学习和接受750毫克·天−1之前收到的crizotinib ceritinib 66。PFS中位数是6.9个月的患者接受了乙醇治疗,而在ALKi-naive病人中位数PFS没有达成,但> 18.4个月。PFS总人口的8.2个月。反应率分别为55%、66%和59%,分别。值得注意的是,毒性导致剂量减少39%的病人,停止在10%。
反应ceritinib观察患者的耐药性突变,包括L1196M看门人突变,以及没有检测到突变的病人。此外,反应也出现在脑转移的患者crizotinib之前收到。ASCEND-1研究,包括124例脑转移(98预处理,26 therapy-naive),总体反应率为54%,平均PFS是6.9个月(50,51]。在这些的基础上初步数据,为碱性ceritinib获得FDA的批准+患者耐药或不能容忍crizotinib [42),和一个特殊的访问计划在其他国家已经批准。
一些正在进行的第二和第三阶段研究正在评估ceritinib在NSCLC筛选的作用+患者在其他设置,包括患者抗crizotinib (ASCEND-5;NCT02040870),作为一线治疗(ASCEND-4;NCT01828099ROS1-mutated患者(中)NCT02186821),结合热休克蛋白(HSP) 90抑制剂(NCT01772797)(补充表S2)。
Alectinib
Alectinib (CH5424802 / RO5424802)是另一个第二代乙醇旨在提高选择性和活动患者L1196M, F1174L或R1275Q突变(52]。结果从第一I / II期研究(japiccti - 101264)是最近出版的43]。这项研究是在碱性的日本人+病人已收到至少一行前化疗和ALKi-naive。患者接受alectinib剂量300毫克每日两次。6周的反应率为87%,其中包括两个完整的46名患者的反应。PFS和整体生存没有报道。主要的毒性是味觉障碍(30%),海拔在天冬氨酸转氨酶(28%)、胆红素(28%)和肌酸酐(26%),以及皮疹(26%)。三年级毒性(37%)包括2%的患者的肝功能异常、中性粒细胞减少和肌酸磷酸激酶海拔4% 4%。虽然没有毒性死亡或4级毒性报道,48%的患者中断治疗由于毒性明显高。
结果与alectinib I / II期研究(NCT01588028)患者接受之前crizotinib最近发表(53]。55%的反应率报告44例可评价的有效性,包括一个完整的响应,23部分反应(14日证实,9个未经证实)和16个稳定的疾病患者。脑转移是在21日报告病人的研究,其中包括12大脑进行性疾病。11这12个病人的反应,包括6个完整的反应脑损伤;四个病人不需要放射治疗,两个其中有一个完整的反应,一个反应部分和一个稳定的疾病。值得注意的是,在21日在诊断脑转移患者,没有经验的中枢神经系统发展。
这一结果与乙醇的二线设置让人想起看到ceritinib。研究病人之前已经收到crizotinib alectinib (NCT01801111)或与crizotinib首次治疗患者(亚历克斯;NCT02075840)目前正在招聘(补充表S2)。
AP26113
AP26113设计作为一个多功能抑制剂阻止碱和表皮生长因子受体,以及克服L1196M T790M电阻突变(54]。的I / II期研究结果最近可用(NCT01449461)[55,56]。推荐剂量为180毫克·天−1。18碱性反应率为67%+患者被报道,包括两个完整的反应,和一个等价的反应率被认为无论之前crizotinib。值得注意的是,四个,五个脑转移患者的反应。副作用包括恶心(33%)、疲劳(22%)、腹泻(20%),7%的3 - 4级的事件。44岁的患者停止治疗由于有毒副作用和两个死亡报道。特定的肺毒性,早期缺氧呼吸困难的外观与双边毛玻璃结节可见扫描,观察并导致的弥漫性间质性肺疾病患者或氧依赖。尽管如此,呼吸道毒性坚持四个(9%)的44个病人治疗。
其他疗法
其他几个乙醇疗法正在开发,包括NMS-E628 (Nerviano医学科学,意大利米兰),x - 396(美国佛罗里达州西棕榈滩,Xcovery), asp - 3026(阿斯特拉制药、东京、日本),cep - 37440(以色列梯瓦制药产业公司,克瓦),pf - 06463922(美国辉瑞、纽约、纽约)和临时避难所- 011 (Tesaro, Inc .,沃尔瑟姆,妈,美国)。
化疗
而存在的碱性易位是一个强有力的预测标记乙醇的反应,这个问题已经提出的预测是否应对其他疗法。一些回顾性研究显示潜在的功效与培美曲塞在碱性的证据+患者(57,58]。只有相对较少的患者(89(19筛选+)病人在一项研究中,95(15筛选+在碱)在另一个病人),PFS+培美曲塞患者结合铂被发现与碱性相比显著提高−患者,持续时间约为9个月。
一个特别引人注目的结果是在一个小组的分析概要1014患者的研究(NCT00932893)。人力资源恶化或死亡的病人接受培美曲塞或多烯紫杉醇与患者相比,二线设置crizotinib 0.59是0.30多烯紫杉醇和培美曲塞反应率为7% (95% CI 2% - -16%)和29%(95%可信区间21% - -39%),分别为。这表明,在多西他赛培美曲塞提供了一个真正的好处。
年代的回顾性研究山楂et al。(59)报道,碱性+病人比碱性反应−患者铂/培美曲塞紧身上衣一线设置;然而,这种优势不再明显从未/轻度吸烟者。铂/培美曲塞作为一线治疗,PFS是8.5个月患者的突变筛选,这是与PFS报道后在控制臂(培美曲塞/铂)1014年的概要文件的研究(41]。在一项研究cagliottiet al。(60的肺腺癌患者培美曲塞/顺铂,PFS是5.3个月,维护与培美曲塞治疗最重要的研究给了PFS的6.9个月(61年]。
培美曲塞的作用机理尚未明确指出,虽然在碱性低thymidylate合成酶的表达+细胞已经唤起了(58),之前建议的一个预测因素响应该代理(60]。虽然碱性的预测作用在培美曲塞尚不清楚,目标人群的特点,低反应速率与多西他赛和趋势报告所有支持政府培美曲塞的筛选+人口。
电阻筛选+非小细胞肺癌患者
而乙醇的使用显然是碱性的治疗管理的基础+肺癌,相关问题出现收购阻力和逃避(62年]。的经验研究表皮生长因子受体TKIs [63年]是无价的,和阻力的研究应该是所有乙醇的早期发展的一个不可或缺的方面。耐药机制并提出治疗方案是下面讨论和总结图1。

抵抗crizotinib机制和潜在的治疗方案。碱性+:肿瘤依赖间变性淋巴瘤激酶(碱性)信号;碱性−:失去依赖筛选途径;天然气:拷贝数增加;HSP90i:热休克蛋白90抑制剂;IGF1R:胰岛素样生长因子1受体;表皮生长因子受体:表皮生长因子受体;TKI:酪氨酸激酶抑制剂。的数据(64年]。
主要的阻力
大约有25%的患者crizotinib目前主要阻力(48),这可能是直接关系到碱性异常的类型。耐药性的存在与否可能是由于碱性的融合蛋白除了EML4或碱性变体的差异,一直在观察一些细胞模型(14]。尽管如此,评价子组的初步研究并没有证实这一假设,虽然病人人数不多(46]。同样重要的是要考虑,在实践中,可能出现假阳性,与技术或解释的困难30.]。值得注意的是,crizotinib反应率从来没有真正与突变细胞的百分比。TKI治疗反应的异质性可能与细胞凋亡的生物学上的差异,特别是与pro-apoptotic BIM蛋白(65年,66年]。
二次电阻
中等抗性机制通常分为两个不同的组:一个肿瘤仍然依赖于筛选信号,和其他碱性独立(64年]。ALK-dependent肿瘤,电阻引起的突变或放大靶向激酶本身,或改变药物的代谢。在ALK-independent肿瘤中,电阻发生通过激活的信号通路。
第一个(最常见)的抗性鉴定机制涉及修改的crizotinib目标(67年),占大约25%的电阻(68年]。这些突变的研究最多的是替换一个亮氨酸蛋氨酸在1196位置(L1196M)在筛选酪氨酸激酶域的等效T790M EGFR突变。这种突变导致构象改变ATP的口袋,防止crizotinib绑定。其他七个突变已确定到目前为止,影响其他地区的激酶,如氨基和C-helix [69年,70年]。碱性放大似乎足以赋予抵抗crizotinib如图所示在体外(71年和在诊所64年),并可能获得抗病性的占15%。情况下的损失碱性融合基因也被描述为一种电阻(64年]。应该注意的是,突变(s)和放大可能发现同时在同一病人(72年]。与此一致的是,几个电阻突变可以开发同样的筛选+病人,如病人进展的报道L1196M和C1156Y同时出现(67年]。
病人总是复发在crizotinib治疗和开发了第二代乙醇来克服这种获得性耐药。Alectinib ceritinib,最好这两个特征代乙醇,可以克服crizotinib阻力在临床前模型(52,70年),取得了可喜的活动在病人进展crizotinib > 50%的反应率(51]。
阻力与克隆的出现的另一个机制替代扩散途径,如表皮生长因子受体的激活(72年- - - - - -74年一半寿命),(75年- - - - - -77年],PI3K AKT mTOR [78年),cKIT放大(72年)或胰岛素样生长因子1受体(IGF1R) [79年]。这种机制占报告病例的大约20%的crizotinib逃脱(80年]。事件的另一个信号通路的激活,联合治疗的乙醇与另一个抑制剂或multi-kinase抑制剂的发展可能是有效的。几项研究结合表皮生长因子受体抑制剂或一半抑制剂耐药患者目前正在进行的(补充表S2)。
如前所述,获得耐乙醇特性之一的可能性的存在这些机制的几个发生在相同的肿瘤病变(64年,72年]。
这些耐药机制的多样性的直接后果是需要启用重复活检在进展。尽管re-biopsying技术上是可行的(81年),鉴于tumoral异质性和风险重复活检的患者往往很脆弱,非侵入性的方法,如使用循环肿瘤细胞的DNA将是一个优势62年,82年]。一些突变异常报告使用这种技术(83年]。由于重新进行活组织切片检查不应影响治疗策略,讨论。就目前而言,这应该是留给耐药机制的探索在临床试验中。
另一个有趣的角度与研究表明,免疫调节和分子信号通路相互作用。各种信号通路的激活增加的表达程序death-ligand 1 (PD-L1),起着关键作用的肿瘤逃避免疫反应(84年]。值得注意的是,这是碱性的情况下所示+t细胞淋巴瘤,PD-L1的表达增加通过STAT3 (85年]。为理解这些交互是至关重要的设想与靶向治疗免疫疗法的结合。
治疗策略
简介1014年的研究后,crizotinib在碱一线治疗被认为是最优的选择+患者的良好的毒性。不过,鉴于进展在这个病人人口系统的治疗,还需要进一步的治疗选项。这就提出了一个问题:是否继续crizotinib后进展(62年]与的第二代TKIs,化疗应该优先考虑。
与肿瘤呈现一种瘾EGFR通路,它可能感兴趣的继续治疗针对碱性尽管固体肿瘤反应评估标准(RECIST)进展,在下列情况下。首先,在发生无症状复发和进展缓慢,进一步密切监视治疗可能是一个选项在忍受治疗的患者,有冲突的风险效应,可能由于快速增长的细胞克隆对乙醇敏感,后停止抑制剂(86年]。其次,对于oligometastatic复发crizotinib可以持续,可以结合当地治疗。例如,脑复发影响三分之一的患者(47)和放射治疗通常是提出(87年),导致长时间反应继续crizotinib [88年]。然而,增加剂量似乎没有临床有效的在这种情况下(89年]。C的研究ostaet al。(90年)可以解释的重要性crizotinib的脑复发,显然低比率的crizotinib脑脊液中浓度与血清表明穷人转移穿过血脑屏障。
这种方法继续crizotinib也可能是有用的extracerebral oligometastatic发展与当地手术或放射治疗的可能性,ALKi-resistant克隆的出现的原因可能是由当地治疗根除(91年]。患者持续TKI政府已成功实现表皮生长因子受体突变(92年]。无法访问本地治疗进行性疾病时,小说乙醇的治疗选择,特别是alectinib [53]和ceritinib [42]。响应率很高(58% alectinib [93年与ceritinib[]和59%42]),和这些代理活动对脑转移。
因此,小说乙醇的作用作为一线治疗,而不是作为一个二线post-crizotinib选项,目前正在评估在第三阶段的研究。在当前的实践中,考虑到在这些二线治疗反应率和缺乏明确的预测指标,对响应,系统re-biopsying目前被认为是必不可少的。在这些治疗的情况下不可用或二线TKI失败时,化疗与培美曲塞/铂紧身上衣是治疗的选择,并可能与贝伐单抗相关。而言,其发展在化疗后,几个病例的灵敏度re-acquisition乙醇作为三线治疗后二线化疗(94年]。图2总结了非小细胞肺癌患者的治疗策略。
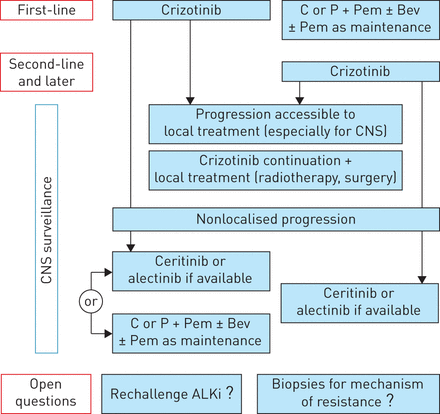
提出了处理算法nonsmall细胞肺癌的治疗与重组的间变性淋巴瘤激酶(碱性),考虑到当地的发展。C:卡铂;P:铂;Pem:培美曲塞;贝芙:贝伐单抗;中枢神经系统:中枢神经系统;乙醇:筛选抑制剂。
结论
现在的诊断和定位ALK-activating突变形式常规治疗肺癌的管理。结果与前乙醇是没有先例的PFS和整体生存。耐药性的机制的理解,以及更具体的目标的筛选突变,引发了有前景的结果对病人进展在乙醇中。几个挑战留在这些肿瘤的管理,包括当前策略的协会与抗血管生成等补充疗法和免疫治疗,希望进一步改善这些患者的结果。
脚注
本系列之前的文章:没有。1:鲍威尔哈,鲍德温胸部肿瘤多学科团队管理博士:不仅仅是一个概念吗?欧元和J2014;43:1776 - 1786。2号:Shlomi D, Ben-Avi R, Balmor GR,et al。肺癌筛查:时间的大规模筛选胸部计算机断层扫描。欧元和J2014;44:217 - 238。3号:De Ruysscher D,中川K,手术和非手术治疗方法Asamura h .小型nonsmall细胞肺癌。欧元和J2014;44:483 - 494。4号:韦德Van Schil PE、Opitz我,W,et al。恶性胸膜间皮瘤的多通道管理:我们今天在哪里?欧元和J2014;44:754 - 764。5号:金正日L,曹女士为肺癌肿瘤组织抽样管理个性化治疗的时代:分子测试足够好是什么?欧元和J2014;44:1011 - 1022。6号:布卢姆T联系n .肺癌病人pneumologist和姑息治疗:发展联盟。欧元和J2015;45:211 - 226。7号:Paesmans M, Grigoriu B, Ocak年代,et al。系统的随机试验进行定性评审nonsmall或等效设计非细胞肺癌。欧元和J2015;45:511 - 524。8号:Grigoriu B, Berghmans T, Meert p。表皮生长因子受体突变nonsmall细胞肺癌病人的管理。欧元和J 2015;45:1132 - 1141。
可以从本文的补充材料www.qdcxjkg.com
利益冲突:披露可以找到与本文的在线版本www.qdcxjkg.com
- 收到了2014年12月26日。
- 接受2015年3月14日。
- 版权©2015人队















