摘要
胆红素是一种强抗氧化剂。血清水平升高与下呼吸道疾病和死亡风险有关。我们在瑞士的成人空气污染与肺部疾病研究(SAPALDIA)队列中研究了胆红素与肺功能的关系。
自然对数胆红素与1秒用力呼气量(FEV)的关系1.)、强迫肺活量(FVC)、FEV1./FVC和平均用力呼气流量在FVC的25%-75%之间(FEF25 - 75%)采用多元线性回归对整个研究人群(n=4195)和长期吸烟和高体重指数(BMI,由最高分布四分位数定义)的人群进行检验。用单核苷酸多态性rs6742078(胆红素的遗传决定因素)重新检测相关性。
高胆红素水平与高FEV显著相关1./ FVC和FEF25 - 75%整体。在分层研究中,吸烟者的FEV增加了1.1% (95% CI 0.1-2.2%)1./FVC和116.2ml·s−1.(95%可信区间-15.9-248.4毫升·秒−1.) FEF25 - 75%高BMI吸烟者胆红素暴露的每四分位范围。在高BMI从不吸烟者中,相关性为正,但不显著。同样,rs6742078基因型TT与FEV增加相关1./ FVC和FEF25 - 75%.
提示胆红素可能对肺组织有保护作用,对预防和治疗具有重要意义。
摘要
在普通人群中,血清胆红素与低级别炎症受试者的肺功能相关http://ow.ly/tD3FP
介绍
胆红素是血红素在体内降解的最终产物,在过去十年中引起了广泛的研究兴趣[1.]在回顾性和前瞻性临床研究中,血清胆红素升高反复与冠状动脉疾病、心肌梗死、外周动脉疾病和中风风险降低相关[2.,3.].血清胆红素升高的有益作用得到了动物和动物的支持在体外显示抗氧化和抗炎特性的实验[4.].
血清胆红素升高对呼吸健康也有有益的影响。在以前的基于人群的研究中,较高的胆红素浓度与较低的肺癌发病率、慢性阻塞性肺病和肺癌死亡率以及身高标准化肺功能相关[5.–7.].这些结果表明,胆红素可能对暴露于外部环境的组织(如肺)有保护作用,可能是通过对抗亚临床炎症。
此外,血清胆红素水平与体重指数(BMI)呈负相关[8.,且随着吸烟时间或强度的增加而降低[9].
血清胆红素的主要遗传决定因素是UDP葡萄糖醛酸转移酶1A1(UGT1A1) [10].这种酶通过葡萄糖醛酸作用降解胆红素,并使胆红素随后排泄到胆汁中。多态性在UGT1A1解释10-30%的血清胆红素变异[1.,11].启动子区域的功能重复多态性是吉尔伯特综合征的基础,该综合征在5-10%的白种人中普遍存在。与每条染色体上有6个胸腺嘧啶二核苷酸(TA)的野生型等位基因相比,7个TA重复的纯合子减少了70%UGT1A1活动[11].一项对胆红素水平的全基因组研究表明,单核苷酸多态性(SNP) rs6742078接近UGT1A1与功能启动子重复多态性处于高度连锁不平衡状态,其T等位基因增加胆红素浓度[10].
8项研究试图证实胆红素和心血管结果之间的因果关系,使用孟德尔随机化,一种工具变量分析方法,其中UGT1A1对变异进行分析,以获得胆红素效应的无偏估计[12–19]最近的一项研究对67068名健康对照者和11686名缺血性心脏病患者进行了研究,结果表明,即使在与早期研究进行荟萃分析后,胆红素的遗传性升高也没有明显的相关性[19].
在呼吸领域没有进行可比的遗传学研究,胆红素在呼吸健康中的潜在作用也几乎没有被评估。因此,我们的目的是在瑞士关于成人空气污染和肺病的研究的普通人群样本中研究胆红素血清水平是否与肺功能相关(SAPALDIA)队列研究。肺功能水平是潜在病理性肺过程(如炎症和组织重塑)的早期临床前标志物。我们先天的检测胆红素和肺功能之间的关系是否因主动吸烟或与超重相关的亚临床炎症引起的易感性增加而改变。为了评估观察到的胆红素关联的因果关系,我们研究了变异rs6742078附近的关联UGT1A1与肺功能有关。
方法
设计和研究人群
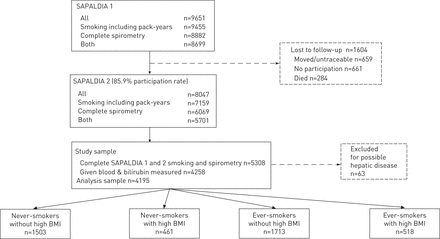
SAPALDIA是一项队列研究,从八个瑞士社区招募18-60岁的成年人。SAPALDIA方法已在前面详细描述[20.].本研究以4195名参加两项检查的参与者为基础,进行了肺功能测试,并提供了有关吸烟暴露和胆红素测量的完整数据(图1).
研究参与者的选择。高体重指数(BMI)定义为在观察到的BMI分布中处于最高的四分之一(BMI≥28.36 kg·m)−2.).萨帕迪亚:瑞士关于成人空气污染与肺部疾病的研究。
获得所有研究参与者的书面知情同意书,该研究得到瑞士医学科学院以及各地区伦理委员会的批准。
健康问卷调查
所有研究参与者都接受了关于吸烟行为、二手烟暴露、职业暴露、先前存在的呼吸、过敏和心血管疾病和症状以及社会经济因素的访谈。
教育包括最高学历,直到随访考试,并分为三类:低(小学),中等(高中)和高(大学或大学学位)教育水平。
从不吸烟者被定义为一生中吸烟量小于20包或360克的人。以前的吸烟者在体检前至少1个月戒烟,而现在的吸烟者在接受采访时报告说正在吸烟。在曾经吸烟者中,包年吸烟量是通过除以每天的香烟数量来计算的到20岁时,每天给香烟盒,这要乘以暴露的年数。
预先存在的心肺疾病被定义为在随访检查前的12个月内自行宣布患有心脏病、肺气肿或慢性支气管炎,或因呼吸问题而使用卫生服务。详细的问题在网上的补充材料中有。
BMI和肺量测定法
参与者不穿鞋子或厚重的衣服来测量体重和身高。BMI的计算方法是体重(公斤)除以身高(米)的平方。
肺功能测试使用Sensormedics型号2200 (Sensormedics devices, Yorba Linda, CA, USA)进行。每天对设备进行校准,并检查设备之间的可比性。根据欧洲共同体呼吸健康调查方案进行测量。参与者以直立姿势坐着,进行3到8次强迫呼气动作。演习必须符合美国胸科协的质量标准[21], 1秒内强迫呼气量(FEV)至少两个可接受值1.)记录用力肺活量(FVC),FEV比值1./FVC是由同一机动测量得出的。平均用力呼气流量为FVC的25-75%25 - 75%)从显示FEV最高总和的曲线中记录1.和FVC。
生物标记物
2002年采集全血样本,使用模块化P自动分析仪(Roche Diagnostics, Rotkreuz, Switzerland)测定血清血液标志物。总胆红素用重氮法测定[22].采用酶促紫外(UV)试验(包括吡哆草酸磷酸酯)测定丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST),并采用光度法测定γ-谷氨酰基转移酶(GGT)。变异系数在1-3%之间。
胆红素值>17 μmol·L−1.谷丙转氨酶(ALT)、谷草转氨酶(AST)、谷草转氨酶(GGT)均达到或超过正常值(50、52、66 U·L)的2倍−1.,分别)由于可能的肝脏疾病而设置为缺失。
在对982名无哮喘个体进行的GABRIEL哮喘全基因组研究中获得了UGT1A1附近rs6742078的基因型数据[23,24]使用标准化问卷,非哮喘被定义为既非自我报告也非医生诊断的哮喘[20.]。基因分型详情可在网上补充资料中查阅。
易感人群的定义
考虑了肺功能的两种易感性情况。第一种包括吸烟。第二种包括BMI高,因为相关的亚临床炎症可能会干扰胆红素的保护作用。由于不同的原因,使用BMI分布的最高四分之一(BMI≥28.36 kg·m)进行统计学定义−2.)作为阈值。首先,与亚临床炎症关系更密切的腰围没有得到;其次,在没有有效的BMI阈值来识别炎症的情况下,按照最高的四分之一进行分类是合理的,因为通常的超重定义是BMI≥25 kg·m−2.我们的老年研究人群中有很大一部分人满足了这一要求(平均BMI为25.7 kg·m)−2.).肥胖(BMI)≥30公斤·米−2.)由于样本量小及其对肺功能的机械影响而未选择。对体重指数进行分类还可以结合吸烟史确定亚组。
我们定义了三组易感人群:BMI高的从不吸烟者、不吸烟的吸烟者和BMI高的吸烟者。BMI不高的从不吸烟的人作为参照组。
统计分析
将整个研究人群及易感人群的性别、年龄、文化程度、吸烟状况、吸烟包年、身高、体重、BMI、FEV等分布情况制成表格1.FVC, FEV1./ FVC, FEF25 - 75%,既往心肺疾病,胆红素,C反应蛋白水平和基因型UGT1A1SNP rs6742078。为了解释性别和年龄分布的差异,通过对数胆红素对性别、年龄和成员的多元线性回归模型预测值,计算了每组校正后的胆红素平均浓度和标准误差。对预测结果进行幂运算,得出单位为μmol·L−1..
胆红素值使用自然对数转换,以实现更对称的分布。对数转化胆红素值与FEV之间的横截面关联1.FVC, FEV1./ FVC和FEF25 - 75%从2002年开始,采用多元线性回归逐步调整性别、年龄、身高和体重,然后是教育水平和研究区域,最后是吸烟状况和包年。为了检验相互作用,我们将编码易感性组成员和对数胆红素乘法项的虚拟变量纳入模型。然后根据易感性分组进行分析。BMI不高且从不吸烟的参与者作为参照组。
作为敏感性分析,将胆红素水平升高(但肝酶正常)的参与者排除在外,以评估观察到的相关性是否在血清胆红素正常范围内持续存在。排除服用哮喘药物的参与者(定义为对“你目前是否服用任何治疗哮喘的药物,包括吸入器、气雾剂或药片?”这一问题的肯定回答)后,分析也重复进行。最后,根据心肺疾病的存在对分析进行分层,以评估现有病理在研究中的关联作用。相互作用用乘法相互作用项进行类似测试。
孟德尔随机分析是基于减数分裂期间,遗传位点的等位基因会随机传递给下一代的想法。如果基因位点高度影响生物标志物的水平,这个自然随机实验可以推断生物标志物效应的因果关系[25].因此,采用Wilcoxon秩和检验rs6742078基因型与血清胆红素的相关性。rs6742078基因型与肺功能之间的相关性在回归模型中进行检验,回归模型的协变量与血清胆红素分析相同。隐性模型分析(等位基因TT对抗GG/GT),以对应的功能影响UGT1A1启动子(助教)7.纯合性(3.].鉴于样本量小(n=982),没有进行分层分析。
所有分析使用STATA 10.1版本(StataCorp, College Station, TX, USA)进行。使用“调整”后回归估计命令预测调整后的平均胆红素浓度和标准误差。选择双侧α-值分别为0.05和0.1作为主效应和交互作用的显著性阈值。
结果
研究人群的特征
我们的研究共有4195名受试者,其中1503名从不吸烟,461名体重指数高,1713名从不吸烟,518名体重指数高。总体而言,53.2%为女性,22.1%为当前吸烟者,31.0%为前吸烟者(表1).平均年龄为51.9岁,平均FEV1., FVC和FEF25 - 75%分别为3.2 L、4.2 L和2.6 L·s−1.曾经吸烟者的中位烟草烟雾暴露量为17.0包年(四分位间距6-35)。所有参与者的中位血清胆红素为7μmol·L−1.(四分位范围5-10 μmol·L−1.).通过易感组,FEV1./ FVC和FEF25 - 75%随着高BMI和吸烟暴露而降低。高BMI组年龄较大,受教育程度较低,而吸烟组中男性较多。各组之间的胆红素血清值明显具有可比性,但在调整性别和年龄分布差异后,浓度逐渐从7.84μmol·L降至6.77μmol·L−1.BMI和吸烟暴露增加(在线补充表S1)。
胆红素与肺功能值的关系
在基本分析模型中,调整性别、年龄、身高和体重,FEV1., FEV1./ FVC和FEF25 - 75%与血清胆红素(表2).胆红素增加一个log单位,对应于2.72倍的血清浓度增加,与以下增加相关(β估计(95%置信区间)):FEV1.36.4毫升(6.7 - -66.1);FEV1./ FVC 0.9 (0.5 - -1.4) %;和FEF25 - 75%115.2(58.5 - -172.0)毫升·s−1..调整烟草烟雾暴露后,效应估计值降低,这也导致FEV失去了统计意义1.协会。相比之下,FEV1./ FVC和FEF25 - 75%相关性仍然显著,估计增加0.5(0.1-1.0)%和66.9(11.4-122.5)mL·s−1.每对数单位胆红素。这相当于FEV增加0.3(0.1–0.7)%1./FVC和46.4(7.9-84.9)mL·s−1.在FEF25 - 75%在观察到的四分位接触范围内(5–10μmol·L−1.胆红素、即浓度增加一倍)。
用于钒铁1./FVC、对数胆红素与有或无高BMI的吸烟者之间的相互作用具有统计学意义(p交互0.007-0.023,数据未显示)。相互作用在FEF上也很显著25 - 75%(p交互0.012-0.086),但包年调整后除外(p交互0.111 - -0.163)。根据易感性分组对分析进行分层,证实了相互作用(表3):没有高BMI的从不吸烟者没有显著的相关性。在高BMI的从不吸烟者中,FEV的β估计值较高,但观察到无显著性差异1., FEV1./ FVC和FEF25 - 75%.对数胆红素与FEV的关系1., FEV1./ FVC和FEF25 - 75%在没有高BMI的吸烟者中有显著性差异。他们不能承受FEV的包年调整1.和钒铁1./每对数单位胆红素的FVC(分别为21.7(-23.6–67.0)mL和0.6(-0.1–1.2)%增加,但仅FEF增加25 - 75%(88.7(3.6-173.8)毫升·秒−1.).β估值最大的是在所有FEV中BMI高的吸烟者1./ FVC和FEF25 - 75%模型。经过包年调整后,每log单位胆红素与1.6(0.1-3.2)%的FEV显著相关1./FVC,与167.6 (-23.0-358.3)mL·s相关−1.高铁25 - 75%.在观察到的胆红素四分位范围内,这对应于1.1(0.1–2.2)%FEV的增加1./FVC和116.2(-15.9-248.4)mL·s−1.FEF25 - 75%.
敏感性分析
排除胆红素水平高于正常范围的参与者或受哮喘药物影响的参与者对关联模式没有实质影响(图2).在患有和不患有心肺疾病的人群中观察到显著的相关性(在线补充表S2)。用于钒铁1./FVC,在患病组中,教育和吸烟调整模型的估计显著更高(p交互分别为0.086和0069;未显示数据)。
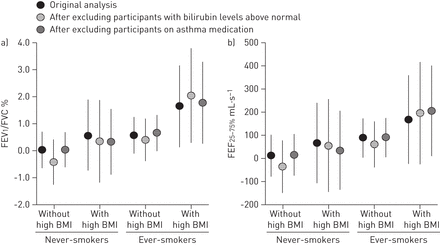
胆红素与1秒用力呼气量(FEV)相关性的敏感性分析1.)/用力肺活量(FVC)和b) 25-75%用力呼气流量(FEF)25 - 75%).估计显示胆红素每对数单位的增加。模型根据性别、年龄、身高、体重、教育程度、学习区域进行了调整,在经常吸烟的人群中,另外还根据烟龄进行了调整。BMI:身体质量指数。
rs6742078 t等位基因与血清胆红素和肺功能值的关联
血清胆红素值根据rs6742078 t等位基因数量有显著差异(在线补充表S3)。中位浓度分别为6和7 μmol·L−1.对于gentoypes GG和GT,与13μ摩尔·L−1.(Wilcoxon秩和检验的p值<0.001)。
rs6742078 t等位基因纯合子携带者的FEV水平显著升高1./ FVC和FEF25 - 75%在逐步调整的线性回归模型(表4),导致FEV升高1.7 (0.4-3.0)%1./FVC和192.5 (30.8-354.2)mL·s−1.高铁25 - 75%比GT/GG承运人在包装年调整后。FEV未观察到显著相关1.和FVC。
讨论
在以人群为基础的SAPALDIA研究中,我们发现血清胆红素水平与肺功能参数FEV之间存在显著正相关1./ FVC和FEF25 - 75%在调整了性别、年龄、教育程度、身高和体重以及吸烟暴露的影响后。当根据易感性增加的状态对研究人群进行分层时,相关性仅在BMI高的参与者中持续存在,而在经常吸烟的人群中,相关性增加且显著。我们的结果对敏感性分析是可靠的,并且观察到遗传胆红素升高的一致性关联(由于rs6742078)。
这些发现与先前的流行病学证据一致,这些证据表明血清胆红素升高对呼吸系统预后有有益影响[5.–7.].这些发现表明对肺功能有有益的影响,但将其范围细化到亚临床炎症和氧化应激暴露(或心肺疾病)患者。与FEF显著相关25 - 75%和钒铁1./FVC可能与小气道梗阻呈反比关系。由于小气道表面积大,是慢性呼吸系统疾病发展的重要隔室[26,27],其中亚临床变化通常首先表现出来,因此,在我们的一般人群样本中,该位点呈现出最强的相关性。吸烟调整显著降低了相关性估计值,这是由于其与肺功能和血清胆红素的已知负相关,从而导致了对胆红素肺功能相关性。
目前我们只能推测血清胆红素可能影响肺功能的机制。细胞内机制在肺中可能比已知的血清和血管中的作用更重要,因为胆红素在生理pH值下穿透细胞壁[28]除了清除氧化剂外,胆红素还抑制膜结合烟酰胺腺嘌呤二核苷酸磷酸氧化酶,这是细胞内活性氧的主要来源之一[29].此外,胆红素输注已被证明可下调小鼠肺损伤模型的炎症反应[30.].
由于横断面设计,观察到的关联不能清楚地解释结果和暴露的时间关系:这些发现可能来自于血清胆红素升高的保护作用,防止炎症和氧化应激反应造成的组织损伤,或者胆红素水平可能代表个体氧化应激负担和随后胆红素消耗的反应标志物。我们的研究结果显示了不同原因的因果关系。首先,观察到的血清胆红素水平和肺功能之间的关联在血清胆红素基因升高的参与者中得到了一致的复制。其次,随着亚临床炎症和氧化应激状态的增加,相关性增强(即体重指数高、经常吸烟或两者都有),甚至在心肺疾病患者中持续存在。这可能不是反应性生物标志物的情况。最后,我们在正常的血清胆红素范围内观察到类似但较弱的相关性。
除了横断面设计外,我们的研究几乎没有限制。基因分型数据仅在部分人群中可用。我们的数据可能会受到测量误差的影响,肺功能只测试了两次,但由此产生的错误分类是随机的,主要影响研究能力。相比之下,我们的研究有几个优点。以人群为基础的设计允许调查肺功能作为疾病过程的临床前标志物。大量的研究样本和血液标记物、体型和生活方式因素的详细数据使得分析能够分层研究炎症和氧化应激亚临床条件之间的关系。这为胆红素可能的健康相关影响提供了新的见解。我们的大样本研究也意味着可以进行不同的敏感性分析。最后,我们的研究得益于标准化的肺测量方案和严格的质量控制标准。
总之,我们发现炎症和氧化应激增加的患者血清胆红素水平与肺功能显著正相关。从公共卫生的角度来看,重要的是要通过包括遗传信息的前瞻性研究来阐明观察到的关系是否是因果关系鉴于西方人群吸烟的普遍性和高BMI,d具有很大的预防和治疗潜力。
致谢
研究指导委员会如下:T. Rochat(肺气学;大学医院,日内瓦,拥抱,日内瓦,瑞士),新墨西哥州。流行病学/遗传和分子生物学;瑞士热带和公共卫生研究所巴塞尔,瑞士stph,瑞士日内瓦),JM。Gaspoz(心脏病;N. Künzli(流行病学/暴露;和C. Schindler(统计;SwissTPH)。
科研团队如下:J.C. Barthélémy(心脏科;Université Jean Monnet,圣艾蒂安,法国),W. Berger(遗传与分子生物学;Universität Zürich,苏黎世,瑞士),R. Bettschart(肺病;Hirslanden Klinik, Aarau,瑞士),A. Bircher(过敏学;Universitätsspital,巴塞尔,瑞士),O. Brändli(肺炎学;Schweizerische Lungenstiftung,瓦尔德,瑞士),C. Brombach(营养学;Zürcher Hochschule für Angewandte Wissenschaften,苏黎世),M. Brutsche(肺病;瑞士圣加伦Kantonsspital St. Gallen;Hôpital intertonal de la Broye, Payerne,瑞士),M. Frey(肺气学;Klinik Barmelweid, Barmelweid,瑞士),弗雷大学(儿科; Universitäts-Kinderspital beider Basel, Basel), M.W. Gerbase (pneumology; HUG), D. Gold (epidemiology/cardiology/pneumology; Harvard School of Public Health, Boston, MA, USA), E. de Groot (cardiology; Academic Medical Center, Amsterdam, the Netherlands), W. Karrer (pneumology; Luzerner Höhenklinik Montana, Crans-Montana, Switzerland), R. Keller (pneumology; Klinik Barmelweid, Barmelweid), B. Martin (physical activity; Universität Zürich, Zurich), D. Miedinger (occupational health; Schweizerische Unfallversicherungsanstalt SUVA, Luzern), U. Neu (exposure; ProClim, Bern, Switzerland), L. Nicod (pneumology; Centre Hospitalier Universitaire Vaudois, Lausanne, Switzerland), M. Pons (pneumology; Ospedale Regionale di Lugano, Lugano, Switzerland), F. Roche (cardiology; Université Jean Monnet, St. Etienne, France), T. Rothe (pneumology; Zürcher Höhenklinik Davos, Davos Clavadel, Switzerland), E. Russi (pneumology; Universitätsspital Zürich, Zurich), P. Schmid-Grendelmeyer (allergology; Universitätsspital Zürich, Zurich), A. Schmidt-Trucksäss (physical activity; Universität Basel, Basel), A. Turk (pneumology; Zürcher Höhenklinik Wald, Faltigberg-Wald, Switzerland), J. Schwartz (epidemiology; Harvard School of Public Health, Boston), D. Stolz (pneumology; Universitätsspital Basel, Basel), P. Straehl (exposure; Bundesamt für Umwelt BAFU, Bern), J.M. Tschopp (pneumology; Centre Hospitalier du Centre du Valais, Crans-Montana), A. von Eckardstein (clinical chemistry; Universitätsspital Zürich, Zurich) and E. Zemp Stutz (epidemiology; SwissTPH).
协调中心的科学小组如下:M. Adam(流行病学/遗传和分子生物学;E. Boes(遗传和分子生物学;SwissTPH),阿宝。Bridevaux(肺病学;D.卡瓦略(心脏病学;E. Corradi(流行病学;I. Curjuric(流行病学;J. Dratva(流行病学;a.di Pasquale(统计学;E. Dupuis Lozeron(统计学; HUG), M. Germond (statistics; HUG), L. Grize (statistics; SwissTPH), D. Keidel (statistics; SwissTPH), S. Kriemler (physical activity; SwissTPH), A. Kumar (genetic and molecular biology; SwissTPH), M. Imboden (genetic and molecular biology; SwissTPH), N. Maire (statistics; SwissTPH), A. Mehta (epidemiology; SwissTPH), H. Phuleria (exposure; SwissTPH), E. Schaffner (statistics; SwissTPH), GA. Thun (genetic and molecular biology; SwissTPH), A. Ineichen (exposure; SwissTPH), M. Ragettli (epidemiology; SwissTPH), M. Ritter (exposure; SwissTPH), T. Schikowski (epidemiology; SwissTPH), M. Tarantino (statistics; SwissTPH), M. Tsai (epidemiology; SwissTPH) and M. Wanner (physical activity; SwissTPH).
如果没有研究参与者、技术和行政支持以及当地研究地点的医疗队和现场工作人员的帮助,这项研究是不可能完成的。
当地田野工作人员如下。阿劳研究中心:S. Brun, G. Giger, M. Sperisen和M. Stahel;巴塞尔研究中心:C. Bürli, C. Dahler, N. Oertli, I. Harreh, F. Karrer, G. Novicic和N. Wyttenbacher。达沃斯研究中心:A. Saner, P. Senn和R. Winzeler。日内瓦研究中心:F. Bonfils, B. Blicharz, C. Landolt和J. Rochat。卢加诺研究中心:S. Boccia, E. Gehrig, M.T. Mandia, G. Solari和B. Viscardi。蒙大拿州研究中心:A.P. Bieri, C. Darioly和M. Maire。Payerne: F. Ding, P. Danieli and A. Vonnez。Wald: D. Bodmer, E. Hochstrasser, R. Kunz, C. Meier, J. Rakic, U. Schafroth和A. Walder。
行政人员分别为:C. Gabriel (HUG)和R. Gutknecht (SwissTPH)。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明:瑞士国家科学基金(批准号:33cco -108796, 3247BO-104283, 3247BO-104288, 3247BO-104284, 3247-065896, 3100-059302, 3200-052720, 3200-042532, 4026-028099)、联邦森林、环境与景观办公室、联邦公共卫生办公室、联邦道路与交通办公室,阿尔高、巴塞尔施塔特、巴塞尔地、日内瓦、卢塞恩、提契诺、瓦莱士和苏黎世州政府、瑞士肺脏联盟、巴塞尔施塔特/巴塞尔Landschaft、日内瓦、提契诺、瓦莱士和苏黎世肺脏联盟、SUVA、Freiwillige Akademische Gesellschaft、瑞银财富基金会、Talecris生物治疗公司、雅培诊断公司、欧洲委员会018996 (GABRIEL),惠康信托WT 084703MA。
利益冲突:可以在本文的在线版本旁找到披露www.www.qdcxjkg.com
- 收到2013年3月28日。
- 认可的2013年10月6日。
- ©ERS 2014