致编辑:
肺动脉高压(PH)是一种疾病,其特征是肺血管的进行性重塑,最终导致右心衰竭。各种动物模型被用来模拟这种疾病,包括猪、狗、大鼠和小鼠[1.].最常用的模型是野百合碱(MCT)大鼠模型。在该模型中,MCT被皮下注射,并通过肝细胞色素P450 3A作为吡咯里西啶生物碱被代谢激活[2.,3.].活性MCT吡咯具有肺毒性,可损伤肺动脉内皮细胞(PAECs),导致屏障功能紊乱[4.].mct诱导的肺血管重塑的其他特征是轴动脉内侧增生、间质水肿、外膜炎症、出血,最终纤维化[1.,2.,5.,6.].结果,肺血管阻力(PVR)增加,右心室通过肥厚代偿,最终衰竭[7.,8.].
除MCT PH大鼠模型外,采用慢性缺氧伴或不伴Sugen 5416及肺动脉带束法对实验PH进行研究[1.]选择的肺动脉高压动物模型主要取决于需要回答的研究问题。理想情况下,动物模型将再现进行性和不可逆的肺血管重建,这是人类肺动脉高压的标志[1.,4.,9]然而,没有一种动物模型符合这一标准。人们对MCT大鼠模型提出了担忧,因为许多疗法在MCT大鼠身上取得了成功,但在患有PH的人类身上却没有[4.].
因此,我们研究了mct诱导大鼠PH在12周内的长期进展和可逆性,剂量为40 mg·kg−1.在一项随机安慰剂对照研究设计中。由于已知高剂量MCT(60或80 mg·kg−1.)在3-6周内是致命的,研究MCT长期影响的唯一可能方法是使用较低剂量[7.,8.,10,11].在使用MCT或生理盐水后4、8和12周测量肺和心脏的变化。
我们随机分配22只雄性Wistar大鼠(荷兰霍斯特哈兰实验室)皮下注射40 mg·kg−1.当大鼠体重为175–200 g时,给予MCT或生理盐水。在4周(n=3个对照组,n=5个MCT)、8周(n=3个对照组,n=4个MCT)或12周(n=3个对照组,n=4个MCT)处死大鼠.在MCT注射后3周进行超声心动图检查,以确定基线血流动力学,并在处死当天进行。处死前,所有动物均接受右心导管插入术,以构建右心室压力-容积环。采集内脏器官进行组织学检查。所有方法均已在之前详细说明y[12].数据以平均值±表示sd.这项研究得到了当地动物伦理委员会的批准。
基线超声心动图显示,MCT注射后3周,所有MCT大鼠的PVR指数均高于对照组(三组均值:4.33±2.58 mmHg·mL)−1.·敏−1.·镁−1.对对照组:0.50±0.13 mmHg·mL−1.·敏−1.·镁−1.p<0.001),心脏指数降低(0.14±0.06)对0.29±0.04毫升·分钟−1.·g−1.;p<0.001)和下三尖瓣环平面收缩偏移(TAPSE)(2.3±0.5)对3.6±0.3毫米;p < 0.001)。4周时处死的MCT大鼠体重(311±21 g)明显低于对照组(354±6 g;p < 0.05)。8周和12周后MCT大鼠的体重(分别为405±27和455±27 g)与年龄匹配对照组(分别为408±36和496±46 g)相似。
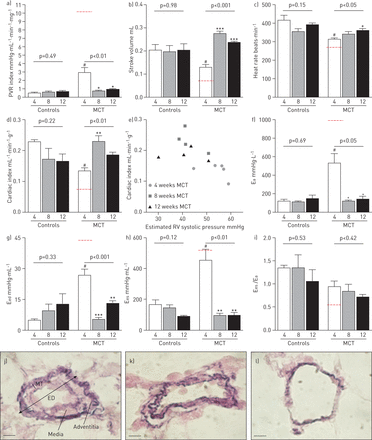
我们观察到在4周时处死的MCT大鼠的PVR指数明显高于对照组(图1一个)右心室收缩压升高(57.8±10.3对15.6±2.3毫米汞柱;p < 0.05)。虽然每搏量和心率降低,但心脏指数相对保持(图1罪犯).然而,在所有MCT大鼠中,心脏指数与估计的右心室收缩压呈负相关(r = -0.65;p = 0.02,图1 e),而对照组大鼠则没有(r = 0.30;P = 0.46,数据未显示)。与对照组相比,TAPSE降低(2.0±0.6),右心室功能下降对3.7±0.3毫米;P <0.05),有增加右心室壁厚度的趋势(1.4±0.2)对1.0±0.1毫米;P = 0.07),右心室舒张末期内径增大(6.2±1.3)对3.5±0.5mm;p<0.05)。与这些发现一致,有创血流动力学测量显示右心室后负荷较高(EA.),增加右心室舒张刚度(E预计起飞时间右心室收缩弹性增加(E锿,一种测量收缩力的方法),与年龄匹配的对照组(图1 f-h).因为EA.和E锿心室-动脉耦合,以E锿/ EA.比率,在所有动物(图1我).有趣的是,上述所有参数均在MCT注射后8周和12周恢复正常(图1 -ⅰ).
超声心动图、有创血流动力学和组织学测量。数据表示为平均值±扫描电镜.a)肺血管阻力(PVR), b)每搏量,c)心率,d)心脏指数,e)心脏指数对估计右心室收缩压(eRVSP), f)动脉弹性(EA.)(右心室后负荷),g)舒张末期弹性(E预计起飞时间)(右心室舒张硬度),h)收缩末期弹性(E锿)(右心室收缩性),i)右心室-动脉耦合(E锿/ EA.在a–i)中,红色虚线表示注射60 mg·kg后4周的数值−1.野百合碱(MCT),数据来自DEM一等[12].三个对照组和mct组使用Bonferroni单因素方差分析相互比较事后在图上给出了检验和p值。*: p < 0.05;* *: p < 0.01;***:与4周时处死的MCT大鼠相比,p<0.001。#: MCT大鼠与年龄匹配对照Mann-Whitney检验值比较p<0.05。j) 4、k) 8和l) 12周MCT后大鼠肺小动脉的组织学变化。用Elastica von Gieson方法对肺小动脉进行染色,以显示4周时动物的中膜肥厚。此外,与对照组和8周和12周处死的MCT大鼠相比,外膜层增厚。介质厚度测量为:(2×media厚度(MT)/外径(ED))×100%。
尸检时也发现MCT 4周后右心室适应高后负荷的迹象,因为与对照组相比心脏重量增加(1.54±0.02)对1.27±0.08克;p<0.05)。这主要是由于右心室/左心室+间隔重量比值高(0.63±0.11)表明右心室重量增加所致对0.28±0.06控制;p < 0.05)。4周时处死的MCT大鼠肺重量较大(1.73±0.06)对1.36±0.19g;p<0.05),但与对照组相比,肝脏重量减少(11.8±0.4)对14.8±1.1克;p < 0.05)。8周和12周处死的MCT大鼠与4周处死的MCT大鼠相比,右心室/左心室+室间隔重量比降低,但未完全恢复正常(8周:0.37±0.03,12周:0.40±0.07,p均<0.01)对4周MCT)。此外,8周处死的MCT大鼠的肺湿重降至1.74±0.17 g,12周处死的MCT大鼠的肺湿重降至1.59±0.10 g。在第8周和第12周处死的MCT大鼠中,肝脏重量增加至对照值(分别为14.0±0.67和15.2±1.4 g)。
肺组织学显示,MCT 4周后,最小微动脉(<40 μm)中膜肌肉化增加(32±4%;p < 0.01对对照组)在给予MCT后8周(25±6%)和12周(21±7%;p<0.05)恢复到对照值(24±1%)对4周MCT) (图1 j-l).第4周处死的MCT大鼠右心室心肌细胞截面积显著增加(388±91 μm)2.),对照组为258±44 μm2.;p<0.001),并在第8周和第12周保持在该水平(344±76μm)2.和358±57μm2.分别)。尽管MCT大鼠右心室心肌细胞较大,但所有MCT组毛细血管数量相似(平均1.2±0.5毛细血管/心肌细胞)。MCT动物和对照组右心室纤维化在所有时间点相似(0.6±0.3)对0.6±0.4%的胶原蛋白;p = 0.88)。此外,以单位面积CD45阳性白细胞数量表达的右心室炎症在所有MCT动物中相似(平均25.8±15.4 CD45)+核·毫米−2.),与对照组相似(平均19.5±15.8 CD45)+核·毫米−2.;P = 0.17),提示右心室有补偿而非衰竭。
有些人认为MCT模型是一种毒性模型,有人认为MCT大鼠死于肝静脉闭塞性疾病伴肝衰竭,而不是右心室衰竭[13].在本研究中,与对照组相比,4周时处死的MCT大鼠肝脏重量较低。然而,这些大鼠右心室收缩压和PVR大幅升高,肺小动脉肌化增加,不能单独用肝损伤来解释。
最后,我们证明了40 mg·kg−1.MCT在给药4周后引起肺小动脉急性肌化,并发高PVR和右心室肥厚。然而,在MCT给药8和12周后,肺小动脉异常恢复,右心室功能恢复正常,尽管心肌细胞肥厚得以维持。这表明,MCT诱导的PH在4周后是可逆的,不像人类PH的进行性。因此,该模型不适合低剂量MCT 4周后的治疗研究。
脚注
利益冲突:未声明任何利益冲突。
- 收到了2013年1月21日。
- 认可的2013年3月24日。
- ©2013人队