摘要
磺胺甲恶唑(磺胺甲恶唑)和甲氧苄氨嘧啶(甲氧苄氨嘧啶)的组合在体外活动对结核分枝杆菌.然而,到目前为止,尚缺乏SXT在耐多药结核病(MDR)中的药代动力学和药效学参数。因此,我们评估了其药代动力学和药物敏感性,以及治疗期间的耐受性。
根据药物敏感性测试,耐多药结核病患者接受了SXT作为其耐多药治疗的一部分。研究了磺胺甲恶唑的药代动力学参数结核分枝杆菌,进行评估。曲线下面积从0到24 h的比值(AUC0-24以最小抑菌浓度(MIC)为最佳药代动力学/药效学参数,预测磺胺甲恶唑的疗效。同时评估了SXT的不良反应。
10例耐多药结核病患者(其中1例患有广泛耐药结核病)接受了480 mg的SXT,中位剂量为6.5 mg·kg−1(范围6.1-6.8 mg·kg−1)每日一次,平均治疗期为381天(范围129-465天)。在两名患者中,剂量增加到960毫克。免费AUC0-24仅有1例患者磺胺甲恶唑MIC超过25。除了一名患者在接受960 mg SXT后出现胃肠道副作用外,SXT是安全且耐受性良好的。需要进一步的研究来找到药代动力学和药效学靶点,从而确定用于耐多药结核病治疗的SXT的最佳剂量。
简介
世界许多地区正在出现耐多药结核病和广泛耐药结核病[1].此外,易感性结核分枝杆菌对当前抗结核药物的使用减少,因此,耐多药结核的治疗变得越来越复杂[2].因此,迫切需要新的有效且毒性最小的药物。像复方新诺明(SXT)这样一种旧的、便宜的、耐受性好的药物,它被注册用于除结核病以外的其他适应症,可能成为治疗MDR- TB和XDR-TB的一种新的有效药物。3.].
SXT是甲氧苄啶(TMP)和磺胺甲恶唑(SMX)以1:5的比例组合。它是一种有效的抗菌药物,可以对抗引起人类感染的各种病原体。SXT目前用于治疗尿路感染、中耳炎、志贺氏菌病、慢性支气管炎和卡氏肺孢子虫肺炎(4].
SXT表现为浓度无关或时间依赖杀伤。因此,0 ~ 24 h自由浓度-时间曲线下面积之比(auc0-24)相对于最低抑菌浓度(MIC)被认为是预测SXT疗效的重要药代动力学/药效学参数[5].关于SXT的药效学知之甚少[5].关于SXT药代动力学参数的出版物很少,没有一篇包括结核病患者(表1) [6- - - - - -9].只有两项研究调查了在体外SXT对的敏感性结核分枝杆菌并显示出有希望的结果[3.,10].从这些研究可以得出结论,只有SMX是有效的结核分枝杆菌,而TMP不是[3.,10,11].在一项研究中,一个SXT AUC0-24> /MIC比值25是有效治疗类鼻疽的必要条件伯克举办[12].数据的缺乏可能是由于SXT是一种古老的药物在体外在感染模型中评估药代动力学和药效学参数是相当新的。
总的来说,SXT是一种安全且耐受性良好的药物。胃肠道并发症,包括恶心、呕吐、厌食和腹泻,是SMX最常见的不良反应[13,14].肾脏副作用,包括高钾血症、血清肌酐水平轻微升高和低钠血症,尤其是肾功能不全的患者[14- - - - - -16].报告的其他副作用是血液学方面的副作用,如已患有巨幼细胞贫血或叶酸储备不足(酗酒者、营养不良患者和孕妇)的巨幼细胞贫血、白细胞减少、血小板减少和再生障碍性贫血等[17].
尽管已对结核病患者使用了SXT,但数据非常稀缺,其在结核病治疗中的作用仍不清楚。本研究的目的是评估SXT在耐多药结核病患者中的药代动力学、药效学和药代动力学/药效学参数以及安全性/耐受性
方法
病人
2006年1月1日至2012年7月1日期间转诊到格罗宁根大学医学中心(荷兰格罗宁根)结核病中心Beatrixoord的耐多药结核病患者,并对其进行了SXT药敏试验,有资格进行评估。年龄、性别、体重、种族、潜在疾病、MIC结核分枝杆菌记录了接受SXT的耐多药结核病患者的隔离、结核的定位、其他抗结核药物、SXT治疗的持续时间和抗结核方案的总给药情况。患者接受常规医疗护理,没有特定的研究相关干预。我们描述了在常规护理期间获得的患者数据,因此,根据荷兰法律,不需要伦理许可。
药代动力学和药效学
血液样本仅在稳定状态下进行评估,即给予SXT≥3天后[18].分别于给药前和给药后1、2、3、4、8 h收集。
在格罗宁根大学医学中心医院和临床药学系的临床毒理学和药物分析实验室,通过有效的液相色谱-串联质谱法分析了人类血浆样本中SMX的浓度。简单地说,每个血浆样品5 μL与750 μL沉淀试剂(甲醇和乙腈4:21体积/体积)混合。5 μL从透明上层注入50×2.1 mm反相C18, 5 μm分析柱(hypsecurity Aquastar;Interscience, Breda,荷兰)用于色谱分离。检测器在电喷雾正电离模式下操作,并将选定的反应监测作为扫描模式。的转变米/z在扫描宽度为0.5的情况下,测量了SMX的254.1-155.9(碰撞能量25ev)米/z.不同浓度的加样回收率为97.7% ~ 102.9%。SMX的准确度在97.7%至102.9%之间,取决于浓度水平。在5 ~ 100 mg·L范围内,分析内和分析间变异系数均<5.1%−1.定量下限为5 mg·L−1.
SMX的药代动力学参数,包括AUC0-24,分布体积(VD)、清除率(Cl)及半衰期(t½)使用MW/Pharm 3.60 (Mediware, Groningen,荷兰)的KINFIT模块,采用标准的非区室药代动力学方法进行测定。的AUC0-24在等离子体中按对数线性梯形规则计算。在这种情况下,口服给药后24小时SMX的浓度估计等于0小时时(给药前)的浓度。
抗菌药物的游离非蛋白结合部分是这些药物临床疗效的主要原因[19].免费AUC0-24(ƒAUC0-24)值通过乘以总AUC来估计0-24值由0.23的未绑定分数计算,该分数从早期的研究中检索[19].免费药AUC0-24/MIC比值通过划分auc来计算0-24为SMX的MIC值。
采用迭代两阶段贝叶斯程序(MW/Pharm 3.60),从先前研究的药代动力学估计开始,开发了SMX的单区室药代动力学种群模型(popp - pk),具有无滞后时间的一级吸收[9].使用KINFIT计算每个患者的个体药代动力学参数。KINPOP基于SMX的个体浓度和患者的体重、年龄、性别和肌酐清除率等特征,计算出耐多药结核病患者的参数[20.].
为了确定MIC值,结核分枝杆菌分离株在荷兰国家分枝杆菌参考实验室(荷兰比尔托芬国家公共卫生与环境研究所(RIVM))采用Middlebrook 7H10琼脂(Becton Dickinson and Company, Sparks, MD, USA)稀释法进行药敏试验[21].根据欧洲抗菌药物敏感性测试委员会指南,SXT的MIC以1:19的比例表示为TMP:SMX。
安全
通过使用来自结核病中心Beatrixoord的标准化数据抽象表,回顾性评估了SXT报告的副作用,评估了SXT在结核病治疗期间的安全性。特别注意了SXT可能引起的副作用,如胃肠道副作用(恶心、呕吐和腹泻)、肝毒性和贫血以及血细胞计数异常[22].
肝损伤定义为在用SXT治疗期间,其中一种肝酶升高至正常上限的5倍(3级常见毒性标准)。这些酶包括天门冬氨酸氨基转移酶(ASAT) (>200 U·L−1),丙氨酸转氨酶(ALAT) (>225 U·L−1)和γ-谷氨酰转肽酶(> 200-275 U·L−1) [23].对于其他副作用,定义的正常值为:贫血(血红蛋白正常范围为7.5-9.9 mmol·L−1(女性)8.7 ~ 10.6 mmol·L−1(男性)),白细胞计数(4×109·L−1)和血小板计数(150-350×109·L−1).对于多药治疗方案患者(如耐多药结核病患者)的药物不良反应(adr),需要一个标准的因果关系评估工具(Naranjo算法)[24].使用该工具,SXT引起adr的可能性评分为:≥9确定,5-8可能,1-4可能,≤0怀疑。
统计分析
当数据非正态分布时,采用Wilcoxon符号秩检验进行统计分析。通过建立基于n-1的POP-PK模型和预测AUC,交叉验证了POP-PK模型0-24在模型开发过程中遗漏的主题。预测AUC之间的相关性0-24基于POP-PK模型和计算出的AUC0-24采用Bland-Altman分析进行检验。
结果
病人
对17例耐多药结核病患者进行了SXT药敏试验。由于药物敏感性试验显示分离株对SXT敏感,仅在10例患者中使用了SXT作为结核病治疗方案的一部分。在其他病例中,可使用耐SXT (n = 4)或更传统的结核病药物(n = 3) (表2).总体而言,这些结核病患者相对年轻,中位年龄为29岁(四分位范围(IQR) 24-31岁),身体质量指数中位较低,为21.1 kg·m−2(IQR 19.1-23.6 kg·m−2).抵抗结核分枝杆菌至少异烟肼和利福平经培养诊断。8名患者患有肺结核,这是耐多药结核病患者中最常见的诊断;1例患者患有泌尿生殖系统结核病;还有一位同时患有肺结核和肺外结核病。处方每日480毫克SXT。这相当于6.5毫克·千克的中值剂量−1(IQR 6.1-6.8 mg·kg−1)中位期为381天(IQR 129-465天)。SXT的日剂量任意增加到960 mg(14和13 mg·kg)−1),因为这些患者血液中的SXT水平低于MIC。除1例患者有糖尿病外,其余患者基础疾病史均为阴性。没有人被诊断为同时感染艾滋病毒。10例患者中有8例成功完成治疗,无复发迹象。在撰写本文时,有两名患者仍在接受治疗;痰培养成功,临床情况良好。10例患者的临床资料见表3.对所有耐多药结核病患者进行了药敏试验。易感性和耐药性结核分枝杆菌抗结核药物的比例显示在表2.
药代动力学和药效学
SMX的稳态药代动力学参数只能在10名每天接受一次480 mg SXT的患者中评估,因为在另外两名患者中,在使用SXT的治疗期间没有进行血浆采样。药代动力学参数总结于表4.在患者接受480 mg SXT后,观察到SMX的血药浓度-时间曲线,见图1.
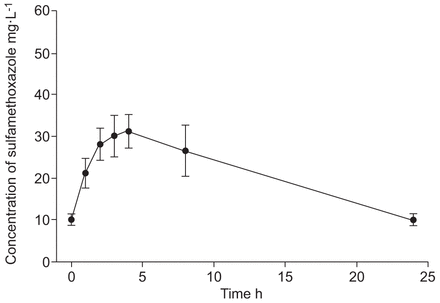
磺胺甲恶唑的血药浓度-时间曲线。N = 8。
SMX的POP-PK模型参数如图所示表5.模型交叉验证表明,POP-PK模型(n-1)的几何平均值为Cl 1.28±0.52 L·h−1/ 1.85米2;VD0.22±0.03 L·公斤−1瘦体重;吸收速率常数(0.44±0.18)h−1).这些结果与POP-PK模型并无不同(表5).基于POP-PK模型的预测值与AUC计算值之间的个体差异0-24被低估的中位数百分比为-0.7(范围为-6.2-2.8)。POP-PK模型预测结果与AUC计算结果吻合较好0-24SMX的值显示在图2.该图显示了AUC的值0-24意见一致;只有一个不在协议范围之内。基于POP-PK (n-1)模型的预测值与AUC计算值之间差异的中位数百分比0-24为-3.92(范围-6.3-1.7)。
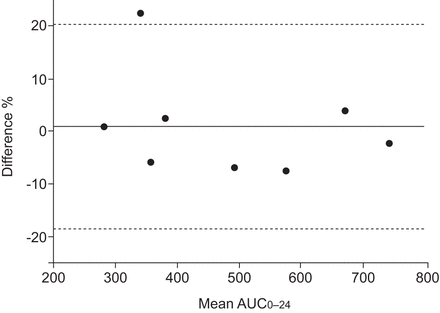
Bland-Altman图显示剂量后24小时浓度-时间曲线下预测面积与计算面积之间的一致性(AUC0-24)磺胺甲恶唑。
药敏试验表明,SMX的MIC值为结核分枝杆菌中位数范围为9.5 mg·L−1(IQR 4.8 ~ 25 mg·L−1).
auc比值0-24每例患者SMX的/MIC均在表6.AUC的几何均值0-24/MIC和auc0-24接受480 mg SMX后的/MIC比值分别为48.4 (IQR 34.8-71.3)和11.1 (IQR 8−16.4)。8名接受480mg SXT的患者中有1名患者的auc为负值0-24SMX > /MIC比25。
安全
总的来说,SXT耐受性良好。然而,有一些轻微的副作用,包括一名患者出现腹泻和呕吐的腹部症状(Naranjo评分= 4)。在分别接受480和960 mg SXT的两名患者中观察到肝酶(ASAT和ALAT)升高(两例患者的Naranjo评分均为5)。这两例患者在480 mg SXT治疗期间ALAT值分别为47.50和48 U·L−1(基线29 U·L−1)和960 mg SXT组分别为46和71 U·L−1(基线43 U·L−1),分别。480和960 mg SXT后ASAT值分别为48和99 U·L−1,而基线值为35 U·L−1.虽然肝酶比基线高2倍,但ASAT和ALAT值不超过正常上限的5倍。480 mg SXT治疗前患者的中位血红蛋白水平为7.6 mmol·L−1(范围7.6-8 mmol·L−1),处理期间为7 mmol·L−1(范围6.6-7.2 mmol·L−1);差异有显著性(p = 0.002),但可能在临床上不相关。低血红蛋白的纳兰霍评分值为3或4。1例患者在接受480和960 mg的SXT后出现白细胞减少。白细胞计数为2.2×109细胞·L−1和3.2×109细胞·L−1,而基线值为4.2 cells·L−1(Naranjo评分= 3)。1例患者出现轻度血小板减少,血小板计数为146×109细胞·L−1(247×109细胞·L−1(纳兰霍得分= 3)。
讨论
此前没有研究描述了SXT在耐多药结核病患者中的药代动力学、药效学和药代动力学/药效学参数。有趣的是,SMX在结核病患者中的药代动力学参数,包括AUC0-24,VD和清除率,均低于脑膜炎、艾滋病毒感染或皮肤细菌感染患者(表1) [6- - - - - -9].低药物接触可能是由于肠道吸收减少导致抗结核药物的血清浓度低。其他因素如酗酒、吸烟、减肥、低白蛋白和血红蛋白水平也可能是通透性降低的原因通过细胞旁肠转运[25].为了进一步探索耐多药结核病患者的药代动力学参数,我们建立了一个群体模型。该模型在计算的AUC和预测的AUC之间没有显著差异(p = 0.78)0-24根据Bland-Altman分析。因此,耐多药结核病患者似乎对SMX表现出一致的药代动力学特征。因此,开发的模型可用于评估前瞻性研究中的药物暴露,以评估安全性和有效性,并找到最合适的SXT剂量作为结核病治疗方案的一部分。
本研究中SMX的MIC值与之前的研究一致,即SMX在MIC为19 mg·L时能抑制全部117株菌株80%的生长−1[10].
药代动力学/药效学参数(AUC0-24/MIC)对SMX疗效的最佳预测还没有确定。根据之前的一项研究,auc0-24/ SMX的MIC必须为>25,才能充分治疗类鼻疽病[12].从结果中可以看出,8例患者中只有1例为隐性auc0-24SMX > /MIC比25。然而,这一比例可能小于25,仍然对结核病治疗有效。特别是,这个参数的大小可能因不同的细菌种类而异。例如AUC0-24氟喹诺酮类药物/MIC比值不同铜绿假单胞菌及其他革兰氏阴性杆菌[26].在接受耐多药结核病多药治疗的患者中,较低的比率可能是可以接受的。其他药物可能会降低这一比例,正如之前研究中的小鼠气溶胶感染模型所示,其中AUC0-24与疗效相关的利福平与莫西沙星联合用药时,其/MIC比值降低[27].因此解释AUC的价值0-24目前在我们的耐多药结核病患者中用于SMX的/MIC是困难的。与治疗其他传染病的常用剂量相比,给予耐多药结核病患者的SXT剂量较低。然而,更常规的SXT剂量用于治疗快速复制的细菌,通常作为单一疗法使用。在我们的例子中,目标是缓慢增长的结核分枝杆菌,与其他抗菌药物联合使用。对于未来的MDR-TB的SXT研究,我们建议探索更高的剂量,以达到更高的药物暴露,但耐受性可能是长期治疗的一个问题。
正如之前的一项研究所提到的,当利福平与SXT合用时,HIV合并感染的结核病患者可能会发生药物-药物相互作用[9],但这在耐多药结核病中无关紧要。的确,利福平显著降低了血清中TMP和SMX的浓度,但对于可以用利福平治疗的个体,不会开SXT,而且在开始用SXT治疗之前,没有人接受过利福平。
虽然我们的样本量很低,但这项回顾性研究证实了SXT的安全性,这与早期的研究一致,这些研究表明,当SXT被用于预防患有肺结核的HIV感染成人时,它是安全的,并且耐受性良好[28,29].耐多药结核病患者对SXT具有良好的耐受性,在8名患者中,任何一名患者在治疗结束前以及两名仍在接受治疗的患者中未停用SXT。只有一名患者在每天服用960毫克的SXT后可能出现胃肠不适的副作用。因此,剂量降低到480毫克,直到治疗结束。在我们的患者中,最高Naranjo评分达到了5分,换句话说,观察到的副作用与SXT之间可能存在关系。然而,治疗期间的血液学副作用,包括贫血、白细胞减少和血小板减少,可能是由利奈唑胺等其他抗结核药物引起的[30.,31].
本研究的主要局限性是缺乏靶标(AUC)的数据0-24/MIC值)来预测SXT治疗结核病的疗效。未来,需要前瞻性的研究来评估SXT在结核病患者中的药代动力学和药效学参数。确定auc0-24以SMX /MIC比值进行有效治疗,抑制耐药的出现在体外感染模型可能是合适的策略,如先前报道莫西沙星[32].
与其他未注册用于结核病治疗但用于耐多药结核病治疗方案的药物相比,SXT具有巨大的优势,即它便宜且在世界各地都可获得。
这是结合药敏试验和SXT浓度测量将SXT纳入耐多药结核病治疗的首次结果。根据我们的初步数据,我们显示了SXT在结核病患者中具有良好的药代动力学特征。
进一步在体外药代动力学和药效学研究,如中空纤维感染模型或小鼠模型,是建立目标AUC的必要条件0-24/MIC值来预测SXT的疗效,从而设定治疗MDR-TB治疗的最佳剂量。最好单独测量药代动力学/药效学参数和药代动力学参数,以及在其他抗结核药物存在的情况下测量药代动力学/药效学参数,以检测这些药物之间可能的协同作用。根据临床结果,无停药或严重副作用,药代动力学值一致,MIC值相对较低,本研究可作为进一步探索SXT治疗MDR-TB的起点。
致谢
我们要感谢Beatrixoord结核病中心(荷兰哈伦)的护理人员在收集患者数据方面的合作,也要感谢自愿帮助获取这些数据的患者。
脚注
利益冲突:可以在本文的在线版本中找到信息披露www.www.qdcxjkg.com
- 收到了2012年7月23日。
- 接受2012年9月19日。
- ©2013人队















