摘要
II阶段Nonsmall细胞肺癌(NSCLC)已在肿瘤,节点,转移(TNM)分类的第七版中重新定义为肺癌。阶段IIA和IIB都包含节点负(N0)和节点正(N1)子组。本研究的目的是评估切除的N1-阶段II NSCLC患者整体存活的预后因素。
1992年1月至2010年12月,我们回顾性分析了163例以根治性切除为主要治疗方法的n1期(T1a-T2bN1M0)非小细胞肺癌的临床病理特征。
中位随访时间为37.2个月。1年、3年和5年总生存率分别为85.3%、62.1%和43.5%。多因素分析显示,肺门/叶间淋巴结区肿瘤受累和组织学分级低分化是较差的总生存率的显著预测因子(p = 0.001和p = 0.015)。在年龄较大的患者和肿瘤体积较大的患者中,总生存率有下降的趋势(p = 0.063和p = 0.075)。
在切除的n1期II型NSCLC中,肺门/叶间淋巴结受累和低分化的组织学分级是较差的总生存率的重要预测因子。这些亚组患者的生存差异可能导致使用不同的辅助治疗或术后随访策略。
肺癌是全世界癌症相关死亡的主要原因。在台湾,它也是女性癌症相关死亡的最常见原因,以及男性中的第二个最常见的死亡原因[1].手术切除是早期非小细胞肺癌(NSCLC)的首选治疗方法。即使采用根治性手术切除,IIa期的5年总生存率在52% - 61%之间,IIb期在43% - 47%之间[2- - - - - -4].
肺癌的预后因素已被广泛调查,以适当识别高危患者,并提供其有效治疗。肿瘤,节点,转移(TNM)分类的第七版[5,6],发表于2009年,重新分类是恶性胸膜生效和单独的肿瘤结节。其他更改包括T1(进入T1A和T1B),T2(进入T2A和T2B)的新尺寸截止点和新分区,以及M1(进入M1A和M1B)描述符。然而,节点描述符保持不变。
淋巴结阳性(N1)疾病代表一组生存率不同的非小细胞肺癌[7].近几十年来,许多作者提出,在病理性N1疾病患者亚群中,预后可能因涉及淋巴结的数量、水平或类型而异[8- - - - - -14.].阶段II NSCLC包括相对较少数量的患者,而患有阶段I NSCLC的患者。在本研究中,我们评估了N1-阶段II NSCLC中的预后因素,特别强调了N1淋巴结病亚组的预后意义。
患者和方法
患者选择
台北退伍军人总医院(台北,台湾)机构审查委员会批准本研究,并同意放弃知情同意程序。从1992年1月至2010年12月,台北退伍军人总医院共210例以治疗为目的的病理n1 - II期非小细胞肺癌(T1a-2bN1M0)患者接受肺切除术。充分的淋巴结采样可以保证淋巴结状态的准确性。ludwiget al。[15.]提示,取样的淋巴结数目在11到16之间,以评估肺癌手术中淋巴结的状态。因此,我们的分析仅限于在手术期间采样≥12个区域淋巴结的患者,以确保淋巴结状态评估的质量。手术死亡率(n = 6, 2.9%),定义为手术后30天内住院死亡的患者被排除在我们的研究之外。共纳入163例患者进行分析。
术前检查
术前检查包括体格检查、血清生化检查、柔性支气管镜检查、胸部和上腹部计算机断层扫描(CT)、放射性核素骨扫描和大脑CT或磁共振成像。此外,如果术前组织诊断可行,则在2007年之后进行正电子发射断层扫描(PET)-CT扫描。纵隔镜检查并不是经常进行术前分期,除非肿大淋巴结(直径> 1.0厘米)观察CT和位于侧一侧的纵隔肿瘤,或纵隔淋巴结吸收对PET >标准摄入值的2.5倍。怀疑远处转移的患者被排除在手术考虑之外。一旦分期完成,所有患者将进行全部肺疾病切除和淋巴结取样或根治性清扫。
淋巴结评估
N1和N2淋巴结根据国际肺癌研究协会(IASLC) 2009年公布的淋巴结图定义[16.].根据解剖位置,将N1节点分为“HILAR / Interlobar”和“外围”区域。Hilar节点(站10)包括立即与主干支气管和肺门口相邻的节点,包括肺静脉和主要肺动脉的近侧部分。中间隙节点(站11)包括洛氏支气管的起源之间的节点。
典型的淋巴结解剖或取样,包括在左侧的右侧和5L,6L,7L和10L上的节点站2R,4R,7R和10R。在Lobectomy中,常规采样站11(中间淋巴结淋巴结)。外科医生采样的淋巴结被标记为病理检查。然而,主站12,13和14主要由病理学家检查。病理学家将切除的肺组织沿着主要支气管分解为肺实质。如果沿支气管树发现淋巴结,则根据其解剖位置标记它们。整个肺组织后来以1cm间隔切片。如果发现淋巴结,它们被命名为“肺内淋巴结”。
手术切除淋巴结总数定义为外科医生在手术过程中解剖或取样的淋巴结(包括送往冷冻诊断的淋巴结)和病理学家检查的肺内淋巴结总数;所有淋巴结均由病理学家检查。从纵隔镜采集的淋巴结也包括在本研究中。病理分期是在检查切除的标本和所有切除的淋巴结检查转移癌。疾病分期基于第七版非小细胞肺癌TNM分类[17.].我们的患者都没有先前的新辅助放疗或化疗。除非患者无法耐受它,否则对手术切除后给予患者的辅助化疗。在此后在初始2 YRS期间,所有患者在我们的门诊部门进行了三月,此后在初始2年后在初始2年前随访。结果被定义为癌症或非癌症原因归因于癌症的死亡。存活的长度被定义为手术切除日期和死亡日期之间的数月和死亡日期或最后一次随访。
统计分析
采用Kaplan-Meier法计算总生存率。采用Cox比例风险模型,使用SPSS软件(16.0版本;SPSS Inc.,芝加哥,伊利诺伊州,美国)。采用逐步回归程序。临床病理因素,如年龄、性别、肿瘤大小、组织学类型(鳞状细胞或其他组织学类型)、组织学分级(良好-中等分化)与低分化),有内脏胸膜侵犯(VPI),累及淋巴结数(单发)与受累淋巴结比率(定义为阳性淋巴结数除以总切除淋巴结数)和受累淋巴结水平(肺门/叶间区)与外周区)包括在单变量分析中。在多变量分析中具有p值<0.10的变量进入多变量分析。p值<0.05被认为是统计学上的显着性。
结果
163例手术切除的n1 - II期NSCLC患者中位随访时间为37.2个月(平均50.4个月,范围1.2-186.0个月)。在最后一次随访期间,61例(37.4%)患者存活,102例(62.6%)患者死于癌症或非癌症原因。1年、3年和5年总生存率分别为85.3%、62.1%和43.5% (无花果。1).这些患者的人口学和临床病理特征总结在表格1.
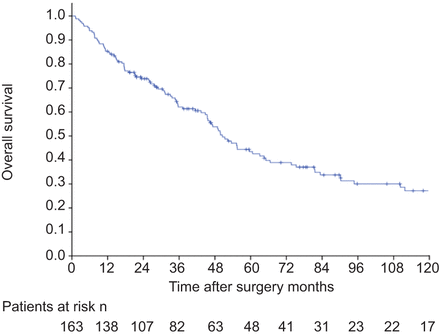
Kaplan-Meier生存曲线为163 n1-阶段II II的Nonsmall细胞肺癌患者治疗外科切除后。
我们队列的平均年龄为65岁,男女比例为2.40。右肺内有肿瘤85例(52.1%),左肺内有肿瘤78例(47.9%)。手术切除肿瘤以叶切除术为主(131例,80.4%),叶下切除术仅1例。测量并记录每个肿瘤的最大尺寸。肿瘤大小≤3cm的患者77例(47.2%),肿瘤大小> 3cm的患者86例(52.8%)。
腺癌是我们的队列中的主要组织学类型(90%(55.2%)患者)。根据病理报告,组织学分级分为良好,中度和差异差的癌。然而,在我们的队列中有45名(27.6%)患有缺失或组织学级别的患者“未描述”。67例(41.1%)患者中观察到具有内脏胸膜胸膜侵袭的肿瘤。然而,有14例(8.6%)患者有关内脏胸膜侵袭的“未知状态”。在手术解剖淋巴结中,在88例(54.0%)患者中发现了一种孤立的转移性淋巴结。75(46.0%)患者发现≥2淋巴结转移。淋巴结比定义为涉及淋巴结与移除节点总数的比率。获得0.06的截止点以使我们的队列分为两组以进行比较。根据IASLC淋巴结地图,将淋巴结分为“区域”,在61例(37.4%)患者中观察到肝脏/中间隙区的癌症累及,并在86例(52.8%)患者中注意到外周带的涉及。 16 (9.8%) patients had both zones involved.
使用单变量分析评估与肺癌预后相关的因素。该分析表明,年龄(作为连续变量,p = 0.001),癌症涉及的淋巴结比(p = 0.044)和癌肠/中间淋巴结癌的癌症(p = 0.013)对整体存活有重大影响(表2.).较年轻的患者、较低的癌涉淋巴结比率(≤0.06)的患者以及转移性N1淋巴结累及肺门/叶间区以外其他区域的患者的生存率明显更好。肿瘤大小>3 cm的患者死亡危险更大(风险比(HR) 1.440, 95%可信区间(CI) 0.970-2.138;p = 0.070),低分化细胞型(HR 1.589, 95% CI 0.968-2.609;p = 0.067),多发性肿瘤累及N1淋巴结(HR 1.325, 95% CI 0.896-1.961;p = 0.159)。尽管这些因素没有达到统计学意义,但预测生存率的趋势与其他文献报道具有可比性。p值<0.10的变量进行多变量分析。多因素分析显示,只有组织学分级(p = 0.015)和肿瘤是否累及肺门/叶间淋巴结(p = 0.001)是重要的预后指标(表3).年龄较大的患者(P = 0.063),大肿瘤大小(P = 0.075)和高涉及的淋巴结比(P = 0.199)表现出较差的整体存活率的趋势。
讨论
分期对于预测患者预后和选择合适的肺癌治疗非常重要。IASLC成立了一个国际分期委员会来制定肺癌TNM分类的修订版,该修订版于2009年发表在国际对抗癌症联盟和美国癌症联合委员会(AJCC)癌症分期手册第七版[5,6].第七版肺癌TNM分类对T描述符进行了修订,根据新的肿瘤大小截断点,将T1分为T1a和T1b, T2分为T2a和T2b [17.].尽管在新版本的TNM系统中N描述符保持不变,IASLC分期委员会开发了一个修订的淋巴结图,将淋巴结站分组为“区域”,即。对于N1,上部或下纵隔或N2节点的主体或下纵隔或下纵隔或母动或母动或母动物[16.].
第一张淋巴结图由Naruke[18.在20世纪60年代,最初在北美,欧洲和日本广泛使用。然而,随后尝试改进纳鲁克地图的解剖学描述符导致美国胸部社会(ATS)的地图和ATS地图(MD-ATS)的所谓的山地Dresler修改的发展。修订后的淋巴结地图在日语(Naruke)和MD-ATS地图之间协调差异,并为每个淋巴结站提供更具体的解剖定义[16.].在新版本的TNM分类系统中,阶段IIA和阶段IIB都包含节点正数(阶段IIA包含T1A-T2AN1和舞台IIB包含T2BN1),节点否定(阶段IIA包含T2BN0和舞台IIB包含T3N0)案例。在本研究中,考虑到修订后的淋巴结地图和新的分期系统,我们研究了用于预测节点阳性阶段II NSCLC中存活的预后因素,重点是N1淋巴结病的特征。
区域淋巴结的状态是一个强有力的预后指标,对NSCLC患者的治疗决定有重大影响[19.].虽然新版TNM系统中的N描述符没有改变,但有几项研究报告称,在N1类中,有几个预后调节剂。这包括受累淋巴结的数量(单发)与多个)[19.- - - - - -21.,所涉及淋巴结的比率[20.,21.,受累淋巴结的水平(肺门)与大叶性)7,11.,12.,22.,23.,以及所累及淋巴结的类型(直接浸润)与单独的转移)(24.,25].若干研究突出显示N1疾病代表了影响预后的不同淋巴结相关因素的异质组。鉴定不同结果的患者亚组可以有助于定制术后管理,例如侵略性化疗或更紧密的后续战略。
受累淋巴结的数量被认为是N1型非小细胞肺癌生存率的重要预测因素。Jonnalagadda等.[21.[分析了来自监测,流行病学和最终结果数据库的数据,包括3,399名N1 NSCLC患者。他们得出结论,阳性淋巴结的数量是N1 NSCLC患者存活的独立预后因素。在我们的研究中,具有相对较小的样本量,具有肿瘤的多个淋巴结涉及较差的整体存活趋势(HR 1.325,95%CI 0.896-1.961; P = 0.159)。然而,通过去虫淋巴结的数量本质上混淆了生存和肿瘤淋巴结数之间的关联。因此,W.isnivesky.等.[26]报道了淋巴结比(LNR)对1682例年龄>65岁诊断为病状N1型NSCLC患者的预后影响[26].在其队列内的每位患者中都切除了八个淋巴结的中值。它们根据LNR:≤0.15,0.15-0.5和> 0.5将患者分为三组。在研究人口中,他们发现整体存活率随着LNR的增加而显着差。在我们的系列中,切除了23个淋巴结的中位数,这比W的研究中的中位数大3倍isnivesky.等.[26].我们还发现,LNR> 0.06的患者比单变量分析的LNR≤0.06患者有明显较高的危险性死亡风险(HR 1.499,95%CI 1.010-224)(P = 0.044)。我们的研究回应了其他先前的研究,其中发现LNR是N1 NSCLC患者存活的预后因素。
除了淋巴结受累的数量和比例外,淋巴结受累程度也是常被调查的N1 NSCLC预后因素,与叶间或更多的外周淋巴结转移相比,肺门部位受累的预后更差。年代Himada等.[22.,利用Narukeet al。[27]总结,患有节点10(HILAR) - 阳性N1疾病的患者具有不利的预后,因为疾病的表现类似于N2疾病[22.].利用IASLC淋巴结图,我们发现肿瘤累及肺门/叶间区患者在单因素分析中均有显著较高的死亡危险(HR 1.651, 95% CI 1.112-2.452;p = 0.013)和多因素分析(HR 2.595, 95% CI 1.490-4.427;p = 0.001)。肿瘤累及肺门/叶间淋巴结区和未累及肺门/叶间淋巴结区患者的5年总生存率分别为37.1%和49.9% (p = 0.012) (无花果。2).我们的研究表明,肿瘤累及肺门/叶间区是II期NSCLC的一个独立预后因素。
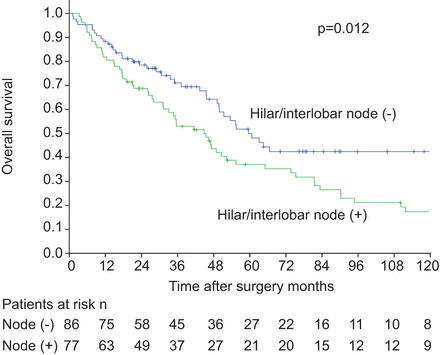
163例n1期非小细胞肺癌患者肺门/叶间结阳性和阴性的Kaplan-Meier生存曲线日志等级p < 0.001。
我们还发现组织学级(细胞分化)是N1-阶段II NSCLC中总存活的显着预测因子。癌患者患者在单变量分析(HR 1.589; 95%CI 0.968-2.609; P = 0.067)和多变量分析(HR 1.997; 95%CI 1.154-3.455; P = 0.013)中,患有危险性死亡风险增加在发表的文献中,主要在I阶段NSCLC患者中讨论了细胞分化对存活的影响。H苏等.[28]报道了在Ib期NSCLC患者(pT2N0M0)中,细胞分化是总生存的重要预后因素(p = 0.0024)。在之前的一项研究中,我们也表明,细胞分化与I期NSCLC的总生存率相关(p = 0.04) [29].然而,细胞分化在II期NSCLC中很少被讨论。我们注意到,在将其他预后因素纳入相互调整后,低分化癌患者的总生存率较低(p = 0.015)。然而,需要更大的样本量来证实这一发现。
内脏胸膜侵袭(VPI)对II阶段NSCLC的影响尚不清楚。V一个V埃尔松等.[11.据报道,在T2N1M0 NSCLC患者中存在VPI不利影响的生存(P = 0.0093)。但是,在研究的研究中iquet等.[12.] VPI与病理N1 NSCLC患者的整体存活率无关(P = 0.65)。在我们的研究中,VPI的患者表现出与单变量分析的同行相比略高的危险风险略高;然而,结果不显着(HR 1.251,95%CI 0.808-1.937; P = 0.315)。
大多数II期NSCLC患者存在淋巴结转移。然而,任何非淋巴结因素的影响都不如I期疾病清晰。H洞螈[30.]报道了在T1N1和I型鳞状细胞肺癌患者中存在显著的生存差异中华蛇等.[31在T1-2N1疾病中也有类似的结果。然而,无论是米artiniet al。[32]也没有ano.et al。[8发现鳞状细胞肺癌比非鳞状细胞肺癌有显著的组织学优势。C汉斯基et al。[33[发表了一项9137例经手术处理的I期至IIIA期NSCLC患者的预后分析(IASLC分期项目)。在他们的研究中,鳞状细胞癌可能比非细支气管肺泡癌型腺癌有更好的预后,特别是在男性早期疾病患者中。我们对T1a-2bN1非小细胞肺癌人群的研究结果显示,与非鳞状细胞癌相比,鳞状细胞癌没有生存获益。在性别调整分析中,两组患者的生存预后仍然相似。因此,我们的研究未能确定在手术治疗的n1期NSCLC患者中,癌细胞类型是一个重要的预后因素。C的结果汉斯基等.[33[我们的研究可能反映了与节点状态相比细胞类型的预后影响在N1 NSCLC中不太重要。
II期NSCLC中的肿瘤大小似乎没有显着影响整体存活率。米artiniet al。[32]发现直径小于3cm的肿瘤与直径小于5cm的肿瘤相比存活率更高。在我们的n1期II期NSCLC系列中,与直径≤3cm的患者相比,肿瘤大小> 3cm但≤7cm的患者死亡危险风险增加(HR 1.631;p = 0.075)。虽然我们的结果没有达到统计学意义,但它暗示,如果研究的是更大规模的人群,肿瘤大小可能对n1期II NSCLC的生存有影响。
我们的研究有几项局限。我们在很长一段时间内进行了回顾性分析。一些患者缺乏某些变量的数据,例如内脏胸膜侵袭和组织学等级,可能影响了我们的结果。几种不同的外科医生表演了肺切除术,并非所有患者都接受了群组中的根治纵隔淋巴结解剖。此外,同一组病理学家未检查并报告切除的N1节点。因此,所有患者之间的淋巴结解剖/取样的数量和质量在我们与<12种采样的淋巴结的研究中排除在外的情况下,我们的所有患者都不一样。无复发生存的数据缺乏数据是我们研究的另一个限制。
结论
II期NSCLC包括一组异质性的淋巴结阳性和阴性肿瘤。预后因素分析对这一亚组患者提供了更好的评价。在目前的n1期II NSCLC研究中,肺门/叶间淋巴结受累和低分化的组织学分级是较差的总生存率的重要预测因子。这些亚组患者的生存差异可能导致使用不同的辅助治疗或术后随访策略。未来的临床试验必须考虑这些亚组患者的生存差异,对辅助治疗进行分层是必要的。
脚注
支持声明
This work was supported in part by Taiwan National Science Council (NSC 100-2314-B-075-004-MY2) (Y-C. Wu), Center of Excellence for Cancer Research at Taipei Veterans General Hospital (DOH101-TD-C- 111-007) (Y-C. Wu), KS Lu Lung Cancer Foundation (Y-C. Wu and J.J. Hung), National Science Council (NSC-101-2314-B-075-010) (J.J. Hung), and Taipei Veterans General Hospital (V102B-021) (J.J. Hung).
感兴趣的语句
没有宣布。
- 已收到2012年4月8日。
- 接受2012年6月2日。
- ©2013年















