文摘
大多数情况下是由社区获得性肺炎链球菌引起的肺炎肺炎球菌主机上,大多数研究是基于细胞培养和动物实验的互动。因此,对人类感染的肺部组织。
Cyclooxygenase-2及其代谢物在肺部炎症发挥重要的监管作用。因此,我们建立了肺炎球菌感染模型对人类肺组织展示增殖蛋白激酶(MAPK)端依赖诱导cyclooxygenase-2及其相关代谢物。
除了肺泡巨噬细胞和血管内皮,cyclooxygenase-2是调节在肺泡II型而不是I型上皮细胞,证实在肺的病人患有急性肺炎。此外,我们证明了所有四个E前列腺素类受体的表达谱在mRNA水平E前列腺素类和显示功能4环腺苷酸受体的生产。此外,与先前的研究相比,cyclooxygenase-2 /前列腺素E2相关支持和抗炎中介监管在一定程度上证实了人类后肺组织肺炎球菌感染。
总的来说,细胞特定类型和MAPK-dependent cyclooxygenase-2表达和前列腺素E2形成人类肺组织可能扮演重要的角色在肺炎球菌感染的早期阶段。
肺炎是最常见的死亡原因之一,在全球范围内(1),链球菌引起的肺炎是最常分离病原体肺炎患者2]。疫苗可用,但只提供保护选定的血清型(3]。此外,耐药菌株的数量增加(4)和多重耐药血清型的出现(5]。因此,重要的是要调查宿植病原体相互作用为基础的设计新颖的辅助治疗方法。
大多数宿主-病原体相互作用的研究,包括肺炎链球菌感染,都是基于培养,经常被永久细胞系或动物实验6]。这些模型代表当前肺炎研究不可或缺的一部分,但明显限制的模型应该考虑7,8],主要调查或,至少,应该执行验证的结果尽可能的在人类原始材料。
因此,我们建立了一个肺炎链球菌体外人类感染模型肺组织,从接受肺切除术的患者由于肺癌。
环氧合酶(COX)派生的一代的前列腺素(后卫)怀疑先天免疫中发挥重要的监管作用的肺9]。COX-1通常被认为是持续表达,而cox - 2诱导同种型(10]。感应是由各种刺激,包括细菌、病毒和表示细胞/趋化因子(11- - - - - -14]。他们可以导致增殖作用的激活蛋白激酶(MAPKs),造成各种重要的细胞功能,包括调节炎症。例如,p38 MAPK-dependent诱导细菌和cox - 2的连续PG形成已被证明在支气管上皮细胞培养11- - - - - -13]。
最著名的后卫是铂族元素之一2,这已被证明有助于各种细胞类型的炎症反应(15- - - - - -18]。铂族元素2似乎信号通过四个不同G protein-coupled E前列腺素类受体,EP1ep4(9]。
在这项研究中,我们使用新孤立的人类肺组织被感染体外与肺炎链球菌。我们提出,肺炎球菌感染可能诱发cox - 2以及相关花生四烯酸的形成acid-derived产品和研究细胞类型特异性cox - 2表达模式和底层信号转导途径。结果清楚地建立在肺泡,肺泡巨噬细胞(AMs)旁边,cox - 2在II型主要是诱导,但不是I型肺泡上皮细胞(aec)。相似的表达模式,cox - 2在原子能委员会还演示了在肺的病人患有急性肺炎。p38 MAPK或抑制细胞外调节激酶(ERK) 1/2废除cox - 2的感应和随后的铂族元素的释放2。在人类的肺组织,激活EP4环腺苷酸的诱导显著增加(营)。总的来说,这项研究,据我们所知,第一个建立健壮的肺炎球菌感染对前列腺素类代谢的影响在人类主要的肺部组织。
材料和方法
方法的详细描述,请参阅在线补充材料。
材料
铂族元素2和铂族元素1酒精(铂族元素1-哦)从开曼购买化学公司(美国安阿伯市MI)。3-isobutyl-1-methylxanthine和forskolin从默克公司购买(达姆施塔特,德国)。三氯乙酸是来自Sigma-Aldrich(德国慕尼黑)。U0126, SB202190和ns - 398从Calbiochem购买(德国默克,坏Soden)。肿瘤坏死因子(TNF) -α和白介素(IL) 1β得到从研发系统(德国威斯巴登)。所有其他化学物质均为分析纯和从商业来源获得。
菌株
封装肺炎链球菌D39血清型2 (NCTC7466)(来自美国的礼物哈默施密特,格赖夫斯瓦尔德大学格赖夫斯瓦尔德,德国)是培养如前所述19]。
人类的肺组织
新鲜肺外植体获得从接受肺切除术的患者在当地胸外科诊所。此外,肺组织样本三个急性肺炎患者和一个控制病人被随机选择从日常情况。书面知情同意是来自所有患者,这项研究是经伦理委员会批准的诊所,柏林,德国(协议号EA2/050/08和EA2/023/07)。对感染肺炎链球菌,肿瘤自由正常肺组织印成小气缸(∼8×8毫米)和体重。标本孵化24小时的RPMI 1640 10%(卷/期)heat-inactivated胎牛血清(细菌生长除外)在实验感染。200μL准备控制或感染中是每100毫克注射组织,从而保证彻底刺激的组织。肺为进一步分析处理时间点。
集落形成单位分析
人类感染的肺部组织肺炎链球菌(102cfu·毫升−1)为0 h(控制负载后直接感染)和8 h。后来,标本中断使用FastPrep-24匀浆器(MP生物医学、海德堡、德国)和上层清液镀在哥伦比亚琼脂。细菌菌落数和cfu·g−1肺组织进行了计算。
西方墨点法
西方墨点法进行如前所述[20.]。反对COX-1使用的抗体,cox - 2, ERK2,肌动蛋白(圣克鲁斯生物技术,帕索罗伯斯、钙、美国),EP4受体(开曼化工有限公司),磷酸化ERK和p38(细胞信号,丹弗斯、马、美国)。ERK2或肌动蛋白作为加载控制。蛋白质被二次想起IRDye 800——或者Cy5.5-labelled抗体奥德赛红外扫描仪(LI-COR Inc .,糟糕的小礼帽,德国)。
免疫组织化学和共聚焦免疫荧光
人类肺组织的感染后,标本在福尔马林固定,嵌入在石蜡处理和组织学。主cox - 2抗体(开曼化工有限公司)在一夜之间被孵化和发现超级敏感的链接标签检测系统(美国Biogenex, Fremont, CA)。迈耶的苏木精(德国卡尔罗斯,卡尔斯鲁厄)是用于复染色细胞核和幻灯片与Aquatex安装(默克公司)。使用阻塞肽抗体特异性验证了。共焦成像,cox - 2与Alexa萤石贴上488或594(表达载体,达姆施塔特,德国;所有的稀释下)。I型上皮细胞和抗体检测窖蛋白1(圣克鲁斯生物技术),而II型pneumocytes与表面活性剂抗体蛋白C标记前体(pro-SP-C)(美国微孔,Billerica的)。肺炎链球菌沾有抗体吗肺炎链球菌分析了由美国哈默施密特(捐赠)和幻灯片使用蔡司Axioskop 2年检[21]或蔡司LSM 780共焦显微镜(蔡司,耶拿,德国)。
铂族元素2ELISA
人类的肺组织标本被感染肺炎链球菌表示。铂族元素2按照制造商的指示是浮在表面的测量(研发系统,明尼阿波利斯,美国)。
质谱分析
人类的肺组织标本被感染肺炎链球菌免费16 h和上层清液进行分析和脂质matrix-bound二十烷类所描述的其他地方(22]。
定量聚合酶链反应
使用执行总RNA提取试剂盒(表达载体)。组织破坏后,定量PCR(20μL反应体积或CFX96 10μL反应体积;iCycler Bio-Rad,慕尼黑,德国)。EP受体拷贝数的计算,与克隆质粒的互补编码EP-receptors和glyceraldehyde-3-phosphate脱氢酶被用作模板准备复制数字定义的标准曲线。
营ELISA
营测量,肺组织在三氯乙酸重和加工。样本单一化和营地ELISA是根据制造商的指示(开曼化工有限公司)。
Bioplex蛋白质阵列系统
测定细胞因子释放,人类肺组织感染106cfu·毫升−1肺炎链球菌16 h。分析了收集上层清液和细胞因子释放和珠子具体使用Bioplex蛋白质阵列系统TNF-α,IL-1β,IL-17,集落刺激因子(gm - csf), il - 1受体拮抗剂(IL-1RA), il - 10, IL-15,血小板源生长因子(PDGF)、血管内皮生长因子(VEGF)、il - 6、引发和巨噬细胞炎性蛋白(MIP) 1α(BioRad、大力神、钙、美国)。
统计方法
数据意味着±扫描电镜至少三个独立的实验。单侧魏克森讯号等级测试用于测试方法之间的显著差异。的假定值< 0.05被认为是显著的。
结果
肺炎链球菌,诱导表达cox - 2在人类的肺部组织
确保可再生的肺炎球菌感染人类的肺组织,细菌生长以八肺组织样本展示强劲和常规细菌复制在8 h (图1)。没有发现细菌生长在无血清培养基(数据未显示),证实肺炎双球菌的增长依赖于人类肺组织发布的因素。

的增长链球菌引起的肺炎在人类的肺部组织。人类感染的肺部组织肺炎链球菌(应变D39;102cfu·毫升−1)和集落形成单位确定0 h和8 h。数据均值±扫描电镜八个不同的样本。* *:p < 0.01与0 h的增长。
感染后,我们观察到一个强大和时间cox - 2蛋白诱导,而持续表达COX-1仍影响所有的人类肺组织样本调查图2一个(四个样本)和b(3)样本)。在初步实验中,我们发现2 (D39)血清型菌株相比,侵入性和非侵入性肺炎球菌临床分离株也诱导cox - 2表达类似的模式(数据没有显示)。在下一步中,免疫组织化学进行研究细胞特定类型的cox - 2的表达,揭示感应主要在原子能委员会,AMs和肺炎球菌感染后血管内皮细胞(10个样本)以及后TNF-α/ IL-1β(5样品)治疗人类肺组织(图3)。有趣的是,我们也发现强大的cox - 2表达在原子能委员会的肺组织炎症网站三个患有急性肺炎(图3 b)。cox - 2的特异性染色证实了pre-incubation相应阻断肽与受感染的肺部分(数据未显示)。双重染色的组织部分anti-caveolin 1 (I型细胞)[23]或anti-pro-SP-C (II型细胞)肺炎链球菌来华和TNF-α/ IL-1β-stimulated组织被用来确认的原子能委员会类型cox - 2的表达。值得注意的是,尽管使用的刺激,几乎所有COX-2-positive原子能委员会显然是标记为pro-SP-C从而确定为II型细胞,而没有cox - 2在I型细胞染色观察(图3 c和d)。这些观点被证实的肺组织三个肺炎病人(数据未显示)。有趣的是,cox - 2表达不仅是检测到细胞直接面对肺炎双球菌,而且在细胞没有依恋的肺炎双球菌(图3 e五个样本所示)。
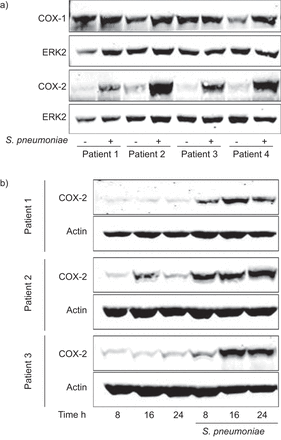
环氧合酶(COX) 1和COX - 2的规定链球菌引起的肺炎在人类的肺部组织。人类的肺组织被感染)24小时或b)与10指定的时间段6cfu·毫升−1肺炎链球菌。COX-1和cox - 2蛋白表达被免疫印迹分析。代表实验)4和b)三个不同的样本所示。
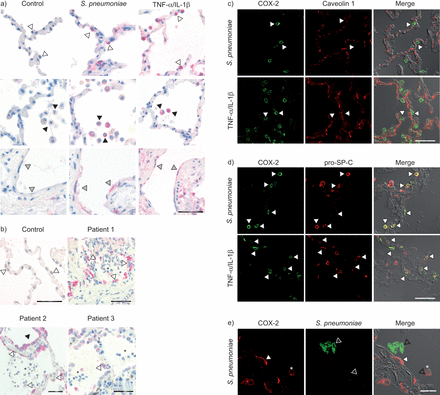
人类肺部组织刺激了)链球菌引起的肺炎或肿瘤坏死因子(TNF) -α/白介素(IL) 1β。免疫组织化学染色显示环氧酶2 (COX)表达式(用红色表示)在肺泡上皮细胞(aec)(开放箭头)、肺泡巨噬细胞(黑色箭头)和内皮细胞(灰色箭头)肺炎链球菌以及TNF-α/ IL-1β-stimulated组织,而没有染色观察肺刺激与介质(控制)。酒吧= 50μm规模。b)在急性肺炎患者的组织,也发现cox - 2表达的原子能委员会(开放箭头)。急性炎症明显可以看到中性粒细胞的浸润到肺泡空间(黑星号)。黑色箭头指示彩色远端支气管上皮细胞(病人2)。健康,noninflamed控制组织从病人肿瘤切除。没有发现cox - 2表达可以控制的组织。前孵化的主要抗体与其相应的阻断肽废除染色,表明抗体特异性(数据未显示)。酒吧= 50μm规模。c)多色immunofluorescent cox - 2(绿色通道)和窖蛋白1(红色通道)染色肺炎链球菌和TNF-α/ IL-1β-stimulated组织和随后的共焦成像显示没有colocalisation cox - 2和1窖蛋白的表达。这意味着cox - 2不是诱导型我原子能委员会。代表细胞是由白色箭头表示在每一个频道。酒吧= 50μm规模。相比之下,d)肺炎链球菌和TNF-α/ IL-1β-stimulated肺显示cox - 2表达(绿色通道)pro-surfactant蛋白C (pro-SP-C)阳性细胞(红色通道),表明cox - 2表达II型原子能委员会。代表与colocalisation细胞cox - 2和pro-SP-C表达式合并频道(黄色)是由白色箭头表示在每一个频道。合并面板展示肺结构利用微分干涉对比。酒吧= 50μm规模。e)殖民地的肺炎链球菌(绿色通道、开放箭头)检测cox - 2在肺泡空间相邻——积极(红色频道,白色箭头)II型原子能委员会以及肺泡巨噬细胞(白色星号)。酒吧= 20μm规模。合并面板展示肺结构利用微分干涉对比显微镜。代表人物的10肺炎链球菌来华的肺、五TNF-α/ IL-1β-stimulated肺部和三个不同的急性肺炎患者a) - d)所示。代表人物的五个独立实验e)所示。
cox - 2诱导铂族元素2形成p38和ERK的依赖
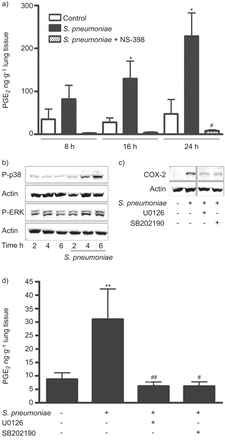
六人肺组织样本被感染肺炎链球菌存在与否的cox - 2抑制剂ns - 398和铂族元素2分析了解放。铂族元素2水平显著增加24 h后感染和废除了ns - 398 (图4)。以前的在体外研究使用培养的肺上皮细胞系(11- - - - - -13]表明cox - 2表达依赖于MAPK活性。我们观察到p38磷酸化增加肺炎双球菌而ERK的磷酸化已经发现的人类肺组织无毒性(图4 b五个样本)。七个肺组织样本的预处理ERK抑制剂U0126或p38抑制剂SB202190废除cox - 2蛋白表达(图4摄氏度)以及铂族元素2释放在上层清液(图4 d)。
时间环氧合酶(COX) 2, extracellular-signal调节激酶(ERK) 1/2和p38促分裂原活化蛋白激酶(MAPK)介导的诱导前列腺素(PG) E2通过链球菌引起的肺炎。人类肺组织)和b)是感染106cfu·毫升−1肺炎链球菌或与选择性cox - 2抑制剂预处理(ns - 398 10μM 1 h)和感染表示时间。一)时间铂族元素2释放被抑制cox - 2以ELISA抑制。b)西方墨迹演示p38 MAPK的激活肺炎链球菌,而ERK的磷酸化已经出现在未受感染的组织。c和d)预处理的1 h和ERK组织MAPK抑制剂(U0126 10μM)或p38 MAPK抑制剂(SB202190 10μM)和感染106cfu·毫升−1肺炎链球菌8 h . c) cox - 2和d)铂族元素2感应被MAPK抑制剂抑制免疫印迹和ELISA所示,分别。数据意味着±扫描电镜)6 - d)的七种不同的样品。5 b)和c)的代表七个墨迹图所示。P-p38:磷酸化p38;P-ERK:磷酸化ERK。*:p < 0.05与控制;* *:p < 0.01与控制;#:p < 0.05与受感染的组织没有pre-incubation抑制剂;# #:p < 0.01与受感染的组织没有pre-incubation抑制剂。
cox - 2的表达并不是由一个积极的反馈回路
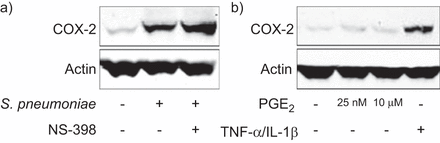
在小鼠的肺成纤维细胞,用铂族元素2刺激,一个积极的反馈回路是证明了Vichai等。(24),这表明COX-2-related铂族元素2生产进一步培育cox - 2的表达。因此,我们测量了cox - 2表达pre-incubation五肺组织样本后cox - 2抑制剂ns - 398 1 h (图5)。然而,在人类的肺组织,肺炎链球菌之前全身的cox - 2表达不受抑制cox - 2 (图5)。曝光以来三个肺组织样本不同剂量的铂族元素2未能影响cox - 2蛋白表达,没有积极的反馈循环,在小鼠成纤维细胞,在完整的人类肺组织被发现。TNF-α/ IL-1β刺激作为积极的控制(图5 b)。
免疫印迹的链球菌引起的肺炎全身的环氧合酶(COX) 2显示没有反馈调节。人类肺组织被感染10)6cfu·毫升−1肺炎链球菌或与选择性cox - 2抑制剂预处理(ns - 398 10μM, 1小时)前感染。cox - 2诱导免疫印迹分析显示没有抑制cox - 2的表达。b)肺组织孵化24 h表示浓度的前列腺素(PG) E2或与肿瘤坏死因子(TNF) -α(100 ng·毫升−1)和白介素(IL) 1β(10 ng·毫升−1)。)5和b)的代表三个墨迹图所示。
cox - 2诱导代谢产物肺炎链球菌
原则上,各种高度的生物活性介质可以生产通过cox - 2 (25]。因此,五人肺组织样本感染或没有预处理的cox - 2抑制剂ns - 398和质谱进行检测6-keto-PGF1α凝血恶烷(TX) B2,铂族元素2,PGH2,铂族元素2ethanolamide, PGF2α和8 -iso铂族元素1。增加感染和减少后ns - 398 pre-incubation测定铂族元素2,6-keto-PGF1α和TXB2(图6 a - c),而其他代谢物保持不变(数据没有显示)。
诱导环氧合酶(COX) 2代谢物肺炎链球菌。人类肺组织pre-incubated与选择性cox - 2抑制剂(ns - 398;10μM) 1 h在感染前106cfu·毫升−1肺炎链球菌16小时。一)前列腺素(PG) E2,b) 6-keto-PGF1αB和c)凝血恶烷(TX)2释放在上层清液用质谱测量。数据意味着±扫描电镜5个不同的样本。ND:没有检测到。*:p < 0.05与控制;#:p < 0.05与受感染的组织没有pre-incubation ns - 398。
EP受体表达谱在人类的肺部组织
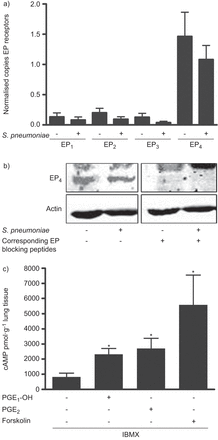
铂族元素2信号主要是由前列腺素类受体转导EP1 - 4(9]。因此,我们调查了他们的监管三个感染后肺组织样本肺炎链球菌。低拷贝数的mRNA为EP检测1 - 3而高水平观察EP4(图7)。EP4还演示了在蛋白质表达水平在三个肺组织样本(图7 b)。然而,在18 - 24 h肺炎球菌感染的调查时间不改变受体表达水平在mRNA和蛋白水平(图7 a和b)。自从EP4激活导致营地EP感应我们分析受体功能4受体激动剂铂族元素1-哦。选择性EP4激活以及铂族元素2或forskolin显著增加细胞内营水平六个人类肺组织样本(图7 c)。
E前列腺素类(EP)受体表达模式在人类的肺部组织。人类肺组织被感染)18 h或b) 24 h 106cfu·毫升−1肺炎链球菌。一)EP1 - 4信使rna使用定量PCR分析,证明对EP表达水平最高4。b) EP4蛋白质是由免疫印迹检测细菌感染后没有感应。使用相应的阻断肽抗体特异性验证了。c)人类肺组织与非特异性磷酸二酯酶抑制剂预处理3-isobutyl-1-methylxanthine (IBMX)(20μM) 2 h和刺激特定的EP4受体激动剂(前列腺素E1酒精(铂族元素1-哦)(10μM)、前列腺素(PG) E2(铂族元素2)(10μM)或forskolin(20μM) 30分钟。环腺苷酸的形成是由ELISA展示人类肺组织明显增加。数据意味着±扫描电镜)3和c)的六种不同的样品。代表性的样本三个墨迹图所示b) . *: p < 0.05与控制。
cox - 2的规定肺炎链球菌全身的细胞因子释放人类的肺部组织
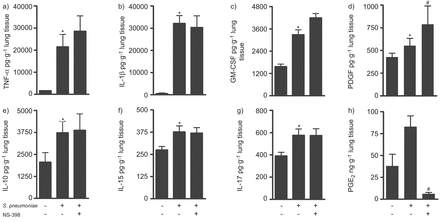
铂族元素2归纳证明,已经大大有助于化疗——/细胞因子调节[15- - - - - -18]。因此,我们分析了五个感染人类的肺组织样本对化疗/细胞因子释放的存在与否,cox - 2抑制剂ns - 398。肺炎双球菌显著诱导TNF-αIL-1β,PDGF, gm - csf IL-17, il - 10, IL-15解放(图8 g)。此外,IL-1RA显著增加,而VEGF、il - 6,引发和MIP-1α水平保持不变后肺炎球菌感染(数据未显示)。正如所料,cox - 2抑制减少铂族元素2在四个肺组织样本和PDGF导致显著增加,TNF-α和轻微的增加(p < 0.09)和gm - csf (p < 0.15)的表达,但显示没有影响其他化疗/细胞因子在同样的实验中(图8 a -)。
链球菌引起的肺炎诱发pro和抗炎细胞因子在人类的肺部组织。人类肺组织预处理与不选择性环氧合酶(COX) 2抑制剂(ns - 398;10μM) 1 h,然后感染106cfu·毫升−1肺炎链球菌16 h)肿瘤坏死因子(TNF) -α,b)白介素(IL) 1β,c)粒细胞巨噬细胞集落刺激因子(gm - csf), d)血小板源生长因子(PDGF), e) IL - 10, f) IL-15和g) IL-17释放在上层清液用Bioplex细胞因子测定(BioRad、大力神、钙、美国),展示TNF-α略有增加,显著增加对cox - 2抑制后血小板源生长因子。h)前列腺素(PG) E2释放在同一样本作为积极的控制。数据意味着±扫描电镜5 (g)和4 (h)不同的样品。*:p < 0.05与控制;#:p < 0.05与受感染的组织没有pre-incubation ns - 398。
讨论
COX-2-derived代谢物炎症(有重要的调控作用25]。研究使用的肺癌细胞系(11- - - - - -13和老鼠26,27)表示一个杰出的免疫调节作用,cox - 2在肺炎。以来几乎没有研究,系统地分析了生物学中cox - 2的人类肺部发炎,我们使用了一个体外肺炎球菌感染模型(28新鲜的孤立的外围人类肺组织探索细胞特定类型cox - 2监管和功能。我们的模型系统的一个重要优势是不同肺癌细胞类型仍到独特的肺组织架构和特异性行为因此可以研究。居民细胞包括AMs仍存在于组织和有能力导致观察到的响应如图所示之前类似的模型(28]。然而,这个模型并不允许调查等方面的免疫免疫细胞从血液的招聘。此外,断开的肺组织血液供氧和气体交换只能适应部分赔偿的细胞培养条件。因此,炎症反应可能的影响,例如,细胞死亡的细胞凋亡和坏死。因此,一个24小时的时间内已经使用的乳酸脱氢酶释放和增加caspase-3激活观察(数据没有显示)。此外,不同的感染途径的感染模型自然由于细菌直接注入到肺组织,允许细菌绕过路线从气管肺泡。虽然这种方法不能反映自然感染途径它不过地允许直接交互的研究与肺泡间隔的细菌,揭示居民的炎症反应的细胞群。然而,从这个模型获得的结果的有效性应尽可能与样本肺炎患者相比,这在目前的研究也可以执行。此外,这样的人类肺组织样本的可用性是有限的,导致小尺度实验样本。这就是为什么强大的生物信号所需的具有统计学意义的结果。 We found significant and tissue-dependent growth of肺炎链球菌在人体肺部的诱导表达cox - 2 /铂族元素2营/轴,从而一定程度上调节bacteria-induced化疗- /细胞因子表达。介质诱导的面板是可比的研究调查在体外受感染的支气管上皮细胞系(29日]。
这项研究的结果证实肺炎双球菌能够诱导强烈的cox - 2的表达,而COX-1是表达起来从而感染肺仍不受影响。免疫组织化学显示cox - 2的表达在AMs,原子能委员会和血管内皮。这些发现进一步的相关性由原子能委员会的积极染色急性肺炎患者的肺。有趣的是,在肺泡上皮细胞,诱导cox - 2是几乎完全在II型而不是类型我原子能委员会。因为TNF-α/ IL-1β暴露肺组织产生了相同的模式,似乎合理的假设II型细胞,一般来说,炎症的重要肺泡上皮起搏器。肺炎球菌感染或细胞因子治疗后炎性环境也促进了cox - 2的表达在肺泡巨噬细胞和肺内皮。除了这些细胞类型我们偶尔观察到COX-2-positive基质细胞,这既不是1也不是pro-SP-C窖蛋白阳性。值得注意的是,类似的cox - 2的表达模式中看到猕猴急性重症肺炎在活的有机体内(30.]。我们发现肺炎链球菌地区没有发现和cox - 2阳性细胞反之亦然。这一发现表明cox - 2诱导不一定相关细胞的附件肺炎链球菌。因素在肺组织的上层清液从肺炎双球菌或可能促进cox - 2表达,支持我们的数据从TNF-α/ IL-1β-stimulated肺也表现出强烈的cox - 2表达相同的细胞类型。
感染的肺部组织化学抑制剂ns - 398年几乎完全封锁了铂族元素的释放2cox - 2主要产品。另外,我们观察到6-keto-PGF的生产1α和TXB2。然而,没有发现其他释放前列腺素类在我们的实验。先前的研究证明了这一点,铂族元素2似乎是主要的人类肺细胞产生的前列腺素类(31日]。由于铂族元素2由肺细胞会使中性粒细胞反应可能抑制中性粒细胞的促炎潜力,从而防止上皮损伤(31日]。
在体外实验先前建立的感应cox - 2在细菌感染取决于MAPK [11- - - - - -13]。符合X的研究u等。(28),我们观察到激活p38 MAPK在人类肺部肺炎球菌感染,而ERK已经激活控制肺部。抑制激酶的抑制肺炎链球菌全身的cox - 2诱导和随后的铂族元素2在人类肺部感染模型。在一些研究中铂族元素2是显示在一个积极的反馈回路调节cox - 2的表达,而其他的研究甚至公布了压抑的铂族元素的影响2(24]。在人类的肺,抑制cox - 2和铂族元素的直接刺激不同剂量2对cox - 2有任何影响,证明反馈回路是最有可能没有出现在人类的肺部组织。
铂族元素2施加其影响通过四个不同的前列腺素类受体(EP1ep4),显示细胞特定类型表达式(9),以前,我们已经证明莫拉克斯氏菌属复活感染导致upregulation EP2和EP4蛋白质在支气管上皮细胞(13]。此外,在肺炎链球菌来华的老鼠,EP的不足3是有利于细菌清除率和生存,突显出EPs在细菌感染的作用32]。完善,激活EP受体的铂族元素2随后改变细胞内营的水平,最后,可能导致炎症反应(9]。然而,无论是EP受体表达还是营代已被证明在pneumococcal-infected人类迄今为止的肺部组织。因此,我们调查了EP mRNA表达,展示低EP1ep3对EP水平和高水平4。虽然肺炎球菌感染周围肺组织没有改变本构EP4受体信使rna和蛋白质水平表达,特定受体受体激动剂EP4诱导在肺组织的显著增加,这可能会影响后炎症介质的调节肺炎链球菌感染。
几项研究已经证明了强化疗- /感染后细胞因子诱导炎性刺激,甚至肺炎链球菌,在体外以及在活的有机体内(15- - - - - -18,29日,33]。同样,肺炎球菌感染人类的肺组织也揭示了重要的感应TNF-α,IL-1β,gm - csf, PDGF, il - 10, IL-1RA, IL-15 IL-17。然而,其他介质,如白介素、引发,MIP-1αVEGF,未能被诱导,表明特异性表达在支气管间不存在在这个模型或中介调节的差异在人类的肺部组织本身。此外,它已经表明cox - 2 /铂族元素2通过诱导il - 10可能导致炎症控制,或抑制gm - csf, TNF-α,il - 12和PDGF表达吗在体外(15- - - - - -18,34]。符合这些研究cox - 2抑制导致显著诱导PDGF [18TNF-α[],但只是轻微上涨16,34)和gm - csf (15]。由于铂族元素的影响2已被证明在孤立的细胞类型的不同来源,小型或抵消细胞因子的调节肺泡间可能不是从整体强度和信号的肺部组织。此外,另一个可能的轻微影响抑制cox - 2可能是铂族元素的测量2主要是针对入侵的免疫细胞,这并不代表这个器官模型。
总之,使用外围人类肺组织感染体外与肺炎链球菌我们演示了MAPK-related cox - 2和随后的铂族元素的感应2释放。在II型肺泡cox - 2是诱导,而不是I型肺泡上皮细胞以及AMs和血管内皮。在人类的肺组织,激活EP4增加阵营。铂族元素2生产由肺细胞调节免疫细胞的功能,可能导致肺炎球菌病炎性介质的控制生产人类的肺。使用人类的肺组织需要进一步的研究来理解复杂的肺部炎症,尤其是II型pneumocytes所扮演的角色,并与细胞株和动物模型验证结果。
确认
d·斯托尔的优秀的技术援助和a·库恩的校对以及j . Lienau(所有在内科/传染病和肺药,柏林,德国),我将非常感谢。这部分工作将包括在而Szymanski博士论文。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明
本研究支持的跨地区协作研究中心的SFB-TR84德意志Forschungsgemeinschaft(授予交流Hocke C5和s Hippenstiel Z1a交流Hocke和Z1b公元Gruber)和德国联邦教育和研究(格兰特C8交流Hocke;进步——肺炎研究网络进化的遗传抗性和易感性严重脓毒症)。
感兴趣的语句
没有宣布。
- 收到了2011年10月26日。
- 接受2012年2月23日。
- ©2012人队