编辑:
哮喘是一种以炎症和气道重塑为特征的复杂疾病。在过去的几十年里,在了解哪些基因与哮喘的发展有关以及基因和环境因素之间的相互作用方面取得了巨大的进展。对遗传和基因表达谱的研究,以及单核苷酸多态性分析,有助于更好地理解哮喘的潜在分子机制。然而,最近对转座子和转座子遗传因子(TEs)的新调节功能的鉴定可能是帮助理解导致哮喘病理异质表现的遗传学的重要和新的关键。
大约45%的人类基因组由te组成[1].绝大多数te来源于被称为短、长分散核元件的遗传元件的逆转录转位、长末端重复超家族和含有te的基因组DNA的直接转位。以前被认为是垃圾DNA,现在越来越明显的是,TEs经常发挥调节和微调基因表达的功能[2,3.].te驱动的转录通常控制蛋白质编码基因的表达通过替代启动子,顺式调控非蛋白编码rna以及通过双链短rna的形成。Faulkner和Carninci[3.证明了te中启动子的转录起始是一种普遍现象,即使它们已损坏且不容易被识别为真正的转座子。此外,TE插入基因序列影响RNA稳定性和剪接变异[4,5].大约30%的人类mRNA包含至少一个逆转录转座子,mRNA水平被证明与逆转录转座子的百分比成反比[6].这些发现表明,te是蛋白质编码位点转录区域的内在成分,具有重要的调控作用。此外,这些新数据暗示了一个未知的控制机制,选择性和特异性地促进了细胞类型特异性的te积累。在基因结构水平上,TEs通过1)插入突变改造基因;2) DNA双链断裂修复;非等位基因同源元件之间的重组,3)缺失;4)重复;5)反演。te编码的蛋白质通常具有dna结合或修饰功能,如复制、断裂、连接和/或双螺旋的降解。然而,在错误的位置,te可能会导致(复杂的)疾病的发展。 Specific expression patterns of TEs in germ-line and cancer cells have been associated with numerous human diseases, usually due to novel insertions across protein coding exons [7].
哮喘是一种异质性很强的疾病。哮喘通常与特应性有关,但并不是所有特应性患者都有哮喘。一些哮喘患者随着年龄的增长症状会消失,而另一些患者则会在晚年患上哮喘。还有一些患者在儿童早期患上这种疾病,并终生遭受哮喘的折磨。此外,种族、性别和年龄影响哮喘的易感性和严重程度[8,9].我们如何解释这些不同的模式?一个具有挑战性的假设可能是,哮喘的异质性是由于te调节的哮喘易感性基因的差异。TEs不仅是遗传的,也可能是在一生中获得的。TE重复序列的数量在不同人群和个体之间存在差异。基因组不同部分TE序列的同源区域之间的重组促进了重复、缺失和倒置。人类群体之间甚至个体之间的逆转录转座子拷贝数变异(代表缺失和/或插入)证明了TEs的高度动态特性[2].te的动态特性,以及它们作为移动基因开关的作用,使它们成为解释哮喘表型异质性和复杂性的理想候选基因。TE动力学可以解释为什么哮喘患病率在过去几十年迅速增加。TEs还可以解释为什么人们会在一生中患上这种疾病。由于复制-粘贴机制,新获得的te将成为基因组的可遗传部分。然而,TEs的动力学是否可以被环境线索调节,还是纯粹随机行为,这仍有待确定。
到目前为止,已有12个哮喘易感基因被定位克隆(DPP10,CYFP2,HLAG,GPRA,SFRS8,PHF11,ADAM33,PCDH1)或全基因组关联(CH13L1,ORMDL3,PDE4D,DENND1B) [10].这些基因可能是te调控的哮喘易感性基因研究的首选起点。12种哮喘易感基因的表达已被证明是组织特异性的[10].如何确定组织特异性基因表达仍然是一个密切关注的问题,但一个显著的巧合是组织特异性的调节作用的te。因此,基因表达阵列可能是一种合适的筛查工具,以发现组织特异性哮喘基因。
重复的DNA元素确实可能影响儿童哮喘的发展。研究表明,微卫星DNA的遗传不稳定性存在于成人哮喘患者中,也存在于哮喘儿童中[11,12].历史上,白介素(IL)-3、IL-5和粒细胞-巨噬细胞集落刺激因子(GM-CSF)与哮喘的发展有关联,特别是,因为这些基因的表达已被证明在哮喘患者的几种细胞类型中上调,它们被认为是导致嗜酸性粒细胞增多的原因。有趣的是,IL-3, IL-5和GM-CSF在染色体5q31上共线,都是由相同的上游,但未识别的增强子调控的[13,但这一发现与te的新功能是一致的[6].在哮喘易感基因内或附近的te的存在可能作为这些基因的转录调节剂。因此,在健康对照和哮喘患者中,精确地确定TEs在哮喘易感基因中及其周围的位置和数量,并评估这些基因元素在转录组中的功能后果是很重要的。
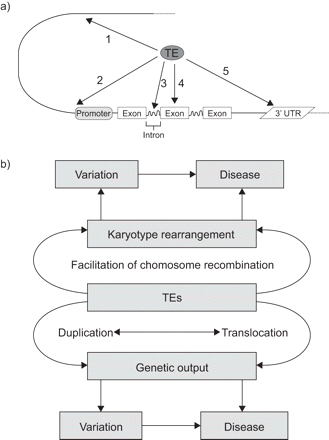
在健康和病变组织中检测te调控的转录组的最后一步是评估检测到的序列是否具有生物学功能。这里的主要问题是,在哮喘易感基因内部或附近的TEs是否调节这些基因的基因表达。这可以通过cap基因表达分析来实现,这种方法可以明确明确地确定基因的准确转录起始位点[6].一旦了解健康组织中受调控的逆转录转座子转录组,就可以将其与哮喘患者或其他复杂疾病的转录组进行比较。这将提供关于基因和基因表达模式以及它们如何与复杂疾病的发展和/或建立相关的前所未有的细节。te对表型(变异)和疾病的影响见图1.
a)转座子和转座子(transposable and transposed elements, TEs)对人类基因组结构的影响及其如何影响基因表达。TEs决定和微调mRNA的遗传输出和稳定性,因为它们的功能是:1)增强子;2)替代启动子;或者通过整合:3)进入内含子;4)外显子;5)转化为未翻译区域(UTR)。b) te在(复杂)疾病发展中的作用。由于扩增和/或易位,TEs可能在疾病易感基因内部或附近跳跃,并开始干扰正常的遗传输出。然而,te可能会促进基因重排,导致核型改变,导致基因组变异和/或疾病。
随着下一代测序和快速基因组和转录组分析的到来,TEs的动态特性及其在形成个体内和个体间变异中的作用可能很快就会得到解决。由于这些进展将以越来越高的分辨率分析te诱导的变异,它们将有助于更好地理解te及其对基因表达、人类健康和构成复杂肺病(包括哮喘)基础的(epi)遗传结构的总体影响。我们已经确定了上述12个哮喘相关基因中te的数量、位置和类型,我们正在哮喘患者中筛查相同的基因组。很可能哮喘的某些表型主要与免疫腔室te调控基因有关,而哮喘的其他表型则与肺组织细胞中一组特定的te调控基因有关。因此,对健康和疾病转录组的细胞和表型特异性理解可能会导致更好的治疗和个性化药物。我们希望鼓励肺部科学家进一步研究几乎完全未开发的TE领域,该领域整合了诊所、实验室和生物信息学。应该设想开发完整的新策略来治疗复杂的肺部疾病。
脚注
支持声明
M. Roth、M. Tamm和P. Borger获得了瑞士国家科学基金会的研究资助。
兴趣表
没有宣布。
- ©2012人队