摘要
成人肺移植是一种公认的治疗选择,然而对其对儿童生存的积极影响仍有争论。我们报告我们的经验前20年的儿童肺移植在一个单一的中心在奥地利。
Kaplan-Meier曲线估算了患者存活,器官存活和来自支气管炎障碍的自由。评估预移植后和移植后参数,并通过单变量试验和逐步多变量分析对患者和器官存活的影响。
43例患者共进行55例移植手术。移植后的1年和5年生存率分别为72.1%和60.6%,5年无闭塞性细支气管炎综合征的患者占52.6%。对不同移植时期的分析表明,随着时间的推移,移植的改善,在第二个十年的5年生存率为70.6%。新药物他克莫司对移植前糖尿病和免疫抑制有积极作用,而移植前住院治疗有消极作用。再次移植成功率高,延长了患者的总生存率。
肺移植已成为成人终末期肺病患者可接受的治疗方法,但在儿科人群中仍有争议[1- - - - - -3.].自1983年实施环孢菌素后第一个成功的肺移植以来,全球肺移植数量增加到每年约2,500日[4].在20世纪90年代甚至今天只代表了少数总程序,甚至今天只有少数计划,每年占全球大约80个程序[5].因此,儿童的移植被保留给一个非常少量的中心,只有30到40所机构报告儿科肺移植[5].原因是多方面的,包括捐助者和受援者都缺乏,发展儿童肺移植中心需要投资,以及对结果的怀疑。
肺移植后的存活率仍远低于其他实体器官移植,但在过去几十年已有所增加[2,5- - - - - -7].据反复报道,儿童和青少年这一亚组的结果较差[3.,6- - - - - -8],引发了对肺移植对这些患者生存的有利影响的持续讨论[2,3.,6].
维也纳医科大学(维也纳,奥地利)的胸外科部门是欧洲最大的肺部移植中心之一,全球每头部移植率最高(每百万居民14.1百百万居民)[9].1990年,在儿科和青少年医学院治疗的青少年囊性纤维化(CF)患者的第一次肺移植是在1990年进行的。从那时起,我们的儿科部门在肺移植前后都有43名患者。
本研究描述了奥地利一中心的前20年的儿科肺移植的经验。我们评估了患者和移植物存活,并分析了哪些协变量对程序的结果产生影响。
材料和方法
该研究由当地伦理委员会批准,并由奥地利的所有参与者提供书面同意。
患者集体
该研究人群包括在移植前参加了儿科和青春期医学部的所有肺移植患者,从1990年4月到2010年1月开始。大多数患者在我们的中心接受了移植后护理;然而,一些患者在重症监护病房中死亡,其他患者在各自的祖国或当地成人移植病房中收到了他们移植后护理的一部分。所有移植均在维也纳医科大学的胸外科部进行。
我们的患者队列包括12名年轻人(移植时年龄>为17岁),这是因为所有CF患者(不计年龄)直到1995年都是在儿科接受治疗的。
由于维也纳位于奥地利东部边界的地理位置,我们的患者人群中有很大比例(n=11)的外国儿童和青少年,他们的社会和医疗背景非常不同。自2003年首例意大利儿童移植以来,共有11名来自国外的患者在我们中心接受了移植,其中包括匈牙利、意大利、捷克共和国、德国、罗马尼亚和希腊。这些儿童的移植选择和准备工作是在各自的祖国进行的。在维也纳,只有4名病人接受了移植后护理,5名病人接受了共同护理。两名儿童仅在当地中心接受了长期随访。由我们外科移植但在移植前未在我们儿科病房就诊的国外青少年患者不包括在本研究中。
研究了参数
我们评估了移植前和移植后的各种参数,并将这些数据纳入详细的患者登记中。移植前参数包括患者年龄、性别、体重指数(BMI)、潜在疾病、国籍、肺功能、细菌感染、巨细胞病毒(CMV)状态、预形成抗体和糖尿病,以及移植时有创通气和住院情况。围手术期参数包括移植程序的选择,体外膜氧合(ECMO)的实施,缺血时间,交叉匹配,免疫抑制和诱导治疗。术后因素为重症监护时间、移植后住院总时间、闭塞性细支气管炎综合征(BOS)和其他移植后并发症(肾功能损害、淋巴增生性疾病和神经系统并发症)的发生,以及移植物衰竭和死亡的原因。
统计分析
计算Kaplan-Meier曲线以估计来自BOS,患者存活和器官存活的自由。对所有预先和亚过分植物参数的测试进行(移植前4个月内)以鉴定移植后生存和博斯的危险因素。这是由单变量的Cox回归模型进行,用于每个终点的第一次移植:患者存活,移植存活和来自BOS的自由。最后,针对单变量分析中的每个终点核算计算了多个扩展Cox回归模型(P <0.05)。所有分析都使用SPSS版本17.0(SPSS Inc.,Chicago,IL,USA)或R 2.9.2进行www.r-project.org.).
移植程序
手术方法是单侧或双侧前外侧胸廓切开术或双侧胸廓切开术,横向胸骨切开术(蛤壳技术)。自2001年以来,术语术中均已应用于大多数患者(69.8%),如a报道Igner.等等。[10].平均缺血时间(双肺移植的第二肺)为335.3±72.7分钟。
移植时的免疫抑制包括皮质类固醇(100%),抗增殖剂(偶氮嘌呤18.6%和霉酚酸酯MofeTil 79.1%)和钙调素抑制剂(环孢菌素A 46.5%和Tacrolimus 53.5%)的不同组合。在15名患者中,在术后课程期间切换免疫抑制。其中,五(11.4%)在移植后某个时间点接受雷帕霉素。在大多数患者中进行诱导,在54.8%和抗白细胞介素-2受体抗体中使用Antrithymocyte球蛋白,9.5%。再移植后,一名患者接受抗CD3抗体。
CMV预防用CMV超微母球蛋白进行一次,每周进行一次移植后4周,持续3个月。自2006年以来,在高风险患者(CMV阳性供体,CMV阴性受体)中,在整个第一次移植后的预防年度已经给出了甘昔韦尔预防。
结果
43例患者(男22例,女21例)共55例移植(双肺31例,单肺6例,双叶8例,单侧叶2例,裂肺7例,心肺1例)。进行了两例活体供体移植。在分析时,21例患者死亡(其中3例在再次移植后),8例再次移植,2例再次移植。
平均值±SD.第一次移植的年龄是15.0±7.1毫升,范围为6个月至30.4岁。31(72.7%)患者18岁,10(23.3%)为18岁(23.3%)。移植最常见的原因是CF(56.4%),然后在第一次移植后的博斯(21.8%)。介绍了移植的适应症表1.在32个月(2天至144个月的中位数后进行再移植进行。
几乎一半的患者(40%)在移植时需要住院治疗,25%的患者需要有创通气。5例患者接受体外膜肺氧合移植。本文详细列出了所有移植手术前后的因素表2.根据不同移植时期的病人特征在表3.
30天移植存活率为89.1%;早期死亡或移植物失败的原因是多器官衰竭,原发性移植衰竭,脑内出血,脑内梗死和急性排斥反应。总随访期间最常见的死因是感染和博斯(28.6%)。其他原因是脑内出血/梗死和急性排斥(9.5%),以及心脏并发症,肺出血,初级器官衰竭,癌症和多器官衰竭,每次患者(23.3%)。我们没有观察到潜在疾病的复发,尽管我们的队列包括患有(可能)免疫介导的疾病的八名患者(特发性肺纤维化,特发性肺癌,移植物相对宿主病和原发性肺动脉高压)。
移植后5年,66.7%的患者肾功能受损(轻度46.7%,中度76.7%),其中9例(20.1%)患者在移植随访期间需要透析。14例(32.6%)患者出现脑栓塞、脑出血、后天性可逆性脑病综合征、癫痫发作等神经系统并发症,无移植后增殖性淋巴细胞增生性疾病。一名患者发生了肺腺癌。
所有43名患者的中位存活估计(卡普兰 - 迈耶)为112个月(95%CI 65.6-158.4),范围从2天至201个月(无花果。1A).移植后的1-,5-和10-YR患者存活率分别为72.1,60.6和38.9%。
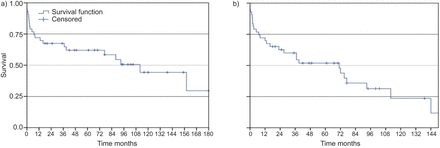
a)患者存活(n = 43)。中位生存期为112个月,1-,5-和10 yr患者存活分别为72.1,60.6和38.9%。b)移植存活(n = 55)。中位存活率为71个月,1-,5-和10 yr器官存活分别为70.9,51.2和15.0%。
所有55例移植的中位估计存活时间为71个月(95% CI 26.2-115.8),范围从2天到158个月(无花果。1B.).1年、5年和10年的移植存活率分别为70.9、51.2和15%。再移植的移植物生存期(中位生存期76个月;95% CI 22.2-115.7)与原发移植相当(中位生存期71个月;95%可信区间0 - 206.6)。
在移植后1-和5-YRS的96.3和53.8%的患者中报告了来自博世的自由。博斯出现的中位时间为48个月(95%CI 29.8-66.2)。博斯出现后的中位移植存活是31个月(95%CI 13.9-48.1)。
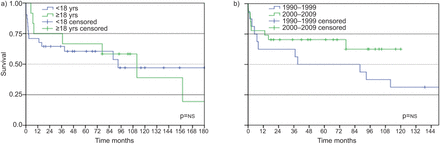
在31例首次移植时年龄小于18岁的患者中,结果与总样本具有可比性。中位患者生存期为93个月,中位器官生存期为39个月(95% CI 0-88.4) (无花果。2A).1-和5-YR患者存活率分别为71和57.1%,分别为1-和5-YR器官存活率71和42.9%。分别在移植后94.1和52.6%1-和5-YRS中观察到BOS的自由。博斯的中位时间为40个月(95%CI 30.4-49.6)。
根据a)在第一次移植和b)移植时代的患者存活率(1990-1999相对2000-2009)。a)在6个月至17岁至17岁的儿童中,存活率为93个月,分别为71%和57.1%。在18-30岁的成年人中,中位数存活率为112个月,分别为75%和66.7%。b)1990 - 1999年,中位生存率为39个月,分别为62.7和50.0%。2000 - 2009年,中位存活率不可用(由于少数事件),1-和5-YR存活分别为77.8%和70.6%。ns.:不重要的。
在比较不同观测时期(1990-1999年)的结果时相对2000-2009),在第二十年中出现了更好的结果趋势(无花果。2B.).中间移植存活从37个月增加到75个月(95%CI 25.5-124.5)。1 yr器官存活率从62.7%增加到77.8%,5年份存活率从43.8%增加到52.9%。发现患者存活率相同的趋势(1-YR存活:62.7至77.8%; 5-YR存活:50至70.6%)。然而,这些差异没有统计学意义。从移植后5岁的博斯的Freddom从14.3增加到75%(p = 0.019)。博斯的时间从39至81个月(不显着)的中位数增加。
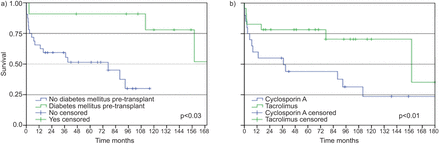
移植前糖尿病与患者显着更好的患者(p = 0.007),但没有器官存活,以及增加的5 yr患者存活率(47.8相对90.0%, p = 0.023) (无花果。3A).这种效果持续存在于多变量分析中。
根据a)移植前糖尿病和b)钙调磷酸酶抑制剂(环孢素a相对他克莫司)。a)预移植糖尿病中位数存活(少量事件),1-和5 yr存活分别为90.9%和90.0%。没有预移植前的糖尿病中间生存率为77个月,1-和5 yr存活分别为65.6和47.8%。b)环孢菌素中位生存率为39个月,分别为62.7和50.0%的生存率分别为62.7和50.0%。Tacrolimus中位数存活(由于少量事件),1-和5 yr存活分别为77.8%和70.6%。
在接受较新免疫抑制药物Tacrolimus的患者中,与在单孢子素A(CSA)治疗的患者中,观察到更好的患者存活率。据报道了中位数患者(P <0.03)(无花果。3B.)和器官存活(边缘线,P = 0.049),以及5年的患者(P <0.01)和器官存活率(边界,P = 0.056)。我们还观察到患者在Azathioprine过度霉菌霉素的不显着优势(37相对158个月)和器官存活率(12相对72个月)。近年来,CsA和霉酚酸酯的使用越来越频繁;因此,其他未评估的时间相关参数可能与结果相互影响。
此外,在单因素分析中,移植时住院是一个重要参数。需要住院治疗的患者(40%)的1年移植生存率低于在家治疗的患者(p=0.009)。这一效应在5年生存率中没有出现,这在两组中是相似的。在移植前进行有创通气(25%)的患者中也发现了类似的趋势(1年移植生存率50相对76%),但这仅显示出边缘性显著性(p=0.06)。
我们发现,患者年龄、基础疾病(CF)等参数对移植后BOS发生、患者和器官生存无统计学意义相对非cf)、国籍、移植类型、肺功能(强迫肺活量、1秒内强迫呼气量和平均最大呼气流量)、BMI、细菌定植(Burkholderia cepacia,金黄色葡萄球菌和铜绿假单胞菌),等待名单的时间,交叉迁移,预先形成的抗体存在,对Ecmo的移植,诱导治疗,CMV状态或术中的缺血时间。
在多变量分析中,发现糖尿病和具有巨饰血症的免疫抑制对患者存活(P = 0.033)产生阳性影响,而对于器官存活率和来自BOS的自由度没有鉴定出独立的危险因素。
讨论
在我们中心的儿童,青少年和年轻成人中分析前20年的肺移植,我们观察了112个月的中位数估计总患者存活率。移植后的1-,5-和10-YR患者存活率分别为72.1,60.6和38.9%。根据移植的不同时代数据分层(1990-1999相对2000 - 2009年)朝着改善移植和器官存活率的指向,多年来减少了博斯的出现,第二十年的5岁生存率为70.6%。此外,已显示移植前糖尿病和较新的免疫抑制剂的糖尿病与改善的存活相关,而移植前的入住前患者的入学率与单变量分析的早期存活率下降有关。
我们的研究结果超过了2010年国际心肺移植协会(ISHLT)的全球研究结果(5年生存率:1990-2008年,48%;2002 - 2008年,52%)5].分析大型单一中心的数据我们显示了可比的结果:汉诺威,2009:1-YR存活69%,5 yr Survival 44%[7];伟大的奥蒙德街医院(英国伦敦),2004年:1994年的5-YR生存27%,最近的时代57%[11];圣路易斯儿童医院(圣路易斯,莫,美国),1990-2002:1-YR生存77%,5 yr Survival 54%[12];苏黎世,1992-2007年儿童和成人:1年生存率86%,5年生存率68% [2].同样,多年来的改善也已在其他儿童和成人肺移植的报告中得到证实[2,5,11].然而,由于我们的样本具有各种特殊特征,因此很难将我们的结果与其他肺移植中心进行比较。
首先,我们患有越来越多的海外患者,移植前后的共用程度不同。这在很多方面都是挑战。现场预移植评估,特别是关于心理社会方面,因语言障碍而受到时间和质量的限制。语言障碍还使在我们的移植中心发生的早期移植后护理。长期随访是患者祖国的共享或当地护理;在这一时期,大多数问题都产生了有限的进攻单元,不同的医疗中心和财务问题之间的沟通问题。与居住在奥地利的患者相比,我们展示了外国患者的类似短期存活;然而,长期数据仍然缺失并且往往难以获得。
其次,我们有很高的危重儿童比率,这表明在移植前必须住院治疗(40%)、有创通气(25%)或ECMO(12.4%)的患者比例很高(表2).这可能会在我们的队列中的第一个移植后一年中的死亡率相当高。事实上,我们表现出统计上显着下降的1毫升在移植前患者入院(P <0.01),以及侵入式通风(边界意义)的患者。这符合描述预移植前机械通气的其他报告,是成人和儿童发病率和死亡率的显着危险因素[5,13,14].
第三,我们有很高比例的患者接受了再次或再次移植(23.3%)。在一些严重原发性移植物功能障碍、严重无法治疗的急性排斥反应和晚期BOS病例中,再移植仍然是唯一的治疗选择。然而,由于捐献器官的缺乏和不确定的结果,它的价值受到了质疑。对我们的高再移植率的一个解释可能是奥地利的捐赠立法(假定同意制度),导致了相当好的器官供应[15].总体而言,儿科重新移植数量低,自1994年以来仅在全球范围内进行了74个小儿移植[5].重复移植据报道,与儿童和成人的原发性移植相比,生存率较差[16- - - - - -20.].在我们的中心,先前已显示重新移植在选定的成年患者中具有良好的存活率[21.].此外,在目前的研究中,我们报道了再次移植后的儿童受者的存活率与初次移植后的存活率相当。这就增加了患者的总生存率,从而获得了很好的长期生存率。
最后,我们的样本涉及在该计划的第一年移植的一些年轻人,这是由于当时的成人CF患者缺乏护理中心。当我们计划作为单一中心分析的研究时,我们决定将这些患者纳入一般分析。儿童和年轻人之间的结果没有显着差异。
我们报告了在第二十年中移植的患者的更好结果的趋势。然而,在2000年后移植后的5 yr发生后的BOS的发生显着降低,患者存活率的增加也没有进入移植存活表现出统计学意义。有几个因素可能有助于这些结果,包括多次依赖性因素(诱导治疗,免疫抑制和抗微生物治疗,移植技术,涉及护理员的重症监护者)在随访期内变化。此外,小患者数字可能限制统计分析。在ISHLT的年度登记处,其中包括来自全球所有小儿移植的数据,仅在过去几年中显着提高了生存率率[5].在我们的队列中,患者移植在移植程序的第一和第二时代(表3)在年龄,潜在的疾病,移植比例对ECMO,免疫抑制治疗,强制呼气量,1 s和假单胞菌殖民化。其中一些因素,例如新的免疫抑制药物,可能对结果产生积极影响,而其他因素可能会产生积极的影响,而其他因素则可能会损害生存率。
有趣的是,对于在移植前患有糖尿病患者的患者的单变量和多变量分析中发现了一个显着更好的患者生存。这已经报道了[2,3.];然而,这种观察的原因并不完全清楚。胰岛素治疗的另一个未知的有益效果[2]如果在移植前移植前表现出糖尿病,则对移植后存活率的严重效果较小,与移植后的新发生[3.已经讨论过了。
在许多移植中心中,使用躯干和霉酚酸酯Mofetil已经取代了CSA和Azathioprine,尽管存在一致的数据在对另一个药物治疗儿科肺移植受者的情况下缺失[22.- - - - - -25.].在我们的队列中,我们发现较新免疫抑制药物CSA的生存态度明显的积极影响,也可能也是霉酚酸酯的MoFetil。这些药物的使用随着时间的推移没有均匀分布,具有巨积司和霉酚酸酯Mofetil在后来使用的更常见。随着Tacrolimus的有益效果在多变量分析中证实,其优势似乎只是一种用于更新的移植患者更好的结果的标记。但是,不能排除与随时间变化的其他未评估参数的交互,不能排除。
没有随机试验评估肺移植的存活效果,因此需要通过统计建模来接近结果[26.].2008年,李借据和C.一座山丘[27.]使用来自美国CF基础患者登记处和器官采购和移植网络的数据进行了研究。作者使用多种临床协变量和这些协变量与肺移植的相互作用应用了比例危险模型,作为时间依赖的协变量。他们表示,评估的大多数患者(514名患有CF的儿童)随移植的死亡风险增加,而只有<1%的患者显示出现清单[27.].然而,若干作者质疑此结果,并在儿科肺移植后显示出清除的存活效果[28.- - - - - -30.].
儿科数据中关于存活益处的相互矛盾的数据构成了器官移植的一般伦理问题,如供者权利、病人分配、再移植和活体供者移植。这方面的一个重点是通过移植改善生活质量(QoL),这是除生存益处之外的一个重要参数。不幸的是,关于生活质量的数据,特别是在肺移植后的儿童年龄组,是稀缺的[31.- - - - - -33.].因此,需要从器官功能数据中得出结论。根据ISHLT登记,幸存者的功能状态非常令人满意,大多数报告没有活动限制[34.].根据我们的经验,尽管有大量的并发症,特别是在移植后的头几个月,如果患者能在术后早期存活下来,生活质量一般会有相当明显的改善。我们的患者一般生活比较正常,只要肺功能不受BOS的明显损害,就可以上学,参加体育活动。心理问题,如恐慌发作或抑郁,经常在移植后的头几周内观察到,通常在患者病情好转时减弱;然而,这仅仅反映了个人经验,并没有在我们的研究中进行系统的评估。
我们研究的另一个限制是小患者数量,这减少了统计分析的力量。我们专注于预移植前参数的准确性,仅在移植前4个月内包括数据。这导致某些患者中缺少数据,从而进一步限制分析。低患者数是用于评估小儿移植的一般障碍。根据2008年的ISHLT注册表,其中36个中心报告儿科移植,每年只报告五个以上的程序[5].有关儿童肺移植的文献主要包括单中心描述性研究,患者相对较少。因此,迄今为止,儿童肺移植领域的大多数建议和实际处理都是基于成人肺移植或其他实体器官移植数据的推断,而这往往是不可行的。因此,在未来,多中心研究对提供信息至关重要,特别是在肺移植的不同的儿科方面,如发育参数、生活质量或应用药物的药代动力学。
脚注
通过回答有关本文的问题获得CME认证。你可以在本刊印刷版的背面或网上找到这些资料www.www.qdcxjkg.com/misc/cmeinfo.xhtml
兴趣表
没有宣布。
- 已收到2011年5月31日。
- 接受2011年11月29日。
- ©2012年