摘要
具有正常肺功能的个体的人类呼吸道保持细微调节的平衡,在上呼吸道中的正常微生物群和较低的道路中的无菌渐变。这种平衡可能被暴露于诸如香烟烟雾的侮辱。在呼吸道中,吸入卷烟烟雾的复杂和有害性质改变了所有解剖学水平的宿主微生物相互作用动态,在许多情况下引起感染。此外,连续暴露于卷烟烟雾本身对宿主引起有害影响,可以引发慢性呼吸系统疾病的发展,例如慢性阻塞性肺病(COPD)和肺癌。COPD是一种不可逆转的气流梗阻,通过机会性病原体,纤维化,纤维化,粘液粘膜的渗透性和持续的较低气道的持续定植。COPD患者保持稳定(不加剧),但病情逐渐恶化,并且在大多数情况下患有周期性的恶化,在大多数情况下引起的感染。虽然吸烟和吸烟相关的疾病与感染风险很高,但大多数疗法旨在减少炎症参数,但不一定考虑到持久性殖民者的存在。讨论了香烟烟雾对呼吸道中的宿主 - 病原体相互作用动力学的影响,以及电流和新的疗法。
暴露于卷烟烟雾对人体呼吸道的影响
人类呼吸道的一般特征
人的上呼吸道由呼吸微生物群从出生中殖民。殖民者是共同的微生物和/或机会主义病原体[1].微生物包围人呼吸道菌群是高度适合于主机,并已用于几种人类限制条件致病菌,如描述于共同进化的实例Neisseria Meningitidis.那淋球菌和莫拉克斯氏菌属复活[2].相反,具有正常肺功能的个体的下呼吸道是无菌的。肺不育的维持在生理学上相关,鉴于肺部是肺部发生的区域。物理,解剖和机械屏障,包括鼻毛,咳嗽和粘液自动架,构成第一道防线,避免微生物进入下部道。粘液自动扶梯是肺组织上方的水合层,即与粘液结合在呼吸上皮上存在的粘液,是外来颗粒和入侵病原体的捕获和去除系统[3.].肺泡上皮由I型和II肺细胞组成。I型肺细胞具有解剖功能;通过覆盖95%的肺泡表面,它们在肺泡空间和血管之间产生薄壁。II型肺细胞,尽管仅占肺泡表面的5%,比I型肺细胞的数量更加丰富[4.]. 肺细胞在肺防御中起着至关重要的作用:1)通过合成、分泌和重吸收肺表面活性物质,维持低的肺表面张力,阻止气体交换表面粘在一起;2) 水和钠的运输;3) 外源化合物的代谢;4) 肺再生;5) 模式识别受体识别病原体相关分子模式(PAMP);6) 抗菌肽的分泌;7) 分泌细胞因子和趋化因子,协调宿主炎症反应;8)通过上皮细胞之间的紧密连接形成病原体进入的屏障[5.-9.]. 肺泡巨噬细胞是驻留在肺中的专业吞噬细胞,负责通过吞噬作用和吞噬溶酶体处理清除微生物。肺泡巨噬细胞也会分泌炎症介质,必要时引导中性粒细胞从血流向肺泡腔募集[10.].此外,气道细胞产生的可溶性分子的曲目,这些分子是下部小型微生物间隙中的必要球员。这些分子存在于呼吸道表面的水性流体中,包括补体系统,抗微生物肽,溶菌酶,乳蛋白,分泌白细胞抑制剂(SLPI),表面活性剂蛋白(SP)-A和SP-D [11.].
精心安排以保证肺泡无菌性的精细平衡在宿主持续暴露于环境中存在的有害颗粒和气体时被改变。在这篇综述中,我们将重点关注持续接触烟草的有害影响,以及这种有毒物质对呼吸菌群的影响。
香烟和烟草烟雾:功能和组件
香烟由一种烟草混合物和一张有明确规格的纸组成。大多数香烟都有过滤嘴和烟嘴。尖端通风意味着主流烟雾被稀释与确定数量的空气在一口。烟草混合物、卷烟纸、过滤嘴的类型和效率、尖端通风程度决定了卷烟烟气的化学成分。当吸烟时,一种复杂的混合物被吸入呼吸系统。从点燃香烟到吸入一缕烟雾的过程中,会发生各种重叠的化学、物理和生理现象,即燃烧,热解,吡咯化合,蒸馏,升华和缩合过程[12.]. 烟草烟雾是一种气溶胶,由气相中的固体和液滴(微粒(“焦油”)相)组成。在新鲜烟草烟雾中已鉴定出大约4700种不同的物质。这些包括中性气体、碳氧化物、氮氧化物、酰胺、酰亚胺、内酰胺、羧酸、内酯、酯、醛、酮、醇、酚、胺、挥发物N-Nitrosamines,N-杂环,碳氢化合物,腈,酸酐,碳水化合物,醚,硝基化合物,金属和短/长寿命的自由基。一根香烟的主流烟雾中所含成分的数量从毫克(水、一氧化碳、二氧化碳和尼古丁)到微微克(杂环胺和重金属)[12.]. 吸入颗粒物根据颗粒大小沉积在呼吸道中,较大颗粒沉积在上部和较大气道中,较小颗粒深入肺泡腔。这种微粒物质清除无效会导致微粒滞留在肺组织中,导致慢性低度炎症,这可能在与长期吸烟相关的慢性肺部疾病的进展中起重要作用[13.].除了化学品,还在香烟中记录了微生物的存在。所有烟草都是治愈的,在此期间有多种细菌和真菌的快速增长,以及微生物毒素的积累。在新鲜和固化的烟草叶中发现了嗜苯胺的细菌。一系列额外的细菌和真菌在少量中被发现;此外,在高湿度下储存香烟导致香烟烟草中的真菌水平升高,导致烟雾中的Ergosterol浓度增加[14.].此外,基于卷烟的研究的细菌偏心组揭示了15种不同的细菌和广泛的潜在病原体(不动杆菌那芽孢杆菌那伯克德利亚那Clostridium.那克雷伯氏菌那假单胞菌铜绿假单胞菌那Serratia.那弯曲杆菌那肠球菌那蛋白质和葡萄球菌)[15.那16.].潜在病原体从吸入主流烟雾感染的风险目前未知。
与烟草吸烟有关的病理学:概述
吸烟烟草造成所有肺癌的90%,是中风和心脏病发作的重要风险因素。吸烟也被认为是儿童和成人的各种呼吸道和全身感染的危险因素,包括普通感冒,流感,肺炎和结核病[17.].重要的是,吸烟是慢性阻塞性肺病(COPD)的主要危险因素。慢性阻塞性肺病的特征是缓慢进行性和不可逆的气流阻塞,肺组织丧失导致肺气肿和组织重塑(纤维化),这两者都有助于进一步的肺功能下降,降低生活质量和高死亡率[3.那18.].烟草烟雾中的有害颗粒和气体引发免疫系统的变化,导致炎症细胞浸润和明显的慢性肺部炎症。这进而导致其他病理改变,包括慢性阻塞性支气管炎伴纤维化和小气道阻塞,肺气肿伴气腔扩大和肺实质破坏,肺弹性丧失和小气道关闭[19.那20.].吸烟还会导致致病菌和病毒引起肺部感染,这是COPD急性恶化的主要诱因[21.].加剧是由COPD引起的发病率和死亡率的额外主要因素,以及与疾病相关的医疗保健费用的主要来源[22.-24.].
与COPD进展相关的分子和细胞机制
吸烟对气道免疫功能的影响在慢性阻塞性肺病中已被广泛描述,并在图1[19.那25.].慢性阻塞性肺病的进展与腔内炎性粘液渗出物的积累以及固有和适应性炎性免疫细胞对壁的浸润有关;这些变化与修复和重塑过程相结合,最终使气道壁增厚[26.].长期吸烟的额外后果是通过机会性病原体的较低呼吸道持续的殖民化,这通常对疾病的进展进行了扩增作用并有助于[27.那28.].
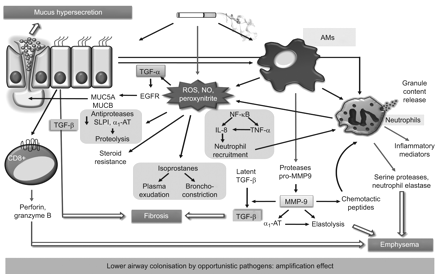
慢性阻塞性肺疾病进展的分子机制慢性阻塞性肺病进展的三种主要宿主改变特征:纤维化、肺气肿和粘液分泌过多。COPD进展的第四个特征是条件致病菌在气道下定植(见下图)。微生物持久性是相关的,因为它极大地促进了慢性阻塞性肺病特征的有害放大。图中显示了参与COPD患者气道的主要宿主细胞、上皮细胞、肺泡巨噬细胞(AMs)、中性粒细胞和CD8+淋巴细胞。香烟烟雾激活上皮细胞产生炎症介质,激活和/或招募AMs和中性粒细胞。上皮细胞还分泌局部纤维化诱导转化生长因子(TGF)-β。由上皮细胞和AMs产生的趋化因子激活CD8+淋巴细胞,释放出肺气肿介质穿孔素和颗粒酶。AMs分泌中性粒细胞趋化剂并释放蛋白酶。基质金属蛋白酶(MMP)-9可以直接或通过α激活纤维化诱导因子TGF-β并引起弹性溶解1- 钛合金(AT)失活。由AMS和中性粒细胞产生的蛋白酶促进肺气肿。与蛋白酶一起,中性粒细胞分泌炎症介质和颗粒含量。中性粒细胞趋化物由AMS和上皮细胞直接产生,并通过AM蛋白酶MMP-9的酶活性产生。COPD患者气道显示氧化应激。香烟烟雾本身含有高水平的活性氧(ROS),ams和中性粒细胞均响应香烟烟雾增加呼吸爆发。高浓度的ROS和反应性氮物质具有多种后果:1)减少防滴发酵酶防御和蛋白水解;2)核因子(NF)-κB和中性粒细胞招募的激活;3)类固醇抗性;4)增加等前己烷生产; and 5) mucus hypersecretion. SLPI: secretory leukoprotease inhibitor; IL: interleukin; TNF: tumour necrosis factor; EGFR: epidermal growth factor receptor; NO: nitric oxide; MUC: mucin.
香烟烟雾对粘液纤毛系统有有害影响,通过促进纤毛跳动频率降低、纤毛上皮脱落、杯状细胞增多、粘膜下腺肥大和鳞状细胞上皮化生[29.].吸烟还会损害上皮连接,这是由于与紧密连接形成有关的基因(如occludin、ZO-1和claudin-1)的显著下调,导致了转上皮细胞抗性的降低,而后者与上皮细胞通透性的增加相关[30.那31.].
香烟烟雾激活呼吸道上皮,导致炎症介质(肿瘤坏死因子(TNF)-α、白细胞介素(IL)-1β、粒细胞-巨噬细胞集落刺激因子、白细胞介素-8和白三烯(LT)B)的产生4.),负责激活和/或募集肺泡巨噬细胞和中性粒细胞。几项研究表明,肺实质和COPD患者的外周和中心气道中的中性粒细胞,巨噬细胞和T淋巴细胞的总数增加了[20.那32.].小气道中的上皮细胞还分泌转化生长因子(TGF)-β,诱导局部纤维化[19.]. 众所周知,香烟烟雾诱导上皮细胞死亡,这也放大了正在进行的炎症反应[19.].关于香烟烟雾对通过气道上皮细胞产生抗微生物分子的影响,发现来自COPD患者的刷式支气管上皮细胞中的抗微生物肽人β-DECENSIN(HBD)-2的表达被发现低于来自组织健康的科目[33.];此外,与不吸烟者相比,吸烟者的SP-A和SP-D水平显著降低[34.].由香烟烟雾激活的肺泡巨噬细胞分泌炎症介质的曲目,其中一些(IL-8,生长相关的癌基因α,LTB4.单核细胞化学蛋白-1)是中性粒细胞趋化剂[19.].肺泡巨噬细胞显示出呼吸爆发和释放弹性酶的增加,包括基质金属蛋白酶(MMP)和组织蛋白酶K,L和S.这些酶,特别是通过增强中性粒细胞释放的弹性蛋白酶的作用有助于肺泡肺气肿[19.].尽管吸烟者的炎症反应与非吸烟者显然不同,但香烟烟雾对肺泡巨噬细胞和单核细胞的表达的表达响应于其配体的肺泡巨噬细胞和单核细胞的影响目前尚不清楚[35.那36.]. 由于上皮细胞和巨噬细胞释放的化学吸引物水平升高而招募的中性粒细胞显示呼吸爆发增加,并因脱颗粒而分泌丝氨酸蛋白酶(中性粒细胞弹性蛋白酶、组织蛋白酶G、蛋白酶3、MMP-8和MMP-9)。三肽脯氨酸-甘氨酸-脯氨酸(PGP)(和N-acetylated form of PGP)是一种选择性中性粒细胞趋化剂,由细胞外基质蛋白通过MMP-8和MMP-9催化的酶促反应产生。英国网球协会4.水解酶(LTA.4.H)通过中性粒细胞和上皮细胞产生的具有双重功能。它生成LTB.4.并且它具有氨肽酶活性,从而灭活PGP,这有助于在急性肺部感染中的嗜中性炎症的分辨率,一旦病原体不再存在。烟雾抑制LTA4.H氨基肽酶活性并通过乙酰化稳定PGP;以这种方式,中性粒细胞迁移到肺部增加,导致持续炎症[37.]. 香烟烟雾暴露也会抑制中性粒细胞caspase-3样活性,最终损害其吞噬活性[38.].重要的是,卷烟烟雾暴露会导致肺泡巨噬细胞和中性粒细胞吞噬活动的损害[39.-42.].
氧化应激是一种不平衡,当反应性氧物质(ROS)不能通过抗氧化剂防御机制(酶保护机制:过氧化氢酶,超氧化物歧化酶,谷胱甘肽过氧化物酶,等等。;非酶防御机制:谷胱甘肽(GSH)、抗坏血酸盐、尿酸盐、等等。)并导致有害影响[19.].氧化应激在吸烟相关疾病的病理生理学中起着关键作用[43.-45.].来自香烟烟雾本身的ROS(气相估计含有> 1015.自由基 [46.])由炎症细胞(由香烟烟雾引起的肺泡巨噬细胞和中性粒细胞呼吸爆发)产生的炎症和破坏性损伤效应[43.].这些影响包括:1)蛋白酶活性的整体增加导致肺气肿;2) ros诱导的核因子(NF)-κB活化导致炎症反应放大,导致IL-8和TNF-α分泌增加,随后中性粒细胞募集;3)类固醇抵抗(见后面);4)花生四烯酸氧化增加,产生异前列腺素,引起支气管收缩和血浆渗出;5)激活TACE (TGF-α转化酶),促进TGF-α的脱落和表皮生长因子受体(epidergrowth factor receptor, EGFR)的活化,导致粘蛋白(mucin)表达增加(MUC5AC和MUCB.)基因和粘液分泌细胞的分化[19.].脚杯细胞的分化通过EGFR活化和粘液分泌也受IL-13刺激[47.].过量的粘液产量有助于COPD中小气道的闭塞。独立地,ROS也激活C-Jun N末端激酶通过SRC,触发MUC5ACEGFR独立的方式表达[48.].
香烟烟雾也对宿主自适应免疫产生影响。已经显示出吸烟可以减少人类中的免疫球蛋白(Igs)的血清水平[49.那50.].此外,COPD患者肺实质及外周、中央气道的t淋巴细胞总数增加,其中CD8+细胞增多更为突出[19.那51.].这些患者外周气道成熟树突状细胞(DCs)增加,吸烟者的DCs显示CD80和CD86表达增加[52.];吸烟者肺部的物质很可能被这些细胞所吸收,并由DC主要组织相容性复合体I类分子呈现给CD8+淋巴细胞。一旦被含抗原的树突状细胞激活,t细胞可能通过其组织特异性趋化因子受体进入肺实质[20.].确实,COPD患者外周血管t细胞CXC趋化因子受体(CXCR)3表达增加,特别是CD8+细胞。CXCR3配体(CXC趋化因子配体(CXCL)9、CXCL10和CXCL11)由支气管上皮细胞、气道平滑肌细胞和肺泡巨噬细胞表达,有助于CD8+细胞的聚集[19.那53.].COPD患者肺部CD8+细胞毒性t细胞丰度与气流梗阻、肺气肿程度相关;CD8+细胞通过释放穿孔素和颗粒酶A和B引起肺泡上皮细胞死亡[20.那54.].在COPD患者的气道和实质中也发现大量CD4+ t细胞,它们表达STAT-4(信号传感器和转录激活器)、干扰素(IFN)-γ和t辅助细胞(Th) 1型细胞因子,促进炎症细胞向气道的穿越内皮迁移;随着慢性阻塞性肺病恶化,这种招募进展[20.].然而,香烟烟雾通过干扰MyD88 / IL-1受体相关激酶信号传导来抑制Th1介导的免疫应答对革兰氏阴性细菌感染,从而减少脂多糖(LPS)诱导的TLR4表达;这可能有助于解释COPD中对细菌感染的易感性增加[55.].
香烟烟雾暴露对细菌感染的影响
持续接触香烟烟雾与鼻咽菌群组成的变化有关。在吸烟者中,这包含更大比例的机会致病菌(链球菌引起的肺炎那嗜血杆菌流感那复活的和链球菌Pyogenes)而不是从未吸烟的人,主要含有α-甲基溶解的链球菌,消化链球菌属SPP。和普雷沃菌属SPP。[56.].有趣的是,戒烟与从不吸烟者体内的微生物群的恢复有关,这表明吸烟确实有利于病原体的定植[57.].支持这种观点,香烟烟雾增强了对上皮细胞的细菌附着,并通过改变细菌基因表达来促进毒力的变化[58.-60.].
吸烟会影响上呼吸道。吸烟是患牙周炎的一个危险因素[61.-63.],在吸烟者中是一种比在从不吸烟者中更严重的疾病[62.那64.]. 烟草烟雾促进了机会性病原体(如细菌)在龈下空间的定居牙龈卟啉单胞菌,弯曲杆菌,中间普雷沃氏菌,连翘坦奈菌,牙密螺旋体和fusobacterium核心术[63.那65.-67.].戒烟可减低牙周病的发病率[65.那68.].P. Gingivalis.是慢性牙周炎的病原体;当细菌暴露于香烟烟雾时,观察到细菌菌毛蛋白FimA的表达增加,这可以消除细菌引发的炎症反应,并促进生物膜形成和细菌粘附于气道上皮[58.].香烟烟雾还促进Sinonasal Microbiota的变化,驾驶可逆的鲁棒生物膜的形成,该生物膜可参与鼻腔中的顽固性细菌持久性[69.].吸烟与由细菌病原体引起的急性感染的发生率和严重程度的增加有关[61.那70].此外,二手烟导致儿童广泛的疾病。父母吸烟增加了婴儿运输S.肺炎一般而言,尤其是结合七价疫苗中包含的血清型的携带[71].父母吸烟还增加了脑膜炎球菌脑膜炎的风险[72那73,中耳炎[1]2岁以下婴儿的下呼吸道感染[74].
恶性循环假设
香烟烟雾暴露的额外后果是通过机会性微生物病原体的下呼吸道持续的殖民。这种慢性微生物定子通过进一步扩增先前描述的炎性方法而有助于COPD进展。提出了“恶性圆圈”假设,解释吸烟者中较低气道的慢性细菌定植如何延缓炎症并有助于吸烟疾病的进展(图2)[28.那75].这一假设的核心是,一旦病原体由于吸烟引起的粘液纤毛清除障碍而在下呼吸道获得立足点,它们就会通过进一步阻断粘液纤毛清除而持续存在[28.那75].吸烟还会增加粘液分泌,损害上皮弹性,降低IgA水平,影响专业吞噬细胞的吞噬活性[19.那41.].总之,这些改变促进了下呼吸道的细菌定植,这与由于识别PAMPs而导致的炎症反应加剧有关。细菌产物和细菌产生的上皮损伤都有助于宿主免疫损伤,进一步允许微生物以无限循环的方式进入下呼吸道,最终转化为高度慢性炎症和微生物在肺部的持久定植[75].这种无休止的循环被称为恶性循环。28.那75].经常从吸烟者和持续定植的病人的下呼吸道分离出来的微生物是不可分型的H流感(NTHi),复活的那S.肺炎和P.铜绿假单胞菌.最常见的分离病原体,以及负责COPD中显着百分比的恶化发作的一个负责的人是nthi [76那77].
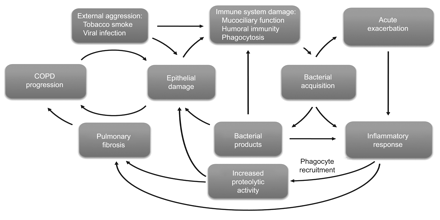
慢性阻塞性肺疾病(COPD)恶化的恶性循环假说。香烟烟雾是外部损伤,损害呼吸道免疫力,从而允许由微生物下呼吸道定植。这种定殖是对于逐步向高电平慢性炎症,组织损伤和纤维化,与下气道的持续性细菌感染一起事件的循环序列的起点。总之,这些过程持续有助于慢性呼吸道病的不可逆的进展。
吸烟对nthi的影响,复活的那S.肺炎和P.铜绿假单胞菌感染
H流感是人类呼吸微生物区系的一员,主要位于口腔和鼻咽。它在40-80%的健康个体中定居,儿童携带频率高于成人[1那78].传输发生通过气溶胶或与粘膜表面直接接触。H流感载体同时在连续更新中与多种菌株进行殖民,主要是不可缺乏(非分子)[79那80].H流感具有适应宿主的分子策略,逃避捕食,与来自同一或不同物种的其他细菌竞争或共存,如金黄色葡萄球菌和S.肺炎[81].同时存在的H流感和S.肺炎在上呼吸道引发协同炎症,导致中性粒细胞聚集到呼吸道粘膜[82].这种中性粒细胞招聘能够选择性地杀死补充opsoniseS.肺炎.Co-colonisation由S.肺炎和H流感提供刺激(H流感肽聚糖)诱导中性粒细胞和补体介导的清除S.肺炎以依赖nod1的方式从粘膜表面[83那84].H流感共定植似乎有利于调理吞噬性的选择S.肺炎胶囊血清型。因此,竞争H流感在共生状态下,肺炎球菌变成毒性更强的种群,这可能是侵袭性疾病进一步发展的原因[85].虽然香烟烟雾似乎没有改变nthi活力[41.],宿主细胞暴露于这种刺激物减少了呼吸上皮细胞的细菌侵袭(未发表的数据)和肺泡巨噬细胞吞噬能力[39.-42.]. 正常情况下,肺泡巨噬细胞通过吞噬体融合有效吞噬和降解NTHi。香烟烟雾极大地损害了细菌的摄入,但不影响惰性颗粒的摄入。肺泡巨噬细胞吞噬NTHi需要磷酸肌醇3-激酶(PI3K)信号,包括Akt磷酸化。细胞暴露于香烟烟雾会降低磷酸化Akt水平,这可能是观察到的吞噬细胞缺陷的原因;使用永生化巨噬细胞和来自吸烟者和COPD患者支气管肺泡灌洗液(BAL)的巨噬细胞与从不吸烟者的巨噬细胞进行了相同的观察[41.].吸烟者和慢性阻塞性肺病患者的脂多糖结合蛋白(LBP)和CD14水平高于从不吸烟者[86].此外,卷烟诱导气道上皮细胞中LBP和CD14的表达。这两种蛋白都抑制NTHi依赖的IL-8分泌,以及NF-κB和p38丝裂原活化蛋白激酶(MAPK)信号通路,但它们增加NTHi进入上皮细胞[86].考虑到的NTHi可以驻留晚期内体样舱内[87LBP和CD14可以确实可以通过有利于亚细胞内部内部的细菌位置有助于NTHI定植。关于适应性免疫细胞,响应于NTHI刺激而导致的主要淋巴细胞亚群是CD8 +和天然杀伤细胞[88];NTHi特异性CD4 + T细胞具有与记忆表型中度到高CD27和CC趋化因子受体7表达,并在这两个健康个体和COPD患者[外周血在低频循环89].
社区获得性肺炎(CAP)是住院治疗的主要原因,死亡率高。S.肺炎是来自帽患者最常见的病原体[90].吸烟是肺炎球菌性肺炎的重大风险因素,特别是在COPD患者[91那92],以及侵袭性肺炎球菌病[93]. 吸烟似乎也会加重细菌的粘液纤毛清除障碍S.肺炎摄入乙醇诱导[94].已经显示香烟烟雾以防止补体介导的吞噬作用S.肺炎通过肺泡巨噬细胞,而非银屑病细菌或IgG包被微球的摄入不受影响,从而损害肺部细菌清除[95].
复活的原因∼慢性阻塞性肺病(COPD)加重的10%,稳定患者的下呼吸道也有定植。慢性阻塞性肺病患者治疗前后痰液样本中炎症参数的收集分析复活的采集显示感染后IL-8,TNF-α和中性粒细胞弹性蛋白酶水平显着增加[96].检测到一个独立的研究复活的特异性Th1细胞在COPD感染患者的支气管肺泡灌洗液[97].此外,卷烟烟雾已被证明可以减少复活的- 诱导的HBD-2抗菌肽表达和前列腺素E.2诱导,增加吸烟者支气管上皮上的细菌载量[33.].
P.铜绿假单胞菌是一种经常从肺炎患者分离的另一种病原体。暴露于卷烟烟雾增加宿主炎症并降低速率P.铜绿假单胞菌间隙(98].增加易感性的机制P.铜绿假单胞菌感染可能与吸烟降低囊性纤维化跨膜传导调节器的表达有关(CFTR.gene [99].流行病学研究表明,慢性阻塞性肺病患者通常感染一种P.铜绿假单胞菌多年来留在肺部的克隆,没有内在传播的证据;在慢性感染期间,病原体发展朝向增加的突变率,增加的抗生素耐药性和降低蛋白酶的产生,不同的共存Mor型,以及类似于在囊性纤维化中观察到的感染和演化的模式[One hundred.].
吸烟者也更有可能患有军团患者的疾病[101- 结核病[102].烟草烟雾通过损害CD4 + T淋巴细胞反应而导致体重减轻和增加的死亡率增加结核分枝杆菌连接,对巨噬细胞的IFN-γ依赖性活化和细胞内杀死后续的关键因素玉米菌菌[103].最后,肺炎支原体在COPD患者另一种常见的病原体[104].由于吸烟,肺试图通过维持高水平的GSH和GSH还原酶(GSH自适应反应)来维持氧化还原环境。M.肺炎感染会干扰对吸烟的反应,导致氧化应激,这可能导致慢性病的进展[105].
抗炎疗法对呼吸道细菌感染的影响
鉴于炎症是吸烟相关疾病的一个主要特征,控制与病情恶化相关的慢性和急性炎症是治疗这些患者的一个主要问题。COPD治疗通常是姑息性的,如氧疗、支气管扩张剂、黏液溶解剂和抗生素。在这些患者中使用消炎药也是一种常见的做法;糖皮质激素是一种广泛使用的治疗方法[106那107].考虑到接受抗炎治疗的患者的较高(且较低的)气道可能被殖民,应考虑皮质素对病原体 - 宿主相互作用和/或微生物间隙的影响。对宿主炎症反应对感染的外源性堵塞可能对宿主有害。实际上,尽管糖皮质激素(特别是特定地)治疗感染后的培养细胞S.肺炎那N. Meningitidis.或aspergillus fumigatus.已被证明在减少炎症方面有效[108那109],已报道类固醇治疗对抗感染的不良影响[110].作为一个例子,地塞米松似乎受损P.铜绿假单胞菌通过抑制诱导型一氧化氮合酶(iNOS)表达和过氧亚硝酸盐产生清除[111].独立地,地塞米松衰减NTHI诱导的NF-κB活化,但也协同增强了NTHI诱导的TLR2表达通过MAPK磷酸酶(MKP)-1的特异性上调导致P38 MAPK的去磷酸化和失活。糖皮质激素介导的nthi诱导的抑制MUC5A表达也会发生通过MKP-1依赖性抑制p38 mapk [112-115].
烟道上皮暴露于香烟烟雾不会与地塞米松的存在无关的粘附对宿主细胞表面的粘附性。相比之下,当细胞同时用地塞米松治疗时,卷烟烟雾介导的肺泡巨噬细胞能力的损伤造成的肺泡巨噬细胞能力衰退[41.].相反,糖皮质激素丙酸氟替卡松似乎通过S.肺炎[116].
这些观察结果以及在COPD中使用吸入的皮质醇的事实增加了肺炎住院风险[117,支持皮质类固醇可能促进感染的观点,尽管它们在减少吸烟引起的炎症方面有效。此外,有证据表明,暴露于卷烟烟雾可能会影响组蛋白乙酰转移酶(histone acetyltransferases)和组蛋白去乙酰化酶(histone deacetylases, HDACs)之间的平衡,从而限制皮质激素减弱炎症基因转录的效率(图3)[118].
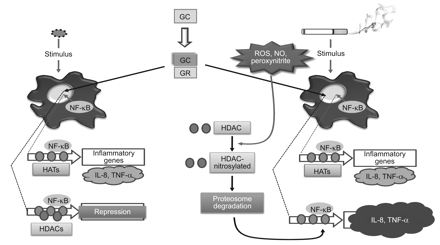
香烟烟雾和宿主对皮质激素不敏感。吸烟引起的组蛋白去乙酰化酶(HDAC)降低可能是炎症反应放大(右图)和对皮质激素的抗炎作用不敏感(左图)的原因。香烟烟雾激活肺泡巨噬细胞核因子(NF)-κB(右图)。基因表达由组蛋白乙酰转移酶(HAT)介导的核心组蛋白乙酰化激活;慢性阻塞性肺疾病中NF-κB激活的炎症基因启动子组蛋白乙酰化增加。乙酰化的增加是由于HDACs的减少。HDACs逆转组蛋白乙酰化并关闭基因转录。氧化和亚硝化应激可使HDACs失活。氧化和亚硝化应激导致过氧亚硝酸盐的形成,过氧亚硝酸盐将HDAC亚硝基化,导致其降解,导致低HDAC水平,随后,炎症反应放大。吸烟引起的氧化应激降低HDAC会损害对皮质激素的反应。 Glucocorticoids (GCs) bind GC receptor (GR) and recruit HDAC to activated inflammatory genes; by reversing the acetylation of those genes, their transcription is switched off and the inflammation is reduced (left). IL: interleukin; TNF: tumour necrosis factor; ROS: reactive oxygen species; NO: nitric oxide.
因此,替代治疗成为强制性。虽然有几种新的可能性,但其他新的可能性是临床试验的不同阶段[107那119-121.[应该注意,在大多数情况下,没有关于它们对宿主的影响的信息。此外,这个重要方面几乎没有被认为是正在进行的临床试验中的结果。通过抑制过氧硝酸盐的产生,诱导型Inos的抗氧化剂和抑制剂可能是有效的。可用的抗氧化剂是维生素C和E,和N- 乙酰琥珀酸盐;选择性Inos抑制剂和过氧硝酸盐清除剂正在开发[118].HDAC激活物茶碱[122.和对PI3K的治疗性抑制[123.]已经显示出能够逆转由香烟烟雾诱导的类固醇抗性。其他疗法有:1)长效支气管扩张剂(长效β2-激动剂沙美特罗或长效抗胆碱能噻托溴铵);2)介质拮抗剂(LTB抑制剂)4.,IL-8,TNF-α或EGFR);3)蛋白酶抑制剂(内源性抗辐剂,如α1-抗胰蛋白酶、SLPI、弹力蛋白酶、胱抑素或小分子抑制剂);4)新的抗炎治疗(磷酸二酯酶(PDE)4抑制剂、p38 MAPK、NF-κB或PI3K或白藜芦醇)[119那121.].Salmeterol已被证明有助于保护气道上皮屏障P.铜绿假单胞菌[124.]. 沙美特罗和丙酸氟替卡松的联合应用已被证明能减轻感染哮喘的人气道上皮细胞的炎症反应S.金黄色葡萄球菌[125.]. 尽管沙美特罗似乎也能保护呼吸道上皮免受感染H流感引起的伤害[126.],在活的有机体内数据显示,吸入这种支气管扩张剂可能会对NTHi从小鼠呼吸道的有效清除产生负面影响[127.].相比之下,白藜芦醇已经显示出改善Serratia marcescens.诱导大鼠急性肺炎[128.],抑制蜂鸣和毒力因子表达Proteus mirabilis.[129.],成为各种潜在的候选人幽门螺杆菌- 相关的胃病病变方法[130.,选择性地抑制N.淋病术和N. Meningitidis.[131.].最后,通过减少上皮细胞的细菌侵袭(A.López-gómez,FundaciónCaubet-cimera,Mallorca,西班牙Mallorca,Mallorca,西班牙,Mallorca,Mallorca,西班牙,Mallorca Caubet-Cimera,Mallorca,Spain;个人沟通,在治疗Nthi感染时,所述真核环化酶活化的促进循环AMP水平的增加可能是有益的。在尿羟致原因引起的尿路感染中已经进行了类似的观察结果大肠杆菌[132.].PDE4抑制剂Rolipram也显示有效预防P.铜绿假单胞菌诱导的上皮损伤[133.]. 此外,PDE4抑制似乎会削弱宿主对PDE4的防御Klebsiella肺炎肺炎小鼠模型的感染[134.].这些观察结果在一起加强了谨慎的观念,以将用一种病原体与不同微生物引起的感染产生的发现外推。
最后的评论
造成主机暴露于外部因素,如吸烟正常呼吸菌群的改变对宿主健康勿庸置疑的影响,并且构成了慢性呼吸系统疾病和呼吸道感染的危险因素。理解宿主 - 病原体动态的性质是有效的治疗方法的发展至关重要,但主机暴露在环境因素的动态的调节也应予以考虑。此外,疗法集中于慢性呼吸疾病的治疗中也应考虑到微生物组分,如果有的话,所述慢性疾病的,因为这种治疗可能影响,正或负,病原体清除,因此,慢性进展疾病。总之,我们想提出的是,由主管部门批准前,可能会采取长期定植患者任何治疗应在其对宿主 - 病原体动态的潜在影响来评估的概念,通过测试的相关面板病原体,并且优选包括体外和在活的有机体内方法。
脚注
支持声明
(授予CP05-0027,PI06-1251和PS09-0130)在J.迪亚的实验室工作是由来自德研究所Salud的卡洛斯三世(ISCIII,西班牙)资助项目和基金会穆图阿MadrileñA-2008 J.迪亚。在J.A.工作Bengoechea的实验室是由从生物医学计划(SAF2009-07885,部:西恩西亚ēINNOVACIÓN,西班牙)的资助。CIBERES是ISCIII的一项举措。
利益陈述书
没有人申报。
- 收到了2011年4月8日。
- 公认2011年6月28日。
- ©2012年