摘要
磷酸肌肽3激酶(PI3Ks)通过调节炎症介质的激活、炎症细胞募集和免疫细胞功能参与哮喘的发病机制。最近的研究表明,pi3k也调节白细胞介素(IL)-17的表达,IL -17被认为是参与气道炎症的重要细胞因子。
在本研究中,我们利用小鼠哮喘模型研究了PI3Kδ在变应性气道疾病中调节IL-17表达的作用。
吸入卵清蛋白后,给予选择性p110δ抑制剂IC87114,可显著减弱气道总细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞的浸润,以及气道高反应性,并减弱IL-17蛋白和mRNA表达的增加。此外,IC87114降低了IL-4、-5和-13水平,降低了角质细胞趋化蛋白和mRNA的表达,降低了核因子(NF)-κB活性。此外,NF-κB抑制剂BAY 11-7085显著降低IL-17蛋白水平的升高。我们的研究结果还表明,用抗IL-17抗体抑制IL-17活性可显著减少气道炎症和高反应性。
这些发现表明,抑制p110δ信号通路通过调节NF-κB活性来抑制IL-17的表达,因此具有治疗哮喘的潜力。
哮喘是一种以可逆性气道阻塞和气道高反应性为特征的气道慢性炎症性疾病1。哮喘气道炎症增加了炎症级联反应中各种成分的表达,包括细胞因子、趋化因子、粘附分子、生长因子和酶。这种炎症级联反应的核心是受体信号传导与下游脂质和蛋白激酶之间的复杂相互作用。特别是磷酸肌肽3-激酶(PI3K)是参与炎症过程的重要激酶。
PI3K是一个大的信号激酶家族,产生负责调节许多细胞活动的脂质第二信使。pi3k介导免疫和炎症反应过程中的关键信号转导反应,因此是各种炎症性疾病治疗发展的一个有吸引力的靶点2,3.。过去几年进行的研究强调了pi3k在支气管哮喘中的重要性。我们之前对哮喘小鼠模型的研究表明,与攻毒前相比,卵清蛋白(OVA)攻毒后PI3K活性增加4。此外,给予PI3K抑制剂wortmannin或LY-294002可减少t -辅助细胞(Th) 2型细胞因子的产生、肺嗜酸性粒细胞增多、气道炎症和支气管高反应性4。越来越多的证据表明,pi3k通过调节炎症介质的表达和激活、炎症细胞募集和免疫细胞功能参与哮喘的发病机制2,4。最近的研究已经开始探索不同PI3K亚型的具体作用,p110δ和p110γ被认为是参与PI3K介导的免疫应答的主要亚型5。用于研究PI3K的生物学作用和分析PI3K驱动途径的两种市售PI3K抑制剂wortmannin和LY-294002在PI3K i类的四个成员中选择性较差。因此,开发PI3K异构体特异性抑制剂一直是一个相当感兴趣的领域。最近合成了一种p110δ催化活性的选择性抑制剂IC87114,并用于探索PI3Kδ在中性粒细胞迁移中的作用6,7。此外,先前使用IC87114的研究表明p110δ在变应性哮喘的发病机制中起重要作用8,9。
白细胞介素(IL)-17家族是最近发现的一组细胞因子,由6个成员组成,即IL-17(也称为IL- 17a)、IL- 17b、IL- 17c、IL- 17d、IL- 17e和IL- 17f10。IL-17是该家族中研究最广泛的成员,与许多免疫和炎症反应有关,主要作为促炎调节剂,诱导许多炎症介质的表达,如细胞因子、趋化因子、粘附分子和生长因子11,12。在过敏性哮喘小鼠模型中,吸入过敏原后炎症气道中IL-17 mRNA表达上调13。与动物实验一致,哮喘患者的痰液、支气管肺泡灌洗液和外周血中IL-17 mRNA和/或蛋白表达升高14- - - - - -18。此外,哮喘患者气道中IL-17的表达水平与气道超敏反应的严重程度相关14。这些发现提示了IL-17在哮喘发病机制中的潜在作用。最近的研究,包括我们自己的研究,已经发现IL-17的产生是通过激活PI3K/Akt通路介导的12,19- - - - - -21。然而,个体PI3K亚型对IL-17表达上调的贡献尚未得到检验。在本研究中,我们通过小鼠哮喘模型研究了PI3Kδ参与IL-17表达及其分子机制。
材料与方法
在线补充材料中提供了更详细的方法。
动物和实验方案
雌性C57BL/6小鼠,8-10周龄,无小鼠特异性病原体,来自Orientbio Inc. (Seoungnam, South Korea)。所有的动物实验都得到了机构动物护理和使用委员会(全北国立大学,全州,韩国)的批准。小鼠在第1天和第14天腹腔注射20 μg的OVA (Sigma-Aldrich, St Louis, MO, USA),乳化于1mg的氢氧化铝(Pierce Chemical Co., Rockford, IL, USA),总体积为200 μL,如上所述8,9。在初始致敏后的第21、22和23天,小鼠使用超声波雾化器(NE-U12;欧姆龙,东京,日本)。最后一次攻毒后48 h进行BAL。在灌胃时,小鼠被过量的戊巴比妥钠(每公斤体重100毫克,腹腔注射)杀死。
注射IC87114、LY-294002、抗il -17抗体、同型对照单克隆抗体、Akt抑制剂或BAY 11-7085
IC87114(0.1或1mg·kg−1·天−1), LY-294002 (PI3K的选择性抑制剂;1.5毫克·公斤−1·天−1;BIOMOL Research Laboratories Inc., Plymouth Meeting, PA, USA)或用0.9% NaCl稀释的对照品(二甲基亚砜(DMSO)),以50 μL的体积气管内滴注给药,第21天(第一次OVA攻毒前1小时)一次,第23天(最后一次OVA攻毒后3小时)再次给药。8,9。抗il -17抗体(Ab)或同型对照单克隆(m)Ab (5 mg·kg)−1·天−1;每只动物腹腔注射R&D Systems, Inc., Minneapolis, MN, USA),第21天和第24天(最后一次OVA攻毒后24小时)腹腔注射一次。Akt抑制剂,1l6 -羟甲基-肌醇-2-(R)-2-O-methyl-3 -O十八醇,sn-碳酸甘油(3mg·kg−1·天−1;Calbiochem, Darmstadt, Germany)用DMSO溶解,0.9% NaCl稀释,每只动物腹腔注射,第21天1次,第24天1次。核因子(NF)-κB活化抑制剂BAY 11-7085 (20 mg·kg)−1·天−1;BIOMOL Research Laboratories Inc.),溶解在DMSO中,用0.9% NaCl稀释,每只动物腹腔注射,第21天一次,第24天再次注射。
Western blot分析
如前所述,通过Western blot分析蛋白表达水平8。使用的一抗有:抗il -17 Ab (R&D Systems, Inc.)、抗il -4 Ab (sertec Ltd, Oxford, UK)、抗il -5 Ab (Santa Cruz Biotechnology, Santa Cruz, CA, USA)、抗il -13 Ab (R&D Systems, Inc.)、生物素化抗小鼠角质细胞化学引诱剂(KC) Ab (R&D Systems, Inc.)、抗Akt Ab (Cell Signaling Technology Inc., Beverly, MA, USA)、抗磷酸化Akt (p-Akt) Ab (Cell Signaling Technology Inc.)、抗κBα抑制剂(I-κBα) Ab (Santa Cruz Biotechnology)。
RNA分离和RT-PCR
采用快速提取法从肺组织中分离总RNA (TRI-Reagent;Sigma-Aldrich),如前所述12。
实时定量RT-PCR
使用LightCycler进行实时定量RT-PCR分析®如前所述,FastStart DNA Master SYBR Green I (Roche Diagnostics, Mannheim, Germany)12。
Th2细胞因子的测定
采用酶免疫分析法(R&D Systems, Inc.)定量IL-4、IL-5和IL-13的水平。
细胞质或核蛋白提取用于分析NF-κB p65
如前所述进行细胞质或核提取9。
肺组织中PI3K酶活性的测定
如前所述,测量肺组织中PI3K酶活性9。磷脂酰肌醇(3,4,5)-三磷酸(PIP)3.)用PIP进行量化3.竞争酶免疫测定(Echelon, Inc.,盐湖城,UT,美国)。
气道反应性测定
如前所述,气道反应性评估为雾化甲胆碱刺激后气道功能的变化9。
密度分析和统计
所有免疫反应和磷酸化信号通过密度扫描(Gel Doc XR;Bio-Rad Laboratories Inc., Hercules, CA, USA)。数据以平均值±表示扫描电镜。采用单因素方差分析和Scheffe检验进行统计学比较。p<0.05为差异有统计学意义。
结果
IC87114对ova致敏和ova致毒小鼠肺组织IL-17蛋白水平和mRNA表达的影响
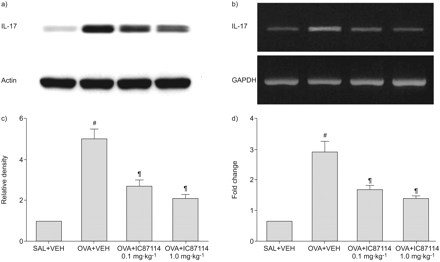
Western blot分析显示,与对照组相比,末次吸入OVA后48 h肺组织中IL-17蛋白水平显著升高(无花果1和1 c)。吸入OVA后IL-17蛋白水平的升高被IC87114显著减弱。RT-PCR和real-time RT-PCR分析显示,IC87114 (无花果1 b和1 d)。
IC87114对卵清蛋白(OVA)致敏和OVA攻毒小鼠肺组织白细胞介素(IL)-17蛋白水平和mRNA表达的影响最后一次攻毒48 h后,盐雾化小鼠给药载体(二甲基亚砜)(SAL+VEH), OVA雾化小鼠给药载体(OVA+VEH), OVA雾化小鼠给药0.1 mg·kg−1IC87114 (OVA) +IC87114 0.1 mg·kg−1ova雾化小鼠1.0 mg·kg−1IC87114 (OVA) +IC87114 1.0 mg·kg−1)。a) IL-17蛋白的Western blot分析。b) IL-17 mRNA表达的代表性RT-PCR分析。c)密度分析用OVA+VEH、OVA+IC87114中IL-17的相对比值1.0 mg·kg表示−1对那些在SAL+VEH的人。SAL+VEH肺组织中IL-17的相对比值任意表示为1。d) real-time RT-PCR定量分析IL-17 mRNA表达。数据代表平均值±扫描电镜每组7只老鼠。GAPDH:甘油醛-3-磷酸脱氢酶#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费。
IC87114对ova致敏和ova攻毒小鼠BAL液中IL-17蛋白水平的影响
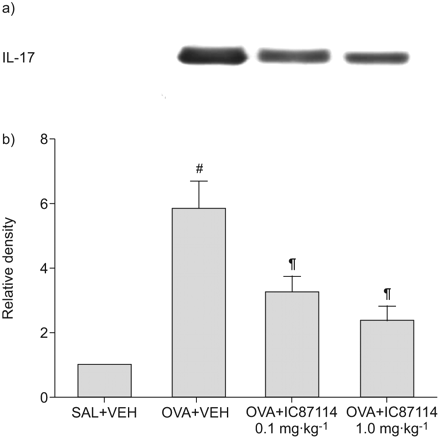
Western blot分析显示,与对照组相比,吸入OVA后48 h BAL液中IL-17蛋白水平显著升高(图2)。吸入OVA后IL-17蛋白水平的升高被IC87114显著抑制。
IC87114对卵清蛋白(OVA)致敏和OVA攻毒小鼠支气管肺泡灌洗液中白细胞介素(IL)-17蛋白水平的影响最后一次攻毒48 h后,分别用盐水雾化小鼠给药(SAL+VEH)、OVA雾化小鼠给药(OVA+VEH)、OVA雾化小鼠给药0.1 mg·kg进行取样−1IC87114 (OVA) +IC87114 0.1 mg·kg−1ova雾化小鼠1.0 mg·kg−1IC87114 (OVA) +IC87114 1.0 mg·kg−1)。a) IL-17蛋白的Western blot分析。b)密度分析以IL-17与肌动蛋白的相对比值表示。SAL+VEH肺组织中IL-17的相对比值任意表示为1。数据以平均值±表示扫描电镜每组7只老鼠。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费。
IC87114或抗il -17 Ab对BAL液细胞变化的影响
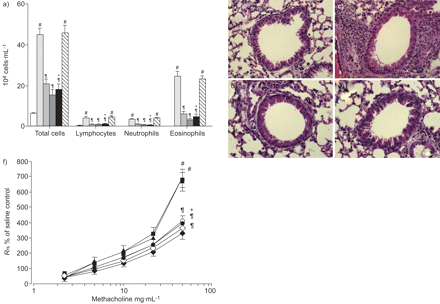
吸入OVA后48 h BAL液中总细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞的数量较吸入生理盐水后显著增加(图3)。IC87114显著降低了总细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞数量的增加。此外,与给药载体或同型对照单抗的ova雾化小鼠相比,给药抗il -17 Ab显著降低了ova致敏和攻毒小鼠的总细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞数量的增加。
a) IC87114或抗白介素-17抗体(anti-IL-17 Ab)对卵清蛋白(OVA)致敏和OVA攻毒小鼠支气管肺泡灌洗液中总细胞和分化细胞计数的影响。盐水雾化小鼠给药(SAL+VEH) BAL液中细胞计数的差异□)、OVA-吸入小鼠给药(OVA+VEH;●ova雾化小鼠0.1 mg·kg−1IC87114 (OVA) +IC87114 0.1 mg·kg−1;烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧烧−1IC87114 (OVA) +IC87114 1.0 mg·kg−1;*), OVA雾化小鼠给予抗il -17 Ab (OVA+抗il -17 Ab;▪),OVA雾化小鼠给予同种型对照单克隆抗体(OVA+对照单抗; )。b-e) IC87114或抗il -17 Ab在ova致敏和ova致毒小鼠肺组织中的作用。肺的典型血红素和伊红染色切片。最后一次攻毒48 h后取样,b) SAL+VEH, c) OVA+VEH, d) OVA+IC87114 0.1 mg·kg−1e) OVA+抗il -17 Ab小鼠。标尺= 20 μm。每组7只小鼠的结果相似。f) IC87114或抗il -17 Ab对ova致敏和ova挑战小鼠气道反应性的影响。最后一次给药48 h后测定SAL+VEH(♦)、OVA+VEH(♦)、OVA+IC87114 (0.1 mg·kg)的气道反应性−1(〇)、OVA+IC87114 1.0 mg·kg−1OVA+anti-IL-17 Ab(•)和OVA+control mAb(†)。数据以平均值±表示扫描电镜每组7只老鼠。Rrs:呼吸系统阻力。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费;+: p < 0.05与卵子+马伯的控制。
)。b-e) IC87114或抗il -17 Ab在ova致敏和ova致毒小鼠肺组织中的作用。肺的典型血红素和伊红染色切片。最后一次攻毒48 h后取样,b) SAL+VEH, c) OVA+VEH, d) OVA+IC87114 0.1 mg·kg−1e) OVA+抗il -17 Ab小鼠。标尺= 20 μm。每组7只小鼠的结果相似。f) IC87114或抗il -17 Ab对ova致敏和ova挑战小鼠气道反应性的影响。最后一次给药48 h后测定SAL+VEH(♦)、OVA+VEH(♦)、OVA+IC87114 (0.1 mg·kg)的气道反应性−1(〇)、OVA+IC87114 1.0 mg·kg−1OVA+anti-IL-17 Ab(•)和OVA+control mAb(†)。数据以平均值±表示扫描电镜每组7只老鼠。Rrs:呼吸系统阻力。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费;+: p < 0.05与卵子+马伯的控制。
IC87114或抗il -17 Ab对ova诱导哮喘病理改变的影响
组织学分析显示ova暴露小鼠哮喘的典型病理特征。细支气管周围浸润大量炎性细胞,细支气管管腔内积聚黏液和碎屑(图3 c)与对照组(图3 b)。注射IC87114 (图3 d)或抗il -17 Ab (图3 e)显示细支气管周围区炎症细胞的浸润和气道管腔内碎片的数量明显减少。
IC87114或抗il -17 Ab对气道高反应性的影响
气道反应性以呼吸系统阻力增加的百分比(Rrs),以应对不断增加的甲胆碱剂量。在ova致敏和攻毒小鼠中,百分比的剂量-反应曲线Rrs与对照组相比向左移动(图3 f)。另外,百分比Rrs由甲胆碱产生(剂量为50mg·mL)−1)与对照小鼠相比明显增加。IC87114对ova致敏和攻毒小鼠呈百分比的剂量-反应曲线Rrs它向右移动了吗,百分比显著降低了吗Rrs50 mg·mL产生−1与未治疗小鼠的对比。此外,给ova致敏和攻毒小鼠注射抗il -17 Ab也显著降低了该百分比Rrs50 mg·mL产生−1与ova雾化小鼠给药或同型对照单抗比较。这些结果表明,IC87114或抗il -17 Ab治疗可降低ova诱导的气道高反应性。
IC87114对ova致敏和ova攻毒小鼠肺组织和BAL液中IL-4、IL-5和IL-13水平的影响
Western blot分析显示,吸入OVA后48 h肺组织中IL-4、IL-5、IL-13蛋白水平较对照组升高(图1A在网上补充资料)。IC87114降低了这些细胞因子水平的升高。与Western blot分析结果一致,IL-4、IL-5和IL-13的酶免疫分析显示,IC87114显著降低BAL液中这些细胞因子的水平(图1B在网上补充资料)。
IC87114对ova致敏和ova致毒小鼠肺组织KC蛋白水平和mRNA表达的影响
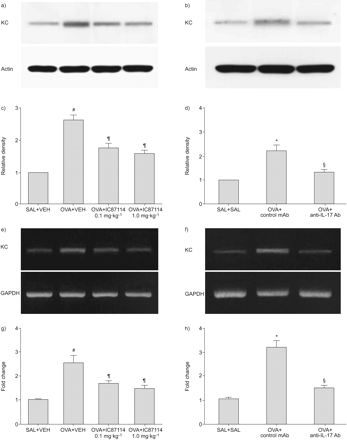
Western blot分析显示,与对照组相比,吸入OVA后48 h肺组织中KC蛋白水平显著升高(图4c). IC87114显著降低了吸入OVA后KC蛋白水平的升高。RT-PCR和实时RT-PCR分析显示,IC87114 (图4 e和g)。
IC87114或抗白介素-17抗体(anti-IL-17 Ab)对卵清蛋白(OVA)致敏和OVA攻毒小鼠肺组织角质形成细胞趋化物(KC)蛋白水平和mRNA表达的影响a、c、e、g)末次攻毒48 h后取样,盐雾化小鼠给药(SAL+VEH), OVA雾化小鼠给药(OVA+VEH), OVA雾化小鼠给药0.1 mg·kg−1IC87114 (OVA) +IC87114 0.1 mg·kg−1ova吸入小鼠给药1.0 mg·kg−1IC87114 (OVA) +IC87114 1.0 mg·kg−1)。b, d, f, h)在最后一次攻毒48小时后,对吸入盐水的小鼠进行取样,OVA雾化小鼠给予同型对照单克隆抗体(OVA+对照单抗),OVA雾化小鼠给予抗il -17抗体(OVA+抗il -17 Ab)。a和b) KC蛋白的Western blot分析。c和d)密度分析以KC与肌动蛋白的相对比值表示。SAL+VEH (c)或SAL+SAL (d)肺组织中KC的相对比值任意表示为1。e和f)代表性的KC mRNA表达的RT-PCR分析。g、h)实时RT-PCR定量分析KC mRNA表达。数据以平均值±表示扫描电镜每组7只老鼠。甘油醛-3-磷酸脱氢酶。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费;+: p < 0.05与萨尔+ SAL;§: p < 0.05与卵子+马伯的控制。
抗il -17 Ab对ova致敏和ova致毒小鼠肺组织KC蛋白水平和mRNA表达的影响
Western blot分析显示,与给药同种型对照单抗(mAb)的ova吸入小鼠相比,给药抗il -17 Ab可显著降低肺组织中KC蛋白的水平(图4 bd)。此外,RT-PCR和实时RT-PCR分析显示,与给予同型对照单抗的ova雾化小鼠相比,给予抗il -17 Ab的ova致敏小鼠KC mRNA表达显著降低(图4f和h)。
LY-294002或IC87114对ova致敏和ova挑战小鼠肺组织中p-Akt和Akt蛋白水平及PI3K酶活性的影响
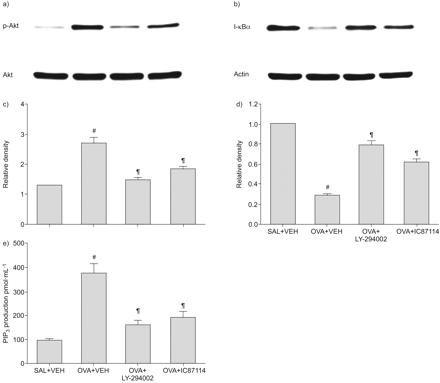
与对照组相比,吸入OVA后48 h肺组织中p-Akt蛋白水平显著升高(图5a和c)。然而,在任何测试组中都没有观察到Akt蛋白水平的显著变化。注射LY-294002或IC87114可显著降低吸入OVA后48 h肺组织中p-Akt蛋白水平的升高而非Akt蛋白水平的升高。与这些结果一致,PIP3.吸入OVA 48 h后,肺组织中含量显著高于对照组(图5 e)。PIP的增加3.注射LY-294002或IC87114后,吸入OVA 48 h后肺组织中的水平显著降低。
LY-294002或IC87114对卵清蛋白(OVA)雾化小鼠肺组织磷酸化Akt (p-Akt)和Akt蛋白水平、磷酸肌肽3激酶(PI3K)酶活性和κBα抑制剂(I-κBα)蛋白水平的影响。最后一次攻毒48 h后,分别对盐吸入小鼠给药载体(二甲基亚砜)(SAL+VEH)、OVA雾化小鼠给药载体(OVA+VEH)、OVA吸入小鼠给药LY-294002 (OVA+LY-294002)、OVA吸入小鼠给药1.0 mg·kg进行取样−1IC87114(卵+ IC87114)。a) p-Akt和Akt蛋白的Western blotting。b) I-κBα蛋白的Western blotting。c)密度分析以p-Akt与Akt的相对比值表示。SAL+VEH肺组织中p-Akt的相对比值任意表示为1。d)密度分析用I-κBα与肌动蛋白的相对比值表示。SAL+VEH肺组织中I-κBα的相对比值任意表示为1。e)磷脂酰肌醇(3,4,5)-三磷酸(PIP)的酶免疫分析3.)在肺组织中通过pi3k产生。数据以平均值±表示扫描电镜每组6只老鼠。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费。
LY-294002或IC87114对ova致敏和ova致毒小鼠肺组织I-κBα蛋白水平的影响
Western blot分析显示,吸入OVA后48 h肺组织中I-κBα蛋白水平明显低于对照组(图5 bd).吸入OVA后I-κBα蛋白水平的下降被LY-294002或IC87114显著抑制。
Akt抑制剂对ova致敏小鼠肺组织I-κBα和NF-κB p65蛋白水平的影响
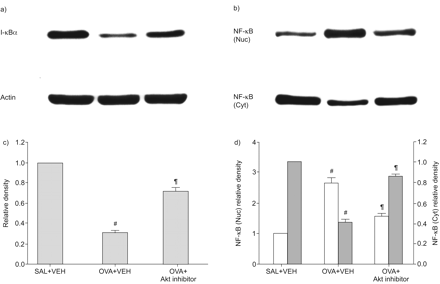
吸入OVA后降低的I-κBα蛋白水平在给予Akt抑制剂(图6a和c)。Western blot分析显示,吸入OVA后48 h,肺组织核蛋白提取物中NF-κB p65水平较生理盐水对照组升高。图6 b和6 d)。给予Akt抑制剂可显著降低吸入OVA后核蛋白提取物中NF-κB p65水平的升高。与对照组相比,吸入OVA后肺组织胞浆蛋白组分中NF-κB p65水平降低。给药Akt抑制剂可显著抑制胞浆蛋白组分中NF-κB p65水平的降低。
Akt抑制剂对卵清蛋白(OVA)致敏小鼠肺组织中κBα (I-κBα)和核因子(NF)-κB p65蛋白水平的影响最后一次给药48 h后,盐雾小鼠给药载体(二甲基亚砜)(SAL+VEH)、OVA吸入小鼠给药载体(OVA+VEH)和OVA吸入小鼠给药Akt抑制剂(OVA+Akt抑制剂)进行采样。a) I-κBα蛋白的Western blotting。b)肺组织核(Nuc)和胞浆(Cyt)蛋白提取物中NF-κB p65水平的Western blot分析。c)密度分析用I-κBα与肌动蛋白的相对比值表示。SAL+VEH肺组织中I-κBα的相对比值任意表示为1。d)密度分析表示OVA+VEH或OVA+Akt抑制剂中NF-κB p65水平与SAL+VEH中NF-κB p65水平的相对比值。SAL+VEH肺组织核蛋白提取物中NF-κB的相对比值任意表示为1。数据以平均值±表示扫描电镜每组6只老鼠。□:Nuc;▓:Cyt。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费。
IC87114对ova致敏和ova致毒小鼠肺组织NF-κB p65蛋白水平的影响
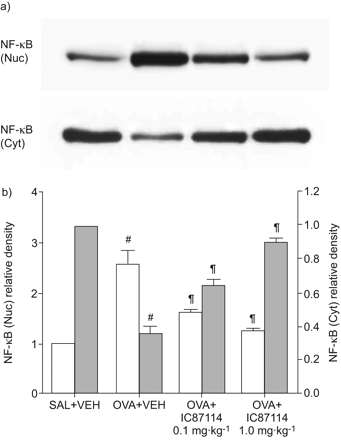
吸入OVA后肺组织核蛋白提取物中NF-κB p65水平的升高被IC87114显著降低(图7)。与此相反,IC87114可显著抑制肺组织胞浆蛋白组分中NF-κB p65水平的下降。
IC87114对卵清蛋白(OVA)致敏小鼠肺组织核因子(NF)-κB p65蛋白水平的影响最后一次攻毒48 h后,分别用盐水雾化给药(SAL+VEH)、OVA雾化给药(OVA+VEH)和OVA吸入给药(0.1 mg·kg)的小鼠检测NF-κB p65水平−1IC87114 (OVA) +IC87114 0.1 mg·kg−1ova吸入小鼠给药1.0 mg·kg−1IC87114 (OVA) +IC87114 1.0 mg·kg−1)。a)肺组织核(Nuc)和胞浆(Cyt)蛋白提取物中NF-κB p65水平的Western blot分析。b)密度分析以OVA+VEH、OVA+IC87114 0.1 mg·kg中NF-κB p65水平的相对比值表示−1或OVA+IC87114 1.0 mg·kg−1对那些在SAL+VEH的人。SAL+VEH肺组织核蛋白提取物中NF-κB的相对比值任意表示为1。数据以平均值±表示扫描电镜每组7只老鼠。□:Nuc;▓:Cyt。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费。
BAY 11-7085对ova致敏和ova致毒小鼠肺组织IL-17蛋白水平的影响
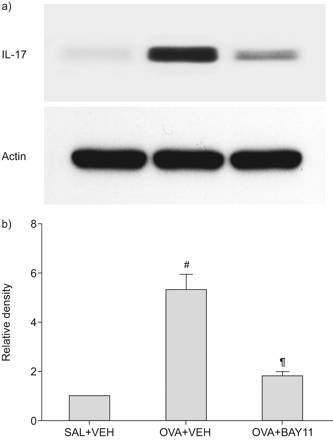
Western blot分析显示,给予NF-κB活化抑制剂BAY 11-7085后,吸入OVA后升高的IL-17蛋白水平明显降低(图8)。
BAY11-7085对卵清蛋白(OVA)致敏和卵清蛋白激发小鼠肺组织白细胞介素(IL)-17蛋白水平的影响最后一次攻毒48 h后,盐雾小鼠给药载体(二甲基亚砜)(SAL+VEH)、OVA吸入小鼠给药载体(OVA+VEH)和OVA吸入小鼠给药BAY11-7085 (OVA+BAY 11)进行采样。a) IL-17的Western blot分析。b)密度分析以IL-17与肌动蛋白的相对比值表示。SAL+VEH肺组织中IL-17的相对比值任意表示为1。数据以平均值±表示扫描电镜每组7只老鼠。#: p < 0.05与萨尔+阿明费;¶: p < 0.05与卵子+阿明费。
讨论
在这项研究中,我们证明了p110δ信号通路的抑制抑制了肺中IL-17蛋白和mRNA的表达,并减轻了过敏原诱导的气道炎症和气道高反应性。本研究ova诱导的哮喘模型表现出典型的哮喘病理特征:气道炎症细胞增多,气道高反应性,Th2细胞因子(IL-4、IL-5、IL-13)、趋化因子KC、核NF-κB水平升高。此外,吸入OVA后肺组织中IL-17蛋白和mRNA的表达均升高。选择性PI3Kδ抑制剂IC87114可显著降低气道总细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞的浸润,降低气道高反应性,并降低IL-17蛋白和mRNA的表达。此外,IC87114降低Th2细胞因子水平、KC蛋白和mRNA表达、Akt磷酸化、I-κBα降解和NF-κB活性。Akt抑制剂也增加了I-κBα蛋白水平,同时降低了NF-κB活性,NF-κB抑制剂BAY 11-7085显著降低了吸入OVA后IL-17蛋白水平的升高。此外,用抗IL-17抗体抑制IL-17活性可显著减少支气管炎症和气道高反应性。这些结果表明PI3Kδ抑制剂在哮喘中的治疗作用部分是通过抑制IL-17的表达介导的通过调节akt介导的NF-κB活化。据我们所知,这是第一个阐明PI3Kδ在调节IL-17表达中的作用的研究。
PI3K家族分为I类、II类和III类,基于结构和底物特异性,I类PI3K进一步细分为IA类(PI3Kα、PI3Kβ和PI3Kδ亚型)和IB类(PI3Kγ亚型)22。在结构上,IA类PI3K由一个110-kd (p110α、β或δ)催化亚基和一个调节亚基(p85α、p85β、p55α、p55γ或p50α)组成的异源二聚体组成。23。这些差异使得PI3K亚型介导不同的功能。在PI3K的这些亚型中,p110δ与免疫反应和炎症有关24。最近的研究已经证明了p110δ信号在过敏性气道炎症中的新的生物学作用,并强调了PI3Kδ异构体作为哮喘潜在治疗靶点的重要性8,9。p110δ基因失活导致抗原受体功能、Th2细胞因子产生和Th2细胞介导的炎症反应降低25。在本研究中,结果表明,给予PI3Kδ特异性抑制剂可显著降低哮喘的病理特征,包括气道炎症、气道高反应性和Th2细胞因子水平的升高。这些结果与以前的研究结果一致8,9,25证实了PI3Kδ抑制剂在哮喘中的治疗潜力。
IL-17是一种新的细胞因子,由于其参与免疫和炎症反应,近年来引起了许多科学家的关注26。气道中的IL-17最有可能是由一种称为Th17细胞的独特Th谱系产生的27。最近的研究表明,嗜酸性粒细胞、中性粒细胞和单核细胞也是IL-17的来源15,26。IL-17的生物学功能似乎与中性粒细胞主导的炎症有关,作为肺中粒细胞生成、中性粒细胞积累和中性粒细胞激活的启动子11,26。经气管内注射IL-17已被证明可增加BAL液中中性粒细胞的绝对数量28。此外,IL-17增加支气管上皮细胞中IL-8 mRNA的表达,IL-17的中性粒细胞趋化作用被抗IL-8 Ab阻断29。因此,IL-17可能能够通过诱导释放强效的中性粒细胞导向趋化因子IL-8,选择性地将中性粒细胞招募到气道中29,30.。在这项研究中,我们评估了抗il -17 Ab对KC表达的影响,KC是IL-8的功能性小鼠同源物。与之前的研究一致,我们发现用抗IL-17 Ab抑制IL-17活性显著降低了吸入过敏原后中性粒细胞气道浸润的增加,以及KC蛋白和mRNA表达的增加。这些结果表明,在我们的变应性气道炎症模型中,IL-17通过诱导IL-8的释放来协调中性粒细胞流入气道。哮喘的病理特征是由嗜酸性粒细胞、肥大细胞和Th2细胞及其细胞因子介导的31。然而,据报道,气道中性粒细胞的数量在严重哮喘中增加32。在哮喘中,中性粒细胞可能导致气道腺分泌过多、气道阻塞和气道重塑17,33。本研究的数据支持il -17诱导的中性粒细胞向气道募集与哮喘发病机制有关的观点。
有趣的是,最近的一项研究表明,IL-17受体基因缺陷的小鼠在抗原攻击下,不仅中性粒细胞招募减少,嗜酸性粒细胞也减少34。此外,在缺乏IL-17受体信号的情况下,肺组织中嗜酸性粒细胞过氧化物酶活性和ova特异性血清免疫球蛋白E浓度降低35。此外,IL-17参与过敏原特异性t细胞的激活也有报道36。IL-17缺陷或IL-17受体缺陷小鼠表现出Th2细胞因子水平降低,这与气道超敏反应降低有关34,35。最近的一项研究表明,哮喘患者痰中IL-17 mRNA水平与IL-5 mRNA水平呈正相关18。因此,IL-17似乎有助于哮喘中Th2细胞介导的嗜酸性粒细胞炎症。与这些观察结果一致,我们目前的数据显示,用抗IL-17抗体抑制IL-17活性显著减少抗原诱导的气道嗜酸性粒细胞浸润和气道高反应性。我们还观察到IL-17活性的抑制显著降低了BAL液中Th2细胞因子水平的升高。综上所述,这些发现表明IL-17在哮喘的发病机制中起着至关重要的作用,有助于中性粒细胞炎症以及Th2细胞介导的嗜酸性粒细胞炎症。
IL-17的产生是通过激活PI3K/Akt通路介导的23,19- - - - - -21。有报道称,LY-294002抑制CD4+ T细胞中IL-17的产生和mRNA的表达20.。与这些一致在体外我们之前曾报道,在哮喘小鼠模型中,使用wortmannin或LY-294002可降低吸入过敏原后IL-17水平的升高12。然而,这些抑制剂不能区分I类PI3K的四种亚型。在本研究中,IC87114药物阻断p110δ活性可显著降低ova炎症肺中IL-17蛋白和mRNA的表达。此外,IC87114能够降低Th2细胞因子水平以及与IL-17表达相关的KC蛋白和mRNA的表达。PI3Kδ已被证明在炎症组织中中性粒细胞的积累和激活中发挥重要作用6,7。然而,PI3Kδ对中性粒细胞趋化作用的信号通路尚未明确。本研究结果表明,IL-17是PI3Kδ介导的中性粒细胞炎症的关键调节因子。综上所述,这些发现表明PI3Kδ抑制剂在哮喘中的治疗作用是通过下调IL-17的表达,从而减弱Th2细胞介导的嗜酸性粒细胞炎症和嗜中性粒细胞炎症来发挥的。
转录因子NF-κB在免疫和炎症反应中起重要作用,因此与哮喘的发病机制有关。正如预期的那样,在ova诱导的哮喘模型中,核NF-κB蛋白水平显著升高,表明NF-κB被激活。该转录因子的激活诱导许多炎症基因编码细胞因子(肿瘤坏死因子-α、IL-4、IL-5、IL-6、IL-9和IL-13)、趋化因子(RANTES(受激活调节,正常t细胞表达和分泌)、eotaxin和IL-8)、粘附分子(细胞内细胞粘附分子-1和血管细胞粘附分子-1)、生长因子和受体,这些都可能与哮喘的发病有关37。此外,在体外和在活的有机体内研究表明抑制NF-κB活化可减少IL-17的产生13,19- - - - - -21。这些发现提示NF-κB是IL-17表达的重要调节因子。PI3K/Akt通路的激活通过I-κBα降解导致NF-κB活性显著增强37,38。然而,没有关于PI3K催化亚基p110δ在NF-κB活化中的作用的数据。本研究表明,PI3Kδ抑制剂可显著降低变应原诱导的Akt磷酸化,显著降低肺组织中I-κBα降解和NF-κB活性。与已发表的数据一致38我们还发现Akt抑制剂增加了ova小鼠肺组织中I-κBα蛋白水平,同时降低了NF-κB活性。此外,给予NF-κB活化抑制剂BAY 11-7085或Akt抑制剂(图2 s见补充资料)。这些发现表明p110δ激活Akt,从而增强I-κBα降解和随后的NF-κB活化,从而调节变应性气道炎症中IL-17的表达。
总之,我们的研究结果表明,PI3Kδ的特异性抑制剂IC87114可以逆转哮喘的所有病理特征,包括气道炎症细胞浸润、Th2细胞因子水平和KC表达。此外,IC87114还能降低虫卵攻毒后肺组织中IL-17蛋白和mRNA的表达。这些结果表明,IC87114下调IL-17的表达,并减弱Th2细胞介导的嗜酸性粒细胞炎症和嗜中性粒细胞炎症。此外,我们还发现该PI3Kδ抑制剂可抑制NF-κB活性,NF-κB抑制可降低IL-17表达的增加。基于这些观察结果,我们认为抑制p110δ信号通路通过下调NF-κB通路并由此抑制IL-17表达而具有治疗哮喘的潜力。因此,本研究为使用PI3Kδ抑制剂预防和/或治疗哮喘和其他过敏性气道疾病提供了重要的机制。
致谢
我们要感谢M.J. Im(全北国立大学医学院,Jonju, South Korea)对手稿的批判性阅读。
脚注
本文的补充资料来自www.www.qdcxjkg.com
支持声明
本研究由韩国卫生、福利和家庭事务部韩国医疗技术研发项目(A084144)资助。
利益声明书
- 收到了2009年7月8日。
- 接受2010年3月15日。
- ©2010人队