摘要
事实上,肿瘤生长和扩散都依赖于血管生成,导致了胸部肿瘤的治疗策略,抗血管生成药物的作用进行调查,如非小细胞肺癌或间皮瘤。由于各种血管生成因子可促进血管新生的调控个体中的肿瘤,在增加临床试验代理量的时代,这是最重要的正确选择患者可能从特定治疗中获益。由于肿瘤血管发生的复杂性,各种生物标志物可以是适用的。例如,活化的血管生成途径的在内皮细胞中的分布可以以使有关选定的代理抑制给定的途径的相关性的结论来确定。另外,在基质和肿瘤细胞,以及在脉管系统中的结构改变蛋白质表达的变化,可用于预测和监测这样的治疗的临床效果。在这次审查中,从临床研究评价预测指标在胸癌抗血管生成药物的最新数据进行了总结。除了提供临床实例,调查基于临床前研究各种参数的理由进行说明。
临床研究正在探索多种针对特定受体或明确信号通路的治疗策略,包括胸肿瘤,如非小细胞肺癌(NSCLC)和恶性间皮瘤。一个这样的策略是基于广泛接受的观察,即肿瘤的发展和生长超过了一个确定的体积,存在一个功能血管系统是强制性的。因此,大多数实体肿瘤需要生成新的血管以进一步生长和转移,而这可以通过从原有的血管系统中诱导内皮细胞发芽来实现(所谓的血管生成)。1-3。可替换地,预先存在的脉管系统可能由肿瘤,其可具有在肺癌特别重要增选4,五。最后,血管生成已被证明起着重要的作用,至少在一些肿瘤实体中是这样,通过循环内皮前体细胞形成新的血管。这些过程受多种促血管生成和抗血管生成因子的调控,这些因子不仅可能由肿瘤细胞产生,还可能由基质细胞产生6。然而,到目前为止,血管内皮生长因子(VEGF)仍被认为是最有效的血管生成和内皮细胞生存因子之一。
最近,两项大型临床试验证明抗vegf抗体贝伐珠单抗联合含铂化疗对晚期非鳞状细胞肺癌患者的疗效,并获得美国食品和药物管理局的批准7,8。在ECOG4599研究中,15 mg·kg对NSCLC患者有显著的临床益处-1贝伐单抗联合卡铂和紫杉醇与用6.2的中值单独化疗被看见(风险比(HR)0.66无进展生存期(PFS)与4.5个月;HR 0.79总生存期的12.3位数与10.3个月)7。这些结果一定程度上被另一个大的III期试验,其中NSCLC患者具有通过添加低剂量贝伐单抗(7.5毫克的改进的PFS确认·公斤-1;HR 0.75)或高剂量贝伐单抗(15毫克·千克-1;以顺铂和吉西他滨作为标准化疗药物8。在后者的研究中,但是,PFS的中位数净增益是分别用于低剂量和高剂量贝伐单抗组,0.6和0.4个月。在两项研究中,有患者相当子集谁没有回应或正在治疗甚至经验进展8,9。因此,预测指标将是选择可以从治疗中获益患者有帮助。此外,附加的新试剂正在临床试验中进行测试(表1)。作为未来可能的后果,临床医生将需要决定哪些代理应该用于哪个病人。
作为一种假设,由于大多数新的药物如贝伐珠单抗都是针对一个确定的靶点,因此由其抑制所引起的假定靶点或结果的表达应该是指示对相应药物的响应性或耐药性的有用标记。一种针对特定途径的抗血管生成药物应该在那些严重依赖特定途径的肿瘤中发挥最大的作用。例如,如果一个肿瘤通过过度表达VEGF而上调了血管生成,那么抗VEGF治疗应该损害该肿瘤中新血管的形成。相反,如果分析显示,肿瘤除了vegf依赖信号外,还上调了血管生成途径,这些结果可能表明抗vegf治疗的耐药性。最后,抗血管生成治疗可能导致各种逃逸机制17,18随着选择性促血管生成途径的激活。这可能导致有必要重复评估选定的标记。因此,应在治疗前和治疗中或治疗后收集癌组织样本。此外,侵入性较小的方法也可能适用,包括测量蛋白质浓度的变化(如。生长因子)在体液中作为治疗的替代标记物。例如,血管内皮生长因子受体(VEGFR)-2阻断可显著提高小鼠血浆VEGF水平,并被认为是抗VEGF -2治疗的替代标记物19。
预测和预后标志物
预后因素是指患者或肿瘤的特征,它反映了肿瘤的生物学特性,并与患者的预后相关,而与治疗无关20,21。相反,预测标记是,应该给信息的患者是否可能受益于给定的治疗的患者或肿瘤特性。因此,预后因素确定对患者的肿瘤的效果,并且在未治疗患者中最好确定,而一个预测因子确定处理对肿瘤的作用20。
然而,大多数的因素都显示了混合预后和预测的关联。例如,增殖的标志物,如Ki-67的,即表现出强烈的预后效果也预测较大的反响,以最化疗方案21。此外,如下文所述,VEGF蛋白表达已被确定为NSCLC的预后因素22,23但ECOG4599研究结果表明,抗vegf治疗的反应增加也可能具有预测价值10。的是,在下文中描述几个分子因素已与肺癌预后的联系。尽管如此,下面将主要讨论当前试图建立抗血管生成疗法预测指标。
为了研究生物标志物是否对特定治疗具有预测性,临床试验应包括对患者来源材料的分子分析。最终的目标是确定一个有助于临床决策的生物标志物。然而,对生物标志物的研究才刚刚开始。即使是迄今为止发表的几项包含分子分析的大型临床试验,也产生了各种各样令人困惑的潜在标记。下面的综述应该对生物标志物检测的基本原理有一个大致的概述,具体取决于各自的靶点。
识别生物标记物的挑战
最常被探索的抗血管生成治疗的生物标志物类型包括肿瘤来源组织的研究和外周血分析检测到的循环标志物的评估。然而,尽管临床前研究的结果为预测生物标志物提供了有希望的候选,但将其转化为实践仍面临着重要的挑战。例如,用于测量各种生物标志物的技术还没有标准化。因此,需要对高质量试剂的选择、最佳方法和使用标准化协议的处理进行明确定义。如组织切片的保存时间、使用的固定剂类型和标记物的选择等变量可能会影响结果的质量。此外,对这些方法产生的数据的解释和评分也没有共识。正如下面所讨论的,目前的研究有时产生相互矛盾的结果,这至少部分是由于不同的方法。然而,诸如微血管密度(MVD)评估等标准化程序的尝试正在进行中24。此外,适当的临床试验设计为生物标志物鉴定和验证的选择是强制性的,因为最近描述25,26. 此外,由于血管生成的异质性和动态性,肿瘤的血管生成特征可能会随着癌症的进展和治疗的持续时间而改变27。因此,第一次处理前进行的活组织检查可能无法反映第二或第三处理前的生物学。然而,组织标记物的重新评估可能是困难的,因为额外的支气管镜或计算机断层扫描(CT)扫描引导的活检是必要的窝藏几个手术相关的风险。因此,不同类型的生物标志物的(如。成像和循环标志物)可以具有要被组合以产生“复合的生物标志物”,使更健壮的预测27。最后,大多数临床研究的一个特点是对包含在一个大的系列,其中的问题调查结果的代表性的患者相当小的比例进行生物标记物的研究。
标志物的肿瘤活检
微血管密度
大多数临床研究调查的患病率和血管生成在实体瘤预后的影响已经使用的组织样本并进行免疫组化后计算微血管。计数微血管的两种方法已被广泛使用:密度的方法,其中高浓度的容器的所有血管区域进行计数28,和Chalkley方法,使用一个网格来计算接触25个随机点读数的血管数量,这类似于相对面积估计,而不是真实的血管计数29。由于方法的不同,对实体肿瘤中不同血管生成参数的评估,包括标准的染色方案和评估标准,已形成国际共识24。
对于非小细胞肺癌,冲突的结果已经报告的MVD的患者各种子集的预后的重要性4,三十-32。一项荟萃分析得出结论,MVD似乎是一种预后因素,与非小细胞肺癌存活率降低相关,而与因子VIII、CD34或CD31阳性率的评估无关33。相反,另一项荟萃分析与这些结果相矛盾,部分原因在于不同的方法和统计分析34。这两项荟萃分析报告的结果在个别研究中存在相当大的差异,这至少在一定程度上是由于用于微血管染色和计数的不同方法造成的33-35。
作为一种假设,MVD也可能拥有关于肿瘤对抗血管生成治疗的反应的有价值的信息,因此,可以作为一种潜在的预测标记36,37。然而,在312分析一个总的813的结直肠癌患者用化疗治疗具有或不具有贝伐单抗,预治疗MVD不是为贝伐单抗添加推定的益处的显著指示器38。然而,据作者所知,尚无临床研究探讨抗血管生成治疗对非小细胞肺癌MVD的影响。由于大多数接受抗血管生成治疗的非小细胞肺癌患者是IV期患者,因此在支气管镜或CT扫描引导下的活检中最常分析肿瘤组织学。这些组织样本的大小是否能代表整个肿瘤是值得怀疑的39. 此外,相当一部分肺肿瘤似乎与先前存在的血管系统相结合,可能对预后和抗血管生成治疗的反应有影响4。最后,抗血管生成治疗不仅影响肿瘤血管也能正常血管40。作为假设,健康组织可因此被用于监测类似于使用抗内皮生长因子受体(EGFR)剂的临床研究抗血管生成治疗41。另外,血管密度和肿瘤内的血液供应可以通过放射学技术来估计,如对比增强磁共振成像或正电子发射断层扫描,这些技术最近已经被其他人研究过42。
肿瘤,内皮细胞和其它基质细胞的VEGF和VEGFR表达
内皮细胞中VEGF的表达和VEGFR的激活状态可能预示着抗VEGF诱导治疗的疗效。一项广泛的荟萃分析总结了VEGF或过表达在60% NSCLC中的报告22。大多数研究表明,VEGF免疫反应活性与肿瘤血管分布呈显著正相关22,43。此外,无论是高VEGF-A和VEGF-C蛋白的表达已与穷人生存的非小细胞肺癌在大多数临床研究的相关22,23。此外,内皮细胞、基质细胞甚至肿瘤细胞中都有VEGFR的表达44。然而,这些发现的临床意义尚不清楚。临床前数据表明,磷酸化的VEGFR的内皮细胞表达可能与VEGFR抑制剂的反应有关45。到目前为止,然而,也有表达相对VEGF已评估,以响应抗VEGF药物在肺癌没有临床研究。在278例转移性结肠癌临床试验,既不上皮和基质VEGF的表达也不MVD是有益的预测从加法贝伐单抗的基于氟尿嘧啶治疗38。另外,细胞内通路或其他影响vegfr依赖信号的生长因子的表达可能是抗vegfr2靶向治疗的潜在生物标志物46,47。来自临床NSCLC研究的数据正在等待中。
循环标记
循环血管生成标记
迄今为止,已经通过测量血清或血浆中的循环血管生成蛋白产生对抗血管生成治疗的潜在预测指标的大多数数据。临床前研究已经带来了多大的见识到了这些因素的作用。但是,这些因素或在治疗开始变化的血浓度是否可以保存预测值仍未确定。由于在临床研究中最抗血管生成药物重点瞄准的VEGFR信号通路,该通路已经被最广泛的探讨。
VEGF属于一个更大的家族,包括6个VEGF分子,VEGF- a到-E和胎盘生长因子(PIGF),以及3个VEGF受体,VEGFR-1到-32,48。在小鼠轴承人VEGF过表达的肿瘤,治疗7天有舒尼替尼,VEGF的小分子抑制剂和血小板衍生的生长因子(PDGF)受体酪氨酸激酶(RTKs),导致了在这两个循环小鼠的剂量依赖性增加,并且如通过物种特异性ELISA测试来确定肿瘤特异性VEGF血浆水平。相反,相反的周期性图案被认为与循环的可溶性VEGFR-2(sVEGFR-2),其可能通过介导的VEGF介导的VEGFR-2的下调49。有趣的是,VEGF的凸起和在sVEGFR-2分别减少也注意到在正常小鼠自由舒尼替尼治疗的任何肿瘤的,这表明这些分子变化是对药物治疗全身性反应和在最佳的抗肿瘤剂量的最大发生的变化范围19。
类似的临床前数据,与各种抗VEGFR抑制剂治疗的癌症患者显示增加的血浆VEGF的水平和降低的sVEGFR-2水平(表2)。在ECOG 4599研究中,一项II期/ III期试验随机选择878例晚期NSCLC患者接受卡铂和紫杉醇联合或不联合贝伐珠单抗,治疗前VEGF水平高的患者更有可能接受含贝伐珠单抗治疗,但这并不能预测生存率10。此外,血清VEGF水平也提示预后。VEGF水平低的患者与VEGF水平高的患者(中位4.5个月)相比,PFS更好(中位6.0个月);p = 0.04)10。然而,总共878名患者中只有166个样本可用于这些ELISA检测。
在一项探索性回顾性分析,在三个随机II期研究,其中包括凡德他尼,一个VEGFR,EGFR和RET RTK抑制剂进行分析预处理循环VEGF水平的预测值,无论是作为单一疗法或联合化疗晚期NSCLC13。在ELISA参考范围内基线VEGF值为健康受试者的患者,无论使用每日300 mg的治疗方案,其PFS都更优-1vandetanib与吉非替尼(HR 0.55;或与100毫克·天的组合-1范德泰尼布和多西他赛与多西紫杉醇(HR 0.25; P = 0.01)。然而,在PFS患者低基线血浆VEGF谁收到多西他赛和300毫克·天之间没有显著差异-1vandetanib与多西紫杉醇(HR 0.66; P = 0.33)。同样,低基线VEGF是不能预测的患者不同的PFS与卡铂,紫杉醇和300mg·天治疗-1凡德他尼与单独卡铂 - 紫杉醇相比(HR 0.72; P = 0.29)。此外,在一个患者子集,35个血管生成因子的血浆水平的多重分析是完成的。几个因素预后价值的,而低的人类生长因子(HGF)和白细胞介素2R水平仅在单一疗法凡德他尼臂分别预测的好处14。
对NSCLC患者类似,有限的数据都可以在恶性间皮瘤患者循环VEGF水平的预测值。在一个多中心,安慰剂对照的随机II期试验,108名间皮瘤患者用顺铂和吉西他滨的具有或不具有贝伐单抗联合治疗。在谁贝伐单抗患者接受,在等于或低于中位数基线VEGF水平与一个显著改善PFS(P = 0.043)和总生存期相关(P = 0.028)52。相反,较高的基线血浆VEGF水平具有预后价值,且与较短的PFS (p = 0.02)和总生存期(p = 0.0066)相关。提示抗vegf治疗对部分恶性间皮瘤患者有益;然而,还需要证实性研究。在另一项II期研究中,51例恶性间皮瘤患者接受了索拉非尼治疗,索拉非尼是一种VEGFR2抑制剂和PDGF受体-b53。相关的研究,包括P-ERK 1/2的表达,基线VEGF和PDGF水平已经完成,但结果尚未公布。
循环粘附分子
对于每一个抗血管生成剂,最终的目的是调节血管内皮细胞的功能和存活,如。通过抑制VEGFR活化。为了适当的内皮细胞功能,包括血管生成和现有血管的维护,内皮细胞必须牢固地粘附于彼此和细胞外基质(ECM)。因此,已经描述了各种细胞粘附分子(CAM)家庭提供特征性结构型态:该钙黏着蛋白,选择素,整联和免疫球蛋白超家族CAM54,55。此外,还存在一些CAM,它们与四个CAM家族的任何结构模式都不相同,例如上皮CAM。在各种血管生成因子的刺激下,CAMs可能会进入血液循环,成为内皮细胞被激活或受损的标志56。因此,选择CAMs已被调查作为潜在的标志物监测抗血管生成治疗。
内皮(E)选择素是由内皮细胞响应于炎症刺激合成,并参与白细胞和肿瘤进展的募集54,57。在外周血中可溶性E-选择素的表达水平通常与持续时间关联和炎性疾病的严重程度和细胞因子活化的血管内皮细胞的上清液中已经检测体外58. 然而,在非小细胞肺癌患者中,与良性肺病患者和健康志愿者相比,血清E-选择素水平升高的患病率在小范围肺癌患者中存在争议59,60。前面提到的ECOG4599研究分析了e -选择素作为一种潜在的外周血预测指标,该研究共纳入878名患者,其中149人使用了e -选择素。有趣的是,e -选择素在治疗7周后显著下降,而治疗组之间的变化幅度没有显著差异10。接受贝伐珠单抗联合化疗的患者e -选择素下降小于5.35 ng·mL-1有显著较长总生存期(HR 1.98; 95%CI 1.1-3.57; P = 0.02)与单独的化疗治疗的患者相比较。
另一类重要的CAMs是免疫球蛋白超家族,包括细胞间粘附分子(ICAM)-1。ICAM-1存在于多种细胞类型,包括静止内皮细胞61,在那里它参与白细胞向炎症位点的附着和随后的反式内皮迁移。活化的内皮细胞产生大量的膜的ICAM-1和棚的可溶形式(sICAM-1的),其本身可以促进血管生成和肿瘤生长62。而据报道,与对照组相比,非小细胞肺癌患者的sICAM-1水平明显升高,且与更严重的疾病相关63其他研究表明,sICAM-1的水平,并不一定反映膜表达的程度,并且可以被独立地调节61。尽管如此,sICAM-1已经在抗血管生成治疗的背景下被研究。ECOG4599研究发现,低基线icam水平是改善PFS的一个重要预测因素(HR 2.14, 95% CI 1.31-3.48),但当贝伐珠单抗加入细胞毒性治疗时,整体生存率(HR 1.39, 95% CI 0.84-2.3)并没有提高10。
钙粘蛋白代表另一个主要CAM家庭。基于序列比较它们可以被分为不同的亚家族,其中有经典的I型钙黏着蛋白,如E-和N-钙粘蛋白,和II型钙黏着蛋白55,64,65。血管内皮(VE)-cadherin,II型钙黏着蛋白,是一个严格的内皮特异性粘附分子,似乎是至关重要的用于内皮细胞接触维护和控制55。除了它的功能的粘合剂,VE-钙粘蛋白调节各种细胞过程,例如细胞增殖和凋亡,和调制VEGFR-2的功能。缺陷的小鼠在VE钙粘蛋白从血管畸形妊娠中期死亡66。因为在调节血管生成的基本作用的,VE-钙粘蛋白可以是用于抗血管生成治疗试验分析了一个有趣的标记;然而,从临床研究结果尚未出炉。
最后,整合素是细胞表面受体的大家庭由α和β链编码,调解cell-ECM以及信息交互67。在肿瘤,包括非小细胞肺癌,整合是通过ECM相互作用的侵袭和转移的介体68。特别有趣的可能是整合素αvβ3增生血管表达但是不一样在正常、血管69。不过,尽管αvβ3整合素已经被评价为在临床前和临床研究的目标70,71和被阐明血管生成的分子成像使用αvβ3有针对性的纳米粒子,它的使用作为抗血管生成疗法的潜在生物标志物仍是投机。
循环内皮细胞
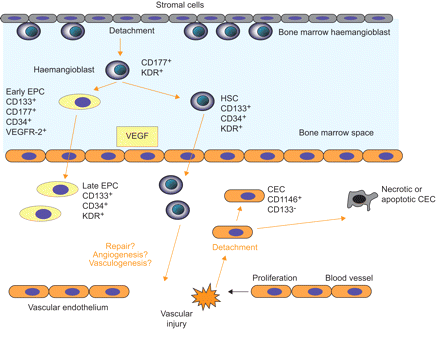
除了血管生成和原有血管的共同选择外,血管生成德新生内皮祖细胞(endothelial progenitor cells,EPCs)合成新的血管在胚胎发育之外发挥着重要作用(图1)73。从1997年开始,不同的研究小组报道了从成年人中培养CD34+祖细胞离体74,75这可能有助于移植物和血管假体的再内皮化75,76。而内皮祖细胞的掺入已被证明在肿瘤血管形成73,这一发现的意义一直争论不休。在健康个体中,EPC码低(77然而,它们的数量在血管损伤和心肌梗死后趋于增加78-80。在不同的研究,矛盾的数据已经报道了肿瘤患者,包括NSCLC,内皮祖细胞的定量相比健康对照77,81。尽管如此,内皮祖细胞的重要性可能增加的促血管生成因子如VEGF和HGF的释放有可能预后影响在一系列的53名NSCLC患者证明81。此外,抗血管治疗可能改变EPCs的数量,这可能对治疗反应具有预测价值。血管阻断剂对荷瘤小鼠的治疗导致循环EPCs的急性动员,这是由VEGFR-2、CD13和CD117阳性测定的结果82。结论是,有兴趣评估EPCs作为药物治疗监测的标志物的作用83。
起源和内皮祖细胞(EPC)的分化的方案。造血干细胞(HSC)衍生的EPC和循环内皮细胞(CEC)能够在血管损伤,修复和血管生成中找到,并且通过不同的标记物表达谱的特征。VEGF:血管内皮生长因子;VEGFR-2:血管内皮生长因子受体2;VEGFR-2 / KDR:激酶插入结构域受体。改编自72得到出版者的许可。
除EPCs外,外周血中循环内皮细胞(CECs)的存在被认为是血管损伤的一个有前途的替代指标。在健康人中,cec很少被发现,而在各种癌症和淋巴瘤患者中,cec的数量有所增加77,84. 乳腺癌研究表明CECs是节拍器化疗患者的预后指标85。此外,体内研究描述了抗血管生成治疗后CEC水平的变化。在EGFR和VEGFR-2抑制剂vandetanib治疗3天后,Lewis肺癌小鼠的CECs增加,但EPCs没有增加,这是在肿瘤体积减少之前86。
然而,争论关于内皮祖细胞和CEC上的识别存在。由于标记物特征已经从培养的单核细胞产生的离体(图2),这些细胞的表型可能由于培养条件的不同而发生了改变,包括来自我们实验室的初步数据(80,87和未发表的结果)。最初,内皮祖细胞被定义为阳性细胞都造血干细胞标记物如CD34和内皮标记物如VEGFR275. 然而,由于CD34也在成熟的内皮细胞上表达到一个较低的水平,评估额外的标记物,如CD133阳性,似乎只在造血干细胞上表达是强制性的80。迄今为止,大多数作者认为重合CD133 / VEGFR2阳性细胞表示与内皮祖容量的人口72,80。类似地,不同标志物表达模式已经被用于的CEC说明。最团体要求的内皮细胞标记物,如CD31或CD34的检测,在没有CD133表达的72,85。此外,大多数作者使用的流式细胞术分析产生的结果可能受到几个因素的影响,如单核细胞的分离、洗涤和离心步骤、单克隆抗体的面板和没有标准化的门控技术。因此,已经尝试了各种改进,包括特异性和非特异性抗体组合88使用一个确定的过滤器来分离EPCs,而不是对血液样本进行离心分离89。
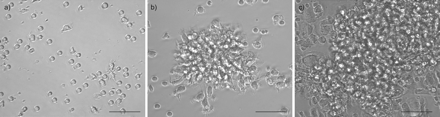
从外周血内皮前体细胞(EPC)的生长。CD34 +细胞的耗竭后,外周血细胞在明胶包被的烧瓶培养。于7天后,菌落通过EPC衍生的内皮细胞形成。在a)之后1天,B EPC衍生内皮形成细胞集落的特性图象)5和c)培养7天后示(倍率×200)。比例尺=100μm左右。
确凿,而关于起源和循环内皮细胞的特征仍然存在许多问题需要解决,这些细胞可能还是看好的预测标志物抗血管生成肿瘤治疗已经没有在大型临床研究解决。
未来发展方向
作为新的治疗选择的出现,希望用我们的肿瘤分子生物学的知识不断增加,优化和个体化癌症治疗。但是,适当的临床试验评价指标的效用一个精心设计是必需的,并已在别处描述21,25,90。除了上面描述的参数,各种其它因素可以适用于抗血管生成治疗的预测价值。例如,其他血管生成因子的宿主也有助于血管形成中的肿瘤。此外VEGF,这被称为用于调节血管生成,其它生长因子,诸如PDGF,碱性成纤维细胞生长因子和血管生成素,以及各种的CAM的关键因素,也已显示出在各种肿瘤模型中的重要性。在临床前研究中,一组六个基因被鉴定为在肿瘤衍生的内皮细胞中选择性超表达91。因此,它可能是合理的屏幕肿瘤或血液样品几个关键调节分子,以确定在其上的血管生成因子的肿瘤很可能是相关的。
此外,影响血管稳定性的血管重构可能是内皮细胞对抗血管治疗反应的重要决定因素。在这一过程中,内皮细胞与周细胞、血管平滑肌细胞、成纤维细胞等基质细胞的相互作用起着基础性作用92,93。周细胞的重要性已经明显证明了在PDGF-B缺陷的小鼠,导致有缺陷的血管发育94。因此,除了作为预后标志物4,血管周细胞覆盖率的测定可能是血管易受抗血管生成和抗血管生成药物影响的预测指标95。
与单一因素相比,标记物或“标记”的组合可能被证明具有更大的预后和预测价值。尽管将来我们可能无法确定每个病人的特征,但我们的主要目标将是定义对所选药物反应异常增强或减弱的子组。随着生物标志物研究数量的增加,我们希望,这将导致更多的特征明确的患者亚群,这可能会改善治疗计划和延长总体生存期。
脚注
感兴趣的语句
没有宣布。
- 收到2009年5月6日。
- 公认2010年3月10日。
- ©2010人队