摘要
α.1-抗胰蛋白酶(AT)缺乏是一种遗传性疾病,可能导致早发性肺气肿和晚年慢性肝病。虽然有验证的测试方法,但绝大多数α1-AT缺陷的个体仍未核准。已发表推荐用于测试和诊断α1- 缺乏;但是,最好的做法指南并不明确。
在我们的文章中,我们回顾了近年来发生的诊断技术的发展,并描述了我们在欧洲的三个中心使用的实践。α含量的测定1-AT和基因分型被报道为主要的诊断步骤,而等电聚焦(也称为表型)保留用于确认分析。
提出了以下最佳实践建议:检测所有PiZZ和其他严重缺陷个体;自动型;参考标准品的制备;质量控制规划;制定标准操作程序文件;以及采集干燥血液样本的标准化方法。建议实验室之间加强合作,共享知识,以提高严重α病的诊断效率1-AT缺乏,增加被疾病检测到的个体的数量,并协助建立新的患者识别计划。
缺乏α1- antiTrypsin(α.1-AT)是世界上最常见的遗传性疾病之一。α的主要生理作用1-AT(也称为α -1蛋白酶抑制剂)是保护肺组织免受蛋白水解酶,特别是中性粒细胞弹性酶的损害。合成α1-AT主要发生在肝脏内。在α1-AT缺陷,α的聚合1-At糖蛋白导致其在肝细胞内积聚,并且减少水平被释放到循环中。当肺α的浓度1-AT低,中性粒细胞弹性蛋白酶不被α中和1-AT并可以破坏肺组织,导致早起的肺气肿,特别是在吸烟者中。用于编码α的Serpina1基因的特定突变的进一步临床表现1-AT是肝病,婴儿疾病作为肝炎和黄疸,作为儿童和成年人的肝硬化。
合成α1-AT是由两个等位基因的共显性表达控制的,且具有α的个体1-AT缺乏遗传了α的两个异常蛋白酶抑制剂(PI)等位基因1-At基因座。主要正常等位基因是M等位基因,PIMM基因型存在于94-96%的高加索人中1.最常见的缺陷变体是Z等位基因,>95%的严重α型患者1-AT缺乏携带PIZZ基因型2.血清α1在具有PIMM和PIZZ基因型中的个体中测量的含量为20-48μm(1.5-3.5g·l-1)和2.5 ~ 7 μM (0.20 ~ 0.45 g·L .-1)分别和<11μm的浓度(0.80 g·l-1放射免疫< 1 ?显示= (fo) ?>扩散,或0.50 g·L-1-Nephelometry,见下文)与肺气肿的风险增加有关3..
α的绝大多数人1-未发现at缺陷;然而,测量α水平的有效方法1-AT在血液中,并为确定诊断α1-AT缺陷通过测定个体在Pi位点的遗传组成,已经有很多年了。世界卫生组织(世卫组织)和美国胸科学会(ATS)与欧洲呼吸学会(ERS)合作编写了报告188bet官网地址3.那4.其中包括筛查和检测α的建议1- 使用这些既定的程序缺乏缺陷。但是,世卫组织和ATS / ERS建议不提供关于实施筛选或诊断程序的最佳实践指南,并且尚于,尚可探测α的理想实验室程序算法1-AT缺陷载体尚未建立。
自从2003年最新的ATS/ERS建议发表以来,诊断α的技术有了进一步的进步1——缺乏。我们的文章将描述我们三个欧洲中心使用的现有做法,这些实践具有在测试和诊断疾病的测试和诊断中的专业知识。我们的实验室利用并利用了诊断方法的改善。我们希望分享我们的经验,以提高α的实验室诊断的质量和效率的目标1-AT缺陷,并促进建立成功的诊断项目,以发现更多的受影响的个人。
流行病学
流行病学研究表明,美国的〜100,000人有α1-AT缺乏3.美国和欧洲也有类似的数字2.α的流行病学和地理分布1-AT缺陷已被许多作者综述2那5.-8..据估计,全球有340万人携带PiZZ、PiSZ或PiSS基因型,1.16亿人携带PiMZ或pim基因型杂合子7..已经在几个国家开展了有针对性的筛查研究,以发现α病例1通过测定慢性阻塞性肺疾病(COPD)患者样本中Z和S等位基因的频率来检测-AT缺陷9.-13..
α的临床识别1-AT缺乏和现有的测试建议
尽管α1-AT缺乏在20世纪60年代首次报道,诊断疾病的个体的数量只是从筛查研究和基因频率估算中预测的少量比例。<美国有10%的人有α1-AT缺乏识别13.-15.据估计,在美国高达3%的COPD患者可能有未诊断的α1-AT缺乏4..对305,009例α预期病例的调查1- 八个其他国家的缺乏表明,这些病例中只有1,068人实际诊断出来8..诊断的长期延迟也是普遍的;而大多数人从未诊断出来,那么在最终被诊断出发现的小群体中进行的一项研究发现,症状发作和α的诊断之间经过的平均值7.2 YRS1-AT缺乏,44%的人报告诊断前至少看到三个医生16..最近,报告了8.3年的平均诊断延迟15..
有至少两个原因来解释为什么α1-AT缺乏没有得到医学界的充分认识。首先,许多医生对这种疾病并不熟悉,也没有意识到肺部疾病与普通(IE。吸烟相关的)COPD实际上可能是由于α1——缺乏。他们也可能没有意识到肝病的症状也可以由α引起1——缺乏。其次,许多具有严重α的受试者1-AT缺乏可能没有在肺功能临床上产生临床显着损害,并且可能没有临床症状8..
在他们关于α的诊断和管理标准的声明中1-AT缺乏3.在美国,ATS/ERS就基因检测是否应该进行提出了建议。考虑到检测的好处和所涉及的不利问题(对个人的心理影响、经济成本和伦理考虑),根据此类检测的支持性证据的水平对其进行分级。明确推荐进行基因检测的临床环境(a类推荐)见表1⇓.ATS/ERS还建议每一个α值较低的人1-AT水平应通过表型(等电聚焦)或基因分型检测一次。
世界卫生组织建议,所有COPD患者、成人和青少年哮喘患者以及所有有家族病史的患者都应进行一次α筛查1定量检测at缺陷4..所有具有异常α的受试者1-AT应随后进行表型分析。
不幸的是,上面描述的检测α的指导方针1-AT缺乏,特别是检测所有有症状的COPD成人的建议,没有常规遵循。为了帮助医生识别这种疾病,ATS和ERS强调了以下应引起怀疑的症状1-AT缺乏:早发型COPD(年龄<45岁);无公认危险因素的肺气肿(如。抽烟);肺气肿突出的基础血清;支气管扩张没有明显的嗜期学;不明原因的肝病;血管综合征(抗蛋白酶-3-血管炎,坏死潘霉炎)3..α.1-AT缺乏症也应怀疑具有肺气肿,支气管扩张,肝脏疾病,Panniculitis或病症本身的家族史。但是,我们必须记住,必须实现的真正目标是测试所有在生活中至少一次的患者3.那4..
与其他成人发病的遗传疾病一样,识别具有α基因突变的个体1-AT缺乏可促使这些人避免出现症状性疾病的危险因素,如吸烟和暴露于环境污染物中。研究表明,在出生时就被认定为α型糖尿病的个体中,青少年吸烟的频率较低1-AT缺陷组与对照组比较17.那18.以及增加了禁止诊断为α基因型的成年人吸烟的动力1-AT缺乏19.那20..然而,这种益处需要权衡对心理效应的权衡,例如个人对疾病的易感性的焦虑,并且存在遗传测试的其他不利影响,例如雇主的歧视和拒绝健康保险。此外,在遗传性疾病的情况下,例如α1-AT缺乏,遗传测试也对家庭成员产生了影响。建议患者提供有关α的信息1-AT缺陷和基因检测的含义(医学、社会、情感)已被仔细解释3..
α的诊断方法1——缺乏
测试α的程序1-AT缺陷自20世纪60年代以来就已经存在,并且在这期间引入了新的技术。方法学的这些进展应该有助于更快速、更方便和更经济的α检测方法的广泛应用1-AT缺乏症,从而导致越来越多的人被诊断患有这种疾病21.目前已被验证的不同方法对疾病的测试和诊断进行评估2⇓和3⇓.
大规模的α筛选计划1-AT缺陷以前由于需要抽取静脉采血,然后将潜在生物危险的样本运送到检测实验室而受到阻碍。在过去几年中,已经开始使用干血点(DBS),即对在滤纸上干燥的几滴血液进行检测(编号903;Schleicher & Schuell, Bioscience Inc., Keene, NH, USA)。研究了DBS方法对α的适用性和可靠性1-AT缺陷检测已被广泛描述9.-11.那21那23-26.表2综述了全血样本和DBS的优缺点⇑.用于测定α的试验1-血液中的at水平(免疫分析技术,比浊法)以及诊断程序(表型和基因分型方法)列于表3⇑.
α的识别程序1——缺乏
我们想要解决的初始问题是,首先是“应该被筛选谁?”并且,第二,“只能通过测量α来进行筛选1-AT血液中的浓度,或者如果α在α的等位基因中应该完全诊断1——基因位点吗?”我们决定将我们的初步检测程序称为“有针对性的检测”,而不是诊断或筛查,因为显然,应该优先考虑COPD患者。然而,“谁应该成为检测的目标?”“不能完全得到回答,这取决于现有的资源。目标检测和诊断的步骤将包括表1所示的类别⇑.
然而,α的检测方法已经被验证1-AT缺陷,没有一个建立的算法来检测和诊断疾病,世界各地的实验室和国家普遍使用。因此,比较和审查不同中心目前采取的程序和倡议是很重要的。通过这种知识分享,我们可以为有效的方法学和诊断算法提出建议。
测试和诊断算法
我们在此报告目前在欧洲的三个实验室中雇用的程序,致力于检测α的国家计划1-AT不足,即意大利帕维亚大学;德国马尔堡大学;西班牙巴塞罗那瓦尔德希布伦医院生物化学实验室。这些中心目前使用的目标检测算法如图1所示⇓-⇓3.⇓.帕维亚(图1)⇓),在算法的第一阶段进行基因分型,同时定量测定α1-AT级别。在另外两个实验室(图2⇓和3⇓),测定α1-AT水平先于基因分型。在巴塞罗那进行的一项研究中,对971例COPD患者的样本进行分析,发现没有一个样本的α值正常1-AT水平来自携带PiZZ表型的个体。由于成本的原因,决定只对含有α的样品进行基因分型1-at以等于<1g·l的dbs浓度-1(∼14μM)。当对另外1166个样本进行这一程序时,与对所有2137个样本进行基因型筛选的成本相比,成本降低了30%11..因此,西班牙注册表推荐的当前实践是用于确定α的实验室1-AT水平,然后只将浓度低于正常的样本送到巴塞罗那中心进行基因分型,以确定Z和S等位基因。
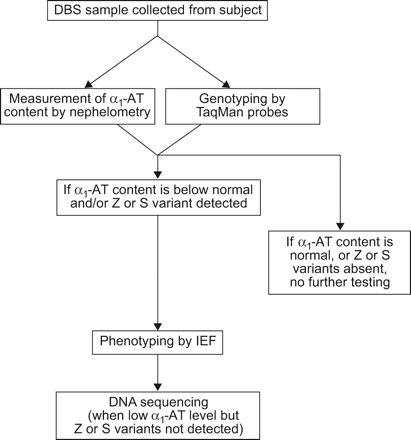
从帕维亚大学,意大利帕维亚大学测试算法。DBS:干血斑;α.1——:α1抗胰蛋白酶;IEF:等电点聚焦。
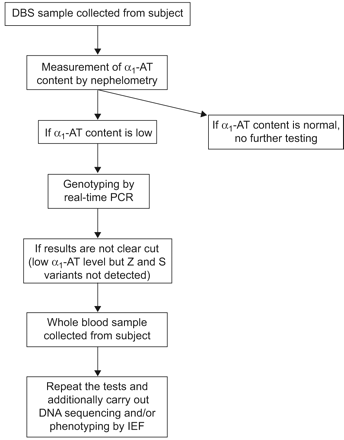
西班牙巴塞罗那瓦尔德希布伦实验室的目标检测测试算法。DBS:干血斑;α.1——:α1抗胰蛋白酶;IEF:等电点聚焦。
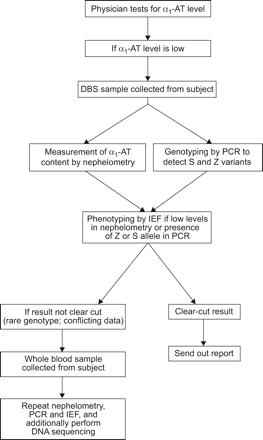
德国马尔堡大学的测试算法。α.1——:α1抗胰蛋白酶;DBS:干血斑;IEF:等电点聚焦。
表型在帕维亚和马尔堡中心仅在具有α的样品上进行1-AT水平以前确定为低于正常,在事先检测Z或S变异后,或在α之间的差异1-AT水平和基因型。相比之下,在巴塞罗那,表型没有在目标检测项目的任何阶段进行,只保留在与帕维亚和马尔堡相同的情况下进行诊断评估,主要是在检测到低α之后1-AT浓度,或者在α不一致的情况下1-AT水平和基因型。
一般来说,最初的样本以DBS的形式进行检测,全血样本仅用于确认性检测和DNA测序。当聚合酶链反应(PCR)无法完全鉴定两种α时,通常采用外显子DNA测序来确定样品中实际存在的变异1——等位基因。我们主张任何诊断程序的首要目标应该是检测所有具有ZZ表型的个体。如果资源有限,S等位基因的检测是次要的目标。利用PCR进行基因分型的优点是可以给出明确的答案,例如,Z或S等位基因是否存在。PCR方法可用于自动化,IE。快速筛查是否存在S和Z等位基因27-29.自动基因分型手术可能比其他筛选更多数量的方法便宜。然而,这种方法不会检测稀有变体,并且在这些情况下,需要进一步的测序分析来获得最终的诊断。
α的检出率1——缺乏等位基因
每个实验室的检出率无法进行比较,因为它们主要取决于筛查患者的特征,就血浆α的截取而言,仅部分取决于算法1-AT水平25.在常规实践中,在帕维亚基因分型测试的样本总数的〜30-35%的〜30-35%中观察到Z和S变体(存在于纯合和杂合子中)的检测,并在12%的基因分型样品中进行在马尔堡。在巴塞罗那,检测程序保留具有低浓度α的样品的基因分型1-AT,根据预先设定的阈值,约占总样本的7-10%。在40%的基因分型样本中检测到Z和S变异。当Z和S变异未检测到时,进行测序以确认缺陷等位基因。在Pavia的所有基因分型样本中,还有10%的样本检测到非z和非s罕见缺陷等位基因。在马尔堡,已经测序的96个样本中发现了3个新突变和45个罕见基因。关于检测方案的个别结果的更多数据可在原始出版物中找到9.那11.那12.那30.那31.
样品收集
我们认识到,在样本到达实验室进行测试之前,我们可以改进样本的收集。尽管DBS的运输比全血更容易,成本更低,而且个人可以自己发送样本,但在DBS的采集过程中出现了问题,高达15%的样本被拒绝。表4列出了改善DBS收集流程和降低拒收率的建议和实际建议⇓.
实验室协议的质量控制与优化
一个关键问题是在执行α的不同实验室中建立有效质量控制过程1——缺乏测试。例如,在德国,实验室注册了外部测试以保持所用PCR方法的质量控制。主要步骤将由从事测试的每个实验室发展参考标准。这些措施将协助许多实验室在继续在长期测试样品时保持一致性。采取此类措施,应考虑的另一个举措是制定标准操作程序文件,以便对实验室提供新计划的质量控制1——缺乏测试。每个实验室内部的一致性被认为是最基本的,使用参考标准的信心将随着时间和经验的积累而建立起来。
成本分析
每个样本的成本取决于应用的协议和当地成本。巴塞罗那检测项目中检测的每个样本的平均成本(保留对低α样本的基因分型)1仅限at浓度)为13.4欧元。在帕维亚,基因分型每个样本的成本为13.5欧元,另外还需要对所有样本进行c反应蛋白水平测定的成本为5欧元。马尔堡的检测项目每个样本的平均成本为33欧元。测序的成本更高,取决于设备,但可能从48欧元到150欧元不等。
讨论
没有α的人数不足1目前正在检测at缺陷。我们这篇文章的目的是通过分享我们在欧洲三个成熟的中心取得的经验,促进在更多的实验室和其他国家建立新的病人鉴定项目。为了协助每一个新的实验室规划建立一个检测方案,我们的目的是提供一个详细的测试方案和当前的诊断技术的描述,并提出改进实验室实践的建议。我们应该强调,我们文章中的建议是基于我们自己的经验,而不是任何科学团体的官方建议。
具有α的个人1-AT缺乏可能导致多年来无法解释和管理不善的肺部疾病。尽管世卫组织和ATS/ERS对诊断的重要性提出了明确的建议,但医生的做法变化很小;许多医生仍然完全不知道这种疾病,可能只看到一个人被诊断为α1-AT缺乏症事实上,α1-AT缺乏是一种被描述为“从阴影中浮现”的状态。α的早期检测1-缺乏at会使个体改变他们的生活方式(如。戒烟;锻炼和肺康复;氧气补充;接受营养支持)以防止发病率的发病。特别是,烟草吸烟与α的受试者的肺气肿的发展高度相关1-AT缺乏32-34.吸烟者可能早几年出现肺部疾病的症状(如。在人生的第四个十年3.),肺功能下降更快35-38.重要的是,该病的早期诊断还能使患者接受对α的有效治疗1-AT缺乏,如增强治疗39.
我们的文章已审查了验证程序,目前可用于屏幕,并诊断α1——缺乏。自α检测以来,这些方法的发展取得了很大进展1-AT缺乏症是40年前首次出现的。然而,一个主要的挑战仍然是利用现有的技术来增加α个体的数量1-AT缺乏症实际上被诊断出患有这种疾病
在我们中心使用的程序方面存在一些差异,但这些差异相对较小,至少在鉴别严重的α患者方面是如此1——缺乏。因此,可能有一些与α杂合子的携带者1- 错过了截止值的等离子体水平。对肺和肝疾病的共同因素的这种条件越来越兴趣,因此我们可以假设将来,检测程序将被设计为将它们包含在诊断流程图中。如算法中所示的主要诊断步骤由三个中心共享。每个算法包括基因分型,并且认为有必要检测与PIZZ基因型的所有个体。我们同意测量α的水平1血液中-AT和基因型的测定是目前主要的两种诊断技术。我们认为等电聚焦的表型不再是诊断α的“金标准”1-AT缺乏(几年前的ATS / ERS声明中提到了3.),并考虑等电聚焦只能作为确认分析的反射工具。此外,应该指出的是,其他两个实验室,都在美国,现在也接受基因分型和测定α1-AT级别作为主要的诊断方法,并公布了他们的算法的细节,基本上与我们自己的相似40那41.
可能有很好的理由需要考虑调整不同实验室和国家的算法。驾驶实验室拥抱新方法的关键动机因素是需要开发更便宜的技术。对于大型案例检测程序,需要简单,廉价的测试。因此,应提高测试方法以提高效率和吞吐量。建议各个实验室应对他们目前正在使用的不同方法进行成本分析,以协助开发最具成本效益的目标检测方法。本课程可能会导致不同的实验室使用更标准化的测试和诊断方法。在开发标准化方法方面可以实现共识的情况下,可以向医生呈现更一致的消息,以鼓励他们参与患者识别。
我们建议各化验室采用参考标准,并建议由专业中心向各化验室提供标准样本,让他们自行制定标准。同样,建议建立质量控制规划,以便现有的筛查和诊断实验室以及将开始参与检测α的实验室参与1——缺乏。最后,技术的发展可以改善和加快DBS的收集过程。
为了增加α的数量1- at缺陷个体的识别,有必要提高对该病的进一步认识。诊断规划的成功在很大程度上取决于医生和其他保健提供者的热情和承诺;因此,提高认识的战略应包括鼓励医学界关注的方法。提高α人群的意识也同样重要1- at缺陷个体以及更广泛的人群中。宣传活动的一个关键方面,以增加对α的知识1-AT缺乏是强调疾病的主要风险因素,以及患者因此需要改变生活方式。如上所述,在α型糖尿病患者中,吸烟与肺部疾病症状的发展密切相关1-AT缺乏症,戒烟是治疗该疾病的首要任务30..有许多不同的方法可以提高对α的认识1- 缺乏;这些总结在表5中⇓.
总而言之,在实验室目前执行严重α的方法中存在着微小而非关键的差异1——缺乏测试。但是,需要更密切的合作,例如在实验室和国家之间分享议定书和技术知识(例如通过Alpha One国际登记处(AIR)方案)43)例如,可以实现协议,例如,更有效和经济高效的方法。建议可以获得改善α的最佳实践1-AT缺陷和增加个体的数量(表5)⇑),我们目前的建议可用于协助实验室建立α的规划1-AT缺陷检测的未来。
兴趣表
M. Miravitlles,I. Ferrarotti,M. Luisetti和R. Bals的宣称。www.www.qdcxjkg.com/misc/statements.dtl
致谢
编辑辅助由Parexel的M. Kenig提供,并由Talecris BiothyApputics提供支持。
- 收到了2009年4月29日。
- 公认2009年10月23日。
- ©ers Journals Ltd















