抽象的
支气管扩漏(BPD)的特征在于肺泡,炎症和异常血管发育受损。磷酸二酯酶(PDE)抑制剂可以影响细胞增殖,拮抗炎症和恢复血管发育和稳态,表明BPD中的治疗潜力。
本研究的目的是探讨高氧暴露小鼠的肺中的PDE表达,并评估PDE4作为BPD中治疗靶标的活力。
新生C57BL/6N小鼠暴露于常氧或85%氧环境中28天。高氧环境下动物的生长和动态呼吸顺应性降低,同时伴有鼻中隔减少、空气体积增大和鼻中隔壁厚度增加。高氧暴露14天后变化明显,28天后更明显。在mRNA水平上,高氧条件下PDE1A、PDE4A上调,PDE5A下调。免疫印迹法在蛋白表达水平上证实了PDE4A和PDE5A的这一趋势。用西洛米司特(PDE4抑制剂,5 mg·kg)治疗-1·天-1)在第14天和28之间,显着降低了平均肺泡距离,隔膜壁厚和总空隙区域以及改善的动态肺顺应性。
药物抑制磷酸二酯酶可改善高氧诱导的支气管肺发育不良患者的肺泡化,从而为临床治疗支气管肺发育不良提供一种新的治疗方法。
支气管扩张性发育不良(BPD)是暴露于高氧水平和机械通气的早产儿的慢性肺病1那2并且其特征在于肺泡的发音。BPD的总体发病率在过去十年中没有改变3..总而言之,75%出生体重≤1,000 g且小于32周胎龄的婴儿存在BPD,这仍然是肺部疾病的主要原因,并持续到成年4..由于改善治疗策略,BPD的病理学图发生了变化。具有突出纤维增生的“旧”BPD现在越来越频繁5..“新”BPD的特征主要是通过具有大,简化的肺泡结构的远端肺生长,疑风毛细血管构型和可变间隙性细胞的破坏5..这导致肺泡和降低的气体交换表面积减少6..
BPD是一种具有多因素的疾病5..BPD的发病机制涉及极端的肺部不成熟,治疗诱导的氧气,卷虫和巴罗拉姆损伤,炎症反应引发肺损伤和不同程度的紊乱修复6..微血管发育也受到损害7.那8.,可并发肺动脉高压(PH)9..病理生理机制包括异常细胞增殖,炎症,氧化应激,感染和微血管发育受损10..
环磷酸腺苷(cAMP)和环磷酸鸟苷(cGMP)在信号转导中起关键作用11.因此,对BPD发病机制的生理过程的调节。这些环状核苷酸通过环状核苷酸磷酸酯酶(PDE)来代谢细胞内12..PDE超家族目前由11名家庭成员组成,具有不同的营地和/或CGMP的选择性11..几种PDE在新生儿和成人肺组织中丰富13.那14.,包括PDE1,PDE4和PDE5同种型11..PDE5在血管稳态中的记录作用导致对PDE5抑制剂的评价用于治疗血管部件的疾病,包括pH值15.那16.和BPD.17..在BPD的背景下,用Sildenafil处理高氧暴露的大鼠幼仔,选择性PDE5抑制剂,保存的肺泡生长和血管生成,并降低了pH的结构证据17..这些数据表明,PDE调节的循环核苷酸水平确实在小鼠中的高氧肺损伤中发挥作用。
大部分细胞camp水解活性归因于PDE4家族11.,由四种不同的基因组成,这是普遍表达的18.并且已经在炎症性疾病(如慢性阻塞性肺病(COPD)中的治疗毒性为治疗靶标的评估,具有PDE4特异性抑制剂西莱拉斯特19..Pentoximiflline,已显示非选择性PDE抑制剂,以减少纤维蛋白沉积并延长高氧肺损伤的存活20..一项初步临床研究表明,己酮可可碱在预防极低出生体重婴儿BPD的治疗益处21..选择性PDE4抑制剂的抗炎作用也已在大鼠的高氧肺损伤中评估。在该模型中,Rolipram和Piclamilast降低了炎症和纤维蛋白沉积,延长了存活率22..这些数据在一起支持BPD中PDE的作用以及靶向PDE4的治疗潜力,特别是在BPD中。为此,本研究的目的是研究来自具有高氧诱导的BPD小鼠肺组织中PDE的表达谱,并评估CILOMILAST作为一种新的治疗方法的PDE4抑制的潜力。
方法
实验动物和高氧暴露
来自查尔斯河实验室(Sulzfeld,德国Sulzfeld)的怀孕C57BL / 6N小鼠保持在12/12-H光/暗循环上。实验是根据国家和国际法规的制度指导进行。在出生后12小时后,将幼崽浸入85%的氧(Hyproxia)或室内空气(常规)28天。每24小时避免氧气毒性,水坝在高氧和常氧笼之间旋转。在产后(P)天P7,P14,P21和P28时记录体重。
药物管理
用PDE4抑制剂,纤氯蛋白处理超氧暴露的动物,溶解在二甲基磺砜(DMSO)中,并在颈部以5mg·kg皮下注射-1每日一次每天一次P14和P28。对照组单独接受DMSO。最初以30mg·kg的剂量注射纤毛石-1·天-1,先前报道的治疗方案在活的有机体内大鼠移植模型23.;然而,所有的动物都在5天内死亡。因此,实验剂量设为5 mg·kg-1·天-1,耐受性良好(西洛米拉斯特治疗组用药14天后生存率为100%)。
组织制剂,肺部形变分析和合规测量
在Days P7,P14,P21和P28,通过腹膜内注射戊巴比妥钠的百叶菌进行安乐死。如前所述处理肺部的蛋白质或RNA分离24..对于组织学分析,如下进行肺的固定。中间胸骨切开术后,气管是插管,固定肺部原位在20cmH的压力下,磷酸盐缓冲盐水(pH7.0)中有4.5%甲醛2o(1.96 KPA)。在4.5%甲醛中过夜固定后,肺部嵌入石蜡中。如前所述,在3μm肺截面中测量平均线性截距,平均隔膜厚度和总空位区域24.那25..动态肺顺应性(Cl,dyn.)通过容量控制压力限制依从性方法评估,小鼠以6 mL·kg的潮气量通气-110分钟24..
半定量RT-PCR
使用Trizol(Invitrogen,Karlsruhe,Germany)从肺和肾均匀分离出总RNA。逆转录(RT)反应如前所述,使用Improm-II RT系统(Promega,Mannheim,德国)进行26..对于cDNA合成,使用2μg总RNA。前向和反向PCR引物是:PDE1A 5'-GCTTCTCATTTTCTCCACTTGTG-3'和5'-AGCCAACTCTTCCACCTCTCT-3'(361bp片段);PDE4A 5'-AGGAGCGGGACTTACTGAAGA-3'和5'-CCTTTTGACCTTTGACTGTTCCAT-3'(1,057 BP片段);PDE5A 5'-CCTGACTTTTCTCGTGTGTT-3'和5'-CTGCTCATCATTTGGTTGA-3'(342 BP片段);和甘油醛-3-磷酸脱氢酶(GAPDH)5'-GCAGTGGCAAAGTGGAGT-3和5'-ACAGTTTCTGGGGTGGCAGT-3'(493BP片段)。在解析琼脂糖凝胶中的PCR产物后,使用Biodoc分析仪软件(Biometra,Goettingen,德国)量化扩增子的带强度,并且PDE同种型的带强度被标准化为来自相同样本的GAPDH扩增子的带强度。
免疫印迹
蛋白质裂解物的标准化后,将50-60μg的总蛋白质加载到10%聚丙烯酰胺凝胶上。电泳后,将蛋白质转移到硝酸纤维素膜中,并用以下抗体之一(ABCAM,剑桥,MA,USA),抗PDE4A(ABCAM),抗PDE5A(Cell Signaling),将蛋白质转移到硝酸纤维素膜中,并探测过夜。Danvers,Ma,USA)或抗GAPDH(ABCAM)。在辣根过氧化物酶标记的二抗(Sigma Aldrich,德国)和使用ECL Plus Western印迹检测系统(Amersham Biosciences,Munich,Munich,德国),通过增强化学发光来孵育膜1小时。用增强的化学发光来检测免疫复合物。
统计分析
所有数据都显示为平均值±SEM..组间差异采用不配对t检验,p值≤0.05为显著性。
结果
PDE1A表达分析
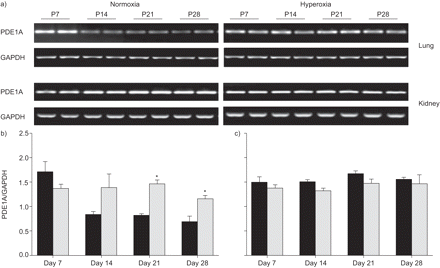
在Days P14,P21和P28中,与常氧对照相比,PDE1A的MRNA水平在高氧处理的小鼠的肺中始终较高(图1⇓).这种效果被限制在肺部上,因为在肾脏在相同的高氧暴露时观察到编码PDE1的mRNA水平的变化(图1A⇓b)。通过免疫印迹检测PDE1A蛋白作为72kDa的单个带(图2A⇓).在DAY P7和P14的初始上调后,与常氧处理的小鼠相比,在高氧处理的小鼠的肺中,在D天P21和P28下测量PDE1A蛋白的表达(图2⇓).
高氧对磷酸二酯酶(PDE)1A mRNA的影响。a)在暴露于高氧的后产后(p)天p7,p14,p21或p28后Neunatal小鼠(每种条件超过8个)的肺和肾脏(85%o2)或常氧(21%O2通过RT-PCR筛选PDE1A mRNA表达。将b)肺和c)肾的甘油醛-3-磷酸脱氢酶(GAPDH)谱带强度归一化后,用密度仪比较谱带强度。▪:normoxia;░:氧过多。*:P <0.05比较鼻氧基缺氧。
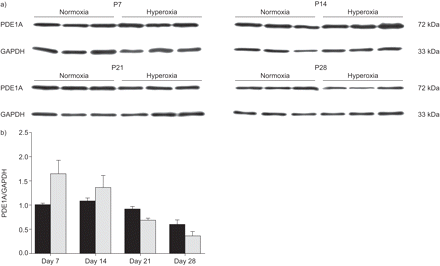
a)在暴露于高氧(85%O)后,新生儿小鼠在新生儿小鼠中肺匀浆(p)天p7,p14,p21或p28(85%2)或常氧(21%O2通过免疫印迹筛选磷酸二酯酶(PDE)1A蛋白表达。b)使用密度测定与甘氨醛-3-磷酸脱氢酶(GAPDH)带强度的正常化后比较带强度。▪:normoxia;░:氧过多。
PDE4A表达分析
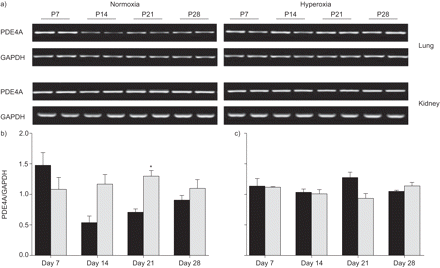
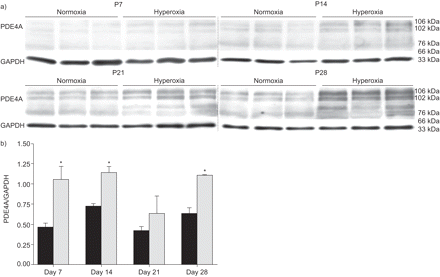
在高氧暴露的时间过程中,PDE4A mRNA表达在小鼠肺和肾脏中升高(图3⇓).在Days P14和P21期间观察到PDE4 mRNA表达的最显着变化,其中表达水平在高氧处理组的肺部升高(图3⇓).常氧对照在D日P7上表现出PDE4A表达中的初始峰,然后在第P14天(与常氧基群中的第P7)下调三倍下调,这增加了P28。在肾脏中观察到PDE4A mRNA表达水平的变化(图3A和C.⇓)。免疫印迹法检测PDE4A的不同剪接亚型:PDE4A1 (66 kDa)和PDE4Ax (76 kDa和102 kDa;图4⇓).通常,在高氧化条件下,小鼠肺部的PDE4A蛋白表达在天P7和P28之间升高。
高氧对磷酸二酯酶(PDE)4A mRNA的影响。a)在暴露于高氧的后产后(p)天p7,p14,p21或p28后Neunatal小鼠(每种条件超过8个)的肺和肾脏(85%o2)或常氧(21%O2),通过RT-PCR筛选PDE4A mRNA表达。将b)肺和c)肾的甘油醛-3-磷酸脱氢酶(GAPDH)谱带强度归一化后,用密度仪比较谱带强度。▪:normoxia;░:氧过多。*:P <0.05比较高氧与常氧。
a)在暴露于高氧(85%O)后,新生儿小鼠在新生儿小鼠中肺匀浆(p)天p7,p14,p21或p28(85%2)或常氧(21%O2通过免疫印迹筛选磷酸二酯酶(PDE)4A蛋白表达。b)使用密度测定法,在甘氨醛-3-磷酸脱氢酶(GAPDH)带强度的标准化后比较106kDa带的带强度。▪:normoxia;░:氧过多。*:P <0.05比较高氧与常氧。
PDE5A表达分析
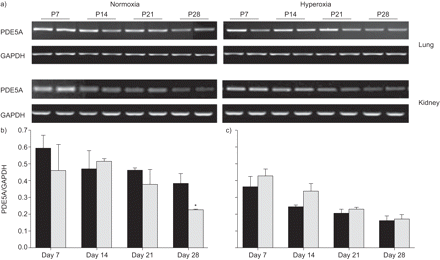
PDE5A在mRNA水平上的表达在P7和P28天之间在肺和肾中均呈进行性下调(图5)⇑)对常氧和高氧暴露的新生小鼠的影响。除了第28天,高氧暴露小鼠肺中PDE5A mRNA表达下调(图5)⇓),常氧组和高氧组之间无明显差异。相反,在高氧处理组中,PDE5A蛋白表达持续下调(图6)⇓).
高氧对PDE 5A mRNA的影响。a)在暴露于高氧的后产后(p)天p7,p14,p21或p28后Neunatal小鼠(每种条件超过8个)的肺和肾脏(85%o2)或常氧(21%O2通过RT-PCR筛选PDE5a mRNA表达。将b)肺和c)肾的甘油醛-3-磷酸脱氢酶(GAPDH)谱带强度归一化后,用密度仪比较谱带强度。▪:normoxia;░:氧过多。*:P <0.05比较高氧与常氧。
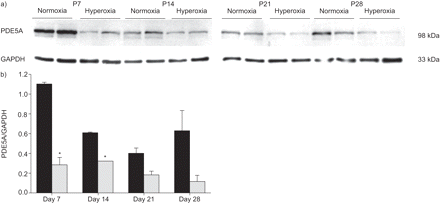
a)在暴露于高氧(85%O)后,新生儿小鼠在新生儿小鼠中肺匀浆(p)天p7,p14,p21或p28(85%2)或常氧(21%O2通过免疫印迹筛选用于磷酸二酯酶(PDE)5A蛋白表达的筛选。b)使用密度测定与甘氨醛-3-磷酸脱氢酶(GAPDH)带强度的正常化后比较带强度。▪:normoxia;░:氧过多。*:P <0.05比较高氧与常氧。
西洛米司特治疗的效果
在高氧暴露的动物中,PDE4的表达在P14和P28天之间显著升高,这表明抑制PDE4对高氧诱导的BPD有潜在的治疗益处。因此,pde4特异性抑制剂西洛米司特(或单独的载体)在P14和P28天的高氧暴露期间被给予幼犬。在常氧和西罗米拉斯特处理组暴露于高氧环境下的所有动物存活,而在常氧和西罗米拉斯特处理组暴露于高氧环境下的平均生存为98%。之前报道24.,NeoNates的连续暴露于85%的氧气对生长产生不利影响,其中高氧暴露的幼虫在P28的比其常氧暴露的凋落物中称重〜50%(图7⇓).西里洛斯特治疗没有改变暴露于高氧的幼崽的体重(图7⇓).西洛米司特未观察到其他副作用。
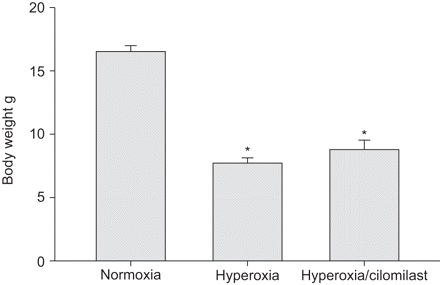
常氧,高氧和高氧和纤维菌治疗在产后日28例中新生小鼠体重的影响(n = 8,n = 8和n = 6)。*:P <0.05比较高氧与常氧。
新生儿小鼠对高氧的暴露引起了在肺组织切片微观分析时显而易见的空体扩大(图8⇓).通过评估平均线性截距(MLI)来量化这些形态学变化,MLI描述了平均肺泡内距离(图9a)⇓),评估SEPTAE的厚度(图9B⇓)和估计的总空域(图9c⇓).新生儿小鼠暴露于高氧环境中产生的MLI是正常缺氧环境下幼鼠的两倍。西洛米司特治疗显著降低了MLI(图9a)⇓),尽管在常氧治疗组中观察到的正常基线值并未恢复。类似地,与常氧处理的幼崽相比,超氧暴露的幼崽表现出隔膜壁厚的显着增加(图9B⇓),西洛米司特治疗显著降低高氧治疗组的间隔壁厚度,使间隔壁厚度恢复到正常组的范围。高氧条件下西洛米司特治疗也显著降低了暴露于高氧环境的幼犬肺部的空气容量(图9c)⇓)与未接受纤毛桶的高氧处理的幼仔相比。这些数据表明,Cileomilast能够部分正确,或防止通过高氧诱导的肺肺泡结构额外损害。
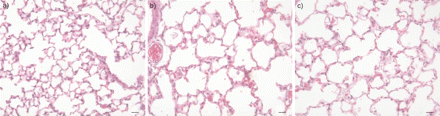
Cileomilast治疗对暴露于85%氧气的新生儿小鼠肺部建筑变化的影响。肺切片(在产后第28天获得)用血红素和曙红染色。从右下叶的右下叶,肾上腺素曝光,B)高氧暴露小鼠和C)鳞片状暴露小鼠和C)治疗的高氧暴露小鼠。秤条=20μm。
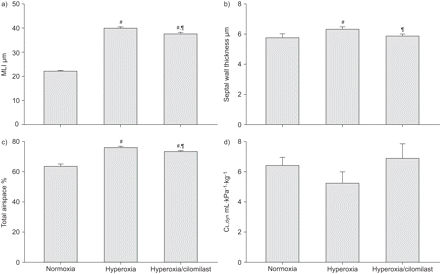
纤毛芪对新生儿小鼠肺部建筑变化和肺功能暴露于85%氧气的影响。从右下叶从10个过氧暴露的小鼠获得肺部(用于动态肺顺应性(Cl,dyn.)n = 6),八个西莨菪碱处理,过氧暴露小鼠(cl,dyn.n = 5)和八个常氧暴露小鼠(Cl,dyn.N = 8),产后28天,苏木精和伊红染色。对a)平均线性截距(MLI)、b)间隔壁厚度和c)总空域进行了定量切片。d)此外,Cl,dyn.对所有三组的幼犬进行了评估。#:P <0.05与常氧群体的高氧比较;¶:高氧组与高氧/西洛米司特组比较p<0.05。
西洛米司特治疗可改善平均Cl,dyn.高氧处理后的幼犬,Cl,dyn.通过容积调整、压力调节方案的全身容积描记术评估到正常水平(图9d)⇑).C.的变异性l,dyn.个体之间的动物产生的平均值,实验组没有统计上的差异,不管组比较。暴露于高氧环境下的幼鼠Cl,dyn.与Cl,dyn.normoxia-exposed幼崽。当高氧暴露的幼犬在第14天和第28天使用西洛米司特时,Cl,dyn.趋于增加,平均值恢复到正常的Cl,dyn.图9d⇑).综上所述,这些数据表明西罗米司特的使用减轻了高氧对新生儿肺结构变化和功能的有害影响。
讨论
新生儿小鼠对高氧的暴露导致肺泡发育不安,肺肺生长和不良生长。循环核苷酸PDE的表达分析揭示了小鼠中高氧诱导肺损伤期间几种PDE同种型表达的变化。除了第7天,PDE1在mRNA水平上上调,并在高氧暴露的小鼠幼崽的肺部蛋白质水平下下调。在高氧暴露的第一周中基因表达的这些差异很可能是由于肺部对较高的氧浓度的适应,并且在暴露期结束时保持在相同的水平。据报道,PDE1A蛋白的下调主要在血管平滑肌细胞中存在27.,可能是由于蛋白质合成受到负面影响,或血管形成的整体减少,这是高氧肺损伤的一个病理方面。PDE5A的表达在mRNA和蛋白水平上均因缺氧而下调,这与Wagenaar微阵列观察结果一致等等。28..相反,在暴露于高氧的时间过程中,在新生儿小鼠肺部肺部肺部表达在新生儿小鼠的肺部中显着上调。这些数据表明PDE4抑制的可能治疗益处。
非选择性PDE抑制剂,如己酮可可碱,降低了新生儿大鼠的纤维蛋白沉积,延长了新生儿大鼠的存活时间,新生儿大鼠肺损伤是由高氧引起的20..试点临床研究还证明了戊豆类症在极低出生体重婴儿预防BPD中的治疗益处,这表明PDE抑制可以代表对BPD管理的类固醇用途的替代品21..西地那非对PDE5的特异性抑制(从而使cGMP水平升高)改善了肺生长和血管化,并减轻了高氧环境下幼鼠的肺动脉高压17.,这与西地那非治疗成人肺动脉高压的疗效一致29.近年来,包括罗利普兰和吡克拉米司特在内的PDE4抑制剂也被证明可以改善新生儿大鼠高氧诱导的肺损伤的存活率和减轻肺部炎症22.,表明PDE在BPD的发展中的作用以及靶向PDES治疗BPD的可能性。
Cilomilast (Ariflo;SB-207499)是第二代PDE4抑制剂,它在PDE4抑制的治疗应用方面引起了新的兴趣,并且具有口服活性的额外优势。与罗利普仑相比,它表现出较低的催吐潜能,并在生理pH值下带负电荷,限制其在中枢神经系统的渗透,导致改善耐受性和较少的副作用30..西洛米司特目前已在I、II和III期试验中进行了评估,剂量反应研究表明,西洛米司特用于COPD患者而非哮喘患者具有临床益处31.
在目前的研究中,在P14-P28期,在P1-P14期暴露于高氧2周后,给新生小鼠注射西洛米司特2周。西洛米司特治疗的开始时间与PDE基因表达的变化相关,PDE基因表达在第14天最显著。因为小鼠的肺泡形成大约在P3天开始,大约在P14天结束32,用Cileomilast治疗不能直接影响肺泡,而是会影响肺的后期成熟和生长过程。早期的治疗开始于P1,凭借抑制炎症,可能具有进一步改善的肺部结构发展。实际上,本研究的弱点之一是番荔枝桶的后期施用(日期为P14);然而,在所需剂量的情况下,在Day P14之前将Cileomilast施用于小鼠的创伤和技术上挑战。然而,从Day P14(耐受性良好)施用的Cileomilast能够限制对肺部架构的损害,这表明Cilomilast在当前模型中的有益作用。
西洛米司特对高氧处理的幼鼠的体重没有任何影响,但对肺的结构和结构有明显的影响。经西洛米司特治疗后,高氧处理过的幼犬的肺显示出显著缩短的平均肺泡内距离(用平均线性截距测量),间隔壁厚度恢复到正常值,总空气空间面积显著减少,与年龄匹配、暴露在高氧环境下、单独接受车辆的幼犬的肺相比。这些结构变化转化为动态呼吸顺应性的改善,趋向于正常值。总之,这些数据表明西洛米司特限制了由长期暴露于常压高氧引起的正在发育的肺的结构和结构损伤。
PDE4抑制在本模型中的有益效果最可能归因于PDE4抑制剂的良好识别的抗炎性质30.那31那33,因为新生儿暴露在正常的高氧环境下会促进肺部炎症34.事实上,一项研究证明PDE4抑制可以影响炎性细胞因子的产生,如肿瘤坏死因子-α35.在另一项研究中,PDE4抑制剂,Rolipram和Piclamilast都显着减弱了白细胞介素-6,趋化因子诱导的中性粒细胞化学援助剂-1,单核细胞趋化剂-1和Amphirogulin的诱导,通过大鼠幼仔22..这些数据表明,Cileomilast的保护作用至少部分地归因于促进小鼠中高氧诱导的BPD中抗炎细胞因子的增加。
PDE4抑制在高氧诱导的BPD中的有益效果也可能延伸到PDE4抑制剂的抗炎作用。转化生长因子(TGF)-β在晚肺发展中具有良好的记录作用36;然而,在BPD中TGF-β信号通路失调,在人类患者中都是如此37,以及高氧诱导的啮齿动物BPD24..有趣的是,PDE4抑制剂是TGF-β信号传导的有效拮抗剂,因为Roflumilast拮抗Concient组织生长因子,胶原蛋白I和纤连蛋白在人类气道平滑肌细胞中的TGF-β感应38.在高氧诱导的BPD中观察到的间隔壁厚度增加被认为至少部分源于基质分子的过度沉积和细胞外基质的不当重塑6.那39.在本研究中,西罗米司特给药恢复了高氧暴露小鼠幼鼠正常的隔壁厚度。人们很容易推测,这可能部分是通过拮抗过度(异常)TGF-β信号转导产生的异常基质而实现的。沿着这些方向,BPD中过量的基质产生也被归因于过度的肌成纤维细胞,它们产生和沉积过量的基质,以及基质代谢酶,如基质金属蛋白酶(MMPs),其过度产生会导致肺泡破坏40.PDE4抑制剂可以钝化该过程,因为PIPLAMILAST已被证明阻断肺成纤维细胞与由TGF-β驱动的肌纤维细胞转化率41.因此,除了抗炎作用外,西洛米司特可能直接拮抗异常的生长因子信号,从而导致BPD中观察到的肺泡结构的病理变化。
还采用了PDE4抑制剂在香烟烟雾诱导的肺气肿模型中使用42一种像BPD一样的病理学,其特征在于持久的肺泡架构的丧失。在香烟诱导的肺气系中,选择性PDE4抑制剂,GDP-1116,通过抑制烟雾诱导的MMP-12生产并保护II型肺细胞凋亡,减弱肺泡破坏42.PDE4抑制剂rolipram和cilomilast也可以直接阻断肺成纤维细胞mmp -1和mmp -2的分泌43.虽然肺气肿和BPD都表现出肺泡建筑的损失,但这两种疾病的疾病差异很大。由于对成人肺的侮辱,肺气肿源于肺泡结构的损失,而BPD则来自未成熟(新生儿)肺的损害。因此,PDE4抑制剂最有可能在肺气肿的情况下促进肺部修复,并相反地,在本BPD模型的情况下,在发育肺的情况下限制过度血清损伤,从而促进改善的肺部发育。然而,MMP的异常生产6.并增加II型细胞凋亡44也是高氧诱导的肺损伤的后果,纤氯醇的保护作用也可能部分归因于预防过量的MMP生产和免受高氧诱导的上皮细胞凋亡的保护。
总之,本研究提供的数据表明,磷酸二酯酶的表达在高氧诱导的支气管肺发育不良中受到影响,特别是磷酸二酯酶的上调,提示在当前模型中磷酸二酯酶亚型的病理作用。西罗米司特在高氧损伤下保护或逆转肺泡结构异常重塑的能力支持了磷二酯酶抑制剂治疗支气管肺发育不良的进一步发展。
支持声明
这项研究得到了德国研究基金会(German Research Foundation)的部分资助(资助SFB547和KFO118;德国波恩),卓越群集心肺系统(德国黑森);和欧洲委员会(布鲁塞尔,比利时)根据第六框架计划(合同编号为。利- ct - 2005 - 018725, PULMOTENSION)。
兴趣表
可以在K.Woyda和F.杂音的兴趣陈述www.www.qdcxjkg.com/misc/statements.dtl.
致谢
目前的作者感谢M. Zoremba(吉森大学医院儿科,吉森,德国吉森)为目前的研究提供的优秀技术支持。
- 已收到2008年7月18日。
- 公认2008年10月9日。
- ©ERS期刊有限公司