摘要
肺纤维化的特征是成纤维细胞堆积和肺泡上皮剥蚀。肺泡上皮细胞凋亡增加和成纤维细胞凋亡减少可能在疾病的发病机制中起重要作用。炎症细胞可以通过清除凋亡碎片和产生细胞因子来调节其他类型细胞的凋亡,从而保持促纤维化的环境。本文就细胞凋亡在特发性肺纤维化发病中的作用机制作一综述。
特发性肺纤维化(IPF)是一种慢性弥漫性肺疾病,其特征是肺功能的进行性恶化,最终导致死亡。IPF的组织学模式是通常的间质性肺炎(UIP),描述为斑块状的肺泡上皮剥蚀、成纤维细胞灶和肺结构扭曲,导致蜂窝状和轻微炎症。有人提出,上皮-成纤维细胞相互作用可能导致肺泡细胞损失和纤维化过程的开始1.
细胞凋亡,或程序性细胞死亡,是组织内稳态发展和维持的重要生理过程,确保几乎所有组织类型的细胞增殖和周转之间的平衡。
细胞凋亡可能参与肺部疾病的发展通过三种不同的机制:1)上皮细胞凋亡增加导致再上皮化效率低下2;2)抗成纤维细胞凋亡,导致纤维化增加2;3)持续炎症状态的粒细胞对凋亡细胞(泡腾症)的清除无效3..
尽管在了解肺纤维化发展的机制方面已经取得了重大进展,但该疾病的发病机制尚不清楚。现有知识的一个重要部分来自动物模型,如博莱霉素诱导的肺纤维化模型。但是,该模型有一定的局限性,特别是该模型与IPF在慢性和发病机制上的差异。在小鼠博莱霉素模型中,急性肺泡炎在短时间内发展为明显的炎症和纤维化,不像人类IPF中看到的惰性纤维化和轻微炎症4.
本综述的目的是描述凋亡作为肺纤维化发展的潜在致病机制的重要性及其与其他致病过程的关系。
细胞凋亡的机制
凋亡细胞发生各种形态变化,包括细胞收缩、膜泡、染色体DNA裂解和膜结合的凋亡小体释放。凋亡机制包括:1)起始期,在起始期,凋亡刺激导致caspase激活;2)执行期,在此期间,半胱天冬蛋白酶诱导细胞死亡。
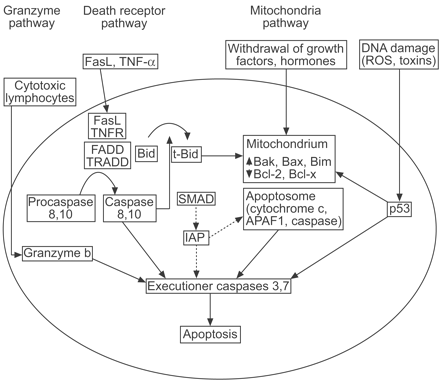
caspase级联可以被不同的途径激活(图1)⇓)5.
图1 -
不同的途径导致caspase级联激活和凋亡。FasL: Fas配体;TNF:肿瘤坏死因子;ROS:活性氧;TNFR: TNF受体;FADD: Fas激活死亡域;TRADD: TNF-α激活死亡域;凋亡蛋白酶激活因子APAF;IAP:凋亡抑制因子。
外部或死亡受体途径
外源性或死亡受体途径涉及到细胞膜上死亡受体的激活,如Fas和肿瘤坏死因子(TNF)受体1。死亡配体与其死亡受体的连接导致一种称为激活死亡结构域的衔接蛋白的激活,以及随后procaspase-8或-10的激活。激活的caspases诱导细胞凋亡。外源性途径至少可以通过三种机制被抑制:1)FLIP (fas激活死亡域(FADD)样白细胞介素-1转换酶(FLICE)样凋亡蛋白抑制剂),与procaspase-8结合而不激活;2)诱骗受体的结合,拮抗膜死亡受体的死亡配体结合;3)热休克蛋白6.
内在途径
这一内在途径是由于线粒体通透性的增加,并被细胞“压力”激活。各种应激因素导致抗凋亡线粒体蛋白表达减少(如。b细胞淋巴瘤(Bcl)-2和Bcl-x)和促凋亡线粒体蛋白表达增加(如。Bak, Bax, Bim)7.其他促凋亡因子如Smac(第二线粒体衍生caspase激活因子)/DIABLO(低pI直接抑制凋亡蛋白结合蛋白)、凋亡诱导因子和内切酶G也从线粒体中释放8.
颗粒酶B途径
细胞毒性淋巴细胞在遇到感染或恶性转化的宿主细胞后,分泌穿孔素,穿孔素是一种蛋白质,能够在感染细胞的细胞膜上产生孔,通过孔,丝氨酸蛋白酶颗粒酶B侵入宿主细胞,诱导细胞凋亡9.
肺纤维化中的细胞凋亡谱
肺泡上皮细胞
肺泡上皮包含两种细胞类型的连续层:扁平的i型肺细胞(覆盖肺泡表面的95%)和ii型肺细胞。ii型肺细胞可以增殖并产生ii型和i型细胞。此外,它们还能分泌许多分子,如表面活性剂相关产物、细胞因子和生长因子、酶和基质蛋白1.
肺泡上皮细胞(AEC)凋亡和随后的纤维化在博莱霉素诱导的IPF纤维化模型中被记录10.此外,Fas-Fas配体(FasL)通路的激活也促进肺纤维化11.此外,过度表达FasL分子的纤维化肺的肌成纤维细胞转移到健康小鼠肺中可诱导AEC凋亡;同样,缺乏fasl的肌成纤维细胞也不表达这种细胞毒性潜能12.caspase抑制剂阻断Fas-FasL通路或灭活caspase均可防止AEC凋亡和肺纤维化13,14.
在IPF患者的肺活检中,AECs显示凋亡阳性信号15例如p53和p21,尤其是在成纤维细胞附近的区域16.在IPF患者的AECs中,p53(一种细胞周期的调节因子和凋亡的触发因子,以应对DNA损伤)过表达15,可能是由于降解程度降低17.在博莱霉素诱导的小鼠肺纤维化模型中,p21基因(G1阻滞和DNA修复的诱导子)可保护AECs不发生凋亡18.IPF患者中存在凋亡的增生上皮细胞,p53、p21、Bax和caspase-3表达上调,Bcl-2表达下调(表1)⇓)19.
表1 -
特发性肺纤维化中肺泡上皮细胞凋亡增加的相关因素
成纤维细胞
成纤维细胞在UIP的纤维化病变中合成并沉积胶原蛋白和其他细胞外基质成分1.在正常伤口愈合过程中,成纤维细胞数量因细胞凋亡而减少20..
据报道IPF成纤维细胞对fas介导的细胞凋亡具有耐药性21.耐药的原因是x -连锁凋亡抑制因子和FLIP蛋白表达增加22以及表面Fas水平的降低和可溶性Fas水平的增加23.盘状结构域受体I是一种酪氨酸激酶,其配体是胶原蛋白,在博莱霉素诱导的纤维化小鼠成纤维细胞中表达增加,并促进对凋亡的抵抗24.
转化生长因子(TGF)-β1是主要的促纤维化细胞因子,可独立激活肺成纤维细胞中两个重要的抗凋亡通路:通过Smad3激活的局部粘附激酶(FAK)通路和磷脂酰肌醇3激酶(PI3K)/Akt通路通过p38丝裂原活化蛋白激酶的活化25.
Thy-1是一种细胞表面糖蛋白,与肺成纤维细胞凋亡增加有关。已有研究表明,成纤维细胞灶的肌成纤维细胞是Thy-1阴性的,而Thy-1阴性提供了细胞凋亡抗性(表2)⇓)26.
表2 -
特发性肺纤维化中成纤维细胞凋亡减少的相关因素
巨噬细胞
巨噬细胞活化与纤维化肺疾病的发病机制有关,如Hermansky-Pudlak综合征27.实验模型显示博莱霉素可诱导肺泡巨噬细胞凋亡28,29,而气管内给大鼠肺部的凋亡巨噬细胞导致巨噬细胞浸润和凋亡增加,胶原蛋白沉积增加30.,31.在博莱霉素诱导的纤维化中,Bcl-x和Bax蛋白以及caspase -1和-3的巨噬细胞表达增加14,32,以及在IPF患者肺泡巨噬细胞中Bcl-2和Fas的表达33,34.
此外,巨噬细胞集落刺激因子(M-CSF)(一种与巨噬细胞存活有关的因子)缺乏的小鼠在安装博莱霉素后,肺纤维化较少,肺中巨噬细胞数量减少。IPF患者的M-CSF水平明显高于正常受试者35.巨噬细胞还可以通过巨噬细胞释放胰岛素样生长因子-1来抑制肌成纤维细胞凋亡(表3)⇓)36.
表3 -
特发性肺纤维化中巨噬细胞参与凋亡的推定机制
中性粒细胞
尽管中性粒细胞凋亡受损与一些呼吸系统疾病有关37但其在IPF发病机制中的作用尚不清楚。IPF患者肺中中性粒细胞增多与预后不良相关38.IPF患者中性粒细胞中抗凋亡蛋白Bcl-2明显上调34.
皮质类固醇,虽然在IPF中作为一种治疗选项具有最低的活性,但已被证明可以显著增加中性粒细胞凋亡率,同时降低博莱霉素灌注后大鼠的肺泡炎和随后的纤维化率39.然而,也有人报道中性粒细胞增多与较差的临床病程无关,而且在中性粒细胞缺失时博莱霉素诱导的纤维化增强40,41.
在疾病末期的中性粒细胞积累是一种重要的致病机制还是晚期纤维性疾病的一种附带现象的不确定性突出了目前关于IPF发病机制的不确定性。目前,炎症并不被认为是IPF的主要致病因素1,2.在晚期疾病中,中性粒细胞的大量流入可能是由于受损肺的亚临床感染或趋化因子的纤维性分泌所致。然而,中性粒细胞也有可能在IPF的急性加重中起主要的致病作用42在某些情况下,这可能是中性粒细胞大量涌入的原因。
细胞凋亡与其他肺纤维化机制的相互关系
肺纤维化的发病机制仍然是一个复杂的问题。许多致病机制相互牵连和相互关联,导致在疾病发展过程中很难区分哪些是主要事件和次要事件。在最近的一篇综述中,提出了由各种因素(慢性病毒感染、香烟烟雾、胃食管反流病和暴露于环境污染物)引起的损伤激活了多种途径(氧化-抗氧化、凝血、炎症和t辅助细胞(Th) 1/Th2型细胞因子),并导致促纤维化分子(TGF-β、结缔组织生长因子和凝血酶)和抗纤维化分子(干扰素-γ和前列腺素E)之间的失衡2).这种不平衡诱导细胞功能的改变,表现为凋亡细胞行为和增殖的改变,上皮-间质转变和细胞外基质生产的增加,最终导致纤维化42.在下一节中,我们将回顾细胞凋亡与其他纤维化机制的相互关系。
血管收缩剂
这已经被证明在体外在动物模型中,血管收缩因子参与了纤维化的发展。研究最广泛的两种血管收缩因子是内皮素-1和血管紧张素- ii。虽然通常与抵抗细胞凋亡有关43在IPF中,内皮素-1促进上皮-间充质转化(上皮细胞获得间充质表型特征)44,而血管紧张素肽则积极参与细胞凋亡。
血管紧张素肽由凋亡的AECs和邻近的肌成纤维细胞在局部产生45.诱导AEC细胞凋亡通过由人肺成纤维细胞产生的血管紧张素ii激活Fas46,47,并可通过给予血管紧张素转换酶抑制剂卡托普利减弱48通过选择性血管紧张素1型受体拮抗剂氯沙坦49或通过反义寡核苷酸对抗血管紧张素原mRNA50.
氧化应激
氧化应激被认为是IPF中上皮细胞损伤的重要原因51.尽管肺中活性氧(ROS)的来源被认为是炎症细胞,肌成纤维细胞也可以产生过氧化氢,从而诱导上皮细胞死亡52.博莱霉素通过增加活性氧诱导AEC细胞凋亡和纤维化53自由基清除剂可降低细胞凋亡和肺纤维化的速率54.博莱霉素诱导的凋亡与巨噬细胞中ROS引起的p53从胞浆向细胞核的易位有关55.
氧化应激也影响成纤维细胞凋亡:过氧化氢引起成纤维细胞凋亡,刺激成纤维细胞增殖或迁移到伤口56.
缺氧
缺氧可显著干扰AEC功能,引发细胞凋亡,促进炎症反应。缺氧诱导因子(HIF)-1是缺氧信号的主要调节因子,在IPF患者中过表达。
HIF-1α引起上皮细胞凋亡增加通过bip 3L活化,bcl2家族成员。阻断HIF-1α或bip3l (Bcl-2/腺病毒E1B 19-kDa相互作用蛋白3L)可显著减弱缺氧诱导的上皮细胞凋亡57.HIF-1α的表达已被证明是IPF的早期事件,并与IPF患者肺部和博莱霉素诱导的纤维化中p53的激活和AEC凋亡的增加有关。HIF-1α在成纤维细胞灶中缺失,而抗凋亡蛋白Bcl-2表达增加,进一步支持AEC凋亡增加伴随成纤维细胞凋亡减少的假说58.
细胞外基质
细胞外基质沉积增加是IPF的一个特征,与基质金属蛋白酶(MMPs)及其抑制剂的失调有关2.
基底膜的完整性为粘附的上皮细胞提供生存信号,而粘附的破坏导致凋亡细胞死亡。细胞外基质可能决定AECs的凋亡谱。在层粘连蛋白/胶原蛋白混合物上培养时,上皮细胞发生凋亡,而在纤维连接蛋白或纤维蛋白上培养时,上皮-间充质转变59.
基质组成可导致不同的成纤维细胞凋亡反应60.可溶性纤维连接蛋白肽可通过破坏黏附促进成纤维细胞凋亡通过整合素- fak存活通路的激活61;然而,纤维连接蛋白也可以减少成纤维细胞的凋亡通过PI3K通路的激活62.
转化生长因子-β1
TGF-β1是一种伤口愈合所必需的生长因子,它的过度分泌会导致疤痕组织的过度沉积和纤维化63.TGF-β1直接诱导上皮细胞凋亡通过激活Fas和caspase-3,并通过增强FasL - Fas相互作用64而小鼠转染可溶性TGF type-II受体后,细胞凋亡和肺纤维化程度明显减弱65.
Bid是Bcl-2家族的另一个成员,在TGF-β1激活后,AEC凋亡和博莱霉素诱导的小鼠纤维化都需要Bid,因为Bid缺乏的小鼠不会发生纤维化66.bax介导的bid激活通路最近被证实参与了肺纤维化的发病机制。TGF-β1显著刺激Bax和Bid的表达,引起小鼠体内MMP-12和金属蛋白酶-1组织抑制剂的释放67.
TGF-β1导致AECs中p21表达增加通过TNF-α信号通路和p21表达缺失与TGF-β1诱导的纤维化和上皮细胞凋亡增加有关68.
据报道,TGF-β受体i型抑制剂可减少博莱霉素诱导的纤维化和肌成纤维细胞凋亡69.如前所述,TGF-β激活肺成纤维细胞中的FAK和PI3K/Akt抗凋亡通路25.
炎症
炎症不被认为是IPF发展的主要致病成分。然而,它在疾病的急性加重中起着重要作用,它可能是纤维化过程开始的必要条件42.
炎症可导致细胞凋亡增加。促炎细胞因子TNF-α使成纤维细胞对fas介导的细胞凋亡敏感,th1型细胞因子干扰素-γ可与TNF-α协同作用,增强细胞凋亡反应70.
中性粒细胞也可诱导AEC凋亡:IPF患者肺活检和支气管肺泡灌洗浸润粒细胞中FasL表达水平明显高于对照组,这与相邻上皮中Fas表达增加有关33.
未能清除过多的凋亡细胞可能导致持续的炎症状态。巨噬细胞被认为是凋亡细胞的专业吞噬细胞,可以吞噬并沉积凋亡残体3..吞噬凋亡细胞的巨噬细胞释放抗炎细胞因子白细胞介素(IL)-10和TGF-β1,它们在局部起作用71.此外,凋亡细胞可产生IL-10和TGF-β1,从而增强巨噬细胞的吞噬能力72.吞噬凋亡小体的巨噬细胞也可以释放促凋亡因子,诱导邻近细胞凋亡73.然而,凋亡残体的切割也可能导致炎症增强74.有趣的是,据报道地塞米松可诱导肺炎症细胞凋亡,减少博莱霉素诱导的纤维化程度39.
Pro-coagulant活动
组织损伤后,凝血级联的激活迅速发生,以便为修复过程的发生提供临时的细胞外基质1.在肺纤维化中,已发现过多的血管外凝血,主要是由于AECs产生促凝血分子,如组织因子和纤溶酶原激活抑制剂75.此外,在动物模型中,抗凝剂可以有效衰减肺纤维化75在一项针对IPF患者的随机临床试验中,在皮质类固醇的基础上加入抗凝剂,显著减少了IPF的急性发作,并提高了生存率76.
AECs的凋亡和随后的基底膜剥蚀是组织修复和凝血级联启动的信号75.此外,已有研究表明促凝剂可引起细胞凋亡。蛋白酶激活受体(PAR)-1是一种凝血酶的高亲和力受体,其激活可诱导肺泡上皮细胞凋亡在体外77.PAR-1也有助于纤维形成通过TGF-β1的激活78.
衰老,细胞凋亡和肺纤维化
肺纤维化是一种与年龄有关的过程。IPF是一种影响老年人的疾病2.患有遗传性肺纤维化的患者,如Hermansky-Pudlak综合征,也会随着年龄的增长发展成肺纤维化79.细胞凋亡通路的失调与衰老有关。衰老细胞影响器官的修复和结构,促进局部炎症80.
p53途径的激活是细胞衰老过程中的一个重要事件80.在IPF患者AECs中观察到的凋亡过程中也显示了p53的激活15.高氧和氧化应激下衰老大鼠AEC细胞凋亡增加已有报道81.衰老的人成纤维细胞对凋亡具有抵抗能力,这种抵抗能力与抗凋亡因子Bcl-2的表达增加和caspase-3的下调有关82.
端粒酶是一种核糖核蛋白酶,它维持端粒长度,保持细胞和随后的有机体寿命。端粒功能失调可引起小鼠细胞周期阻滞或细胞凋亡83.在一些IPF病例中发现了端粒酶组分的突变,与端粒酶活性缺陷和端粒缩短有关84端粒酶调控与博莱霉素诱导的纤维化有关。给博莱霉素后,AECs端粒酶活性降低在体外,导致细胞凋亡增加,而在活的有机体内端粒酶活性升高是为了保护肺泡上皮细胞不受博莱霉素诱导的细胞凋亡的影响85.
然而,端粒酶活性是纤维化所必需的。与对照组相比,端粒酶缺乏的博莱霉素诱导纤维化小鼠的肺成纤维细胞增殖减少,凋亡率增加,而端粒酶活性的恢复导致肺纤维化增加86.
结论
越来越多的证据支持凋亡作为特发性肺纤维化的潜在致病机制的重要性。细胞凋亡对机体可能是有益的,也可能是有害的。不同的细胞类型表现出不同的凋亡行为。促成纤维环境诱导上皮细胞凋亡,增加肌成纤维细胞存活。炎症细胞可以通过自我凋亡和清除凋亡碎片来调节肺的纤维化反应。在特发性肺纤维化等衰弱疾病的治疗干预中,针对特定细胞类型的抗凋亡药物是一个主要挑战。然而,凋亡是参与特发性肺纤维化发展的众多机制之一,这些不同机制之间相互作用的复杂性仍有待解决。
致谢
作者感谢V. Fayngersh(布朗大学阿尔珀特医学院,普罗维登斯,RI, USA)的宝贵意见和对本文的语言审查。
- 收到了2007年12月31日。
- 接受2008年8月6日。
参考文献
- ↵
特发性肺纤维化:关于其发病机制和治疗意义的流行和发展假说。Ann实习医生2001;134:136-151年。
- ↵
Antoniou KM, Pataka A, Bouros D, Siafakas NM。特发性肺纤维化的病理途径和新的药物治疗靶点。Pulm Pharmacol Ther2007;20.:453-461年。
- ↵
Vandivier RW, Henson PM, Douglas IS。埋葬逝者:凋亡细胞清除失败(泡腾症)对慢性炎症性肺病的影响胸部2006;129:1673-1682年。
- ↵
摩尔律师,霍格波姆首席检察官。肺纤维化小鼠模型。m J Physiol肺细胞2008;294:L152-L160。
- ↵
王晓燕,张晓燕,张晓燕,等。细胞凋亡与肺上皮损伤的关系。胸腔镜系统2005;2:214-220年。
- ↵
Beere嗯。死亡与存活:凋亡和应激诱导热休克蛋白通路之间的功能相互作用。J clinin投资2005;115:2633-2639年。
- ↵
Ravagnan L, Roumier T, Kroemer G.线粒体,杀手细胞器和它们的武器。细胞物理2002;192:131-137年。
- ↵
Susin SA, Lorenzo HK, Zamzami N,et al。线粒体凋亡诱导因子的分子特征。自然1999;397:441-446年。
- ↵
罗素JH,莱TJ。Lymphocyte-mediated细胞毒性。免疫2002;20.:323-370年。
- ↵
叶本勇,熊文华,张文华,张文华,等。博莱霉素致小鼠肺纤维化细胞凋亡及Fas/Fas配体mRNA表达的研究。Am J呼吸细胞分子生物学1997;16:91-101年。
- ↵
桥本N,库和野K,宫崎骏H,et al。Fas抗原结扎诱导小鼠细胞凋亡和肺纤维化。Am J呼吸细胞分子生物学1997;17:272-278年。
- ↵
高兰-格斯特尔,华拉赫-达扬SB, Amir G, Breuer R.肺纤维化中fas配体阳性肌成纤维细胞凋亡。Am J呼吸细胞分子生物学2007;36:270-275年。
- ↵
库和野K,桥本N,川崎M,et al。Fas-Fas配体通路在肺纤维化发展中的重要作用。J clinin投资1999;104:13-19年。
- ↵
Kuwano K, Kunitake R,前山T,et al。用半胱天冬酶抑制剂减弱博莱霉素诱导的小鼠肺病。m J Physiol肺细胞2001;280:L316-L325。
- ↵
Kuwano K, Kunitake R,川崎M,et al。特发性肺纤维化中P21Waf1/Cip1/Sdi1和p53与DNA链断裂的关系J呼吸危重症护理医院1996;154:477-483年。
- ↵
Uhal BD, Joshi I, Hughes WF, Ramos C, Pardo A, Selman M.晚期人纤维化肺中邻近肌成纤维细胞的肺泡上皮细胞死亡。Am J physics1998;275:L1192-L1199。
- ↵
N中岛,K久和野,T前山,et al。特发性肺纤维化和非特异性间质性肺炎中上皮细胞p53-Mdm2的相关性临床病理学杂志2005;58:583-589年。
- ↵
Inoshima I Kuwano K滨田Net al。CDK抑制剂p21基因诱导是治疗肺纤维化的新策略。m J Physiol肺细胞2004;286:L727-L733。
- ↵
Plataki M, Koutsopoulos AV, Darivianaki K, Delides G, Siafakas NM, Bouros D.特发性肺纤维化中上皮细胞凋亡和抗凋亡标志物的表达。胸部2005;127:266-274年。
- ↵
伤口愈合和纤维化过程中影响肌成纤维细胞分化的因素。细胞生物学Int1995;19:471-476年。
- ↵
Moodley YP, Caterina P,脚手架AK,et al。fasl诱导细胞凋亡过程中正常人肺成纤维细胞与特发性肺纤维化患者肺源成纤维细胞形态学和生化变化的比较中草药2004;202:486-495年。
- ↵
田中田,田中田,杨春梅,杨春梅,张玉玲,张玉玲。人肺成纤维细胞对fas介导的细胞凋亡的抵抗。欧元呼吸2002;20.:359-368年。
- ↵
布林F,威尔A, Röcken C,et al。膜结合和可溶性CD95/Fas的表达改变有助于纤维化肺成纤维细胞抵抗FasL诱导的凋亡。和物2005;6:37
- ↵
Avivi-Green C, Singal M, Vogel WF。盘西汀结构域受体1缺陷小鼠对博莱霉素诱导的肺纤维化具有耐药性。J呼吸危重症护理医院2006;174:420-427年。
- ↵
霍洛维茨JC,罗杰斯DS,夏尔马V,et al。通过转化生长因子-beta1组合激活FAK和AKT可使肌成纤维细胞产生抗氧化表型。手机信号2007;19:761-771年。
- ↵
桑德斯YY,昆布拉P,哈古德JS。Thy-1增强肌成纤维细胞分化和存活-肺成纤维细胞。Am J呼吸细胞分子生物学2007;36:226-235年。
- ↵
年轻LR, Pasula R, Gulleman PM, Deutsch GH, McCormack FX。Hermansky-Pudlak小鼠对博莱霉素诱导的II型细胞凋亡和纤维化的敏感性。Am J呼吸细胞分子生物学2007;37:67-74年。
- ↵
李丽娟,李丽娟,李丽娟。博莱霉素诱导人肺泡巨噬细胞凋亡。Am J physics1995;269:L318-L325。
- ↵
赵洪伟,胡淑云,Barger MW,马俊杰,Castranova V,马建勇。博莱霉素作用大鼠肺泡巨噬细胞时间依赖性凋亡:TNF受体2的参与。毒物环境卫生A2004;67:1391-1406年。
- ↵
王l, Antonini JM, Rojanasakul Y, Castranova V, scarilloni JF, Mercer RR。凋亡巨噬细胞在肺炎症和纤维化中的潜在作用。细胞物理2003;194:215-224年。
- ↵
王L, scarilloni JF, Antonini JM, Rojanasakul Y, Castranova V, Mercer RR。大鼠气管内灌注凋亡细胞后诱导继发性凋亡、炎症和肺纤维化。m J Physiol肺细胞2006;290:L695-L702。
- ↵
Kuwano K, Hagimoto N, Tanaka T,et al。小鼠肺纤维化上皮细胞中凋亡调节基因的表达。中草药2000;190:221-229年。
- ↵
库和野K,宫崎骏H,桥本N,et al。Fas-Fas配体通路在纤维化肺疾病中的作用Am J呼吸细胞分子生物学1999;20.:53-60年。
- ↵
Mermigkis CM, Tsakanika K, Polychronopoulos V, Karagianidis N, Mermigkis G, Bouros d特发性肺纤维化患者支气管肺泡灌洗细胞群中bcl-2蛋白的表达。Acta Cytol2001;45:914-918年。
- ↵
Baran CP, Opalek JM, McMaken S,et al。M-CSF、CCL2和单核吞噬细胞在肺纤维化发病机制中的重要作用。J呼吸危重症护理医院2007;176:78-89年。
- ↵
Wynes MW, Frankel SK, richards DW。il -4诱导的巨噬细胞源性IGF-I在生长因子退出后保护肌成纤维细胞不发生凋亡。白细胞生物学杂志2004;76:1019-1027年。
- ↵
Bianchi SM, Dockrell DH, Renshaw SA, Sabroe I, Whyte MK.粒细胞凋亡在肺部疾病发病机制和缓解中的作用。临床科学(伦敦)2006;110:293-304年。
- ↵
Turner-Warwick M, Haslam PL.连续支气管肺泡灌洗在评估隐源性纤维化肺泡炎患者临床进展中的价值。Am Rev呼吸Dis1987;135:26-34年。
- ↵
李惠萍,李鑫,何广杰,易晓红,卡普兰等。地塞米松对博莱霉素致肺纤维化大鼠肺炎症细胞增殖和凋亡的影响。Respirology2004;9:25-32年。
- ↵
沃特斯LC,施瓦茨MI,切尔尼克RM,et al。特发性肺纤维化。支气管肺泡灌洗液预处理细胞成分及其与肺组织病理和临床治疗反应的关系。Am Rev呼吸Dis1987;135:696-704年。
- ↵
萨尔RS,潘SH,麦考密克JR,沃德PA。中性粒细胞和补体缺失大鼠博莱霉素诱导肺纤维化的发展。Am J Pathol1981;105:76-81年。
- ↵
Maher TM, Wells AU, Laurent GJ。特发性肺纤维化:多原因、多机制?欧元呼吸2007;30.:835-839年。
- ↵
麦嵬尼R,佩奇科夫斯基DV,周D,et al。内皮素-1诱导人气道平滑肌细胞肥大并抑制细胞凋亡。m J Physiol肺细胞2007;292:L278-L286。
- ↵
Jain R, Shaul PW, Borok Z, Willis BC。内皮素-1通过内皮素A型受体介导的TGF-beta1的产生诱导肺泡上皮-间质转变。Am J呼吸细胞分子生物学2007;37:38-47年。
- ↵
Li X, Molina-Molina M, Abdul-Hafez A,et al。特发性肺纤维化中肺血管紧张素肽合成的血管外来源。m J Physiol肺细胞2006;291:L887-L895。
- ↵
王R, Ramos C, Joshi I,et al。人肺肌成纤维细胞衍生的肺泡上皮细胞凋亡诱导物被鉴定为血管紧张素肽。Am J physics1999;277:L1158-L1164。
- ↵
王瑞,Zagariya A, Ang E, Iburra-Sunga O, Uhal BD. fas诱导的肺泡上皮细胞凋亡需要Ang II的产生和受体的相互作用。Am J physics1999;277:L1245-1250年。
- ↵
Uhal BD, Gidea C, Bargout R,et al。卡托普利抑制人肺上皮细胞凋亡:一种潜在的抗纤维化机制。Am J physics1998;275:L1013-L1017。
- ↵
李晓霞,李晓燕,李晓燕。血管紧张素受体AT1a在博莱霉素诱导的小鼠肺纤维化和细胞凋亡中的作用。Am J Pathol2003;163:2523-2530年。
- ↵
李霞,庄娟,雷福德,张宏,舒锐,Uhal BD.气管内给药抗血管紧张素原mRNA的反义寡核苷酸对博莱霉素诱导的肺纤维化的抑制作用。Curr Pharm Des2007;13:1257-1268年。
- ↵
Kuwano K, Nakashima N, Inoshima I,et al。特发性间质性肺炎患者肺上皮细胞中的氧化应激。欧元呼吸2003;21:232-240年。
- ↵
瓦格雷M,崔卓,霍洛维茨JC,et al。过氧化氢是一种可扩散的旁分泌信号,可通过激活的肌成纤维细胞诱导上皮细胞死亡。美国实验生物学学会联合会J2005;19:854-856年。
- ↵
Wallach-Dayan SB, Izbicki G, Cohen PY, Gerstl-Golan R, Fine A, Breuer R.博莱霉素通过ROS而非Fas/FasL途径诱导肺上皮细胞凋亡m J Physiol肺细胞2006;290:L790-L796。
- ↵
Psathakis K, Mermigkis D, Papatheodorou G,et al。特发性肺纤维化呼气氧化应激标志物。eurj clinin投资2006;36:362-367年。
- ↵
Davis DW, Weidner DA, Holian A, McConkey DJ。一氧化氮依赖性的p53激活抑制博莱霉素诱导的肺细胞凋亡。J临床医学2000;192:857-869年。
- ↵
高桥龙,王晓燕。氧化应激诱导创面成纤维细胞凋亡的研究。Exp肺Res2002;28:275-284年。
- ↵
李文华,李文华,李文华,Hänze;et al。缺氧诱导因子-1α在缺氧诱导原代肺泡II型上皮细胞凋亡中的作用。Am J呼吸细胞分子生物学2005;32:395-403年。
- ↵
Tzouvelekis A Harokopos V Paparountas Tet al。肺纤维化的比较表达谱提示缺氧诱导因子-1 α在疾病发病中的作用。J呼吸危重症护理医院2007;176:1108-1119年。
- ↵
Kim KK, Kugler MC, Wolters PJ,et al。肺泡上皮细胞间充质转变在活的有机体内在肺纤维化过程中,受细胞外基质调控。美国国家科学研究院2006;103:13180-13185年。
- ↵
朱玉凯,乌米诺特,刘晓东,et al。含成纤维细胞胶原凝胶的收缩:初始胶原浓度调节收缩程度和细胞存活。体外细胞发育生物学研究2001;37:10-16年。
- ↵
可溶性纤维连接蛋白肽诱导肺成纤维细胞凋亡。J呼吸危重症护理医院2000;162:1553-1560年。
- ↵
法瑞亚斯E,陆明,李X,施纳普LM。整合素α8β1-纤维连接蛋白相互作用促进细胞存活通过PI3激酶途径。生物化学生物物理学研究2005;329:305-311年。
- ↵
李晓东,李晓东,李晓东。特发性肺纤维化发病机制中的细胞因子网络。肺血管性弥漫性结节病2005;22:91-104年。
- ↵
Hagimoto N Kuwano K Inoshima Iet al。TGF-β1促进fas介导的肺上皮细胞凋亡。J Immunol2002;168:6470-6478年。
- ↵
山田M,库和野K,前山T,等.可溶性转化生长因子II型受体通过体内电穿孔的基因转移减轻肺损伤和纤维化。临床病理学杂志2007;60:916-920年。
- ↵
巴丁格GR, Mutlu总经理,艾森巴特J,et al。促凋亡Bid在肺纤维化中是必需的。美国国家科学研究院2006;103:4604-4609年。
- ↵
姜洪哲,赵世杰,李景刚,侯默RJ, Elias JA。转化生长因子(TGF)-β1刺激肺纤维化和炎症通过这是一种依赖bax、bid激活的途径,涉及基质金属蛋白酶-12。J生物化学2007;282:7723-7732年。
- ↵
山崎明,康洪志,侯默RJ,et al。P21调节TGF-β1诱导的肺反应通过TNF-α信号通路。Am J呼吸细胞分子生物学2008;38:346-353年。
- ↵
卡波恩,贾斯帕,王燕,et al。转化生长因子β受体1型(TGFβRI)激酶活性对TGFβRI诱导的肌成纤维细胞分化和原纤维基因表达是必需的,而不是p38的激活。摩尔杂志2006;70:518-531年。
- ↵
Frankel SK, Cosgrove GP, Cha SI,et al。tnf - α使正常和纤维化的人肺成纤维细胞对fas诱导的凋亡敏感。Am J呼吸细胞分子生物学2006;34:293-304年。
- ↵
凋亡细胞的免疫抑制作用。自然1997;390:350-351年。
- ↵
高原,赫恩登JM,张浩,格里菲斯TS,弗格森TA。CD95配体(FasL)诱导细胞凋亡的抗炎作用。J临床医学1998;188:887-896年。
- ↵
吞噬作用触发巨噬细胞释放Fas配体并诱导旁观者白细胞凋亡。J Immunol1999;162:480-485年。
- ↵
巨噬细胞和凋亡细胞:一种单纯的先天免疫相互作用?免疫学2004;113:1-14年。
- ↵
钱伯斯RC。肺炎症和纤维化中的促凝信号机制:药物干预的新机会?溴J药典2008;153:供应S367-S378。
- ↵
久保H,中山K,柳井M,et al。特发性肺纤维化的抗凝治疗。胸部2005;128:1475-1482年。
- ↵
铃木T, Moraes TJ, Vachon E,et al。蛋白酶激活受体-1介导弹性蛋白酶诱导的人肺上皮细胞凋亡。Am J呼吸细胞分子生物学2005;33:231-247年。
- ↵
Jenkins RG,苏X,苏G,et al。蛋白酶激活受体1的结扎增强αvβ6整合素依赖性TGF-β激活促进急性肺损伤。J clinin投资2006;116:1606-1614年。
- ↵
Brantly M, Avila NA, Shotelersuk V, Lucero C, Huizing M, Gahl WA。HPS-1突变导致的遗传性肺纤维化(Hermansky-Pudlak综合征)患者的肺功能和高分辨率CT表现胸部2000;117:129-136年。
- ↵
衰老细胞,肿瘤抑制,与有机体老化:好公民,坏邻居。细胞2005;120:513-522年。
- ↵
李pj, Alam J, Sylvester SL, Inamdar N, Otterbein L, Choi AM。血红素氧合酶-1表达的调控在活的有机体内而且在体外在高氧肺损伤中。Am J呼吸细胞分子生物学1996;14:556-568年。
- ↵
衰老成纤维细胞通过下调caspase-3抑制细胞凋亡。机械老化开发2004;125:777-783年。
- ↵
Blasco马。端粒长度、干细胞与衰老。Nat Chem Biol2007;3.:640-649年。
- ↵
Tsakiri KD, Cronkhite JT, Kuan PJ,et al。端粒酶突变引起的成人起病肺纤维化。美国国家科学研究院2007;104:7552-7557年。
- ↵
傅德伦德·泽g, Cohen PY, Golan O, Arish N, walluch - dayan S, Breuer R.端粒酶活性在博莱霉素诱导的上皮细胞凋亡和肺纤维化中的作用。欧元呼吸2007;30.:205-213年。
- ↵
刘涛,钟MJ, Ullenbruch M,et al。端粒酶活性是博莱霉素诱导的小鼠肺纤维化所必需的。J clinin投资2007;117:3800-3809年。