摘要gydF4y2Ba
炎症、氧化应激和细胞凋亡参与慢性阻塞性肺疾病(COPD)的发病机制,可能激活丝裂原活化蛋白激酶(MAPKs)的p38亚群。因此,本研究的目的是评估p38 MAPK的磷酸化活性形式(phospho-p38)在COPD患者肺部的表达。gydF4y2Ba
手术标本取自18例不同疾病严重程度的COPD吸烟者,9例吸烟患者和8例肺功能正常的非吸烟患者。用免疫组织化学方法定量检测肺泡间隙和肺泡壁的Phospho-p38+细胞。此外,对肺泡巨噬细胞表达的p38和p38α总亚型进行Western blot分析。gydF4y2Ba
与吸烟和不吸烟对照组相比,重度和轻度/中度COPD患者的肺泡巨噬细胞和肺泡壁中的Phospho-p38+细胞增加。此外,它们与1秒用力呼气量(FEV)值呈负相关gydF4y2Ba1gydF4y2Ba)和FEVgydF4y2Ba1gydF4y2Ba/强制肺活量。Western blot分析显示,COPD患者肺泡巨噬细胞中磷酸化的p38亚型特异性升高,而p38α总亚型不升高。gydF4y2Ba
p38丝裂原活化蛋白激酶通路的激活似乎与慢性阻塞性肺疾病的发病机制有关。目前的研究结果表明,该蛋白可能是治疗干预的一个合适的药理学靶点。gydF4y2Ba
吸烟在慢性阻塞性肺疾病(COPD)的发病机制中起着至关重要的作用。许多关于COPD发病机制的信息来自于动物模型或实验研究gydF4y2Ba在体外gydF4y2Ba系统,这些系统并不总是直接反映人类疾病中发生的情况。然而,众所周知,吸烟引起的氧化剂和氧化应激会促进肺部炎症,这至少部分是由转录因子核因子(NF)-κB和激活蛋白(AP)-1的激活介导的,协调几个被认为在COPD中重要的基因的表达,如白细胞介素(IL)-8和肿瘤坏死因子(TNF)-αgydF4y2Ba1gydF4y2Ba- - - - - -gydF4y2Ba3.gydF4y2Ba.这些促炎细胞因子和趋化因子与IL-1β一起,强烈激活丝裂原激活蛋白激酶(MAPKs)的p38亚群,这是一个信号转导酶家族,还包括细胞外信号调节激酶(ERK)和c-jun NHgydF4y2Ba2gydF4y2Ba-末端激酶(JNK)gydF4y2Ba4gydF4y2Ba.mapk按层次组织成三个模块,运行gydF4y2Ba通过gydF4y2Ba一种磷酸化级联,将其转化为活化形式,从而使其与细胞质底物相互作用并转位到许多MAPK靶标(如转录因子和组蛋白)所在的细胞核gydF4y2Ba5gydF4y2Ba.ERK通路尤其受到g蛋白偶联受体和参与细胞增殖、分化和生存的生长因子的刺激,而JNK和p38模块主要由涉及炎症和凋亡的细胞因子激活gydF4y2Ba6gydF4y2Ba.在MAPK家族中,JNK和p38亚群都参与介导促炎反应,尽管p38似乎在COPD中起着重要作用。事实上,关键炎症细胞类型中的p38激活与疾病的发生和进展相关gydF4y2Ba7gydF4y2Ba.p38似乎也是最有效的MAPK,在转录后水平上稳定与COPD发病机制相关的细胞因子和趋化因子的mrna,如TNF-α, IL-1β, IL-6和IL-8gydF4y2Ba8gydF4y2Ba.相反,p38抑制剂能够减轻COPD动物模型的疾病严重程度;因此,p38目前是基于MAPK抑制的新型抗炎疗法的主要焦点gydF4y2Ba9gydF4y2Ba.已知p38 MAPK的四种不同亚型,分别被命名为α, β, γ和δ,并且似乎具有不同的功能模式和细胞表达谱的特征。特别是肺巨噬细胞主要表达α亚型;这些细胞也表达p38δ,但不表达p38β或p38γgydF4y2Ba10gydF4y2Ba.gydF4y2Ba
导致COPD发病的初始炎症事件可能代表气道对非特异性损伤因子的反应。然而,COPD与异常的肺部炎症有关,即使在已经戒烟的患者中也会持续存在gydF4y2Ba11gydF4y2Ba.可以假设,一些不适当的和自我放大的致病回路可能会阻止易感个体炎症反应的解决。在这种生物学背景下,激活一个关键的促炎信号通路,如p38 MAPK,可能起着至关重要的作用。因此,目前的作者研究了p38磷酸化活性形式在外周肺组织以及肺泡巨噬细胞原代培养中的表达,并与吸烟和不吸烟对照组进行了比较。本研究的初步结果以前已以摘要形式报道过gydF4y2Ba12gydF4y2Ba.gydF4y2Ba
方法gydF4y2Ba
学科特点gydF4y2Ba
该研究招募了四组接受肺切除术的孤立性外周癌或肺减体积手术(LVRS)的受试者:7名严重/非常严重COPD吸烟者(全球慢性阻塞性肺病倡议(GOLD) 3期和4期),11名轻度/中度COPD吸烟者(GOLD 1期和2期),9名吸烟者和8名非吸烟对照组(无症状且肺功能正常)。重度/极重度COPD患者中有5人接受了LVRS, 2人接受了肺癌切除术。轻、中度疾病患者、对照组和非吸烟者均行肺癌切除术。术前一周进行肺功能检查。固定气道阻塞的定义根据最近的指南gydF4y2Ba13gydF4y2Ba一秒钟用力呼气量(FEV)的比值gydF4y2Ba1gydF4y2Ba)至预测的强迫肺活量(FVC) <70%;吸入400 μg沙丁胺醇后,所有患者的可逆性均<12%。gydF4y2Ba
胸片在肺功能研究后48小时内获得。在一部分患者中,肺气肿评分是根据前面描述的肺气肿x线征象评价标准计算的gydF4y2Ba14gydF4y2Ba.简单地说,这些迹象包括过度通货膨胀,gydF4y2Ba即。gydF4y2Ba横膈膜凹陷和变平(后前位和侧位视图均有评估)和胸骨后间隙增加,分别从0到3分。为了评估肺血管异常,在隆突水平将后前膜分为四个象限。分析每个象限是否存在不同的血管异常,并为其分配从0到0.5的个人评分。四个象限的部分分数被求和,并与过度膨胀分数相结合,得出一个0-16的累积分数。gydF4y2Ba
在研究前一个月,COPD患者没有加重,加重的定义是与痰液质量和数量变化相关的呼吸困难加重,导致受试者寻求医疗救助gydF4y2Ba15gydF4y2Ba.所有受试者均无急性上呼吸道感染,且在过去48小时内均未使用支气管扩张剂。受试者为非特应性(常见过敏原提取物皮肤试验阴性),既往无哮喘或过敏性鼻炎史。gydF4y2Ba
本研究符合《赫尔辛基宣言》gydF4y2Ba16gydF4y2Ba,并且每位接受手术或支气管镜检查的受试者都获得了知情的书面同意。gydF4y2Ba
免疫组织化学gydF4y2Ba
组织块取自手术获得的肺叶的胸膜下实质,避免了有肿瘤的区域。如前所述,样品固定在4%甲醛中并包埋在石蜡中gydF4y2Ba17gydF4y2Ba.使用兔单克隆一抗p38 (phospho-p38) MAPK活性形式进行免疫组化(稀释1:100;Cell Signaling Technology Inc., Danvers, MA, USA),亲和素-生物素复合物(abc -复合物试剂盒;Dako Ltd, High Wycombe, UK)和快速红底物染色检测(Dako Ltd)。gydF4y2Ba
磷酸化p38免疫染色在肺泡壁和肺泡巨噬细胞中定量,如下所示。对于肺薄壁中的细胞计数,仅检查具有单层细胞的肺泡壁,以避免技术人工因素(如相邻肺泡壁)引起的偏差gydF4y2Ba18gydF4y2Ba.使用光学显微镜计算肺泡壁内阳性染色细胞的数量(BX41;奥林巴斯,东京,日本),连接到一个录像机连接到计算机图像系统(image - pro Plus;媒体控制论公司,贝塞斯达,MD,美国)。简单地说,在×630的放大倍率下,测量肺泡壁的长度,并计数这些肺泡壁内磷酸化p38阳性MAPK细胞的数量。在幻灯片上随机分布了10个区域,对每个受试者进行评估,结果表示为阳性细胞的数量·mmgydF4y2Ba−1gydF4y2Ba如上所述的肺泡壁gydF4y2Ba17gydF4y2Ba.简单地说,为了评估肺泡巨噬细胞中phospho-p38的表达,评估了肺泡间隙内≥100个巨噬细胞。肺泡巨噬细胞被定义为细胞质丰富的单核细胞,存在于肺泡间隙中,不附着于肺泡壁。结果用阳性巨噬细胞数·高能场(hpf)表示gydF4y2Ba−1gydF4y2Ba.为了纠正巨噬细胞绝对数量可能存在的差异,结果还表示为磷酸化p38阳性巨噬细胞占总巨噬细胞的百分比gydF4y2Ba18gydF4y2Ba.gydF4y2Ba
对浸润肺泡壁的炎症细胞进行免疫组化分析。简单地说,小鼠单克隆抗体被用于鉴定中性粒细胞(抗弹性蛋白酶M752;Dako Ltd),巨噬细胞(anti-CD68 M814;Dako Ltd)和CD8+细胞(anti-CD8 M7103;Dako),如前所述gydF4y2Ba19gydF4y2Ba.在幻灯片上随机分布了10个区域,对每个受试者进行评估,结果表示为阳性细胞的数量·mmgydF4y2Ba−1gydF4y2Ba如上所述的肺泡壁gydF4y2Ba17gydF4y2Ba.gydF4y2Ba
在不了解临床和功能数据的情况下对病例进行编码和测量。gydF4y2Ba
细胞培养和Western blottinggydF4y2Ba
2例COPD患者,1例吸烟,1例非吸烟对照组(肺功能正常),支气管镜下取细胞,无菌生理盐水中收集,500×离心gydF4y2BaggydF4y2Ba5分钟gydF4y2Ba20.gydF4y2Ba.去除上清,洗净细胞球,重悬于10 mL Roswell Park Memorial Institute (RPMI)培养基中,添加抗生素(100 U·mL)gydF4y2Ba−1gydF4y2Ba青霉素和100 μg·mLgydF4y2Ba−1gydF4y2Ba链霉素;Sigma, St Louis, MO, USA)和Fungizone (1 μg·mL)gydF4y2Ba−1gydF4y2Ba;GIBCO BRL,盖瑟斯堡,马里兰州,美国)。采用Diff-Quick染色法通过形态学确定细胞类型(Baxter, Miami, FL, USA);每种细胞制剂中95%的细胞为巨噬细胞。细胞被稀释到1×10gydF4y2Ba6gydF4y2Ba巨噬细胞·毫升gydF4y2Ba−1gydF4y2Ba,镀于六孔板上(1ml·孔gydF4y2Ba−1gydF4y2Ba),孵育2-4小时,以方便附着。随后,去除培养基,加入新鲜培养基。细胞在37°C和5% CO孵育过夜gydF4y2Ba2gydF4y2Ba.gydF4y2Ba
培养后,细胞胰酶化5分钟,在补充的RPMI中重悬,4℃离心5分钟,然后在放射免疫沉淀试验(RIPA)缓冲液(150 mM NaCl, 1.5 mM MgCl)中裂解进行Western blottinggydF4y2Ba2gydF4y2Ba, 10 mM NaF, 10%甘油,4 mM EDTA, 1% Triton X-100, 0.1%十二烷基硫酸钠(SDS), 1%脱氧胆酸盐,50 mM HEPES, pH 7.4,外加磷酸酶和蛋白酶抑制剂混合物,25 mM β-甘油磷酸酯,1mM NagydF4y2Ba3.gydF4y2Ba签证官gydF4y2Ba4gydF4y2Ba, 1 mM苯基甲烷磺酰氟,10 μg·mLgydF4y2Ba−1gydF4y2Baleupeptin, 10 μg·mLgydF4y2Ba−1gydF4y2Ba抑肽酶)。然后使用12.5% sds -聚丙烯酰胺凝胶电泳(SDS-PAGE)分离蛋白质提取物,并转移到聚偏二氟乙烯膜上(Amersham Pharmacia, Little Chalfont, UK)。使用与免疫组织化学相同的抗磷酸化p38单克隆抗体进行免疫印迹。“剥离”后,用抗p38α抗体(Autogen Bioclear;Calne, Wiltshire, UK)。使用增强化学发光观察抗体结合(ECL-Plus;Amersham淀粉微球)。gydF4y2Ba
统计分析gydF4y2Ba
分组数据以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba或者作为中值(范围)。使用以下检验分析组间的差异进行多重比较:临床数据的方差分析;以及组织数据的Kruskall-Wallis检验。适当时,在Kruskall-Wallis检验后进行Mann-Whitney u检验。采用Spearman秩相关系数检验检验组织学参数与功能数据之间的相关性。p<0.05的概率值被认为是显著的。gydF4y2Ba
结果gydF4y2Ba
临床研究结果gydF4y2Ba
表1gydF4y2Ba⇓gydF4y2Ba显示检查对象的临床特征。四组研究对象的年龄相似,三组吸烟者的吸烟年限也相似。三组吸烟者包括目前吸烟者和前吸烟者,所有的前吸烟者都戒烟了>年。从选择标准的预期,FEV的值gydF4y2Ba1gydF4y2Ba% pred和FEVgydF4y2Ba1gydF4y2Ba/FVC比值在四组中存在差异(p<0.0001):重度COPD吸烟者FEV明显较低gydF4y2Ba1gydF4y2Ba% pred和FEVgydF4y2Ba1gydF4y2Ba/FVC比值高于轻/中度COPD吸烟者、功能正常吸烟者和非吸烟者(所有比较p<0.0001)。此外,患有轻度/中度COPD的吸烟者有明显较低的FEV %gydF4y2Ba1gydF4y2Ba和FEVgydF4y2Ba1gydF4y2Ba/FVC比值高于肺功能正常的吸烟者(p<0.0005)和不吸烟者(p<0.002)。在患有COPD的吸烟者中,支气管扩张剂的平均反应为5%。四组受试者在动脉氧张力(gydF4y2BaPgydF4y2Ba啊,一个gydF4y2Ba2gydF4y2Ba)值(p = 0.008)。事实上,患有严重慢性阻塞性肺病的吸烟者的血压更低gydF4y2BaPgydF4y2Ba啊,一个gydF4y2Ba2gydF4y2Ba值高于轻/中度COPD吸烟者(p = 0.03)、吸烟者(p = 0.005)和非吸烟对照组(p = 0.04),而其他三组受试者之间无显著差异。此外,动脉二氧化碳张力无显著差异(gydF4y2BaPgydF4y2Ba,有限公司gydF4y2Ba2gydF4y2Ba)。残余体积平均值(RV;重度COPD吸烟者的% pred)和放射肺气肿评分高于轻度/中度COPD吸烟者,而肺对一氧化碳扩散能力的平均%值则相反(gydF4y2BaDgydF4y2BaL,有限公司gydF4y2Ba).然而,由于测量RV(连同肺气肿评分)和gydF4y2BaDgydF4y2BaL,有限公司gydF4y2Ba仅在一部分患者中进行,没有对这些参数进行正式的统计分析。gydF4y2Ba
受试者临床特征gydF4y2Ba
免疫组织化学结果gydF4y2Ba
肺泡巨噬细胞和肺泡壁中磷酸化p38的定量结果见图1gydF4y2Ba⇓gydF4y2Ba- - - - - -gydF4y2Ba⇓gydF4y2Ba3.gydF4y2Ba⇓gydF4y2Ba.表2显示了表达phospho-p38的细胞的中位数和相对范围gydF4y2Ba⇓gydF4y2Ba.gydF4y2Ba
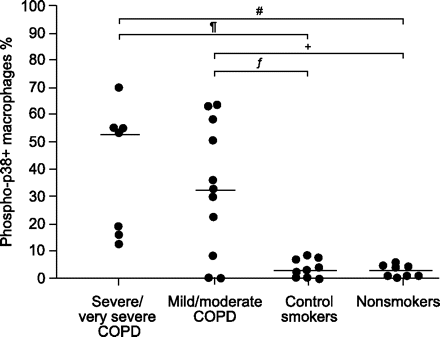
重度/极重度慢性阻塞性肺疾病(COPD)吸烟者、轻度/中度COPD吸烟者、对照吸烟者和肺功能正常的非吸烟受试者肺泡腔中活化p38丝裂原活化蛋白激酶阳性(phospho-p38+)巨噬细胞的个体计数。数据以肺泡巨噬细胞百分比表示。——:中值。gydF4y2Ba#gydF4y2Ba: p = 0.001;gydF4y2Ba¶gydF4y2Ba: p = 0.0008;gydF4y2Ba+gydF4y2Ba: p = 0.02;gydF4y2BaƒgydF4y2Ba: p = 0.01。gydF4y2Ba
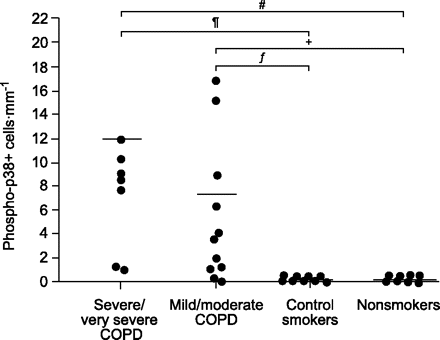
重度/极重度慢性阻塞性肺病(COPD)吸烟者、轻度/中度COPD吸烟者、对照吸烟者和肺功能正常的非吸烟受试者肺泡壁中活化p38丝裂原活化蛋白激酶阳性(phospho-p38+)细胞的个体计数。数据以单元数·mm表示gydF4y2Ba−1gydF4y2Ba肺泡壁。——:中值。gydF4y2Ba#gydF4y2Ba: p = 0.0004;gydF4y2Ba¶gydF4y2Ba: p = 0.0005;gydF4y2Ba+gydF4y2Ba: p = 0.0005;gydF4y2BaƒgydF4y2Ba: p = 0.006。gydF4y2Ba
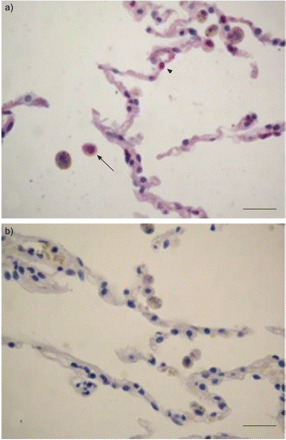
a) COPD吸烟者和b)肺功能正常的吸烟者的免疫染色显示肺泡壁内活化的p38丝裂原活化蛋白激酶阳性(磷酸化p38+)细胞和抗磷酸化p38单克隆抗体的磷酸化p38+肺泡巨噬细胞。箭头:磷酸化p38+肺泡巨噬细胞;箭头:肺泡壁内的磷酸化p38+细胞。比例尺= 150 μm。gydF4y2Ba
肺实质中p38丝裂原活化蛋白激酶(phospho-p38)免疫染色定量阳性gydF4y2Ba
与肺功能正常的吸烟者(p = 0.0008)和不吸烟者(p = 0.001)相比,重度COPD患者的Phospho-p38+巨噬细胞占总巨噬细胞的百分比增加。与吸烟(p = 0.01)和不吸烟对照组(p = 0.02)相比,轻度/中度COPD吸烟者的Phospho-p38+巨噬细胞也增加。重度COPD患者与轻/中度COPD患者之间、肺功能正常的吸烟者与非吸烟者之间均无显著差异。当结果表达为phospho-p38+巨噬细胞的数量·hpf时,也得到了类似的结果gydF4y2Ba−1gydF4y2Ba(表2gydF4y2Ba⇑gydF4y2Ba).gydF4y2Ba
肺泡壁的磷酸化p38+细胞在四组受试者中也有显著差异(p<0.0001)。事实上,磷酸化p38+细胞的数量·mmgydF4y2Ba−1gydF4y2Ba与吸烟组(p = 0.0005)和不吸烟对照组(p = 0.0004)相比,重度COPD患者的心肌梗死发生率升高。与吸烟(p = 0.006)和不吸烟对照组(p = 0.0005)相比,轻/中度COPD吸烟者肺泡壁内的Phospho-p38+细胞也有所增加。同样,重度COPD吸烟者与轻/中度COPD患者之间,肺功能正常的吸烟者与非吸烟者之间也没有明显差异(表2)gydF4y2Ba⇑gydF4y2Ba).gydF4y2Ba
对不同炎症细胞亚型的检查发现,浸润肺泡壁的CD8+ t细胞的数量在四组被检查的受试者中有显著差异(p = 0.002),而巨噬细胞和中性粒细胞则没有。特别是,CD8+ t细胞在两名重度COPD吸烟者中均有增加(中位数(范围):8.3(6.9-14.4)个细胞·mmgydF4y2Ba−1gydF4y2Ba)和轻/中度COPD(5.2(1.8-13)个细胞·mm)吸烟者gydF4y2Ba−1gydF4y2Ba)与对照组(2.4(1.4-2.6)个细胞·mmgydF4y2Ba−1gydF4y2Ba;P = 0.004和P = 0.03)和非吸烟者(2(0-3)个细胞·mmgydF4y2Ba−1gydF4y2Ba;P = 0.008和P = 0.03)。重度COPD患者与轻/中度COPD患者之间、肺功能正常的吸烟者与非吸烟者之间均无显著差异。gydF4y2Ba
肺泡壁的总长度为(平均±gydF4y2Ba扫描电镜gydF4y2Ba重度COPD吸烟者4.3±0.4 mm,轻/中度COPD吸烟者5.3±0.4 mm,肺功能正常吸烟者6.6±0.4 mm,非吸烟者6.8±0.2 mm。gydF4y2Ba
当将所有吸烟受试者视为一组时,phospho-p38+巨噬细胞与FEV呈负相关gydF4y2Ba1gydF4y2Ba% pred值(p = 0.008, r = -0.52)或FEVgydF4y2Ba1gydF4y2Ba/植被覆盖度比值(p = 0.006, r = -0.54)。肺泡壁内磷酸化p38+细胞与FEV值呈负相关gydF4y2Ba1gydF4y2Ba% pred (p = 0.001, r = -0.65)和FEVgydF4y2Ba1gydF4y2Ba/植被覆盖度比值(p = 0.0003, r = -0.71)。此外,肺泡壁内磷酸化p38+细胞的数量与肺泡壁内磷酸化p38+细胞的数量呈负相关gydF4y2BaPgydF4y2Ba啊,一个gydF4y2Ba2gydF4y2Ba值(p = 0.04, r = -0.41)。gydF4y2Ba
当考虑与炎症细胞的关系时,肺泡壁的磷酸化p38+细胞与浸润肺泡壁的CD8+细胞数量呈显著正相关(p = 0.0006;R = 0.75),但既没有中性粒细胞,也没有巨噬细胞。gydF4y2Ba
最后,phospho-p38的表达与累积吸烟史无关,也不受当前吸烟状况的影响。gydF4y2Ba
免疫印迹分析gydF4y2Ba
与吸烟和不吸烟对照组相比,在两名COPD患者肺泡巨噬细胞的细胞蛋白提取物中检测到p38 MAPK磷酸化显著增加(图4)gydF4y2Ba⇓gydF4y2Ba).相比之下,在四名受试者中,肺泡巨噬细胞表达的总p38α MAPK没有观察到差异(图4)gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
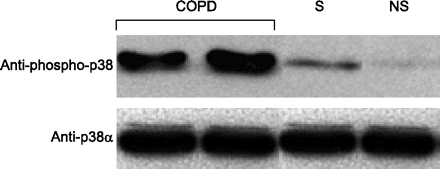
Western免疫印迹分析两名肺功能正常的慢性阻塞性肺病(COPD)患者、吸烟者(S)和非吸烟者(NS)肺泡巨噬细胞中表达的活化p38丝裂原活化蛋白激酶(phospho-p38)和p38α亚型。gydF4y2Ba
讨论gydF4y2Ba
目前的研究表明,COPD吸烟者肺泡巨噬细胞和肺泡壁中p38 MAPK磷酸化形式的增加。Western blot分析证实COPD患者肺泡巨噬细胞中磷酸化p38的表达增加,而总p38α水平没有任何变化。此外,phospho-p38的表达与肺功能损害的程度和浸润肺泡壁的CD8 t淋巴细胞的数量有关。据作者所知,目前的研究首次在人类肺组织中获得证据,证明p38激活在COPD相关炎症过程中所起的潜在作用。gydF4y2Ba
在免疫组化和Western blot实验中,使用了一种抗磷酸化p38单克隆抗体,它能特异性识别p38的两个磷酸化位点(苏氨酸180和酪氨酸182)。由于涉及这些氨基酸位点的双重磷酸化仅发生在p38α和p38β亚型中,并且β亚型的表达似乎仅限于t细胞gydF4y2Ba21gydF4y2Ba,可以合理地认为,在肺巨噬细胞中检测到的磷酸化p38主要是α亚型。因此,磷酸化依赖的p38α激活可能是COPD炎症过程持续的信号机制中的主要分子事件。p38α和-β抑制剂在COPD动物模型中抑制细胞因子产生的能力证实了这一点gydF4y2Ba7gydF4y2Ba.gydF4y2Ba在体外,gydF4y2Ba最近Smith发现p38 MAPK磷酸化增加gydF4y2Baet al。gydF4y2Ba10gydF4y2Ba而在目前的研究中,在肺泡巨噬细胞和肺泡壁中检测到高水平的磷酸化p38表达gydF4y2Ba在活的有机体内gydF4y2Ba.gydF4y2Ba
众所周知,肺泡巨噬细胞通过持续释放蛋白水解酶导致肺组织破坏,在COPD发病机制中发挥核心作用。这些细胞也可能通过分泌大量的细胞因子和趋化因子来调节炎症反应。p38 MAPK激活是多种炎症介质合成的关键步骤,特别是,lps诱导的人肺巨噬细胞TNF-α的释放依赖于p38介导的TNF-α mRNA的稳定gydF4y2Ba10gydF4y2Ba.此外,p38α/β抑制剂引起的p38失活显著减少TNF-α的产生。gydF4y2Ba
目前的结果还涉及到COPD发病机制中涉及的其他细胞类型。在这方面,t细胞在慢性阻塞性肺病的免疫反应中起着重要的作用,在这种疾病中,趋化因子受体CXCR3表达增加,TNF-α和干扰素-γ释放增加,向1型转变已被描述gydF4y2Ba22gydF4y2Ba,gydF4y2Ba23gydF4y2Ba.最近有证据表明,在人支气管上皮细胞中,cxcr3诱导的趋化性严重依赖于p38 MAPK通路的信号通路gydF4y2Ba24gydF4y2Ba.此外,在本研究中,发现肺泡壁内磷酸化p38+细胞数量与CD8+细胞数量呈正相关。总之,这些结果表明p38通路和t淋巴细胞激活之间存在严格的相互作用,这可能导致炎症反应的持续。就目前作者所知,尚不清楚哪种p38同工酶由CD8+ t淋巴细胞表达。然而,这些细胞产生IL-2可以被p38α和-β的选择性抑制剂抑制gydF4y2Ba25gydF4y2Ba.因此,这两种亚型似乎与CD8+ t细胞功能最相关gydF4y2Ba21gydF4y2Ba.在CD4+和CD8+ t细胞中均检测到p38α和p38β的双重磷酸化gydF4y2Ba26gydF4y2Ba.识别不同p38亚型的更特异性抗体的可用性,以及具有更大选择性的p38抑制剂的开发,可能有助于更好地表征CD8+ t淋巴细胞优先表达的p38亚型。这种表达模式可能具有相关的功能含义,例如,与α亚型相比,p38β是一种更有效的激活转录因子2的刺激剂gydF4y2Ba26gydF4y2Ba.gydF4y2Ba
目前在人类肺部样本中获得的发现,证实并扩展了先前在吸烟诱导的肺部炎症实验模型中进行的研究。MarwickgydF4y2Baet al。gydF4y2Ba27gydF4y2Ba研究人员检测了暴露在香烟烟雾中的大鼠肺,发现p38磷酸化增强,与转录因子NF-κB和AP-1激活增加有关。此外,他们观察到组蛋白4的高乙酰化和组蛋白3的磷酸化乙酰化导致染色质重排,同时组蛋白去乙酰化酶(HDAC)活性降低。伊藤gydF4y2Baet al。gydF4y2Ba28gydF4y2Ba最近研究了HDAC在COPD患者外周肺组织中的表达和活性,显示HDAC活性的进行性损害与IL-8 mRNA和组蛋白4乙酰化的显著增加并行。有趣的是,IL-8基因受NF-κB的转录调控,其激活至少部分受p38 mapk介导的组蛋白3丝氨酸10磷酸化控制gydF4y2Ba29gydF4y2Ba.根据所有这些考虑,可以提出磷酸化依赖的p38 MAPK激活可能与组蛋白修饰一起促进肺部炎症的发生和发展。考虑到不仅COPD患者,而且吸烟哮喘患者对类固醇的不良反应,这种相互作用可能变得重要。已经提出了几种机制来解释类固醇抵抗;其中,已知激活的p38 MAPK会磷酸化糖皮质激素受体(GR)gydF4y2Ba在体外gydF4y2Ba,从而降低皮质类固醇的结合亲和力gydF4y2Ba30.gydF4y2Ba.因此,糖皮质激素调控基因的转录活性将受损,随之而来的是MAPK磷酸酶(MKP)-1表达的减少,这确实是由激活的GR诱导的gydF4y2Ba31gydF4y2Ba.因此,在中度至重度COPD中,过量的磷酸化p38活性可能实现前馈电路,进一步放大MAPK通路的作用。在这种情况下,由于MKP-1下调导致的去磷酸化缺陷,p38激活将更加持久。gydF4y2Ba
在本研究中,吸烟本身并没有上调巨噬细胞和肺泡壁中的p38激活,因为在肺功能正常的吸烟者和不吸烟的对照组中也存在类似的免疫反应。此外,phospho-p38的表达不受当前吸烟状况或累积吸烟史的影响。这种情况与在动物模型中观察到的情况不同,在动物模型中,暴露于烟草烟雾足以增强p38磷酸化gydF4y2Ba27gydF4y2Ba.相比之下,人体的p38刺激与疾病的存在严格相关,因为一旦确定了固定的气流限制,即使在戒烟后,p38 MAPK的激活仍然存在。值得注意的是,慢性阻塞性肺病患者的炎症反应在戒烟后很长时间内仍然存在gydF4y2Ba11gydF4y2Ba.总之,这些观察结果支持了这样一种观点,即除了吸烟之外,不同因素(包括遗传易感性、空气污染和呼吸道感染)的复杂相互作用促进了COPD,其特征是表型表达的高度变异性。gydF4y2Ba
目前研究的一个可能的局限性是,它主要是在肺癌患者的手术标本上进行的,癌症本身的存在可能影响了MAPK的激活。目前的作者试图通过只考虑组织学正常的区域来避免这种偏见,这些区域的特征是没有肿瘤并且远离受影响的区域。此外,由于肺癌在轻/中度COPD、吸烟和不吸烟对照组中同样存在,因此COPD中p38磷酸化增加的发现很可能是有效的。最后,目前的结果得到进一步验证,在未受癌症影响的患者中也观察到p38激活(gydF4y2Ba即。gydF4y2Ba严重肺气肿患者行LVRS)。应该承认,理想情况下,像目前这样的研究需要一个真正的对照组,即没有肺癌的非吸烟者;然而,从已完成完整临床和功能特征的健康人身上获得手术标本是极其困难的。gydF4y2Ba
综上所述,目前的研究表明,吸烟者慢性阻塞性肺病肺泡间隙和肺泡壁中活化的p38丝裂原活化蛋白激酶表达增加,提示p38丝裂原活化蛋白激酶通路的激活是该疾病发病机制中的关键步骤。这些发现支持了p38丝裂原活化蛋白激酶作为开发新的、更有效的慢性阻塞性肺疾病治疗策略的合适分子靶点的相关性。gydF4y2Ba
致谢gydF4y2Ba
作者感谢C.A. Drace(帕多瓦大学心脏、胸椎和血管科学系,帕多瓦,意大利)协助编辑本手稿。gydF4y2Ba
- 收到了gydF4y2Ba2007年3月27日。gydF4y2Ba
- 接受gydF4y2Ba2007年10月16日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba















