抽象的
促红细胞生成素(EPO)动员内皮祖细胞,促进心力衰竭的新生血管。本文作者通过血流相关肺动脉高压(PAH)模型研究了EPO对肺血管和心脏重构的影响。
1周后用野百合碱联合腹主动脉下腔静脉分流术(PAH或实验组)诱导成年雄性Wistar大鼠肺动脉高压。随后,将大鼠随机分为接受EPO治疗的大鼠(PAH+EPO组)和对照组。3周后评估肺和全身血流动力学,右室和肺血管重构。
血管内肺血管的血管闭塞(13.4±0.7与PAH + EPO和PAH中的16.7±1.3%)和预缩醛动脉的内侧壁厚(壁到腔比0.13±0.01与Pah + EPO和PAH中的0.17±0.01)在用EPO治疗后减少。此外,通过治疗增加了右心室毛细血管密度(2,322±61与2100±63毛细血管·毫米-2分别在PAH+EPO和PAH中)。EPO治疗未改变模型肺动脉压升高和右心室收缩力下降。
在该流动相关肺动脉高压的大鼠模型中,促红细胞生成素治疗有利地影响肺血管和心脏重塑。这些组织病理学作用不伴随显着改善的血液力学。
Erythropoietin(EPO)最为罕见,以其在蛎肠中的作用,作为缺氧诱导的激素,导致红细胞前体细胞的增殖和分化。最近,EPO已被证明是发挥渗流效应。它显示急性脑和心脏缺血中的细胞保护性能与抑制细胞凋亡相关1-4..此外,已经证明EPO治疗后心脏功能的改善与实验性心力衰竭新血管的形成有关5..
肺动脉高压(Pulmonary arterial hypertension, PAH)是一种疾病,肺血管重塑导致肺血管阻力(Pulmonary vascular resistance, PVR)增加,从而导致右心室衰竭。缺氧肺动脉高压模型大鼠给予EPO可降低肺血管重塑,但对右心室肥厚或肺动脉压力无影响6..此外,EPO产量增加的转基因小鼠似乎对缺氧性肺动脉高压的发展不太敏感7..在最近的一项研究中,缺乏EPO受体的小鼠在缺氧条件下加速了肺动脉高压的发育,具有更明显的肺血管改造8..
因此,EPO可能在肺动脉高压肺血管疾病的发展过程中起着多水平的重要作用。EPO治疗可通过改善肥厚心肌的毛细血管化或直接促进肺血管重构而对肺动脉高压产生有益作用。因此,本研究旨在确定EPO治疗对血流相关肺动脉高压模型大鼠心脏和肺血管重构的影响。
方法
动物和学习设计
总共45只称重315-370g的雄性Wistar大鼠,从Harlan(北京,荷兰)获得。实验方案由制度畜牧业和使用委员会批准(Groningen,Groningen,Groningen,Groningen,Groningen)。调查符合美国国家卫生研究院“实验动物的护理和使用指南“9..
大鼠随机分配到三个实验组,如下所述。1)实验组(PAH组; N = 14),其中产生流动相关的肺动脉高压,如其他地方所述10.简而言之,对大鼠进行偏甲酸碱注射以增加肺动脉压(60 mg·kg-1;Sigma Chemical Co.,ST路易斯,Mo,USA),然后通过创建腹主动脉窝凸族术30后诱导增加流量。2)用EPO接受治疗的实验组(10μg·kg-1半衰期约为50 h, Darbepoetin-α, Aranesp®;安进公司,加州千橡市,美国)通过腹腔手术当日单次腹腔注射(PAH+EPO组;n = 18)。剂量是根据目前作者实验室的试点实验选择的,该实验显示红细胞压积显著上升,与2000 IU·kg的剂量相当-1短效促红细胞生成素。3)进行假手术并注射生理盐水的大鼠作为对照组(n = 13)。
血液动力学测量
EPO给药3周后,用异氟醚(2.0%)在2:1的氧化亚氮和氧气混合物中麻醉动物。肺动脉压力的测量采用标准技术,在目前的作者的实验室常规使用10,如rabinovitch所述11.如果无法获得肺动脉压,则记录右心室收缩压(RVSP)作为收缩肺动脉压。随后,将微型压力传感器(Millar Instr.Inc.,Houston,TX,USA)插入右心室腔中以确定RVSP和右心室舒张舒张压(RVEDP)。作为收缩性指标,右心室压力的最大增加(RVP;计算为压力变化(P.)随着时间(T.),IE。D.P./ dT.马克斯),并校正RVSP (dP./ dT.马克斯指数)。同样,-D.P./ dT.马克斯指数由RVP的最大下降率计算,并作为松弛的指标。
通过引入导管通过测量左颈动脉进入主动脉,全身性动脉压以及心脏频率。
肺血管改造
在完成血液动力学测量后,从上腹主动脉和脉静脉中抽取血液样品,并测定氧饱和度以计算主动脉囊肿饱和差异。胸部打开,切除心脏和肺。通过在20cmH的压力下用3.6%福尔马林填充3.6%福尔马林来固定左肺2O.将右肺冷冻在液氮中进行进一步分子分析。肺切片(5 μm厚)用苏木精和伊红染色和Verhoef弹性蛋白染色进行血管尺寸的形态测量分析,根据先前描述的方案10.在肺切片中,使用图像分析系统(image - pro Plus 4.5;媒体控制论,银泉医学博士,美国)10.直径<50μm的血管通常没有明显可辨别的内部弹性薄层。因此,在这些血管中计算血管闭塞分数,而不是较大肺动脉中的内侧壁/腔比的计算。根据下面的公式在缩醛内肺血管中计算闭塞:
(外部血管区域 - 腔腔区域)/(外部血管面积)(1)
如果它们具有最长/ 2的最长/最短直径,圆形或超过四分之一的血管壁的崩溃,则从测量中排除肺动脉。根据van辛烯评估40个小肺血管的肌肉酶化et al。12.完全肌肉容器定义为具有双弹性薄片的容器,其圆周以上。如果双弹性薄片小于圆周的一半,则将血管分类为部分肌肉。非血管具有单个弹性薄层。
右心室重塑
心脏分为心房、心室和室间隔。切片分别称重,用3.6%福尔马林固定。取5 μm厚的心室中段心肌横切面,用Gomori银染色分析心肌细胞大小Griffonia Simplicifolia内皮细胞凝集素染色(Sigma Chemical Co.)分析毛细管密度13那14.图像分析(Image-Pro加4.5)用于测量毛细血管密度和肌细胞尺寸。毛细密度表示为每个组织区域的毛细管数量(毛细管·mm-2)和肌细胞大小作为横向切割髓鞘的平均横截面积。
基因表达
为了确定肌苷 - 重链(MHC)mRNA和血管生成因子的表达,使用Qiagen RNeasy Mini Kit(Qiagen,Frankfurt,Germany)从肺和右心室组织中提取RNA。如前所述,在基因AMP 5700序列探测器(Applied Biosystems,Nieuwerkerk A / D Ijssel,荷兰)上进行实时PCR实验15.设计用于血管内皮生长因子(VEGF),其两种受体(R)亚型VEGF-R1和-R2,以及α-和β-MHC。表1中提供了各自的引物序列⇓.PCR结果由稀释标准曲线得到。
统计分析
数据显示为平均值±SEM..组间差异采用单因素方差分析,采用Fisher保护最小显著性差异后HOC测试。当数据通常不分布时使用非参数Kruskall-Wallis测试,然后使用Mann-Whitney后HOC用Bonferroni校正测试。用Pearson的相关试验进行相关分析。选择αnα-值0.05。
结果
动物模型和治疗
在45只大鼠中,除5只外,其余均成功进行分流手术。3只动物死于急性手术相关并发症;在实验结束时,两只动物没有进行分流,因此被排除在进一步分析之外。EPO组有1只大鼠因不明原因过早死亡。
在该方案结束时,实验动物的体重减少并开发了呼吸困难,定义为使用配件呼吸肌肉。EPO治疗没有改变体重(表2⇓).用药3周后红细胞压积无显著增加(0.42±0.02)与多环芳烃动物为0.39±0.02;p = 0.41)。
血液力学和心功能
主动脉-下腔静脉饱和差异在分流动物组中减小,但在治疗和未治疗动物之间保持相同(表2)⇑),提示治疗对分流流无影响。与对照组相比,实验组大鼠平均肺动脉压和RVP明显升高。与对照组相比,RVEDP也增加了。动物模型全身动脉压和心率降低。EPO治疗没有显著改变肺动脉或全身动脉压,也没有改变rvp。EPO治疗后,心频明显增加(表2)⇑).心肌收缩力,测量为dP./ dT.马克斯指数,在模型中受损。EPO治疗无法恢复这种受损的收缩力。同样,EPO治疗后没有改变右心室松弛受损(表2⇑).
心脏和肺部重量
实验大鼠表现出增加的心脏重量,通过增加的器官重量/体重比(表2⇑).用EPO治疗没有改变全心全重/体重比。右心室肥大,表达为右心室/左心室加隔膜比例,在未处理的肺高血压群中几乎翻了一番,而EPO没有显着影响该比例(表2⇑).
肺血管改造
预缩醛肺动脉(>50μm)
肺血管重塑的代表图片如图1所示⇓.在未处理的大鼠中,腺泡前肺动脉的壁厚和壁腔比增加,并且在这些动物中数量增加。实验动物腺泡前动脉未见内膜增生。治疗显著降低了这些动脉的壁厚(表3)⇓).增大的壁腔比降低了>50%(图1a-c)⇓和2a⇓).
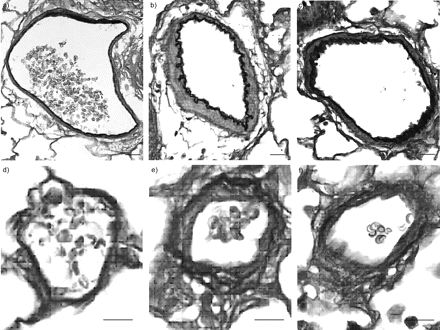
A-C)预丙氨酸肺动脉和D-F中肺组织病理学(Verhoef Elastin染色)的典型例子,D-F)对照(A和D),实验组(B和E)和治疗的实验组和实验动物促红细胞生成素(C和F)。A-C)秤条=20μm,D-F)刻度条=40μm。
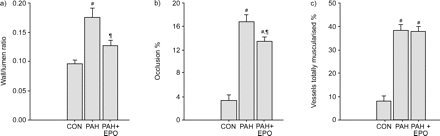
肺血管重塑。a)预丙氨酸前肺动脉中的壁/腔比。b)母癌血管内闭塞分数。c)完全肌肉发达的胰腺炎内肺血管的百分比。数据显示为平均值±SEM..骗子:控制;PAH:肺动脉高压实验组;PAH + EPO:用促红细胞生成素治疗PAH实验动物。#:P <0.05与con¶:P <0.05与PAH。
心脏重塑
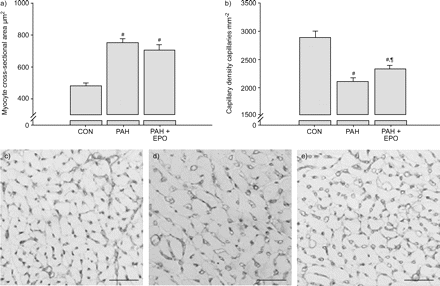
通过测定肌细胞尺寸进一步检查右心室肥大。肌细胞横截面积在PAH组中增加了50%。治疗没有导致肌细胞尺寸的显着降低(图3A⇓).
条形图代表a)心肌细胞横截面面积和b)毛细血管密度的测量值。数据显示为平均值±SEM..c - e) c)对照组(CON)、d)肺动脉高压实验组(PAH)和e)用促红细胞生成素(PAH+EPO)治疗的肺动脉高压实验动物的右室壁凝集素染色组织切片,以确定毛细血管密度。#:P <0.05与控制;¶:P <0.05与PAH。秤条=40μm。
用凝集素染色的毛细血管可以清楚地在心肌恒定和来自每组的代表性实例中进行区分,如图3C-E所示⇑.与对照组相比,实验组毛细血管密度降低(2100±63)与2891±110,p < 0.001与控件)。EPO处理后毛细管密度增加11%(2,322±61,P = 0.049与实验组;图3 b⇑).
基因表达
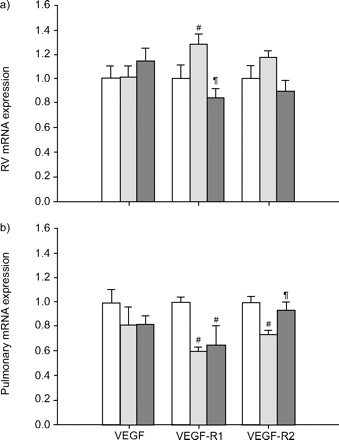
模型右心室VEGF- r1表达增加,VEGF、VEGF- r2表达无变化。治疗后心脏VEGF和VEGF- r2表达未见改变。然而,治疗部分地阻止了未治疗组VEGF-R1表达的增加(图4a)⇓).
用于血管内皮生长因子(VEGF)的实时PCR及其1(VEGF-R1)和2(VEGF-R2)受体。结果与对照动物相比,与A)右心室(RV)组织和B)肺组织的表达的对照动物相比,与对照动物相比。数据显示为平均值±SEM..□:控制(CON);░:肺动脉高压(PAH)实验组;▒:用促红细胞生成素(EPO)治疗的PAH实验动物。#:P <0.05与con¶:P <0.05与PAH。
即使在EPO治疗后,肺VEGF表达在动物模型中没有改变。VEGF-R1和-R2均在本模型中的肺组织中降低。EPO治疗恢复肺VEGF-R2表达到接近正常水平(图4B⇑),而不影响VEGF-R1的表达。
右心室α-MHC表达在模型中降低(0.65±0.08与对照1.27±0.08,P <0.001)但未通过治疗而改变(0.65±0.09,P =不显着(ns.)与多环芳烃组)。β-MHC表达增加(0.90±0.05)与对照0.31±0.06,P <0.001)。治疗没有影响这个(1.00±0.13,p = ns.与多环芳烃组)。因此,在模型中β/α-MHC的表达比例增加,而没有治疗的影响。
讨论
在流动相关PAH的目前动物模型中,EPO治疗改善肺血管重塑和增加心肌毛细血管。这些变化不伴随肺动脉压或右心室心肌收缩性的变化。
本模型中的调查结果与其他形式的肺动脉高压的模型同时。在缺氧肺高血压大鼠中,右心室/体重比和RVPS未被EPO治疗改变,而肺血管重塑改善6..在EPO产生增加的小鼠中,经过长时间的缺氧暴露后,离体灌注肺中的肺血管收缩反应降低,肺血管重构也降低7.那16.因此,对肺动脉高压的不同动物模型的研究强烈表明,EPO有利地影响肺血管重塑,而不改变血管动力学或右心室肥大。有趣的是,EPO给药影响肺血管壁厚,而不会影响较小的肺部血管的肌肉多变,表明对细胞增殖速率而不是血管壁的组成的影响。若干机制可能负责这种逆转肺血管重塑的逆转。首先,EPO施用导致内皮祖细胞(EPC)从骨髓动员17那18.EPO刺激EPC增殖,粘附和分化在体外17那18.通过刺激EPC的掺入新内皮,EPO有利于内皮修复19.因此,EPC可能有益于修复肺动脉高压的受损肺内皮。在六洛曲霉素大鼠模型中,在肺脉管系统中检出了静脉内注射的EPC,并且被证明预防偏霉素诱导的肺血管重塑20.那21.然而,自撒哈拉沙漠以来,文学并不是决定性的et al。22不能证明注射用未分叉的骨髓衍生细胞对大鼠内侧壁厚的有益效果。最近,萨摩et al。8.表明,与野生型小鼠相比,在EPO受体缺陷小鼠中加速了肺压增加和肺血管重塑的增加和肺血管重塑。这些动物的动员和招募对EPC的肺内皮显着损害。
最近,已经提示EPO的抗氧化和抗凋亡作用依赖于Janus激酶-2和蛋白激酶B(Akt)磷酸化,并且可以与Haeme氧气(HO)-1的活化连接。23那24.HO-1是一种受akt信号调控的具有强抗氧化和抗凋亡活性的诱导酶。HO-1在人肺动脉高压中表达降低25,而HO-1的抑制已被证明会加剧鼠偏异醛碱诱导的肺动脉高血压26.增加HO-1在该模型中是有益的27.因此,HO-1可能对EPO在肺动脉高血压的影响中具有核心作用,以获得进一步调查。
可以调节EPO给药的有益效果的另一种化合物是VEGF。增加了VEGF表达的特异性在PAH的患者的丛林病变中表现出28那29.这可能表明VEGF在疾病发病机制中的作用。
体内实验表明VEGF在肺动脉高压中的作用是有益的。首先,新生大鼠的VEGF抑制导致肺动脉高压30..此外,人重组VEGF的给药保留内皮功能并减少新生儿初级肺动脉高压的绵羊模型中的肺血管重塑31那32.VEGF的基因转移降低了兔子的博尔霉素诱导的肺动脉高压33大鼠缺氧肺动脉高压34.当表达vegf的血管平滑肌细胞被运送到经野红花碱处理的Fisher大鼠时,RVP和右心室肥厚降低,肺动脉壁厚度也降低35.已显示EPO在人血管内皮细胞中诱导VEGF在体外36.体内研究显示给EPO后VEGF增加37那38.这些数据在一起表明EPO可以通过VEGF途径介导EPO的有益效果。
在本模型中,不能证明EPO给药后3周的VEGF mRNA表达的变化。然而,VEGF受体mRNA表达在模型和EPO治疗后都改变。
已知VEGF-R1对抗血管形成,可能通过以可溶性形式作为清除剂39那40.相比之下,VEGF-R2信号在促进血管生成方面很重要41.在本动物模型中,右心室VEGF-R1表达增加表明vegf介导的血管形成受到抑制。对实验性肺中受体调节的净效应的解释更为复杂,因为与对照组相比,模型中两种受体亚型均下调。EPO治疗可能会刺激vegf介导的血管生成作用,因为在EPO治疗后,无论是在右心室还是在高血压肺中,VEGF-R1/-R2的表达率都降低了。
在肺动脉高压过程中,右心室肥大和失败是结果的重要决定因素。已显示EPO治疗以改善心脏功能,并在心肌梗死后心力衰竭大鼠诱导新生血管5..在与慢性肾功能衰竭相关的左心室肥厚的大鼠模型中,EPO治疗似乎增加了心肌密度42.在EPO治疗后,这种增加的血管生长与循环EPC的数量相关43.此外,VEGF似乎在增加心肌毛细血管化方面也至关重要,因为通过阻断VEGF活性可以拮抗心动过缓诱导的心肌血管生成44.
EPO是否在预防肺动脉高压右心室肥厚向右心室衰竭发展中发挥作用仍是一个问题。虽然肥厚的右心室毛细血管密度增加,但这与收缩性的改善无关。为了进一步评估毛细血管密度增加的功能后果,我们研究了不同亚型MHC的表达。在正常的心肌细胞中,快速的α-和缓慢的β-MHC均有表达。这两种形式的atp酶活性不同。α-MHC表达增多与收缩性增强有关5.那45.在治疗后的收缩性测量缺乏变化的一致性中,在处理和未处理的大鼠之间的α-和β-MHC的表达中没有发现差异。
因此,EPO治疗可改善心脏毛细血管化,但这与改善右心室功能或减少肥厚无关。对于观察到的影响,一种可能的解释是EPO引起的血液粘度增加。虽然小et al。46最初假设,由于相关的多环血症,EPO给药将恶化缺氧肺动脉高血压,在该组的实验中,肺动脉压未增加,肺血管重塑似乎更加明显6..此外,来自EPO治疗的缺氧大鼠的分离的肺部具有比甘露血致血症患者大鼠血液灌注的血液处理的缺氧大鼠的低pVR6..这表明常规血症血症的ePO处理的动物可能降低PVR,因此,较少的右心室肥大。虽然在给药后3周内发现在血细胞比容中没有显着差异,但可能是可能的初始增加5..因此,EPO导致PVR增加的血红素效应可以抵消心脏的有益结构效应。
限制
本研究不允许鉴定EPO对当前模型中的心脏和肺血管重塑的有益作用的机制。虽然EPO给药后3周已经在3周后进行了血细胞比容和VEGF受体系统,但没有进行连续调查。没有研究其他潜在机制,例如活化EPC或HO-1的诱导。需要进一步的研究来详细探讨EPO的机制。
此外,本研究未解决多剂量EPO的效果。目前的作者选择使用10μg·kg的Darbepoetin剂量-1,剂量与2,000人的人重组EPO相当。这种剂量比在大多数实验中使用的剂量低得多,用于解决EPO在心脏缺血和失败模型中的效果5.那47那48.然而,还在更低的剂量下描述了心脏衰竭中的有益效果49.此外,Prunieret al。50.使用1.5μg·kg的剂量证明了EPC的动员-1·星期-1.
EPO治疗后心脏频率标准化,但不能证明肺血管动力学的变化。如果EPO治疗完全改变血管组织学参数而不具有功能后果,则其临床相关性是值得怀疑的。然而,其他小剂量或给药频率可能导致额外福利的可能性无法排除。其次,仅测量肺动脉压,而不是心脏输出或PVR。由于电阻容器的直径发生变化,因此可以想到这会影响PVR。在目前的分流模型中,EPO后逆转肺血管重塑的有益功能效果可能通过EPO后的肺部流动增加而掩盖,导致PVR降低的肺动脉压不变。可能是,如本研究中所执行的,收缩性的测量不足以检测更细微的变化。
总之,在大鼠血流相关性肺动脉高压模型中,促红细胞生成素对心脏和肺血管重塑都有有益的作用。在目前的研究中,没有肺血流动力学的改善可以证明伴随组织病理学改变。本模型的分子研究表明,血管内皮生长因子及其两种受体亚型可能参与介导红细胞生成素的作用。这些数据为进一步深入研究促红细胞生成素在肺动脉高压中发挥有益作用的机制提供了依据。
- 收到了2007年3月26日。
- 公认2007年9月10日。
- ©ers Journals Ltd