摘要
慢性阻塞性肺疾病(COPD)的特征是实质区域的细胞外基质(ECM)破坏,而支气管壁显示纤维化。此外,还观察到广泛的炎症过程。CD8+ t细胞,位于整个肺,上皮细胞位于中央位置的气道,产生参与炎症过程的细胞因子。这些细胞因子可能影响目前的成纤维细胞,这是COPD中ECM修复和维持缺陷的关键影响因子。
目前的作者探讨了细胞因子微环境对对照(n = 6)的肺成纤维细胞中细胞 - 细胞相互作用基因表达的影响,以及慢性阻塞性肺病阶段II(n = 7)和阶段IV的全局促进程序(n = 7)COPD患者。目前的作者模拟了体内使用从COPD患者外周血中分离的CD3/CD28刺激的CD8+ t细胞上清,支气管上皮细胞系上清,或两者的结合。
目前的数据显示,慢性阻塞性肺疾病患者的成纤维细胞对细胞因子微环境的反应发生改变,这取决于疾病的阶段和肺的中心或外周位置。特别是黏附相关基因在慢性阻塞性肺疾病患者成纤维细胞中表达上调,提示成纤维细胞在慢性阻塞性肺疾病的炎症过程中发挥了更明显的作用,可能导致细胞外基质修复效应的功能降低。
大约有15-20%的吸烟者会患上慢性阻塞性肺病(COPD),其中包括慢性支气管炎和肺气肿1,2.肺气肿的特征在于慢性炎症,肺泡破坏和肺泡附着的丧失,导致空腹扩大和血褐色血管基的弹性反冲丧失,这导致气流限制1,3.,4. 到目前为止,香烟烟雾易感的潜在机制尚未阐明1,2,5,6.
本作者提出,除了氧化剂和抗氧化剂之间和蛋白酶和它们的抑制剂之间的普遍接受的不平衡,导致过量的组织破坏,一个阻碍组织修复过程参与肺气肿的发病机制7,8.通过产生细胞外基质(ECM)蛋白,ECM降解酶及其抑制剂,成纤维细胞对组织修复和调节很重要9目前的作者已经观察到,与对照组的成纤维细胞相比,重度COPD患者的肺成纤维细胞显示出改变的ECM生成谱,这表明成纤维细胞在COPD中观察到的缺陷ECM调节中起着重要作用8,10.- - - - - -12..
除了组织降解和破坏之外,慢性炎症过程是COPD的潜在,具有渗透炎性细胞,产生大量细胞因子3.,6,13.- - - - - -16..此外,香烟烟雾损害上皮细胞,细胞是生长因素的重要来源,如。转化生长因子(TGF)-β3..这种复杂的细胞因子微环境最有可能有助于COPD患者的肺成纤维细胞的行为改变。除了ECM生成,成纤维细胞可以是积极参与炎症过程通过细胞因子和趋化因子的产生以及与炎症细胞的直接相互作用7,17.,18..目前的作者假设,局部细胞因子微环境决定了ECM的产生和成纤维细胞促炎功能之间的平衡。
进行目前的研究以进一步探讨成纤维细胞在COPD中的作用,特别是研究患病肺复合细胞因子微环境对细胞对细胞相互作用和基质生产的影响。作为体内分析人肺成纤维细胞是不可能的,目前的作者设计了一个在体外利用受刺激的上皮细胞和CD8+ t细胞上清建立病变肺局部细胞因子微环境模型。细胞因子微环境复杂,由多种细胞因子和趋化因子组成。通过使用上清液,可以生成一个尽可能接近于体内情况。上皮细胞和CD8+T细胞是病变肺成纤维细胞微环境中细胞因子的主要来源19..因此,用从COPD患者外周血中分离的CD3/CD28刺激的CD8+ t细胞的上清或支气管上皮细胞系的上清或两者的组合处理成纤维细胞。采用cDNA- macro-filter array作为基因表达的初始探索方法,采用实时荧光定量PCR技术,比较了上清液对成纤维细胞相互作用及基质相关基因表达的影响。采用蛋白表达分析确定mRNA表达。研究了来自COPD患者(Global Initiative for Chronic Obstructive Lung Disease, GOLD) II/III期和IV期)和对照组患者的成纤维细胞。
材料和方法
学科
为了探讨mRNA表达,从20个个体获得肺组织。群体的临床特征列于表1中⇓.所有患者给出了知情同意书。COPD严重程度的分类基于2003年的金标准4,20..三组研究:1)GOLD期II/III期(n = 7);该组包括中度(GOLD II期,n = 5)和重度COPD (GOLD III期,n = 2)患者。2) GOLD阶段IV (n = 7);这一组包括非常严重的COPD患者。3)控制(n = 6);这组包括肺组织学正常的个体。患者没有α1抗胰蛋白酶缺乏症。肺气肿是指末梢细支气管远端气管腔的组织学异常增大,伴有肺泡壁的破坏,且无明显纤维化1,2,4,并由经验丰富的肺病理学家对肺组织进行常规组织学检查。
从接受肺癌患者的患者的非血液肺组织获得金阶段II / III组织。组织总是从肿瘤中尽可能远,或来自非血液的叶片。组织病理学上,存在顽育病变,但病变是有限的,但严重程度不同。组织病理学上适度的肺气肿,如可行的肺泡隔膜组织或分离的肺血管分离的横截面的分离的或未附加的段。
来自非常严重的COPD组(金阶段IV)的组织是从接受肺移植或肺部体积的肺部手术的患者获得的。切除的组织显示宏观和显微镜严重的肺气肿病变,通常伴有大疱。
对照组因技术或后期(单侧移植)原因而非用于移植的供体肺组织组成。技术原因与关于有关肺状况的可用接受者或怀疑的技术移植性有关。在后者的情况下,只有在额外的研究(包括组织病理学)之后仅包括肺组织,并且当它显示没有COPD的迹象1,或任何其他显着病理学。
肺成纤维细胞的分离与培养
肺成纤维细胞培养由肺实质组织通过外植技术建立如前所述11..用支原体检测试剂盒(Roche Diagnostics,Almere,Netherlands)证实了成纤维细胞培养物中的缺乏缺乏纤维细胞污染。通过特异性蛋白质的形态外观和表达模式表征分离的细胞作为成纤维细胞11..所有细胞表现出用于平节,纤连蛋白,成纤维细胞标记物脯氨酰-4-羟化酶的特征染色模式,并且缺乏针蛋白的免疫反应性。发现<5%的细胞对于Desmin和α-平滑肌细胞肌动蛋白是阳性的。
上清
上皮上清取自支气管上皮细胞系16HBE21.(来自D.C. Gruenert,佛蒙特大学,加利福尼亚太平洋医疗中心研究所,旧金山,加州,USA)的善意的礼物)。细胞系16HBE在完整的培养基中生长到汇合(Ham的F12媒体; Biowhittaker Cambrex,Verviers,比利时)补充有10%胎牛血清(FCS; PAA Laboratories,Linz,奥地利),2毫米l谷氨酰胺,100µg·L−1链霉素100 U·mL−1青霉素(Bio Whittaker公司Cambrex)中。After confluence, culture medium was replaced with medium containing 0.5% FCS for 24 h. This supernatant was harvested and stored at −80°C.
为了获得CD8 + T细胞的培养上清液,从7名COPD患者收集外周血。所有患者给出了知情同意书。获得肝素化血液并在Ficoll-Paque(Amersham Biosciences,乌普萨拉,瑞典)上分层。收集含有外周血单核细胞(PBMC)的界面。PBMCS重新悬浮在1×107细胞·ml.−1在Hank的平衡盐溶液/2%FCS中纯化CD8细胞。使用抗CD8磁珠和分离珠(Dynal,Wirral,UK)通过阳性选择分离CD8细胞。通过库尔特Epics ELITE(Beckman coulter,Hialeah,FL,USA)上的荧光激活细胞分选仪分析确定分离的CD8 T细胞的纯度使用CyQ标记的抗CD8、藻红蛋白标记的抗CD4和异硫氰酸荧光素标记的抗CD3抗体(英国牛津BD Bioscience)。CD8细胞纯度为87%,含有7%的CD4 T细胞。分离的CD8细胞在含有0.5%FCS的培养基中重新悬浮并培养24小时 h、 用含有5%抗CD3(克隆WT-32)和抗CD28抗体(克隆20–4996;荷兰阿姆斯特丹CLB Sanquin)的0.5%FCS培养基替换培养基,用抗CD3和抗CD28抗体刺激分离的CD8细胞24小时 h、 然后收集上清液,离心并储存在−80摄氏度。
成纤维细胞的cDNA阵列培养
来自融合培养的成纤维细胞在完全培养基中接种在培养板(Corning BV, Amsterdam, Netherlands)中,并生长到融合(第5代)。用含0.5% FCS的培养基替换培养基,培养24小时。介质替换为新的0.5% FCS介质,要么有或没有上层清液的16 hbe细胞线25稀释(1),上层清液的CD8细胞刺激anti-CD3和anti-CD28 10稀释(1)或16 hbe细胞的上清液和CD8细胞(1在25 - 1 10最终稀释浓度,分别)。最优的刺激浓度和持续时间是在初步实验中确定的(数据未显示)。6 h后,收集细胞进行RNA分离。
RNA的制备和cDNA阵列的杂交
用RNeasy迷你试剂盒(Qiagen, Hilden, Germany)分离成纤维细胞总RNA。在260 nm处用光密度测量法测定RNA的数量。每组收集3µg RNA。用DNase I处理总RNA,并在柱上运行以去除基因组DNA (Qiagen)。
Atlas细胞相互作用表达阵列(BD Biosciences Clontech,Palo Alto,CA,USA)用于确定使用16HBE细胞、CD8细胞或其组合的上清液治疗的三个患者组的成纤维细胞中265个已知基因表达模式的差异。Atlas表达阵列基于一种过滤阵列技术(宏阵列),该技术使用一种尼龙过滤器,该过滤器带有可与待分析样本的cDNA杂交的感兴趣基因的cDNA。总共2-5个 使用商业试剂盒(BD Biosciences)将µg总RNA用于cDNA合成。通过掺入[α]标记cDNA-32.P]脱氧胞苷三磷酸−1).当计数·min时,探针杂交−12 - 8×106,具有施用于用户手册(BD Biosciences)之后的CDNA阵列的ExpresshyB杂交溶液。将膜在室温下暴露于磷光起像筛网3天。使用磷定向系统(Molecular Dynamics,Sunnyvale,CA)进行结合cDNA的定量。
CDNA阵列数据分析
当前作者比较与16HBE细胞,CD8细胞,或组合的上清液,并在基础的培养条件培养后从三组成纤维细胞的基因表达模式,使用AtlasImage 2.0软件(BD Biosciences公司Clontech)中。为了减去共同方差和发现差异表达基因的新方法被设计基于该数据缩减工具“主成分分析”22.- - - - - -24..
简而言之,使用放置在列中的所有滤波器数据来制备矩阵。向每个值添加1以避免零值。采用自然对数根据以下公式提高正常性: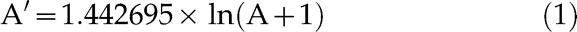
所有列都标准化为均值= 0和SD. = 1. Subsequently, the principal components were calculated and the first principal component was deducted from the data matrix. Of the remaining data, the inverse of the natural logarithm was taken. Ratios were determined and a gene expression ratio of at least a two-fold increase compared with basal culture conditions was considered relevant.
实时聚合酶链反应
为了获得更均匀的患者群,唯一的患者唯一的患者被除以PCR,随后用于可溶性细胞间粘附分子(SICAM)ELISA和免疫组化。为了验证阵列数据的结果,对阵列研究中使用的个体患者成纤维细胞样品上的ICAM-1 mRNA表达进行定量实时PCR分析。通过逆转录酶II(Invitrogen,Breda,Netherlands)将总共3个MRNA转录为cDNA。根据制造商的说明,在ABI7900HT测序仪上对ABI7900HT测序仪进行了测定,根据应用生物系统(福斯特城,USA)。通过Δct方法分析数据25..简而言之,对来自家庭基因的CT值(核糖体蛋白S9)校正感兴趣基因的CT值,导致ΔCT值。该ΔCt被标准化为基础对照组的平均ΔCt值。采集了数值,并计算刺激和基础条件之间的比率。从每个类别的个别患者中取代了中位数。
SICAM蛋白表达
在所有成纤维细胞样品中,收获上清液以确定通过成纤维细胞产生的SICAM水平。SICAM水平由商业SICAM ELISA套件(CLB / Sanquin,Amsterdam,荷兰)确定。简而言之,孔用捕获的SICAM抗体涂覆,随后与上清液样品一起孵育。孵育后,洗涤孔并与标记的抗菌抗体的过氧化物酶一起温育。使用3,3',5,5'-四甲基苯胺可视化染色。在标准的光谱仪上以450nm读取吸收。
免疫组织化学
免疫组化采用标准的两步免疫过氧化物酶方案,对3µm福尔马林固定、石蜡包埋的肺组织进行免疫组化。切片用一种识别ICAM-1的单克隆抗体孵育(来自澳大利亚墨尔本皇家墨尔本医院A.W. Boyd的善意礼物)26..Envision (Dakopatts, Glostrup, Denmark)与3,3'-二氨基联苯胺(Sigma, St. Louis, MO, USA)结合用于可视化抗体结合。在切片上对粘膜下层ICAM-1+细胞的数量进行半定量评分。(1: ICAM-1+细胞数量少,2:ICAM-1+细胞数量中等,3:ICAM-1+细胞数量大量)。
统计分析
使用Kruskall-Wallis检验由曼 - 惠特尼U检验三个研究组之间的学科特点不同,实时数据和免疫组织化学成绩进行了分析。使用Fisher精确检验在吸烟这三个研究组之间的生活习惯和性别差异进行了分析。意义的使用水平为0.05。所有报告的p值都是双侧的。
结果
患者团体
中度/重度和非常重度COPD受试者的吸烟史相似(表1)⇑).患有严重COPD的患者比中度COPD的患者显着小。来自当前研究的阶段II集团的材料主要由雄性,阶段IV组的材料主要由女性组成。从目前的作者的建立者中,无法获得每个COPD阶段在男性和女性中等的材料。对照组对来自COPD组的年龄或性别分布没有显着差异。来自拒绝供体肺的肺部材料用作对照组。可以获得施主的所有临床特征,可以在目前的研究的患者组中获得。然而,通过经验丰富的病理学家分析该材料并被分类为正常组织。
数组结果一般
在细胞相互作用阵列上差异地表达了265个基因中的总共51个。基因分为三组:参与粘附和迁移的基因,参与ECM生产或调制和参与细胞调节的基因的基因。总体而言,细胞相互作用基因在对照和阶段IV组中特别差异表达。阶段II / III组仅显示了基因表达谱的微小变化。
上皮上清刺激下基因表达
上皮上清刺激后,265个基因中有22个与基础培养条件下的成纤维细胞有差异表达(表2)⇓); 尤其是与粘附和调节有关的基因。上皮上清液主要影响对照成纤维细胞的基因表达,但对COPD成纤维细胞几乎没有任何影响。特别是一个基因的差异表达:ICAM-1表达下调(−对照组为4.4倍,相反,两个COPD组均上调(II/III期和IV期分别为4.5倍和5.7倍)。
CD8上清刺激后基因表达
共29个基因在CD8上清刺激下差异表达(表2)⇑),其中23个基因在GOLD IV期COPD患者组中差异表达,在GOLD II/III期和对照组中分别只有9个和3个基因表达。大多数受调控基因反映粘附过程和ECM物质。值得注意的是,ICAM-1表达在两个COPD组中均高度上调(在黄金II/III期和黄金IV期分别为10.2倍和9.5倍),而对照组未显示ICAM-1 mRNA表达的调节。
CD8与上皮上清液联合后的基因表达
在用CD8和上皮上清液组合刺激后,差异调节24个基因(表2⇑).与合并的上清液处理的对照成纤维细胞主要显示改变参与细胞调节过程的基因的表达。GOLD阶段的成纤维细胞的II / III的COPD患者显示最小变化在这些条件下,而GOLD阶段IV COPD组中,ICAM-1显示出mRNA表达高得惊人的增加(25.5倍)。
实时聚合酶链反应
阵列用于寻找最适合实时PCR进一步分析的基因的指示。经RT-PCR检测,ICAM-1表达变化最为显著。目前的作者发现,在上皮和CD8上清组合的影响下,GOLD期IV期成纤维细胞中ICAM-1的表达最高(图1)⇓).单独上皮上清液与GOLD阶段II和对照组相比,也显著升高GOLD IV期的ICAM-1基因的表达。的CD8上清液也引起了GOLD阶段IV组中的ICAM-1 mRNA表达的最高水平,但是这是不显著,由于与相对小数量的受试者在组合大量的患者的变化。
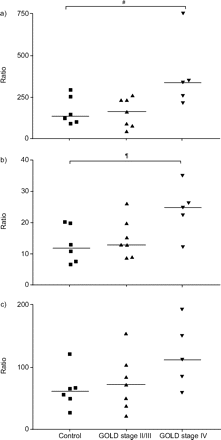
a)上皮细胞和CD8细胞,b)上皮细胞或c) CD8细胞的上清液刺激成纤维细胞实时细胞间粘附分子-1 mRNA的表达。与基础培养条件比较。GOLD:全球慢性阻塞性肺病倡议。——:中位数。#: p =−0.028;¶:p = -0.028。由于技术原因,一个金阶段IV样品丢失。
SICAM蛋白表达
为了验证mRNA的表达,使用sICAM ELISA检测所有成纤维细胞样本上清液中sICAM的水平。在基础条件下检测到非常小浓度的sICAM。在GOLD期IV成纤维细胞中,CD8和上皮上清联合刺激显示了sICAM水平升高的趋势(p = 0.055,图2)⇓).上皮细胞和CD8上清刺激本身并不影响中sICAM的蛋白水平。
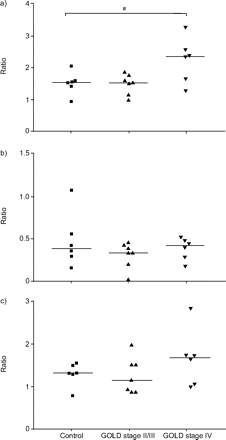
a)上皮细胞和CD8细胞,b)上皮细胞或c) CD8细胞上清刺激成纤维细胞的可溶性细胞间粘附分子-1蛋白表达。与基础培养条件比较。GOLD:全球慢性阻塞性肺病倡议。#:P = 0.055。
免疫组织化学
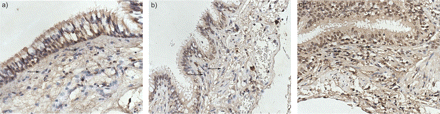
为了进一步验证金阶段IV成纤维细胞的高度升高的mRNA表达,还分析了阵列研究中使用的同一控制和COPD患者的同一控制和COPD患者组织切片中的ICAM-1蛋白表达。在粘膜下,其中大量成纤维细胞具有局部上皮和CD8导出因子的影响,在与对照组相比时,在黄金阶段IV COPD患者中发现了显着大量的ICAM-1 +细胞。金阶段II / III COPD患者(图3⇓).大多数阳性细胞为细长的成纤维细胞样细胞(图4)⇓).这支持了目前作者对GOLD期COPD成纤维细胞中ICAM-1 mRNA表达高表达的观察。
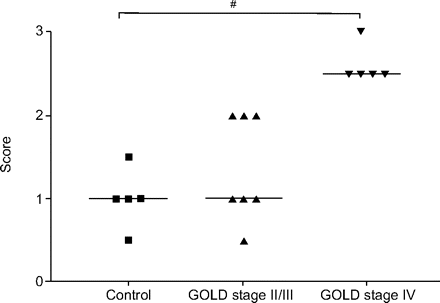
粘膜下层细胞间粘附分子(ICAM-1)+细胞数量半定量评分。在全球慢性阻塞性肺疾病倡议(GOLD) IV期慢性阻塞性肺疾病中,ICAM-1+细胞的相对频率显著增加。
细胞间粘附分子(ICAM)-1染色(棕色)在a)对照组,b)全球慢性阻塞性肺疾病(GOLD) II期COPD和c) GOLD期COPD受试者的肺组织中。在对照组和GOLD II期COPD中,在黏膜下层观察到非常少的ICAM-1+细胞。箭头示粘膜下层ICAM-1阴性纤维母细胞。GOLD期COPD中可见大量的ICAM-1+细胞。箭头表示ICAM-1+延长成纤维细胞。用苏木精对细胞进行反染色。
讨论
已知吸烟可诱导COPD患者气道壁CD8+ t细胞内流和上皮细胞活化。本文作者探索了CD8+ t细胞和上皮细胞来源的介质对GOLD II/III期和IV期以及对照组成纤维细胞基因表达谱的调节作用。目前的作者清楚地证实,与对照组相比,细胞因子微环境在COPD患者中不同程度地调节肺成纤维细胞基因表达。特别是,当成纤维细胞暴露于CD8和上皮上清液的组合时,粘附相关基因的表达有差异,相互作用很明显。因此,成纤维细胞微环境中的因素可能有助于COPD中观察到的成纤维细胞行为的改变。由于成纤维细胞是ECM调节的必要细胞,其行为的改变可能反映COPD中观察到的ECM修复缺陷的潜在原因。
目前的实验与尽可能与实际肺部微环境密切相关,但它们仍然代表一个在体外模型体内情况。上清液的使用代表了不确定性和变化的来源,但是使用单个细胞因子的组合的替代方案将导致选择偏差。将CD8 + T细胞从COPD患者的外周血中使用,作为患病肺中CD8 T细胞的代表。使用初级上皮细胞系,因为不可能获得来自同一患者的初级上皮细胞和成纤维细胞的充分培养物。目前模型是反映COPD中微环境的适当模型,以研究衍生自CD8 T细胞和成纤维细胞上皮细胞的介质的作用。
ICAM-1在COPD和对照组之间显示了显著的差异基因表达模式,这是由COPD患者肺组织中sICAM的生成升高和表达升高所支持的。在这些阵列中,在GOLD期IV成纤维细胞中,上皮和CD8上清组合的差异表达最大。实时PCR结果证实了这一观察结果,同时发现与对照和GOLD II/III期成纤维细胞相比,GOLD IV期成纤维细胞产生的sICAM-1有一个近乎显著的趋势(p = 0.055)。此外,GOLD期IV期COPD患者小气道黏膜底层ICAM-1+细胞数量最多(p = 0.0079),主要为成纤维细胞,预计会受到CD8细胞和上皮细胞的影响。虽然上皮细胞上清和CD8细胞上清对ICAM基因表达的影响似乎在宏阵列中存在,但这不能用RT-PCR来证实。
ICAM-1是一种重要的粘附分子,参与了许多炎症过程,如中性粒细胞和淋巴细胞运输,并在抗原呈递中作为辅助分子27..ICAM-1表达受各种细胞因子调节,如。白细胞介素(IL)-1,IL-4,干扰素γ,TGF-β,肿瘤坏死因子(TNF)-α27.,28..已知在COPD患者中升高的CD8 + T细胞是IL-4和TNF-α的重要来源,而上皮细胞是TGF-β的重要来源。因此,这些细胞因子可以是上清液的关键元件,解释了升高的ICAM-1表达。
几项研究指出了ICAM-1表达在COPD发病机制中的作用。COPD患者的支气管肺泡灌洗中的ICAM-1浓度增加,香烟烟雾提取物增加了巨噬细胞的ICAM-1生产29.,30.. 此外,戒烟后血浆ICAM-1浓度显著下降31..最后,成纤维细胞能够与炎症细胞相互作用通过粘合分子,如ICAM-1和血管细胞粘附分子-128.并且增加的ICAM-1表达与沿成纤维细胞的白细胞迁移相关32..因此,COPD患者成纤维细胞中ICAM-1表达的增加可能表明了与炎症细胞的重要相互作用。众所周知,吸烟COPD患者的整个肺中CD8+ t淋巴细胞的数量增加13.,16.,33.- - - - - -35.,而上皮细胞覆盖更多位于位于位于距离的航空公司。由CD8 + T细胞和上皮细胞产生的细胞因子是COPD中的已知成纤维细胞活性的调节剂2,13.,36.,37..本作者使用刺激的CD8 + T细胞和上皮细胞的上皮细胞来产生在体外模型反映了体内肺成纤维细胞的情况。目前研究的一个重要的方面是,CD8 + T细胞,COPD患者没有慢性支气管炎的外周血中分离出的上清液中所使用的,作为COPD患者的CD8 + T细胞已经显示出具有改变的细胞因子产生特征15.,35..因此,位于中心(支气管)的成纤维细胞受到上皮细胞和cd8源性因子的调节,而位于较远(实质)的成纤维细胞受到支气管上皮细胞源性因子的调节较少。在支气管区域的特定微环境中,两种介质都存在,上皮细胞和CD8+ t细胞介质之间的平衡可能最终决定COPD患者成纤维细胞基因表达的影响。
成纤维细胞是多能细胞,其活性和功能可根据局部环境因素进行调节。成纤维细胞的一个主要特征是产生ECM成分,这部分是由TGF-β刺激引起的。成纤维细胞也参与免疫过程,在从急性、解决炎症到慢性持续性炎症的转变中发挥重要作用17.,18..巴克利et al。18.提示这种慢性炎症的发生是因为成纤维细胞行为紊乱,导致白细胞在炎症组织中不适当的存活和保留38..因此,在局部细胞因子微环境的影响下,COPD组织中的成纤维细胞表现出功能改变的行为就不足为奇了11.,18.CD8上清液刺激的金IV期COPD成纤维细胞中发现的差异表达的粘附相关基因支持了成纤维细胞在COPD慢性炎症过程中显著作用的理论。
除了ICAM-1的强表达外,其他几个粘附相关基因也被显示上调。因此,似乎COPD成纤维细胞,特别是GOLD期COPD,很容易被局部细胞因子微环境诱导与炎症细胞相互作用,从而在持续的炎症中发挥支持作用。分化为更具有免疫学功能的成纤维细胞可能不能完全维持ECM,或者可能表现出改变的ECM修复机制。这些功能改变可能导致ECM的破坏或维持不足,导致COPD的一些特定特征。目前的作者已经证实了GOLD期IV期COPD患者肺组织中decorin和biglycan免疫组织学染色降低,表明ECM调节改变10..
综上所述,慢性阻塞性肺疾病患者的成纤维细胞对慢性阻塞性肺病变肺中细胞因子微环境的反应发生改变,这取决于疾病的分期和肺中的中心或外周位置。局部细胞因子微环境似乎使慢性阻塞性肺疾病成纤维细胞与炎症细胞相互作用,而不是关注细胞外基质的维持,这可能是慢性阻塞性肺疾病发病机制的关键。此外,目前的研究结果表明,组织修复机制在实质中是不同的与慢性阻塞性肺疾病的支气管壁。
致谢
作者要感谢T.R. Bai仔细阅读手稿,G. te Meerman设计了主成分分析工具,D.C. Gruenert提供了16HBE支气管上皮细胞系,J. Liesker提供了特征明确的慢性阻塞性肺疾病患者的血液样本。
- 收到了2005年10月5日。
- 接受2006年3月21日。
- ©ers Journals Ltd