摘要gydF4y2Ba
在慢性阻塞性肺疾病(COPD)中,全身炎症的存在与周围肌肉异常和体重减轻有关。gydF4y2Ba
为了研究炎症因子在这些过程中是否重要,本研究比较了15例患者(一秒钟用力呼气量43±11%)和14例对照组骨骼肌中亚硝酸盐、硝酸盐、硝基酪氨酸、神经元、内皮和诱导型一氧化氮合酶(分别为nNOS、eNOS和iNOS)和炎症标志物(肿瘤坏死因子(TNF)-α、CD154和CD163)的水平。所有这些指标也在正常体重和低体重患者之间进行了比较。gydF4y2Ba
亚硝酸盐(12.5±2.6gydF4y2Ba与gydF4y2Ba17.0±3.4μ摩尔·毫克gydF4y2Ba−1gydF4y2Ba蛋白质),硝酸盐(20.7±2.4gydF4y2Ba与gydF4y2Ba24.4±4.5μ摩尔·毫克gydF4y2Ba−1gydF4y2BaeNOS(31.9±4.6gydF4y2Ba与gydF4y2Ba43.6±7.5 ng·毫克gydF4y2Ba−1gydF4y2Ba蛋白质)低于对照组。硝基酪氨酸(25.6±5.4gydF4y2Ba与gydF4y2Ba6.6±3.3 ng·毫克gydF4y2Ba−1gydF4y2Ba蛋白),iNOS表达(32±9.5)gydF4y2Ba与gydF4y2Ba7.16±2.7 ng·毫克gydF4y2Ba−1gydF4y2BaTNF-α(257±160)gydF4y2Ba与gydF4y2Ba48.3±4.4 pg·毫克gydF4y2Ba−1gydF4y2BaCD163(6.4±2.1)gydF4y2Ba与gydF4y2Ba0.8±0.4 ng·毫克gydF4y2Ba−1gydF4y2Ba蛋白质)在COPD患者中高于对照组。CD154水平为15.7±7.0 ng·mggydF4y2Ba−1gydF4y2Ba而在对照组中检测不到。在体重正常和体重较低的COPD患者中,所有这些标志物的水平相似。gydF4y2Ba
总之,这些发现提示慢性阻塞性肺疾病患者的肌肉组织中存在炎症过程,并支持其参与骨骼肌异常的发病机制。gydF4y2Ba
慢性阻塞性肺疾病(COPD)是一种与显著的肺外表现相关的肺部疾病,包括周围肌肉功能障碍和原因不明的体重减轻gydF4y2Ba1gydF4y2Ba–gydF4y2Ba4gydF4y2Ba。慢性阻塞性肺病的炎症主要影响气道和肺实质,但它也可能在该疾病的全身后果中发挥作用gydF4y2Ba4gydF4y2Ba–gydF4y2Ba8gydF4y2Ba。gydF4y2Ba
尽管外周肌肉功能障碍和体重减轻可能是COPD最广泛的全身效应,但对其发生的机制仍知之甚少。它们的起源可能是多因素的,但有强有力的证据表明与全身炎症有关gydF4y2Ba4gydF4y2Ba–gydF4y2Ba8gydF4y2Ba。gydF4y2Ba
在外周组织中,一氧化氮(NO)是由至少三种不同的一氧化氮合酶(NOS)酶促生成的gydF4y2BalgydF4y2Ba精氨酸。内皮构成性NOS (eNOS)形成的NO负责维持低血管张力,防止白细胞和血小板粘附在血管壁上,而神经元构成性NOS (nNOS)形成的NO则起神经调节剂或神经介质的作用。诱导异构体(iNOS)通过炎症刺激物的激活产生1000倍以上的NO,这介导了防御和病理过程。gydF4y2Ba
同时释放超氧阴离子(OgydF4y2Ba2gydF4y2Ba−gydF4y2Ba), NO的过量生成可形成过氧亚硝酸盐(ONOO-),从而导致NO的细胞毒性作用。由于ONOO-是一种短暂的物种,其生物半衰期甚至比自由基NO还要短,因此无法直接测量,必须通过间接方法来推断其存在。其中之一是硝基酪氨酸的存在和水平,这是一种由蛋白质酪氨酸残基硝化形成的产物。硝基酪氨酸的形成引起了相当大的兴趣,因为:1)它可以改变蛋白质的功能;2)与急性和慢性疾病状态相关;3)被认为是ONOO引起的疾病的重要指标gydF4y2Ba−gydF4y2Ba依赖性组织损伤gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba。gydF4y2Ba
最近的两项研究评估了iNOS在COPD患者骨骼肌中的表达gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba。巴雷罗gydF4y2Ba等gydF4y2Ba。gydF4y2Ba6gydF4y2Ba无法在中度COPD患者的骨骼肌中检测到iNOS。相反,AgustÍgydF4y2Ba等gydF4y2Ba。gydF4y2Ba7gydF4y2Ba核因子(NF)-κB活化和iNOS诱导在重度COPD患者骨骼肌中发生,尤其是在体重较轻的患者中。虽然NO的异常调节可能导致COPD患者的肌肉改变,但这些患者周围肌肉中NO的产生和炎症的作用尚不清楚。gydF4y2Ba
本研究的目的是横断面调查炎症标志物(肿瘤坏死因子(TNF)-α, CD154和CD163)的存在,以及NOS和NO最终产物(亚硝酸盐(NO)的浓度gydF4y2Ba2gydF4y2Ba−gydF4y2Ba)、硝酸盐(NOgydF4y2Ba3.gydF4y2Ba−gydF4y2Ba)和硝基酪氨酸)在慢性阻塞性肺病患者的骨骼肌中。应用免疫组织化学技术(CD68)和电镜观察部分患者肌肉切片中可能存在的炎症细胞。还比较了正常体重和低体重COPD患者的酶、NO终产物和炎症介质,以确定炎症和原因不明的体重减轻之间的潜在联系。gydF4y2Ba
方法gydF4y2Ba
研究对象gydF4y2Ba
研究组包括15名(8名男性和7名女性)临床稳定的COPD前吸烟者(64±8岁),从加拉加斯大学医院(加拉加斯,委内瑞拉)的肺部诊所招募。总共有14名(6名男性,8名女性)健康的久坐不吸烟受试者(59±8岁)作为对照。人体研究委员会(委内瑞拉加拉加斯大学医院)批准了这项研究,所有受试者都签署了知情同意书。gydF4y2Ba
COPD定义为支气管扩张剂后一秒用力呼气量/用力肺活量(FEV)gydF4y2Ba1gydF4y2Ba/ FVC) < 0.7gydF4y2Ba11gydF4y2Ba以及吸烟20包的历史。患者在进入研究前6周处于临床稳定状态,定义为无慢性阻塞性肺病急性加重,并且正在接受最佳的药物治疗,不定期使用全身皮质类固醇。有FEV可逆性的患者被排除在外gydF4y2Ba1gydF4y2Ba支气管扩张剂>12%和200 mL后。患有充血性心力衰竭、肿瘤和代谢性疾病的患者以及定期运动训练的患者也被排除在外。对照组的受试者过着久坐不动的生活方式,不进行定期锻炼。gydF4y2Ba
为了确定低体重COPD患者骨骼肌中是否存在NO终产物和炎症标志物,根据体重指数(BMI)将患者分为两组。低体重定义为BMI≤21 kg·mgydF4y2Ba−2gydF4y2Ba。gydF4y2Ba
肺功能试验和增量运动试验gydF4y2Ba
FEVgydF4y2Ba1gydF4y2Ba、FVC和FEVgydF4y2Ba1gydF4y2Ba/FVC根据美国胸科学会的建议计算gydF4y2Ba12gydF4y2Ba。肺测量正常值取自标准参考源gydF4y2Ba13gydF4y2Ba。gydF4y2Ba
在循环测功仪上进行运动测试(CardiO2 System;MedGraphics Corporation, St Paul, MN, USA),使用标准的1分钟增量周期运动方案gydF4y2Ba14gydF4y2Ba。患者开始以60次/分钟的速度进行2分钟的空载蹬车gydF4y2Ba−1gydF4y2Ba,其次是15瓦增量·mingydF4y2Ba−1gydF4y2Ba。强烈鼓励患者骑行,直到出现不适或疲惫(症状受限运动测试)。使用呼吸记录仪测量微小通气及其组成部分。过期O的浓度gydF4y2Ba2gydF4y2Ba和有限公司gydF4y2Ba2gydF4y2Ba用氧化锆细胞OgydF4y2Ba2gydF4y2Ba分析仪和红外COgydF4y2Ba2gydF4y2Ba分别分析器。心率储备由获得的最大心率和最大预测心率(HRmax = 220-age)确定。预计最大耗氧量(gydF4y2BaV 'gydF4y2BaOgydF4y2Ba2gydF4y2Bamax)是根据Jones和Campbell计算的gydF4y2Ba15gydF4y2Ba。在12秒内直接测定最大自主通气。gydF4y2Ba
肌肉活检gydF4y2Ba
在局部麻醉和消毒条件下,使用Bergström针从股四头肌股外侧肌取肌肉活检。肌肉样本被分成三部分。一组经处理后用于超微结构分析,一组经异戊烷冷冻后液氮冷却用于免疫组化,另一组直接液氮冷冻用于细胞因子、NO产物和酶的测定。gydF4y2Ba
NO评估gydF4y2Ba2gydF4y2Ba−gydF4y2Ba也没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba
冷冻肌肉样本称重,用手工制作的玻璃杵(Krogh研究所,哥本哈根,丹麦)与1 mL缓冲液(Tris-HCl 10 mmol·L)均质组织gydF4y2Ba−1gydF4y2Ba, pH 7.5), NaCl (150 mmol·LgydF4y2Ba−1gydF4y2Ba), EDTA (5 mmol·LgydF4y2Ba−1gydF4y2Ba)、triton x-100 (1% (v/v))、leupeptin (10 μg·Ml)gydF4y2Ba−1gydF4y2Ba),抑肽酶(10 μg·mLgydF4y2Ba−1gydF4y2Ba)和蛋白酶抑素(2.5 g·mLgydF4y2Ba−1gydF4y2Ba)。匀浆后的组织以90倍离心gydF4y2BaggydF4y2Ba5分钟。上清液用于其余的测定。使用BCA蛋白检测试剂盒(Pierce Biochemicals, Rockfort, IL, USA)评估蛋白浓度。gydF4y2Ba
NO的水平是间接确定的定量氧化产物的降解(NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba也没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba),使用硝酸还原酶和Griess试剂gydF4y2Ba16gydF4y2Ba照摩西之法gydF4y2Ba等gydF4y2Ba。gydF4y2Ba17gydF4y2Ba。简单地说,均质组织的上清液用蒸馏水稀释四倍并用硝酸还原酶孵育gydF4y2Ba曲霉属真菌gydF4y2Ba为了量化一氧化氮产物的总量(NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba+没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba)。在没有酶的情况下,只有NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba测定了浓度。在酶及其辅助因子NADPH和FADH存在的37°C下孵育30分钟后gydF4y2Ba2gydF4y2Ba,与丙酮酸钠和乳酸脱氢酶孵育10分钟,以降解过量的NADPH。用硫酸锌脱蛋白,取100 μL上清液与100 μL Griess试剂混合。将硝酸钠溶解在水中或正常血清池中,得到标准曲线。无gydF4y2Ba2gydF4y2Ba−gydF4y2Ba在540 nm处使用ELISA平板阅读器(MCC/340;Labsystems Multiscan,赫尔辛基,芬兰)。gydF4y2Ba
ELISA法测定NOS、硝基酪氨酸、CD163、CD154gydF4y2Ba
采用夹心ELISA法检测eNOS、nNOS和iNOS。首先,根据制造商的说明,使用从研发系统(Minneapolis, MN, USA)购买的商业试剂盒检测eNOS (NOS3)。灵敏度为25 pg·mLgydF4y2Ba−1gydF4y2Ba。其次,如前所述,使用标准的ELISA夹心技术评估nNOS (NOS1)和iNOS (NOS2)gydF4y2Ba18gydF4y2Ba。用于nNOS检测的单克隆抗体和多克隆抗体购自BD Biosciences (San Diego, CA, USA),用于标准曲线的重组酶购自Calbiochem (San Diego, CA, USA)。使用从Serotec (Kidlington, Oxford, UK)购买的一对抗体评估iNOS。两种方法的灵敏度均为25 pg·mLgydF4y2Ba−1gydF4y2Ba
如前所述,用ELISA法测定硝基酪氨酸的总量gydF4y2Ba18gydF4y2Ba。小鼠免疫球蛋白(Ig)-G单克隆抗体、抗硝基酪氨酸多克隆抗体和山羊抗兔igg -过氧化物酶多克隆抗体购自Upstate Biotechnology (Lake Placid, NY, USA)。使用已知化学修饰牛血清白蛋白中硝基酪氨酸浓度的标准曲线进行硝基酪氨酸的定量。灵敏度为50 pg·mLgydF4y2Ba−1gydF4y2Ba。gydF4y2Ba
如Sulahian所述,采用夹心ELISA法测定CD163gydF4y2Ba等gydF4y2Ba。gydF4y2Ba19gydF4y2Ba,只做了一些小改动。简单地说,一个单克隆抗cd163(克隆ED-Hu1;用Serotec)捕获CD163,用生物素化克隆RM3/1检测分子。均匀化的肌肉样本在蒸馏水中稀释1:10,然后加入到培养皿中并孵育过夜。其余的程序按照苏拉希安的描述进行gydF4y2Ba等gydF4y2Ba。gydF4y2Ba19gydF4y2Ba。但是,CD163是从phormol myrystate acetate活化的单核细胞的上清中,用单克隆克隆ED-Hu1亲和层析纯化而来,用纯化后的蛋白做标准曲线。纯化CD163的检出限为100-10,000 pg。特异性在检测前通过均质肌肉组织中CD163的免疫沉淀得到证实。gydF4y2Ba
CD154水平由购买自Chemicon公司(Temécula, CA, USA)的商业夹心免疫酶法检测。唯一的修改是样品在4°C下孵育18小时。定量分析采用标准曲线。检出限为每毫克蛋白质1 ng CD154。gydF4y2Ba
TNF-α的评估gydF4y2Ba
使用第三代TNF-α量化因子测定法(研发系统)按照制造商的说明进行TNF-α评估,除了按照建议对血清样品进行稀释并孵育18小时而不是3小时。灵敏度为0.5 ~ 3 pg·mLgydF4y2Ba−1gydF4y2Ba。gydF4y2Ba
免疫组织化学分析gydF4y2Ba
为了证明肌肉切片中白细胞的存在,对4例患者和4例对照组的样本进行了免疫组织化学分析。Anti-CD68,克隆MB11 (Dako, Carpintería, CA, USA)按制造商描述使用。使用Vecstain ABC Elite化学试剂进行快速染色(Vector Laboratories, Burlingame, CA, USA),使用厂家说明。gydF4y2Ba
超微结构分析gydF4y2Ba
部分肌肉样本固定在3%戊二醛磷酸盐缓冲液中,pH为7.4,mOsmol为320,后固定在1% OsO中gydF4y2Ba4gydF4y2Ba并嵌入到epon中。切片用金刚石刀在Porter-Blum MT2超微切片仪中切割,并用乙酸铀酰和柠檬酸铅染色。在日立H-500型透射电子显微镜下,在100kv加速电压下观察。gydF4y2Ba
统计分析gydF4y2Ba
数据以均数±表示gydF4y2BasdgydF4y2Ba。采用非参数Mann-Whitney u检验比较COPD患者和对照组之间NO终产物、酶、白细胞和炎症标志物的水平。所有这些指标也在正常体重和低体重COPD患者之间进行了比较。检验的可接受的统计显著性水平是概率值≤0.05。gydF4y2Ba
结果gydF4y2Ba
患者和对照组的临床特征和肺活量数据的平均值见表1gydF4y2Ba⇓gydF4y2Ba。患者与对照组在年龄、体重或身高方面没有差异。然而,COPD患者的BMI明显低于对照组。正如预期的那样,COPD患者的静息肺功能值低于对照组,患者表现出严重的气流阻塞。gydF4y2Ba
慢性阻塞性肺疾病(COPD)患者和对照组的人体测量和肺活量数据gydF4y2Ba
运动测试中测量的生理变量峰值见表2gydF4y2Ba⇓gydF4y2Ba。患者运动能力和功能能力下降。因此,平均值gydF4y2BaV 'gydF4y2BaOgydF4y2Ba2gydF4y2Ba·公斤·敏gydF4y2Ba−1gydF4y2Ba在所有患者中,将他们归为中度至重度运动限制的功能损害类(gydF4y2BaV 'gydF4y2BaOgydF4y2Ba2gydF4y2Ba10到16毫升·公斤gydF4y2Ba−1gydF4y2Ba·敏gydF4y2Ba−1gydF4y2Ba)。患者还出现呼吸储备减少和O异常gydF4y2Ba2gydF4y2Ba交货指数(OgydF4y2Ba2gydF4y2Ba脉冲)。gydF4y2Ba
运动测试数据gydF4y2Ba
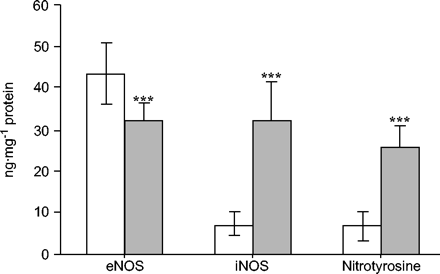
骨骼肌NO最终产物(NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba和硝基酪氨酸)、iNOS、eNOS、TNF-α和CD163见图1gydF4y2Ba⇓gydF4y2Ba–gydF4y2Ba⇓gydF4y2Ba⇓gydF4y2Ba4gydF4y2Ba⇓gydF4y2Ba。无gydF4y2Ba2gydF4y2Ba−gydF4y2Ba,没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba与对照组相比,COPD患者的eNOS表达水平显著降低(图2)。1gydF4y2Ba⇓gydF4y2Ba和2gydF4y2Ba⇓gydF4y2Ba)。COPD患者的nNOS也低于对照组(92.3±21.4和134.6±35.6 ng·mg)gydF4y2Ba−1gydF4y2Ba蛋白质,分别;p < 0.01)。相反,COPD患者骨骼肌亚硝基酪氨酸、iNOS表达、TNF-α和CD163水平明显高于健康受试者(图2)gydF4y2Ba⇓gydF4y2Ba–gydF4y2Ba⇓gydF4y2Ba4gydF4y2Ba⇓gydF4y2Ba)。CD154仅在COPD患者匀浆中观察到(15.7±7.0 ng·mg)gydF4y2Ba−1gydF4y2Ba蛋白质),但在对照组中没有,这低于方法的敏感性(<1 ng·mggydF4y2Ba−1gydF4y2Ba蛋白质)。gydF4y2Ba
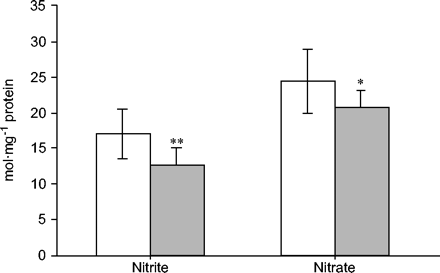
慢性阻塞性肺疾病患者的亚硝酸盐及硝酸盐水平(gydF4y2Ba )和对照对象(□)。*: p < 0.05;* *: p < 0.01。gydF4y2Ba
)和对照对象(□)。*: p < 0.05;* *: p < 0.01。gydF4y2Ba
慢性阻塞性肺疾病患者内皮型一氧化氮合酶(eNOS)、诱导型异构体一氧化氮合酶(iNOS)及亚硝基酪氨酸水平(gydF4y2Ba )和对照对象(□)。* * *: p < 0.001。gydF4y2Ba
)和对照对象(□)。* * *: p < 0.001。gydF4y2Ba
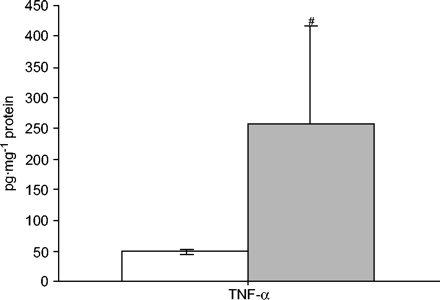
慢性阻塞性肺疾病患者肿瘤坏死因子(TNF -α)水平(gydF4y2Ba )和对照对象(□)。gydF4y2Ba#gydF4y2Ba: p < 0.0001。gydF4y2Ba
)和对照对象(□)。gydF4y2Ba#gydF4y2Ba: p < 0.0001。gydF4y2Ba
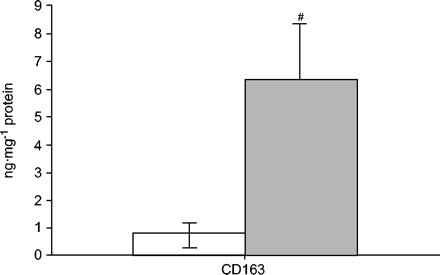
慢性阻塞性肺疾病患者CD163水平(gydF4y2Ba )和对照对象(□)。gydF4y2Ba#gydF4y2Ba: p < 0.0001。gydF4y2Ba
)和对照对象(□)。gydF4y2Ba#gydF4y2Ba: p < 0.0001。gydF4y2Ba
BMI正常和低BMI的COPD患者的特征见表3gydF4y2Ba⇓gydF4y2Ba。正如预期的那样,低BMI组的体重和BMI较低。与体重指数正常的COPD患者相比,他们的身高也较低。两组患者的气流阻塞程度相似。gydF4y2Ba
低体重和正常体重慢性阻塞性肺疾病(COPD)的人体测量和肺功能数据gydF4y2Ba
如表4所示gydF4y2Ba⇓gydF4y2Ba,骨骼肌NO相似gydF4y2Ba2gydF4y2Ba−gydF4y2Ba,没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba观察两组COPD患者中硝基酪氨酸、iNOS、eNOS、nNOS、TNF-α、CD154、CD163水平。gydF4y2Ba
低体重和正常体重慢性阻塞性肺疾病(COPD)患者骨骼肌炎症标志物水平gydF4y2Ba
肌肉组织免疫组化分析显示,患者浸润白细胞数量明显高于健康人(296±98细胞·mm)gydF4y2Ba−3gydF4y2Ba与gydF4y2Ba6±3细胞·毫米gydF4y2Ba−3gydF4y2Ba分别;p < 0.05)。图5显示了COPD肌肉中浸润白细胞的代表性图片gydF4y2Ba⇓gydF4y2Ba。gydF4y2Ba

股四头肌股外侧肌横切面。抗cd68免疫组化反应,克隆MB11。a)对照对象,男性,68岁。黑点是肌肉纤维和内皮细胞核。b)慢性阻塞性肺病患者,男性,68岁。黑色染色代表巨噬细胞浸润。比例尺= 50 μm。gydF4y2Ba
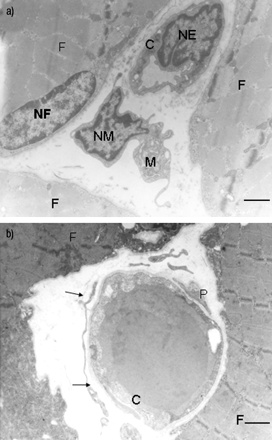
所有COPD患者的肌肉超微结构分析均显示细胞间隙存在巨噬细胞。巨噬细胞经常在毛细血管周围出现细胞质延长(图6)gydF4y2Ba⇓gydF4y2Ba)。gydF4y2Ba
a) 70岁女性慢性阻塞性肺疾病(COPD)患者股四头肌股外侧部分斜切面。b) 69岁女性COPD患者股四头肌股外侧纵切面。箭头显示毛细血管周围巨噬细胞的延长。M:巨噬细胞;NM:巨噬细胞核;F:肌肉纤维;NF:肌纤维核;C:毛细管;NE:毛细血管内皮细胞核;周皮细胞。 Scale bars = 1 μm.
讨论gydF4y2Ba
几项研究报告了不同疾病(包括COPD)患者骨骼肌炎症标志物的增加gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba–gydF4y2Ba23gydF4y2Ba。本研究的结果通过评估COPD患者骨骼肌活检中几种炎症和亚硝化应激标志物以及炎症细胞的存在,扩展了这一观察。gydF4y2Ba
目前作者观察到骨骼肌亚硝基酪氨酸和iNOS的表达水平明显较高,而NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba也没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba与健康受试者相比,COPD患者的水平有所降低。硝基酪氨酸含量的增加说明产生的NO大部分可能与O发生反应gydF4y2Ba2gydF4y2Ba−gydF4y2Ba生成ONOOgydF4y2Ba−gydF4y2Ba而不是NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba也没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba。iNOS产生NO的动力学与eNOS或nNOS产生NO的动力学有很大不同。可诱导的NOS以持续的方式产生大量有毒的NO,而组成型NOS异构体在几秒钟内产生NO,其活性是直接和短效的。NO所遵循的途径部分取决于O的局部有效性gydF4y2Ba2gydF4y2Ba−gydF4y2Ba阿,gydF4y2Ba2gydF4y2Ba和水gydF4y2Ba24gydF4y2Ba。在炎症反应过程中,iNOS形成的NO大量超过NO的生理量,通常由nNOS或eNOS产生。骨髓细胞中大量的炎性NO通常与大量的O同时产生gydF4y2Ba2gydF4y2Ba−gydF4y2Ba。这两者可以形成ONOOgydF4y2Ba−gydF4y2Ba它介导NO的细胞毒性作用,并产生酪氨酸硝化。除了iNOS的表达外,还有其他机制可以最终解释硝基酪氨酸水平的升高和NO的降低gydF4y2Ba2gydF4y2Ba−gydF4y2Ba也没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba这些病人骨骼肌的水平。除了ONOOgydF4y2Ba−gydF4y2Ba途径中,活化的白细胞可通过次氯酸+ NO生成硝基酪氨酸gydF4y2Ba2gydF4y2Ba−gydF4y2Ba,以及一种涉及髓过氧化物酶NO的不依赖氯的机制gydF4y2Ba2gydF4y2Ba−gydF4y2Ba和过氧化氢。没有gydF4y2Ba2gydF4y2Ba−gydF4y2Ba利用作为底物催化蛋白质中的酪氨酸硝化,最终可以解释NO水平的降低gydF4y2Ba2gydF4y2Ba−gydF4y2Ba9gydF4y2Ba,gydF4y2Ba25gydF4y2Ba,gydF4y2Ba26gydF4y2Ba。目前的结果强调需要更好地确定为什么COPD患者骨骼肌中存在的NO增加会导致蛋白质亚硝基酪氨酸化,而不是产生NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba也没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba。更好地理解这一现象可以为干预和调节这一潜在的破坏性途径开辟途径。gydF4y2Ba
骨骼肌活检样本中有肌纤维、结缔组织、微血管和神经纤维。eNOS和iNOS存在于内皮细胞和肌肉纤维中,而nNOS存在于神经和肌肉中,因此无法区分所测酶的来源。检测到的eNOS可能部分来自毛细血管内皮,本研究中发现的eNOS水平较低可能与这些患者骨骼肌中报道的毛细血管数量减少有关gydF4y2Ba1gydF4y2Ba。nNOS起源于肌纤维,COPD患者骨骼肌中nNOS的减少可能与这些患者中纤维类型分布异常有关gydF4y2Ba1gydF4y2Ba。相反,目前的作者假设,iNOS主要是在巨噬细胞中诱导的,因为在这些患者的肌肉样本中检测到CD163水平的升高和这些细胞数量的增加。gydF4y2Ba
目前的结果部分地与巴雷罗报告的结果相反gydF4y2Ba等gydF4y2Ba。gydF4y2Ba6gydF4y2Ba。他们既没有检测到COPD患者和对照组骨骼肌中iNOS的表达,也没有观察到患者和对照组之间eNOS和nNOS水平的差异。然而,与这些作者一致的是,在患者的骨骼肌中发现硝基酪氨酸水平升高。目前的发现与巴雷罗的发现之间的差异gydF4y2Ba等gydF4y2Ba。gydF4y2Ba6gydF4y2Ba这可能是两项研究中用于测定NOS异构体的不同技术造成的。在目前的研究中使用了定量方法(ELISA测定),而他们使用了半定量测定。另一个可能解释结果差异的因素是两组患者气流阻塞的严重程度。他们评估了患有轻中度COPD (FEV)的患者gydF4y2Ba1gydF4y2Ba54±14%,FEVgydF4y2Ba1gydF4y2Ba/FVC 61±7%),而目前的作者纳入了更严重的气流阻塞(FEVgydF4y2Ba1gydF4y2Ba43±11%和FEVgydF4y2Ba1gydF4y2Ba/ FVC 46±6%)。他们报告了硝基酪氨酸水平与FEV之间的负相关gydF4y2Ba1gydF4y2Ba(r = -0.65;P <0.05)支持后一种可能性。gydF4y2Ba
AgustIgydF4y2Ba等gydF4y2Ba。gydF4y2Ba7gydF4y2Ba同样使用半定量方法,报告了6名健康受试者iNOS表达非常低。然而,如果将该研究数据与正常体重的COPD患者和对照组的iNOS平均值联系起来,则与本研究中观察到的结果相似(患者iNOS/对照组iNOS;3.4gydF4y2Ba与gydF4y2Ba分别为3.9)。gydF4y2Ba
COPD患者骨骼肌中TNF-α水平升高。这与拉比诺维奇报告的调查结果是一致的gydF4y2Ba等gydF4y2Ba。gydF4y2Ba27gydF4y2Ba他们研究了9名患者和6名健康对照,发现在休息时,TNF-α mRNA的表达在COPD患者中显著升高。gydF4y2Ba
GoskergydF4y2Ba等gydF4y2Ba。gydF4y2Ba28gydF4y2Ba采用免疫组化技术(CD68)检测COPD患者骨骼肌中的巨噬细胞和白细胞。与对照组相比,这些作者没有发现患者肌肉中这些炎症细胞的异常数量。在目前的研究中,使用相同的抗体,发现COPD患者肌肉组织中的巨噬细胞数量明显高于健康受试者。在所有COPD超微结构研究样本中也观察到巨噬细胞,与正常受试者中很少观察到巨噬细胞形成对比。目前的研究结果与Gosker的研究结果之间的差异gydF4y2Ba等gydF4y2Ba。gydF4y2Ba28gydF4y2Ba这可能是因为他们在对照组中发现的巨噬细胞数量增加了。本研究中正常受试者巨噬细胞数量较低,与Malm报道的相似gydF4y2Ba等gydF4y2Ba。gydF4y2Ba29gydF4y2Ba。gydF4y2Ba
据目前作者所知,以前没有研究评估COPD患者骨骼肌中CD163(一种巨噬细胞标记物)的水平。虽然测量了CD163的总价值,但有可能它也反映了该部分的可溶性部分。尽管如此,CD68免疫反应性的增加支持了CD163的增加反映了巨噬细胞而不是可溶性CD163的增加这一观点。此外,还测量了CD154,这是一种t细胞标记物。慢性t细胞活化依赖于CD154的过度表达。NO由巨噬细胞在抗原呈递给T细胞的过程中产生,激活的T辅助细胞(Th)表达共刺激分子,与几种细胞因子一起诱导巨噬细胞产生NO。其中一个T细胞共刺激分子是CD154 (CD40L)gydF4y2Ba30.gydF4y2Ba。CD163和CD154水平升高与肌肉组织中巨噬细胞数量增加的检测结果相结合,与COPD患者骨骼肌中可能发生炎症过程的假设相一致,Th细胞活化和NO巨噬细胞产生。gydF4y2Ba
最近,AgustIgydF4y2Ba等gydF4y2Ba。gydF4y2Ba7gydF4y2Ba报道NF-κB激活和iNOS表达在COPD低体重患者骨骼肌中发生。作者推测,这些变化可能有助于这些患者体重减轻的分子发病机制。本研究的结果与这些作者报道的结果相反,因为相似水平的NOgydF4y2Ba2gydF4y2Ba−gydF4y2Ba,没有gydF4y2Ba3.gydF4y2Ba−gydF4y2Ba正常体重和低体重患者骨骼肌中可见硝基酪氨酸、iNOS、nNOS、eNOS、TNF-α、CD154和CD163。目前的发现与AgustÍ的发现之间的差异gydF4y2Ba等gydF4y2Ba。gydF4y2Ba7gydF4y2Ba部分原因可能是两项研究中患者气流阻塞严重程度的差异。目前研究中两组患者的FEV值相似gydF4y2Ba1gydF4y2Ba。低BMI患者为45±12%,BMI正常患者为42±7%。相比之下,FEVgydF4y2Ba1gydF4y2BaBMI指数低的人群,通过AgustÍgydF4y2Ba等gydF4y2Ba。gydF4y2Ba7gydF4y2Ba(28±2%)明显低于BMI正常患者(39±2%)。gydF4y2Ba
最后,本研究的一个局限性值得讨论。由于获取骨骼肌样本的过程具有侵入性,因此纳入的受试者数量相对较少。这可能限制了目前研究结果对整个COPD患者人群的直接外推。然而,15名COPD患者和14名正常人构成了使用外周肌肉活检评估炎症标志物的最大数量。gydF4y2Ba
总之,本研究支持慢性阻塞性肺疾病患者骨骼肌存在局部炎症。细胞因子肿瘤坏死因子-α、CD163和CD154水平升高,分别表明存在巨噬细胞和活化的t细胞。内皮型一氧化氮合酶和神经元型一氧化氮合酶以及一氧化氮最终产物(亚硝酸盐和硝酸盐)的浓度降低。诱导型异构体一氧化氮合酶和亚硝基酪氨酸的表达也增加,表明产生的大部分一氧化氮以亚硝基酪氨酸为主,可能与巨噬细胞诱导型亚硝基一氧化氮合酶的表达有关。最后,在正常体重和低体重慢性阻塞性肺疾病患者中,所有这些标志物都没有发现差异,这可能最终有助于解释体重减轻及其与骨骼肌炎症的可能关系。gydF4y2Ba
- 收到了gydF4y2Ba2004年9月15日gydF4y2Ba
- 接受gydF4y2Ba2005年4月19日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba