摘要
的-308ga.和TNFB1/ 2肿瘤坏死因子基因的多态性已经与败血症的易感性增加有关,尽管先前的研究不一致。它们在急性呼吸窘迫综合征(ARDS)中的作用尚未得到评估。目前作者假设了308−等位基因和TNFB22.基因型与ARDS中的易感性和死亡率增加相关。
上述假设在一项嵌套病例对照研究中进行了研究,该研究包括441名白种人对照组和212名因败血症、创伤、误吸或高输血入院的重症监护室患者。
的308−和TNFB1等位基因处于连锁不平衡状态。粗分析表明,这些多态性与ARDS易感性无关。在亚组分析中,根据ARDS的临床风险是否导致直接或间接肺损伤,它们与发生ARDS的几率增加或降低相关。的308−等位基因与ARDS患者60天死亡率增加相关,在年轻患者中发现相关性最强。两者之间没有联系TNFB.多态性和ARDS死亡率。
-308年乔治亚州,但不是TNFB12.,多态性与急性呼吸窘迫综合征的死亡率增加有关,但它们与急性呼吸窘迫综合征易感性的关系取决于诱发急性呼吸窘迫综合征的损伤部位。
为什么有些人会发展并随后死于急性呼吸窘迫综合征(ARDS),而有些人不会,尚不清楚。尽管败血症和创伤等临床预测因子已被广泛认可,但只有少数具有这些风险的患者会发展为ARDS1.同一类型和程度的侮辱可能存在个体对ARDS发生和死亡的易感性差异。急性肺损伤的遗传易感性可以解释观察到的风险和结果的个体间差异2- - - - - -4.
关于肿瘤坏死因子(TNF)-α在ARDS中的作用的研究一直存在分歧。一些研究发现血浆TNF-α与ARDS的发生和死亡率相关5- - - - - -7而另一些则没有8,9.这些差异可能是由于TNF-α释放的时间和区域差异10,11以及测定技术的差异12.TNF-α产生的临床异质性和遗传变异也可能导致这种差异13.
的-308ga.TNF-α基因中的启动子多态性和TNFB1/2甲TNF-β基因中的I限制片段长度多态性(RFLP)似乎影响TNF-α水平。载体的运营商308−等位基因(308−)和纯合子TNFB2等位基因(TNFB22.)增加了TNF-α生产14,15在一些研究中,感染性休克的易感性增加或死亡率增加15- - - - - -19而在其他地方则不然20.,21..
认识到ARDS的临床异质性和肺外ARDS与肺外ARDS的差异22.美国ARDS共识会议(American European Consensus Conference, AECC)建议将肺损伤的病因分为直接和间接肺损伤23..最近,表面活性剂蛋白b基因的−1580C/T错义突变与直接而非间接肺损伤患者的ARDS有关2.因此,有可能-308ga.和TNFB1/2急性呼吸窘迫综合征(ARDS)的发生可能与基因多态性直接相关相对间接的肺损伤。
本作者描述了对ARDS风险的患者嵌套病例对照研究,并假设308−的-308ga.多态性和TNFB22.的TNF.-β基因将与ARDS的易感性增加和增加的死亡率增加相关。此外,还探讨了协会,以确定它是否可能因直接而异相对间接的肺损伤。
方法
研究对象
研究设计的示意图如图1所示⇓.每天为Massachusetts总医院(波士顿,MA,USA)的重症监护单位(ICU)进行招生,每天筛查如前所述的ARDS的研究定义的临床风险因素(表1⇓)3..排除标准包括年龄<18岁,弥漫性肺泡出血或慢性肺病并指令扣除插管。患有免疫抑制或用粒细胞菌落刺激因子治疗的患者被排除在外。2000年11月后,由于在败血症中使用类固醇的使用,不再排除患有皮质类固醇的免疫抑制患者。敏感性分析显示,排除标准变化前后注册的患者具有相同的ARDS(34%),ICU死亡率(22%)和ARDS死亡率(46%)。调整患者是否在丢弃类固醇作为排除标准之前或之后注册,改变了估计308−ARDS死亡率<1%。
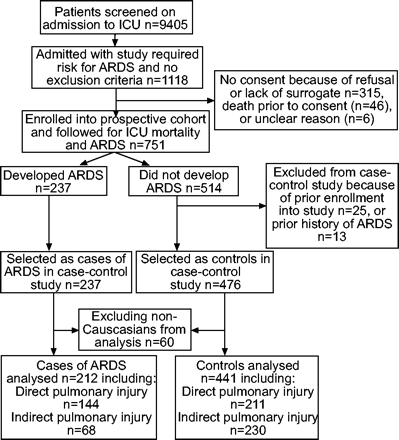
病例对照研究的研究设计和患者选择流程图。ICU:重症监护病房;ARDS:急性呼吸窘迫综合征。
ICU招生至少有一个ARDS的规定危险因素,没有排除标准有资格获得预期队列。人类受试者委员会(波士顿,MA,USA)批准了研究和知情书面同意,从所有科目或其适当的代理人获得。
研究设计
在ICU入院时收集基线临床信息。收集ICU入院后24 h的生命体征和实验室参数,计算急性、生理、年龄和慢性健康评估(APACHE) III25..每日对受试者进行ARDS筛查,如前所述,ARDS定义为需要插管的呼吸衰竭和AECC标准3.,23..每日的胸片由两名肺科和危重科医生在接受渗透性解释共识培训后进行解释,并由第三名医生仲裁意见分歧。所有患者的临床状况都是盲的。与其他报告相比,对双侧浸润的初始解释的一致性κ-评分为0.75(95%置信区间(CI): 0.62-0.89)26..
从预期队列中,设计了一个案例对照研究。案件是在住院期间满足ARDS标准的案件。所有在住院期间没有开发ARD的患者,也没有历史,或者在研究中没有进入该研究的历史记录是对照。所有患者均进行ICU死亡率,并在60天内进行所有死亡原因的ARDS病例。
方法
采血10cc,提取DNA并进行PCR扩增。采用焦磷酸测序进行基因分型-308ga.多态性(Pyrosequencing AB, Uppsala, Sweden),具有正向引物5 ' -CCAAACACAGGCCTCAGGACTC-3 ',生物素化反向引物5 ' -TCCTCCCTGCTCCGATTCCG-3 '和测序引物5 ' -AGGCAATAGGTTTTGAGGGGCA-3 '。的肿瘤坏死因子-βNco我采用改良的PCR-RFLP方法检测多态性,该方法涉及发表的引物序列和Nco I酶切(New England BioLabs, Beverly, MA, USA)19.结果被两个独立调查人员解释,并在随机的5%样品中重复基因分型。实验室人员和研究助手对受试者的病例控制状态或基因型蒙蔽了蒙蔽。
分析
采用卡方拟合优度检验确定符合Hardy Weinberg平衡。单因素分析采用Fisher’s Exact Test、卡方趋势检验、ANOVA或Wilcoxon Rank Sum检验。对单变量分析中p值≤0.2的变量采用逆向选择算法进行研究,如果不满足p值≤0.2,则将其剔除。最终的多因素logistic回归模型包括基因效应、反向消除结果、显著交互作用和临床相关参数,如APACHE III评分对ARDS发展的影响、脓毒性休克对ARDS死亡的影响。在最终模型中对可能的混杂因素进行了调整,而不是在分析中在病例和对照之间进行匹配。给定的小数目308−homozygotes,homozygotes308−等位基因与杂合子(308−),并与之相比−308克最终模型中的纯合子,如之前的报道15,16.作为分布TNFB.案件和控制之间的基因型没有明确表明主导或隐性模型,是TNFB.基因型模型与以前的报道相同17,18通过比较TNFB2homozygotes(TNFB22.)纯合子和杂合子TNFB1.使用C统计(接收器操作特征曲线下的区域)来评估模型适合27..一个先天的决定通过直接分析分析相对间接的肺损伤。用相互作用项测试效果修正。p值为0.05被认为具有统计学意义。
两种多态性之间的键化脱落肌瘤的检测基于Lewontin的对照28..使用分区连接预期最大化(PL-EM)版本1.0产生两种TNF多态性的单倍型29.,如在其他协会研究中30..该软件使用EM算法的一种有效变体,根据非分阶段基因型数据重建个体的概率,同时提供对整体单体型频率及其标准误差的估计。奇数比(OR)是通过比较具有单倍型一个或多个副本的个体与没有单倍型的个体来估计的。
在最初的研究设计中,假设α误差为0.01(允许多次比较),功率为80%,等位基因频率为16%308−31.65%的人TNFB217在美国,一项有560例病例和1120例对照的研究中,对ARDS发展的最低检测OR为1.56308−1.47,TNFB22..假设50%的患者与ARDS的风险有直接的肺损伤,最小可检测或1.9308−1.8,TNFB22..考虑到653名受试者的实际研究规模和α-error的0.05,最低检测OR为1.78308−, 1.68TNFB22..
结果
患者人群
在1999年9月9日至2002年10月15日期间,病例对照研究包括237例ARDS病例和476例对照组(图1)⇑)。92%的患者是高加索人,分析仅限于212个白种人案件和441个高加索人控制。
ARDS的临床危险因素及入ICU的基线特征见表2⇓和3⇓.ARDS发生的中位时间为ICU入院后1天(25-75%;0 - 3天)。逆向选择ARDS发展的结果如下:直接肺损伤(p<0.001)、脓毒症(p = 0.05)、外伤(p<0.001)、年龄(p = 0.002)、女性(p = 0.02)、糖尿病(p = 0.004)、血小板≤80000·mm−1(p = 0.005),异常胆红素>2.0 mg·dL−1(p = 0.1)和输血(p<0.001)。统计学上显著的交互作用仅在肺损伤类型之间发现(直接)相对间接)和-308A等位基因或者TNFB22.基因型。
基因型分析-308ga.和TNFB1/2多态性和ARDS的发展
等位基因频率为0.16308−0.69,TNFB2等位基因,类似于先前的报告19,20.,30.对照组与Hardy Weinberg平衡无差异(p>0.2),重复基因分型无差异。的-308ga.和TNFB1/2基因型与ARDS入院危险因素无显著性差异(p> .4)。的308−等位基因与TNFB1(ď = 0.90)。应用PL-EM算法,个体单倍型的后验概率为0.96-1.0。因此,每个个体分配两个后验概率最高的单倍型。
病例和对照组的基因型频率详见表4⇓.基因型和单倍型频率在病例和对照之间没有差异。ARDS多变量模型的c -统计量分别为0.73和0.74308−和TNFB22.,分别。在多变量分析中,发现与ARDS相关TNFB22.(或调整:0.47;95%置信区间:0.25—-0.86;P = 0.01)308−(调整或:1.7; 95%CI:0.89-3.1)。
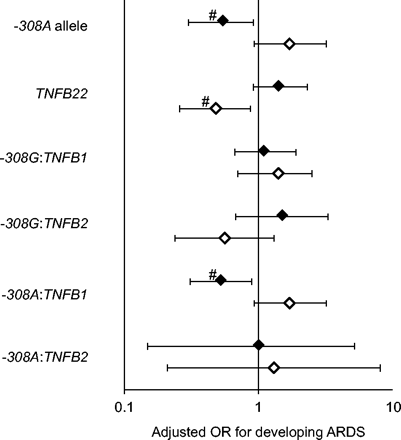
直接分层后相对间接肺损伤,急性呼吸窘迫综合征与308−或TNFB22.根据ARDS的危险因素而不同(图2)⇓)。的308−在直接肺损伤患者中,等位基因与发生ARDS的几率降低相关(调整后OR: 0.52;95% CI: 0.30-0.91),但间接肺损伤发生ARDS的几率增加不显著(调整后的OR: 1.7;95%置信区间:0.93—-3.2)。将69例直接和间接肺损伤患者排除在分析之外,没有改变直接肺损伤导致ARDS的估计值(调整后的OR: 0.52;95%置信区间:0.27—-1.0)。从连锁不平衡中可以预料到,两者之间的关联TNFB22.和ARDS与此相反308−,(调整OR: 1.5;95% CI: 0.91-2.3,调整后的OR: 0.48;95% CI: 0.26-0.87,分别为直接和间接肺损伤)。结果308−:TNFB1单倍型与308−(图2⇓)。损伤的类型显着修改了ARDS和ARD之间的关联308−(p = 0.01),TNFB22.(p = 0.006)308−:TNFB1单倍型(p = 0.007)。如果损伤类型及其相互作用项在最终模型中没有调整,TNFB22.多因素分析不再与ARDS相关(调整后的OR: 0.94;95%置信区间:0.67—-1.3)。
通过直接分层(♦)在分层后,通过单个基因型和多态性的单个基因型和单倍型来调整急性呼吸窘迫综合征(ARDS)的差异(或)相对间接(Ⅳ)肺损伤。有355名受试者,肺部损伤直接肺损伤,ARDS和298名受试者间接肺损伤。伤害类型与伤害类型有显着的影响308−等位基因(p = 0.01),TNFB22.基因型(p = 0.006)和308−:TNFB1单倍型(p = 0.007)。#:p≤0.01。
ARDS中的死亡率
212例ARDS患者60天死亡率为46%。ARDS的临床风险及ARDS存活者与非存活者的基线特征见表2⇑和3⇑.向后消除后ARDS死亡率增加的预测因素包括:年龄(p<0.001)、APACHE III评分升高(p = 0.001)、外伤(p = 0.07)、入院前类固醇治疗(p = 0.005)、总胆红素≥2.0 mg·dL−1(P = 0.05),输血(P = 0.03)。输血之间唯一显着的相互作用308−(p = 0.05)和TNFB22.(p = 0.02)。对于ARDS死亡率的最终模型的C统计数据为0.85308−和TNFB22..
ARDS死亡率取决于-308ga.,但不是TNFB1/2多态性(表4⇑)有数人数308−与增加60天的ARDS死亡率相关的等位基因(p = 0.01;图3⇓)。的308−等位基因与ARDS患者60天死亡率显著增加相关(粗比值比:2.1;95%置信区间:1.1—-3.9;或调整:3.5;95%置信区间:1.4—-8.6;p = 0.007)。这一关联在117名年龄小于67岁的患者中最强(调整后的OR: 14.9;95%置信区间:-74 - 3.0;p < 0.001)。在95例67岁的ARDS患者中,未发现与死亡率相关(p = 0.3)。的308−等位基因与死亡率直接相关(调整后OR: 4.8;95% CI: 1.3-18)和间接肺损伤(调整后的OR: 5.5;95% CI: 0.99-31),没有证据表明损伤类型会改变疗效(p = 0.2)。TNFB22.与ARDS死亡率无关(调整或:0.50; 95%CI:0.21-1.2)。从联动不平衡中预期,308−:TNFB1单倍型与ARDS死亡率增加相关(调整后OR: 3.7;95%置信区间:1.5—-9.1;表3⇑)。
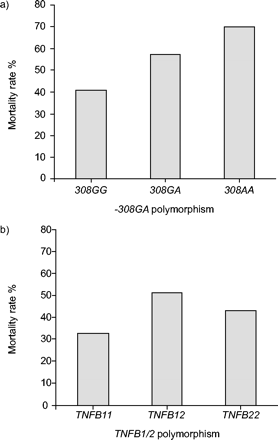
图显示212例急性呼吸窘迫综合征(ARDS)患者60天死亡率-308ga.和TNFB1/2多态性。308年gg:n = 155;308年乔治亚州: n = 47:308 aa:n = 10;TNFB11.: n = 18;TNFB12.: n = 101;TNFB22.: n = 93。趋势卡方检验的p值308−ARDS死亡率等位基因为0.01。在统计上没有显著的趋势TNFB2等位基因与ARDS死亡率(p≥0.8)。
讨论
本研究报告了ICU对ICU患者的分子流行病学研究的结果明确规定了ARDS的常见风险因素。在ARDS中的死亡率之间发现了重大关联308−,但不TNFB22.,特别是在年轻患者中。这些多态性和ARDS易感性之间的关联是异质的,依赖于将患者造成ARDS风险的损伤部位。
目前的研究有很多优点。首先,由于ARDS没有诊断金标准,采用AECC定义的ARDS前瞻性诊断有助于减少表型错误分类。其次,本研究使用了定义明确的风险控制组。使用有机会发展预后的危重症对照比使用健康个体更具有临床相关性。此外,这也减少了基因与疾病风险(如败血症或肺炎)之间任何可能关联的混淆。
支持当前作者的假设,据报道高TNF产生308−等位基因的-308ga.多态性与ARDS死亡率增加有关,这与疟疾和脓毒症的其他研究一致15,16,30.本研究提示,患者之间的遗传异质性可能部分解释了以前在ARDS和脓毒症中循环TNF-α研究的差异5- - - - - -10.
之间的联系308−和308−:TNFB1在年轻的患者中,ARDS中的单倍型和死亡率尤其强烈,即使年轻的ARDS患者往往具有较低的死亡率(表3⇑)。复杂疾病的遗传贡献在患有早期发病的疾病中更大32..
虽然在TNFB22.和ARDS对多变量分析的易感性,这发现这是通过直接和间接肺损伤患者的亚组中与ARDS不同的不同关系驱动。用类似的异质效果308−.通过TNF多态性和ARDS之间关联的损伤类型的这种效果改性表明ARDS可能的基因环境相互作用。这种发现的重要性尚不清楚。肺部的炎症反应和肺部的放射性,组织学和机械性能根据感染部位或ARDS的疾病是肺部或肺部的22.,33.,34..另一种可能是,这些发现是由于AECC标准对直接患有ARDS的患者的敏感性和特异性较低相对间接的肺损伤。最近的一项研究发现,双侧肺炎常被AECC标准误诊为ARDS35..虽然双侧肺炎,双侧吸入和肺挫伤临床无区别,但它们具有不同的组织学和发病机制。因此,难以知道高TNF-α是否产生308−等位基因与双侧肺炎的进展降低或奇数逐渐发育弥漫性肺泡损伤有关。足够或高的TNF-α反应可能限制肺炎的直接肺损伤或口服病原体的吸入,并降低发展双侧肺炎的几率。然而,即使具有这种错误分类,大多数患有AECC标准的直接肺损伤的患者也会组织学上具有ARDS,表明ARDS病例可能更加均匀24..然而,考虑到亚组的样本量减少,这些发现需要在更大的ARDS临床同质风险患者群体中得到证实。
在目前的研究中,单倍型分析的结果与308−等位基因。这表明了-308ga.多态比多态更重要TNFB.多态性与ARDS死亡率的关系不大TNFB.对整体调查结果的多态性。但是,自从此-308ga.和TNFB1/2多态性存在于高度多态性,主要的组织相容性区域,有可能308−多态性与另一种多态性有关,即不能排除疾病基因座。目前的研究专注于两种特定的多态性,特别是因为它们以前与可变函数和败血症相关联,但是TNF基因肯定存在更多多态性。在基因分型多态性后的正式单倍型分析对于在基因中定义基因中的连锁不平衡和与ARD的关系是优选的。
作者承认本研究还有其他一些局限性。这些TNF多态性的功能意义尚未在患者人群中得到证实。由于研究设计的原因,研究结果可能不能推广到社区环境、免疫功能低下的宿主、没有ARDS危险因素的患者或具有不同临床ARDS风险的患者。此外,这些分析仅限于白种人,这减少了不同基因构成造成混淆的可能性,但不允许将结果外推到其他种族群体。
总之,本研究表明了一个关联308−急性呼吸窘迫综合征中的等位基因和死亡率,特别是患者。之间的关联-308ga.多态性和急性呼吸窘迫综合征的发育是异质的,可能取决于促进急性呼吸窘迫综合征的损伤类型。需要额外的研究来确认其他群体中的这些发现与其他危险因素。
致谢
作者要感谢W-L.张,K.Mccoy,T.Mccabe,B. Bean和L.患者招募的线背。A. Solomon,A. Shafer和L. Shimada进行研究支持。L. Su,M. Z. Wang和Y. Sai用于实验室专业知识。J. Freelich,M.Chertok,S. Mucci和R. Rivera为数据管理,以及流行病学咨询的D. Miller。
- 收到了2005年1月3日。
- 接受2005年5月17日。
- ©ers Journals Ltd