抽象的
气道和肺实质的炎症在慢性阻塞性肺疾病的发病机制中起着重要作用。在本研究中,我们使用烟草诱导的肺气肿小鼠模型来研究气道和肺部炎症反应的时间进程,特别强调肺树突状细胞(DC)种群。
一组老鼠要么暴露在香烟烟雾中,要么暴露在控制空气中长达24周。在对香烟烟雾的反应中,炎症细胞(IE。中性粒细胞,巨噬细胞和淋巴细胞)逐渐积累在小鼠的气道和肺实质上累积。此外,在24周时,在呼吸道(10倍增加)和肺实质(1.5倍增加)的肺实质(12.5倍增加)中观察到DC的透明渗透。
与空气暴露小鼠的Bal DC相比,烟雾暴露小鼠的支气管肺泡灌洗液(BAL)DC的流式细胞术分析显示出主要的组织相容性综合体分子和共刺激分子CD40和CD86的上调。肺组织学的形态学分析表明,在烟雾暴露后24周后平均线性截距和肺泡壁破坏的显着增加。
总之,支气管肺泡灌洗炎症和树突细胞变化的时间过程和卷烟暴露小鼠的肺舱。
慢性阻塞性肺疾病(COPD)是一种疾病状态,其特征是气流限制的进行性发展,不能完全可逆1.气道和肺的炎症被认为在COPD发病机制中发挥着重要作用2-5..COPD的进展与炎症细胞的小气道壁的渗透强烈相关,炎症粘液渗透物在腔内6..慢性阻塞性肺病的一个主要危险因素是吸烟。然而,香烟烟雾(CS)诱导COPD炎症的分子和细胞基础仍不清楚。
肺部对抗暴露于有毒气体和颗粒的主要宿主防御机制是先天性和适应性炎症免疫反应。肺的天然防御系统由上皮屏障和组织损伤后的急性炎症反应提供,包括中性粒细胞、嗜酸性粒细胞和巨噬细胞的招募和激活7..相比之下,自适应免疫应答依赖于B-和T淋巴细胞(CD4+和CD8+),并且对以前的损伤有长期的记忆。对不同临床阶段COPD患者手术切除的肺组织进行详细的组织学分析,清楚地显示先天和适应性免疫细胞对小气道壁的进行性浸润。有趣的是,随着慢性阻塞性肺病的进展,含有淋巴滤泡的气道比例增加,这表明在严重慢性阻塞性肺病患者中,淋巴细胞组织中的抗原提呈细胞参与了滤泡6..
树突状细胞(Dendritic cells, DCs)不仅是专门的抗原提呈细胞,它们也非常重要地位于呼吸道和肺实质中吸入空气和肺之间的界面8..DC是危险的主要传感器,通过启动先天免疫应答并控制特定免疫反应的发育来对粘膜表面的任何干扰反应8.-13.由于DCS能够链接先天和适应性免疫,并且由于免疫系统的两种组分在COPD患者的呼吸道中增强,因此目前的作者假设肺部DC数量会因CS暴露而增加,并且泄露烟雾的DC小鼠会显示激活的迹象。因此,研究了气道和肺炎症反应,更具体地,研究了CS诱导的肺气肿小鼠模型中对烟草烟雾暴露的直流反应14.
方法
动物
男性C57BL / 6鼠标,6-8周的老鼠购自Harlan(河荷兰Zeist)。当地伦理委员会(格伦,比利时)批准了所有在活的有机体内操作。
实验设计
小鼠暴露于五支香烟的烟雾(参考卷烟1R3;肯塔基州大学,Lexington,Ky,美国)Q.I.D.有30分钟的无烟间隔。这些动物每周暴露5天,持续24周。对照组则暴露在空气中。第1、3、7和14天(n = 6;短期烟雾暴露),以及第4、12和24周(n = 5;长期)小鼠。这些实验重复了三次。
烟草烟雾室
小鼠暴露于CS,使用吸烟装置(D. Kobayashi, Washington University Medical Center, WA, USA),并使用适合一组小鼠的房间(房间体积= 7500 cm)3.).得到了最佳的烟空气比1:1215.
支气管肺泡灌洗
为了进行支气管肺泡灌洗(BAL),处死动物,插入气管插管。三次通过气管,1ml汉克平衡盐溶液(HBSS;GibcoBRL, Carlsbad, CA, USA),不含游离钙和镁,但补充0.05 mM EDTA (Sigma, St Louis, MO, USA),灌注后轻轻手工抽吸恢复。将回收的BAL液离心,细胞颗粒洗涤2次,最后用1 mL HBSS重悬。总细胞计数在Bürker室(Novolab, Geraardsbergen, Belgium)进行,差异细胞计数在细胞离心制剂(Cytospin 2;山东有限公司,伦考恩,英国)后着色May-Grünwald-Giemsa。
肺单细胞悬浮液的制备
BAL后,冲洗肺循环和体循环。一个肺用于组织学,另一个用于制备细胞悬液,如前所述16.简而言之,彻底切碎右肺部,在37℃和5%CO的潮湿培养箱中在消化培养基中孵育30分钟2.重悬了器官片段,加入新的消化培养基,延长孵育15分钟。在最终重悬浮后,将样品离心并重悬于含有10mM EDTA的钙和无镁的PBS,在室温下含有10mM EDTA。最后,将细胞进行红细胞裂解,在荧光激活的细胞分子 - EDTA中洗涤,通过50μm的细胞过滤器,并在冰上保持直至标记。用Z2 Beckman-Coulter粒子计数器(Beckman-Coulter,Ghent,Belgium)进行细胞计数。
用流式细胞术标记BAL细胞和肺单细胞悬液
DCs、巨噬细胞、粒细胞、T淋巴细胞和b淋巴细胞的流式细胞分析定义如前所述16.用于鉴定小鼠DC群体的单克隆抗体是生物素化的抗CD11C和Phycoerythrin(PE) - 缀合的抗IAB..用于DC表型的其他标记有pe标记的CD40、CD86/B7-2、CD80/B7-1和CD54/细胞间粘附分子(ICAM)-1。同型对照为大鼠免疫球蛋白-G2,河鼠免疫球蛋白2 b和亚美尼亚仓鼠Igg。用于小鼠T细胞亚流染色的标记染色是CD4,CD8,CD3和CD69(活化标志物)。用GR1染色粒细胞,并显示B细胞作为CD19阳性。所有单克隆抗体都是从BD Pharmingen(Becton Dickinson Pharmingen,Erembodegem,Belgium)获得的,除了抗CD54(Research Diageostic Inc.,Flanders,NJ,USA)和抗CD11C(N418杂交瘤;来自M. Moser的礼物,布鲁塞尔自由大学,比利时)。
流式细胞术数据采集是在双激光FACS VATERAGE上进行的TM流动细胞仪运行CellQuestTM软件(Becton Dickinson,山景,加州,美国)。Flowjo软件(www.treestar.com)用于数据分析。
组织学和形态学分析
右肺切除后,在压力和容量控制的条件下(12 mL·h),通过气管插管,用连续释放泵温和滴注固定剂(4%多聚甲醛)固定左肺-1;10分钟)。肺切除后,置于新鲜固定液中浸泡4小时。肺叶石蜡包埋,切3µm横切面。组织样本用苏木精和伊红染色(Klinipath, Geel,比利时)。对于每只动物,使用Zeiss KS400图像分析仪平台(Zeiss, Oberkochen, Germany)盲法捕捉×200放大后的10个场。
肺气肿是一种以肺实质损害为特征的结构性疾病。肺泡壁的破坏会导致肺泡腔的扩大。销毁和扩大进程可以按时间顺序或同时进行17那18.因此,建议评估两个参数以量化肺气肿病变19.
通过平均线性截距,6个月烟雾暴露后测定空域扩大的量化(L.m)20.那21和平均肺泡面(Am).L的测量m采用100×100法随机通过肺。网格中每条线的总长度除以肺泡截取的数量,就得到了肺泡表面之间的平均距离,即Lm.相同的图像用于测量am.肺泡或空体被定义为肺泡壁围绕的空间,其在肺泡上的肺泡上的肺泡上的情况下。计算空间的横截面表面并除以肺泡的数量以获得am.
用破坏指数(DI)量化肺泡壁的破坏程度。17.简而言之,叠加在发际线束中心的网格上,叠加在肺部。在这些点下方的结构被分类为正常(n)或破坏(d)肺泡和/或管道空间。落在其他结构上的点,例如管道墙壁,肺泡壁等没有进入计算。DI从公式计算: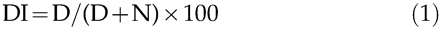
如前所述,采用双免疫荧光染色法对肺组织中DC浸润进行形态学定量22.树突状组织相容性复合体(MHC) II+B220−在气道上皮和伴随血管的组织区域中计数细胞,以及肺实质。为了量化DC渗透,检查每只小鼠的10个气道。结果表示为相对于组织表面的细胞计数(mm2).
统计分析
报告值以平均值±表示se的均值±SEM..肺部,肺泡空间大小的BAL,DC和T淋巴细胞的细胞组成(L.m, 一种m)及肺泡壁破坏(IE。比较不同组的DI)通过多重比较的Kruskal-Wallis检验。当观察到显著差异时,使用带有Bonferroni校正的Mann-Whitney u检验进行成对比较。p值<0.05被认为是显著的。
结果
BAL流体的炎症变化
为了探讨烟雾暴露对气道和肺部炎症的影响,研究了暴露于空气和烟雾的小鼠的三个主要肺室;气道和肺泡腔(BAL)、气道壁和肺实质(通过肺组织切片的组织学和免疫组化,以及通过肺消化液细胞悬液的流式细胞术)。这些实验有三个重复。
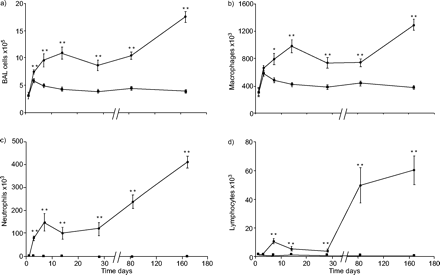
烟草暴露的小鼠在BAL中的炎症细胞总数中产生了逐渐增加的双相增加。在烟雾暴露3天后,观察到总Bal细胞的显着增加(p = 0.008)。在6个月结束时,观察到与空气暴露的小鼠相比,CS暴露小鼠中的4.5倍的总BAL细胞增加(P <0.001;图1A⇓).这种增加是由于单核细胞/巨噬细胞,中性粒细胞,淋巴细胞和DC在BAL流体中的积累(图1⇓和2⇓).随着时间的推移,中性粒细胞、树突状细胞和淋巴细胞的相对增加幅度最大。
香烟烟雾暴露对小鼠支气管肺泡灌洗(BAL)液体总数和细胞分化的影响。a)全灌洗细胞;b)巨噬细胞;c)中性粒细胞;和d)淋巴细胞。•:冒出烟雾的老鼠;▪:暴露空气的小鼠。动物(在第1,3,7和14天,N = 6;在第4周,第12和24周,N = 5)每组每组暴露于五支卷烟,4个实验·日-1,5天·星期-1.*: p < 0.05;* *: p < 0.01相对在相应的时间点暴露在空气中的小鼠)。实验进行了三个重复。给出了三个独立实验的综合数据。
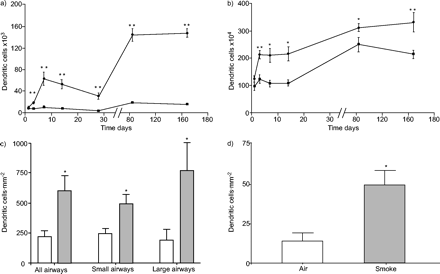
卷烟烟雾暴露在a)支气管肺泡灌洗液中的树枝状细胞绝对数量的时间过程,B)烟雾暴露小鼠(•)和空气暴露小鼠(▪)的肺部造影。24周香烟烟雾暴露对气道墙壁围绕空气暴露小鼠(□)和烟雾暴露小鼠围绕气道墙体的数量围绕气道壁的数量C)的卷曲细胞C)的数量。( ).动物(在第1,3,7和14天n = 6时;在每组4,12和24 n = 5周内,每组每组暴露于五支香烟,4个实验·日-1,5天·星期-1.*: p < 0.05;* *: p < 0.01相对在相应时间点暴露在空气中的小鼠。实验进行了三个重复。给出了三个独立实验的综合数据。
).动物(在第1,3,7和14天n = 6时;在每组4,12和24 n = 5周内,每组每组暴露于五支香烟,4个实验·日-1,5天·星期-1.*: p < 0.05;* *: p < 0.01相对在相应时间点暴露在空气中的小鼠。实验进行了三个重复。给出了三个独立实验的综合数据。
细胞螺旋藻的形态学分析显示出烟雾暴露7天后的单核细胞/巨噬细胞总数的轻微,但显着增加(P = 0.01)。在6个月内观察到显着的增加(6个月的巨噬细胞总数:烟雾= 1289.3±80.1×103.相对空气= 381.4±27.7×103.;p < 0.001;图1 b⇑).流式细胞术证实烟雾暴露后观察到的Bal巨噬细胞数量增加(数据未显示)。
在细胞旋上,中性粒细胞几乎不存在于暴露在空气中的动物BAL中。暴露在烟雾中的动物出现进行性BAL中性粒细胞增多症。3天后中性粒细胞数量显著增加(p<0.001), 6个月后继续增加(6个月时中性粒细胞总数:烟雾= 412.2±24.8×103.相对空气= 0.2±0.1×103.;p < 0.001;图1 c⇑).两组中BAL中的嗜酸性粒细胞数量小,随着时间的推移没有显着变化(数据未显示)。
烟雾暴露的动物在气道中开发了T淋巴细胞的逐步增加(按照细胞离心机制剂列过)。淋巴细胞的量在7天(p = 0.004)显着增加,进一步增加6个月(6个月淋巴细胞总数:烟雾= 60.3±10.0×103.相对空气= 0.7±0.2×103.;p < 0.001;图1 d⇑).
基线时BAL中有少量b淋巴细胞。暴露3天后,b淋巴细胞与暴露于空气的小鼠相比显著增加(p = 0.004;数据未显示)。
BAL及肺树突状细胞增多
烟雾暴露后BAL中单核细胞/巨噬细胞数量的增加使目前的作者好奇dc是否最初来自骨髓中的单核细胞前体23,如果在肺中起重要作用,免疫反应就会增加。
通过使用两种同时免疫荧光标准,通过流式细胞术鉴定DCS,其是低自发荧光和中间至高水平的CD11C24.烟雾暴露小鼠灌洗液中树突状细胞呈明显的双相增加。暴露3天后,BAL患者的DCs已经增加(p<0.001)。到6个月结束时,观察到这些细胞增加了10倍(6个月时BAL DCs总数:烟雾= 148.5±8.0×103.相对空气= 15.8±0.8×103.;p < 0.001;图2⇑).
同样在肺实质中,吸烟引起接触3天后DC数轻微但显著增加(p = 0.005)。6个月时,肺实质DC数增加1.5倍(6个月时肺DC总数:烟雾= 332.6±35.9×10)4.相对空气= 214.6±15.4×104.;p = 0.009;图2B⇑).
根据使用双免疫荧光染色方案的形态,MHC II阳性和B细胞标记B220的组合,还通过免疫组织化学鉴定DCS。CS诱导小(0-1000μm气道周边)和大气道(1000-2000μm;图2C的组织区域中的DCs大量增加⇑).因此,气道壁上的DC浸润与气道大小无关(p = 0.65)。与接触空气的小鼠相比,接触烟草的动物肺实质中也有显著的DCs积累(图2d)⇑和图3.⇓).
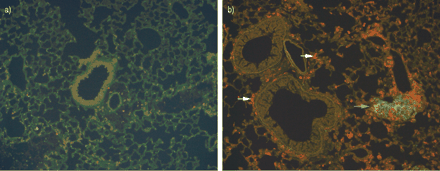
24周时a)空气暴露小鼠和b)烟雾暴露小鼠的肺组织双免疫荧光染色显微照片。根据形态学、主要组织相容性复合体- ii阳性(红色染色)和b细胞标记物B220缺失(绿色染色)的组合鉴定树突状细胞(白色箭头)。蓝色箭头表示b细胞滤泡。
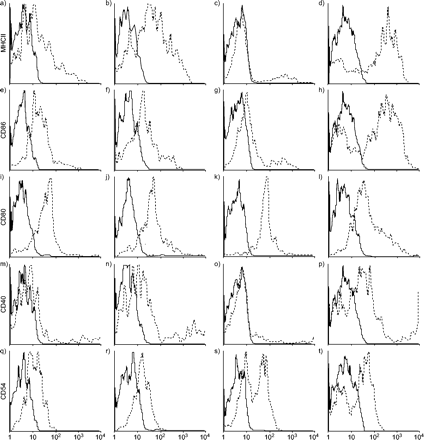
通过检查MHC II和T细胞共刺激分子的细胞表面表达来评估烟雾暴露小鼠中肺部DC的活化状态。均在BAL和肺部进行肺部,高表达CD11(CD11C你好烟草暴露小鼠的MHC II和共刺激分子CD40水平较空气暴露小鼠的DCs高。此外,在BAL室中,暴露于烟雾也增加了DCs上共刺激分子CD86 (B7.2)的表达(图4)⇓).
肺部中鉴定的树突细胞的表型流式细胞术分析(A,B,E,F,L,J,M,N,Q,R)和支气管肺泡灌洗(BAL)(C,D,G,H,K,L,o,p,s,t)在空气和烟雾暴露的小鼠中4周。与空气暴露的树突细胞(a,c,e,g.i,k,m,o,q和s)相比,烟雾暴露小鼠的树突细胞(b,d,f,h,j,l,n,p,r和t)具有上调的主要组织相容性复合物(MHC)II,CD86和CD40在BAL中具有上调水平;肺组织中MHC II和CD40的上调水平。- - - :特异性标记染色;---:同种型控制染色。所示的数据来自一种动物,并从一个实验中,代表两个独立实验。
肺部的炎症变化
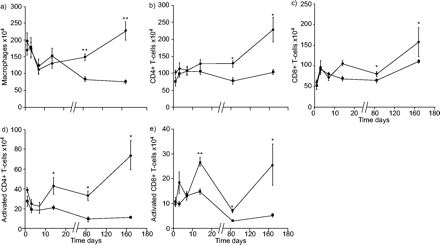
随着时间的推移,肺细胞总数没有显着变化(数据未显示)。肺部消化的流式细胞术分析显示出增加数量的巨噬细胞和CD4+和CD8+烟雾暴露的动物中的T淋巴细胞(图5⇓).
通过流式细胞术中的小鼠肺肺肺肺的影响A)巨噬细胞,B)CD4 + T细胞,C)CD8 + T细胞,d)活化的CD4 + T细胞,E)活化CD8 + T细胞.•:冒出烟雾的老鼠;▪:暴露空气的小鼠。动物(在第1,3,7和14天,N = 6;在第4周,第12和24周,N = 5)每组每组暴露于五支卷烟,4个实验·日-1,5天·星期-1.*: p < 0.05;* *: p < 0.01相对在相应的时间点的空气暴露的小鼠。这些实验一式三份进行。显示了一个代表性实验的结果。
肺巨噬细胞经流式细胞术鉴定为CD11c+高自发荧光细胞。与低自发荧光DC相比,这些细胞具有典型的巨噬细胞形态,并且是MHC II低到负数24.在对照组小鼠的肺中,高自发荧光CD11c+细胞随着年龄的增长而下降,而在与对照小鼠相比,12周后巨噬细胞巨噬细胞数显着增加(p = 0.009)。这种差异随时间持续存在(6个月巨噬细胞总数:烟雾= 226.8±27.4×104.相对空气= 75.4±3.9×104.;p = 0.009;图5A⇑).
具有高表达T细胞性能刺激分子的DCS的逐渐积累促进了烟雾暴露肺中T细胞群的程度,表型和活化状态的检查。在短时烟雾暴露后,肺T淋巴细胞子集群体不会显着变化。相比之下,12周后,淋巴细胞的总数显着增加(p = 0.009),进一步增加至多6个月(CD3总数+6个月的肺部淋巴细胞:烟雾= 414.5±48.3×104.相对空气= 261.4±11.5×104.;p = 0.014)。烟雾曝光诱导CD4的显着增加+和CD8+与暴露在空气中的小鼠相比。CD4总数+肺部淋巴细胞6个月:烟雾= 229.3±36.2×104.相对空气= 103.7±6.7×104.(p = 0.014)。CD8总数+6个月的肺部T淋巴细胞:烟雾= 157.0±35.3×104.相对空气= 110.3±4.2×104.(p = 0.05;图5 b⇑和5 c⇑).
此外,CD3的激活+CD4.+和CD3+CD8.+t细胞是检查。暴露在烟雾14天后,激活的CD4数量增加+和CD8+T细胞存在于肺部消化中。在24周时,早期活化标记CD69在31.82±1.37%CD4中表达+T细胞和15.53±1.79%CD8+暴露于烟雾组的t细胞数量分别为11.09±0.36% (p = 0.014)和4.65±0.60% (p = 0.014)(图5d)⇑和5 e⇑).
流式细胞术分析显示出烟雾暴露的动物和空气暴露小鼠之间的肺中粒细胞的颗粒细胞差异(数据未显示)。
在肺中,在b细胞群中没有观察到差异(数据未显示)。
组织学
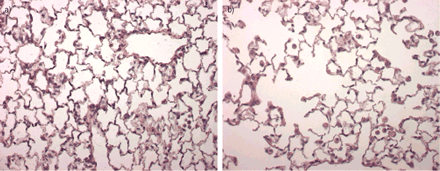
肺气肿是一种结构障碍,其特征在于破坏肺泡壁和肺泡空间的扩大。通过量化L来测量肺泡空间的DI和扩大来确定牙槽壁的破坏m和A.m.肺组织切片的显微镜分析显示出6个月的烟雾暴露后显着程度的肺气肿(图6⇓).烟草烟雾明显引起肺泡壁破坏。暴露在空气中的小鼠的DI范围为0.0-9.8(平均±9.8)SEM.= 4.2±0.5),而暴露于烟雾的动物DI范围为20.2 ~ 35.1(平均±0.5)SEM = 25.8±0.7;p < 0.001相对对照组)。此外,暴露于CS显著导致空域扩大。Lmcs暴露小鼠比空气暴露小鼠高23% (Lm6个月烟雾= 42.2±0.20μm相对空气= 34.3±0.21μm;P <0.001)。一个大幅增加m在烟雾暴露的动物中也观察到(am6个月时:烟= 783.4±79.8µm2相对空气= 511.8±42.41µm2;p = 0.015)。
24周时,苏木精和伊红染色于a)空气暴露和b)烟雾暴露小鼠的肺组织。烟雾暴露明显引起小鼠肺泡壁破坏和空气体积增大。
讨论
在本研究中,在6个月暴露于CS的6个月内,在呼吸道和小鼠的肺部调查主要炎症细胞的变化的时间过程,直至肺气肿的发育。响应于CS,在小鼠的BAL舱中观察到炎症细胞的逐渐浸润炎症细胞,包括DC,中性粒细胞,巨噬细胞,T-和B淋巴细胞。DCS,巨噬细胞和淋巴细胞,但不是中性粒细胞,也在烟雾暴露后累积在肺部。此外,在6个月内接触过6个月后,发育了显着程度的肺泡破坏。
BAL液中不同类型细胞的时间进程显示DCs、中性粒细胞和巨噬细胞相对于淋巴细胞的早内流。这表明气道长期暴露于CS会导致急性和慢性炎症变化的混合3.那6..目前的结果可以用先天性和适应性免疫反应来解释,因为所有增强的细胞类型都出现在两种类型的免疫反应中。
在三个主要肺动器中观察到逐步烟雾诱导的直流募集和直流激活。这些是支气管肺泡腔,气道墙和肺实质。为了针对Bal和Lung Parench中的DCS,目前的作者使用了基于Havenith的工作的战略等等。25谁利用肺泡巨噬细胞的明亮自发荧光,从单核细胞和DCs有效地分离它们。进一步详细阐述了该直流隔离程序,并证明了BAL和肺部实质的DC和单核细胞DC前体在CD11C中+低自发荧光细胞分数的门24.所选细胞表达了高水平的CD11c,CD11b和MHC II,因此可以被认为是髓样DC和/或其立即前体。在暴露于空气或CS(数据未显示的数据),发现表达低水平CD11c和NO CD11b和NO CD11b的血浆酸性DC在暴露于空气或CS的肺部(数据未显示)。通过免疫组织学确认了Bal隔间和肺部薄壁组织中的DCS的增加。烟雾诱导的DC在活性状态下,如MHC II和T细胞共刺激分子,CD40和CD86的上调所示。目前的调查结果与Casolaro一致等等。26在吸烟者的BAL液中发现Langerhans细胞(LC)的聚集,LC是一种已知的树突细胞亚群。太阳系等等。27也观察到吸烟者肺部LC的增加。也有研究认为肺LC组织细胞增多症中CS吸入与含有大量LC的肺间质肉芽肿有关28.LC肉芽肿病与肺实质破坏相关。在一项短期实验中,烟草暴露小鼠的肺LC密度增加,并与LC肉芽肿病肺部特征的组织病理学改变相关15.与目前的研究和以前的其他研究相比,罗宾斯最近的报告等等。29描述了接触烟草烟雾后肺DC数和激活的减少,损害了对腺病毒感染的免疫反应。造成这些结果差异的原因尚不清楚,但这可能是由于流式细胞术方法的差异或接触烟雾的强度(罗宾斯的研究中,低剂量=每天两支烟)等等。;高剂量=本实验中每天20支)。CS对DCs的影响是否具有剂量依赖性,尚需进一步研究。
烟雾暴露后的肺部DC的升高表明该细胞在COPD发病机制中可能作用。现在,DC在先天免疫反应中起主要作用,是呼吸道中最强大的抗原呈递细胞。在导电通气道的上皮内和下方的DC网络理想地定位以对毒性吸入剂进行哨兵作用。目前作者假设烟草烟雾,含有许多毒性低分子量化合物,直接激活支气管肺泡DC。活化的DCS可以分泌整个炎性趋化因子,诱导更多DC和其他炎症细胞的招生和激活30.,如巨噬细胞、中性粒细胞、自然杀伤细胞和淋巴细胞。烟雾诱导直流激活的另一个机制可能涉及热休克蛋白的刺激,热休克蛋白是在细胞坏死时释放的31.这是由体外表明烟草烟雾提取物导致气道上皮细胞的剂量依赖性凋亡和坏死32.
在接触烟草烟雾后炎症细胞释放的众多介质中,蛋白质水解酶是其中之一。中性粒细胞,特别是巨噬细胞是蛋白酶的丰富来源33,激活后释放中性粒细胞弹性蛋白酶、组织蛋白酶和基质金属蛋白酶,降解细胞外基质(ECM)成分。最终的ECM分解产物(例如Elastin片段)有可能吸引和激活更多的炎症细胞,诱导恶性循环。在这种慢性Cs暴露的鼠标模型中,BAL隔室中的中性粒细胞数量增加,但不在肺部。这与COPD患者的观察结果一致,其中在痰和BAL流体中发现了活化的中性粒细胞增加的数量,但在肺实质中观察到肺部的相对较小的增加34.CS-暴露小鼠的BAL和肺动器中巨噬细胞数量的显着增加使得COPD患者中痰,BAL流体和肺实质中的巨噬细胞数量增加。巨噬细胞可能在COPD中发挥关键作用,因为它们被CS提取物激活并不仅分泌弹性酶,而且分泌着许多炎症趋化因子(例如白细胞介素-8和CXCR3-配体),吸引中性粒细胞和CD8+分别是t淋巴细胞33.观察到肺部肺部血管血管数量的年龄相关的减少。Shibata制造了类似的观察等等。35在对照组小鼠Mac-3的肺中+细胞数量随年龄增长而下降。
与人类对烟草烟雾的炎症反应相反,CD4显著增加+T细胞而不是CD8+观察t细胞6.那36.两人都有类似的观察结果等等。37和vitalis.等等。38在豚鼠体内CD4+T细胞增加与烟雾暴露有关,而CD8的增加+T细胞与病毒感染的存在连接。
值得注意的是,BAL中总细胞、DCs和巨噬细胞的增加表现出进行性的双相反应。史蒂文森也发现了类似的情况等等。39在烟雾暴露的大鼠模型中。从接触烟雾的第四周开始,在接触烟雾的动物和对照组动物之间观察到一种“转录转移”。与这种“转变”相关的是上调和下调基因簇,包括蛋白酶和促炎靶点(例如基质金属己酶酶-12),其可参与COPD发病机制。
综上所述,似乎所有不同的炎症细胞共同导致了吸烟引起的肺损伤。然而,尽管中性粒细胞和巨噬细胞在慢性阻塞性肺疾病发病机制中的作用已被明确强调,烟雾诱导的肺炎症中树突状细胞的显著增加促使我们进一步研究这些细胞在慢性阻塞性肺疾病病理生理学中的潜在作用。当然,由于本研究主要是描述性的,这一假设还需要进一步的研究,包括慢性阻塞性肺疾病动物模型的功能研究。
致谢
作者要感谢E. Castrique,C.Snauwaert,K.De Saedeleer,A. Neessen,I. de Borle,M. Mouton,G. Barbier和P. Barbier和P. Degryze为他们的技术援助。
- 收到了2004年8月13日。
- 公认2005年4月9日。
- ©ERS期刊有限公司