抽象的
神经生长因子(NGF)是神经营养因子,对神经元的发育和存活,也是炎症的重要介质。它由白细胞介素(IL)-1β刺激的气道细胞释放。由于IL-1β诱导气道高响应性(AHR)到Tachykinin NK-1受体激动剂[SAR9会见(O2)11.,本研究的目的是确定IL-1β是否能够诱导离体支气管释放NGF,以及NGF是否参与IL-1β诱导的AHR。
il - 1β(10 ng·毫升−1;21°C;15 h)增加了人离体支气管中NGF的释放在体外,并且,在器官浴研究中,人支气管的反应[SAR9会见(O2)11.] -substancy p(0.1μm)。这些反应之间发现了显着的相关性。由IL-1β诱导的AHR被阻断的抗人NGF抗体废除。最后,NGF(1 ng·ml−1;37°C;(0.5 h)引起[Sar显著增加9会见(O2)11.] -substance p响应。相比之下,它没有改变对乙酰胆碱的最大收缩。
总之,目前的研究清楚地表明,神经生长因子可能参与诱导气道高反应interleukin-1β,它支持neuro-immune相声这可能是活跃在人类的航空公司,气道高反应的发展,表明神经生长因子是活跃在哮喘气道。
神经生长因子(NGF)是一种神经营养因子,对神经元的发育和生存至关重要1,2.最近建议用作炎症的重要介质3.- - - - - -5.特别是在气道,动物研究表明NGF有助于气道高反应性(AHR)的发展。首先,NGF阻断抗体消除致敏和受激小鼠产生的AHR6.此外,AHR由气道中NGF的组织特异性过表达诱导7,8.同样,NGF本身也能诱导豚鼠气道的高反应性在体外9和体内10..然而,尽管NGF在哮喘中表达增加,但缺乏NGF促进人类AHR的证据4,5.
以前的研究报告说,白细胞介素(IL)-1β在几种动物模型中诱导AHR11.- - - - - -13..此外,Barchaszet al。14.IL-1β导致AHR对NK-1快速激肽受体激动剂[Sar9会见(O2)11.[人类孤立的支气管中的-substancy p(sp)。这种超反应性的机制尚不清楚。在培养人类气道细胞中进行的实验中,IL-1β从成纤维细胞诱导NGF的释放15.,支气管平滑肌细胞16.以及气道上皮细胞17.,18..但是,IL-1β是否能够从人支气管诱导NGF的释放离体尚未报道。
因此,本研究的目的是确定:1)IL-1β是否能够诱导人离体支气管释放NGF, 2) NGF参与AHR。
方法
人支气管组织的制备
手术组织从42例肺癌(27名男性,15名女性;平均值±SD.年龄61.0±1.8岁)。该方案得到了当地伦理委员会的批准(Comité de Protection des Personnes se Prêtant à la Recherche Biomédicale,凡尔赛,法国)。切除后,取人支气管切片置于含氧的Krebs-Henseleit溶液(成分:NaCl 119 mM, KCl 4.7 mM, CaCl)中22.5毫米,KH2宝41.2毫米,NaHCO3.25毫米和葡萄糖11.7毫米)。取肺黏附组织和结缔组织后,制作相同支气管环(5-7 mm length×0.5-1 mm内径),随机分成两组19..在血红素,嗜素和甘油蛋白染色的液体剪下的级微米用5μm固定在10%甲醛盐水中的5μm石蜡切片的液体氧化丁染色的直径。
将支气管环段在室温(21°C)在IL-1β的情况下在室温(21°C)中置于1ml krebs-henseleit溶液中(21°C)(10ng·ml−1)如先前报告所述14.,15..孵育后,采用成对的支气管进行收缩研究,并将上清液在-80℃下等分,直到NGF测量。在另一组实验中,抗人NGF阻断抗体或无关免疫球蛋白(Ig)-g抗体(200-500ng·ml−1;在服用收缩研究之前,R&D Systems Europe,Lille,法国在21℃下同时孵育至IL-1β,在21°C下孵育15小时。
外源性NGF (0.01-1 ng·mL−1将支气管环段置于4°C Krebs-Henseleit溶液中过夜。直接在器官浴中进行NGF预处理30分钟后的收缩研究。
实验的程序
支气管环段悬浮在含有Krebs-henseleit溶液的5ml器官浴中,含有95%的o2-5%的公司2并保持在37摄氏度。每一种制剂连接到一个等距力位移传感器(UF1;Piodem,坎特伯雷,肯特,英国)和EMKA放大器(EMKA技术,Les Ulis,法国)。张力的变化被记录在测谎仪上。将制剂以1.5 g的初始张力悬浮,每10分钟洗涤3次,并在1-1.5 g中再平衡30分钟。
快速激肽NK-1受体激动剂的收缩反应[Sar9会见(O2)11.] - sp进行了研究。冲洗支气管环段,应用乙酰胆碱使其最大收缩。0.1µM的[Sar9会见(O2)11.在不干扰快速激肽NK-2受体的情况下,选择-SP来获得最大的NK-1收缩反应,选择3 mM乙酰胆碱浓度来获得最大的反应20..
ELISA的量化NGF蛋白
用IL-1β (10 ng·mL)预处理15 h的人离体支气管上清定量NGF−1)或溶剂。在制造商的说明(Promega,Madison,Wi,USA)之后,使用了商业NGF特异性,高度敏感的双座ELISA套件。简要介绍96孔免疫电镀液(MaxisorpTM值,Nunc,Roskilde,丹麦)涂有涂层缓冲液中的多克隆山羊抗人NGF抗体(25mM碳酸盐缓冲液; pH9.7)。在4℃下孵育过夜后,洗涤板(20mM Tris-HCl,150mM NaCl,0.05%(v / v)Tween-20; Sigma-Aldrich,St Louis,Mo,USA),并孵育阻断缓冲液1小时。将上清液和标准重组人NGF稀释液在37℃下温育6小时并洗涤。大鼠单克隆抗人NGF抗体(0.25μg·ml−1)在4°C孵育过夜,洗净。抗大鼠辣根过氧化物酶IgG抗体孵育2.5 h,加入底物(3,3 ',5,5 ' -四甲基联苯胺0.02%和过氧化氢酶0.01%)。加1 M磷酸10 min后停止比色反应,在450 nm处重复测量光密度。检测范围为3.9 ~ 500 pg·mL−1.
结果表达及统计分析
所有值都表示为平均值±扫描电镜.收缩响应以g表示,作为乙酰胆碱(3mm)诱导的最大收缩的百分比。NGF蛋白水平表示为PG的NGF·Mg−1湿重组织。从原始数据分析组间的差异,使用非配对双尾t检验,和双向方差分析与学生-纽曼- keuls检验时,超过两个变量进行比较。数据被认为有显著差异,p<0.05。NGF释放(%增加)与[Sar]收缩之间的相关性9会见(O2)11.-SP(%增加)采用回归分析评估。决定系数(r2)从回归曲线确定。
毒品
使用的药物是9会见(O2)11.] -SP,重组人IL-1β(BACHEM,BUBENDORF,瑞士),重组NGF,抗人NGF阻断抗体和无关IgG抗体(R&D Systems Europe)。将IL-1β和NGF以0.075μm和20μg·mL的浓度溶解在蒸馏水中−1分别在-80℃下等分,分别在-80℃下等分直至使用。将所有药物溶解在蒸馏水中,进一步稀释在克雷斯 - HiseLeit溶液中。
结果
IL-1β对NGF释放和AHR的影响
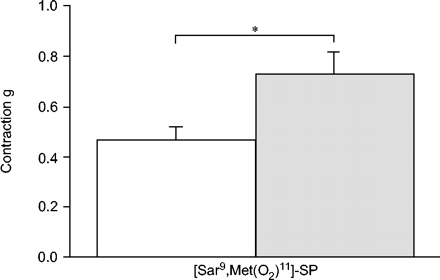
如前所述,与IL-1β一起孵育的人孤立支气管变为对NK-1受体激动剂的高反应性[SAR9会见(O2)11.] - sp(0.1µM)。有效率增加了64.8±13.3% (p<0.001;n = 24;图1⇓).相反,对于IL-1β和盐水,对乙酰胆碱(3mm)的反应不变(2.12±0.18和2.21±0.17g; n = 24)。
白细胞介素(IL)-1β的影响(10ng·ml−1;15小时;[Sar . 21°C]对收缩反应的影响9会见(O2)11.- P物质(SP)(0.1µM)。□:没有il - 1β; :用IL-1β。n = 24. *:P <0.05。
:用IL-1β。n = 24. *:P <0.05。
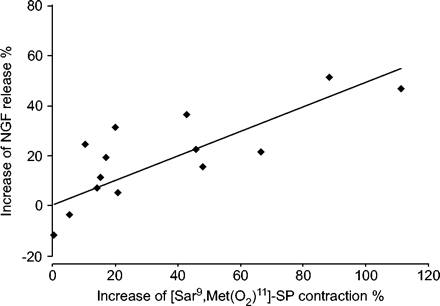
与此同时,在IL-1β处理后的孵育培养基中,NGF水平显著增加(3.1±0.5和2.5±0.5 pg·mg),尽管增幅不大−1分别用IL-1β和生理盐水湿重组织;n = 14;p < 0.05),即。NGF释放增加28.8±5.2%。NGF释放与支气管对IL-1β的高反应性呈正相关(r2= 0.59;p < 0.05;图2⇓).
收缩增加百分比与[SAR的百分比9会见(O2)11.] -substancy p(sp)(0.1μm)和白细胞介素(IL)-1β诱导的神经生长因子(NGF)释放的百分比增加。
NGF阻断抗体对IL-1β诱导AHR的影响
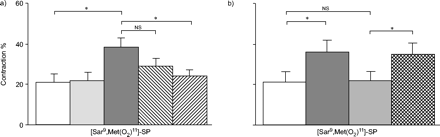
预孵育抗人NGF阻断抗体(500ng·ml−1完全消除IL-1β诱导的AHR对Sar的影响9会见(O2)11.-SP (50 ng·mL, p<0.05)−1;无花果。 3⇓),但对该NK-1受体激动剂的收缩反应没有影响本身.在类似的条件下,与不相关的IgG抗体预孵育对IL-1β诱导的高反应性没有影响[SAR9会见(O2)11.-SP反应,或对这种激动剂的收缩反应。
a)抗人NGF阻断抗体的影响(抗NGF; 200-500 ng·mL−1).□:控制; :抗NGF(500 ng·ml−1);▪:白介素(IL) 1β;汉化:IL-1β +抗ngf (200ng·mL)−1);IL-1β + anti-NGF (500 ng·mL .−1).b)无关免疫球蛋白(Ig)-g(500ng·ml−1il -1β诱导的高反应性[Sar9会见(O2)11.- SP (substance P)(0.1µM)。□:控制;▪:il - 1β;碱:IgG (500 ng·mL .−1);
:抗NGF(500 ng·ml−1);▪:白介素(IL) 1β;汉化:IL-1β +抗ngf (200ng·mL)−1);IL-1β + anti-NGF (500 ng·mL .−1).b)无关免疫球蛋白(Ig)-g(500ng·ml−1il -1β诱导的高反应性[Sar9会见(O2)11.- SP (substance P)(0.1µM)。□:控制;▪:il - 1β;碱:IgG (500 ng·mL .−1); : IL-1β + IgG (500ng·mL)−1).结果以收缩百分比表示与乙酰胆碱(3毫米)。数据均值±扫描电镜n = 8实验。ns:不可思议;*:P <0.05。
: IL-1β + IgG (500ng·mL)−1).结果以收缩百分比表示与乙酰胆碱(3毫米)。数据均值±扫描电镜n = 8实验。ns:不可思议;*:P <0.05。
AHR到NGF.
单纯外源性NGF对支气管平滑肌张力无影响。神经生长因子(0.01 ng·1毫升−1)诱导浓度依赖性增加[SAR9会见(O2)11.] -SP响应,最大增加77.0±31.5%,1ng·mL−1(P <0.05; n = 11;图4⇓).相反,NGF (1 ng·ml−1)没有改变乙酰胆碱(3mm)诱导的收缩(2.7±6.1%,不显着)。
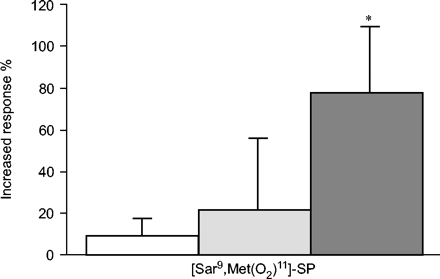
神经生长因子(NGF;0.01, 0.1, 1 ng·mL−1;30分钟)对人离体支气管对速激肽NK-1受体激动剂的反应9会见(O2)11.- P物质(SP)(0.1µM)。□:+ NGF 0.01 ng·mL−1; :+ NGF 0.1 ng·ml−1;▪:+ NGF 1 ng·mL−1.结果表示为从控制值增加的百分比(平均值±扫描电镜n = 11实验)。*:P <0.05与控制。
:+ NGF 0.1 ng·ml−1;▪:+ NGF 1 ng·mL−1.结果表示为从控制值增加的百分比(平均值±扫描电镜n = 11实验)。*:P <0.05与控制。
讨论
目前的结果表明,IL-1β诱导人离体支气管释放NGF,这种释放与对[Sar]反应的增加有关9会见(O2)11.IL-1β诱导的sp。此外,用抗ngf阻断抗体预处理可以消除il -1β诱导的高反应性。最后,NGF本身可诱导人离体支气管对速激肽NK-1受体激动剂的高反应性[Sar]9会见(O2)11.] -sp.在体外.
本研究旨在研究先前报道的炎症条件下AHR的新机制在体外通过促炎细胞因子IL-1β14..在培养的人气道细胞中,IL-1β诱导气道平滑肌细胞释放NGF16.上皮细胞,17.,18.和肺成纤维细胞15..目前的研究表明,IL-1β也能够从人支气管中刺激来自分离的环段的NGF的释放。因此,NGF的过度表达可能是由于在通过IL-1β刺激时从支气管结构细胞,平滑肌,上皮细胞和/或成纤维细胞的NGF释放增加。以前提交了人支气管细胞的分泌表型,以前作为积极参与炎症的气道细胞的新特征15.,18.,20..另外,增加NGF的释放也可以衍生自免疫/炎症细胞,例如淋巴细胞,巨噬细胞或肥大细胞4因为这些细胞也被报道分泌NGF4,21.- - - - - -23..这表明炎症条件可能会出现增加的NGF水平体内.的确,在人类中NGF的过度表达已经被报道过了体内,在IL-1β增加的情况下,特别是在哮喘中24.- - - - - -27..
本研究还证明,抗NGF阻断抗体废除了对[SAR的过度反应性9会见(O2)11.人支气管IL-1β诱导的sp在体外这表明NGF参与了AHR对IL-1β的发展。最近在动物模型中有一致的建议,当给予一种阻断抗ngf抗体可防止小鼠因电场刺激而发生过敏原诱导的AHR6或衰减对敏化和挑战性大鼠卵巢的过敏原特异性早期气道反应28..此外,据报道,外源性NGF在几内亚猪中自身诱导AHR体内9,29.和几内亚猪的气管高光反应性在体外10..本研究结果表明,NGF还诱导人类孤立的支气管中的剂量依赖性AHR在体外.
这些结果提供了潜在的机制,用于解释哮喘患者气道中NGF蛋白的上调的调查结果,尽管已经证明了这些事件之间没有因果关系。实际上,来自哮喘患者的血清中,增强的NGF水平报告,具有更严重的过敏性哮喘患者的NGF水平最高,显示出高度AHR24..此外,与对照对象相比,在从哮喘学中,在哮喘的支气管肺泡灌洗液中检测到NGF蛋白的局部上调,呈AHR,如对照受试者相比25..在轻度哮喘患者中,这些NGF水平在过敏原刺激后进一步增强26..此外,之前的数据来自卡塞尔等.27.支持支气管中NGF的上调作为哮喘中过敏原反应的早期事件,与AHR增加相关。事实上,在轻度哮喘患者暴露于低剂量的过敏原后,在气道组织中检测到NGF转录本和AHR的增加27..所有这些发现表明,NGF水平的增加与AHR密切相关。目前的结果为一个潜在的因果机制提供了支持,因为他们证明外源性NGF负责增加人类支气管的反应性,而IL-1β诱导的高反应性被抗NGF抗体消除。相反,在最大的乙酰胆碱反应中,没有观察到收缩增加。这与先前在人离体支气管中的研究结果一致,即IL-1β既不会改变乙酰胆碱的最大反应,也不会改变乙酰胆碱浓度-反应曲线14..这可能与报告的AHR的异质性联系在哮喘中的收缩激动剂,现在明确建立,但仍然无法解释30..
NGF诱导AHR的机制尚不清楚。据报道,NGF可激活免疫/炎症细胞,如肥大细胞、淋巴细胞、嗜碱性粒细胞或巨噬细胞,以及结构驻留细胞,如成纤维细胞或气道平滑肌细胞5.NGF还能够敏感神经元,并诱导感觉神经元中的汀肝的增强生产。这是由猎人展示的et al。31.,在豚鼠实验中证实NGF诱导气管内给药24小时后气道感觉神经元表型转换,并增加神经元胞体SP含量。此外,霍伊尔et al。7结果表明,转基因小鼠在气道中过表达NGF后,气道神经过度支配,SP含量增加。然而,这些效应在NGF注射后数小时到数天内被观察到,涉及的转录机制可能无法解释在目前的实验条件下NGF的快速效应。在制备过程中没有感觉细胞体,这进一步支持了这一证据,表明在这些条件下,NGF在人支气管中的作用机制不是SP含量的上调在体外.然而,一个早期的局部机制可能被提出,也在皮肤痛觉过敏机制中观察到。事实上,当NGF直接应用于痛觉传入时,在孤立的皮肤神经准备中降低了热刺激的阈值32..同样地,NGF应用于背根神经节神经元10min后,能够消除辣椒素反应中观察到的快速耐受性,甚至增强这些反应33..有趣的是,NGF还近期显示了大鼠炎症疼痛的模型中,对背根神经节的感觉神经的伤害者致敏进行短期影响34..因此,NGF可能有助于增加神经元过度尺寸,可能通过香草受体-1激活而没有转录事件,包括它们增加的表达35.,36..这些结果,加上目前的数据,表明NGF能够诱导神经元和细胞的早期转录后变化,这可能与组织的“致敏”有关。1,37.- - - - - -39.,并提出AHR和痛觉过敏的发生机制。
总之,目前的结果清楚地表明,白细胞介素-1β释放的神经生长因子参与了这种细胞因子诱导的气道高反应性,并支持在人支气管的高反应性中神经免疫交叉谈话的证据。
- 收到了2004年4月23日。
- 接受2005年3月16日。
- ©ers Journals Ltd