摘要
通常假设当吸入或吸出的病原体压倒呼吸道宿主防御系统时,细菌肺炎的发展变得可能,但该假设尚未在临床上或实验测试。
本研究评估了与实验性肺炎骨膜炎肺炎的发生的接种剂量,并估计中位数有效剂量导致健康新西兰白兔中肺炎(平均值±SD.4.75±0.25 kg (n = 27))采用支气管内增加剂量接种家兔链球菌引起的肺炎在以下96小时内观察到肺炎发作。诊断方法基于临床肺部感染评分,修饰用于兔子。
接种S.肺炎用剂量> 4.60日志10.CFU在兔子中发育肺炎更可预测(高达90%)。低剂量的细菌未能引起肺炎的80%的接种动物。通过物流回归,探测分析和簧片麦克解方法估计中值有效剂量,对应于4.32,4.38和4.67日志10.CFU分别。
推测,当接种剂量超过抗菌保护阈值时,肺炎球菌肺炎的发育变得更有可能变得更容易发生疾病发病的危险因素。
社区获得的肺炎仍然是一个常见的和潜在的危及生命的疾病1。在美国,每年有2-300万个案例2,占800,000个住院,不仅昂贵3.,也与大量死亡率相关4.。这些趋势显示没有减速的迹象。链球菌引起的肺炎是社区获得的肺炎最常见的细菌原因,在20-75%的病例中被鉴定5.。这些微生物中广泛的疾病和抗生素耐药性的增加要求迫切需要调查影响肺炎球菌性肺炎发病的致病性和宿主防御机制6.。
肺炎球菌肺炎的动物模型通常用于评估肺抗菌宿主防御机制和肺炎中药理学研究。以前的兔子实验使用了Inculum剂量S.肺炎哪个范围3.70-9.18日志10.CFU.7.那8.。即使在实验中使用相同的肺炎球菌的血清型,这种种类的接种剂量和死亡率的大差异也使这些研究难以解释和比较。对文献的详细审查未揭示专门研究细菌剂量与肺炎的关系,临床或实验药物的肺炎。虽然经常推测细菌造物剂剂量必须压倒肺炎患者发病的呼吸道宿主防御系统9.那10.,这个假设尚未测试。因此,本研究通过调查接种剂量的关系来测试这一假设S.肺炎和肺炎发病的概率。第二个目标是估计这种微生物的剂量,可在50%的健康新西兰白兔(ED)中引起肺炎的发育50.)。
材料和方法
动物和研究设计
该研究经受美国陆军外科研究所(Sam Houston Fort Sam Houston,San Antonio,TX,USA)研究理事会和动物护理和使用委员会批准的,该稿件在提交出版物之前审查了稿件,以及指导方针采用实验动物的护理和使用11.。
男性特异性病原体新西兰白兔(平均值±SD.4.75±0.25千克(n = 27))从Myrtle的Rabbitry,Inc。(汤普森站,美国TN,美国)获得。抵达后,所有动物在单个笼子中被置于检疫7天和喂养自由根据目前的建议,用水和商业饲料。在开始每个实验之前,美国陆军外科研究所的兽医研究所确认每只兔子的健康状况。
如前所述,肺炎球菌性肺炎被诱发7.那8.。简而言之,在实验的当天(第1天),兔肌内麻醉用氯胺酮 - 木嗪混合物麻醉,并用3.5mm袖带的气管内管口口口气。对于接种细菌,无菌地通过气管内管引入无菌硅氧烷导管(直径1mm)进入气管并轻轻插入直至它到达支气管,并通过中缓慢地冲洗1mL新鲜制备的肺炎球菌(见下文)导管。将动物放置在直立位置,以便于通过重力促进远端肺泡迁移。一切努力最大限度地减少麻醉和插管的潜在不利影响。在觉醒和拔管后,将动物放回其各个笼子中,单独的离其他兔子分开,并免费获得食物和水。使用的接种剂量范围为3.27-7.56日志10.CFU·ML.-1。不使用较高的剂量,因为它们总是导致兔子的肺炎7.。总共24只兔子使用20个不同的接种剂量。阴性对照组包括三只兔子,该兔子被插管但未接种S.肺炎。
血清型3.S.肺炎(American Type Culture Collection (ATCC®)6303;本研究采用ATCC, Manassas, VA, USA)制备接种剂。这种血清型常见于社区获得性肺炎患者9.,广泛用于实验医学,包括动物肺炎模型10.那12.。通过在营养肉汤中生长生物体过夜,然后根据美国陆军外科研究所的标准操作程序将有机体在-80℃下冷冻1ml等分试样来制备生物体的工作量。
接种前一天,一小瓶S.肺炎从冰箱中除去ATCC 6303并在室温下解冻,1毫升股票移液到25ml脑心输注肉汤中。将培养物在37℃下在5%CO中孵育18小时2。在接种的当天,过夜培养物在美国陆军外科研究所的标准操作程序中连续地以生理盐水稀释至所需的浓度。
为了确认将活细菌接种到兔子中,此时也进行了活的板数,用于测定接种浓度。用胰蛋白酶大豆琼脂上的标准涂抹板方法重复进行板数。将所有板在37℃下在5%CO中孵育18-24小时2。然后计算菌落,并计算每mL的CFU的数量。所有实验中只使用一个菌株。
在接种后,在96小时内观察到兔子的兔子(第2-5天)。肺炎的诊断标准基于德尼文等。13.方法和临床肺部感染分数14.,略微修饰以考虑兔生理(更高的正常体温,等等。)以及组织微生物和形态学发现。在本研究中,当六个中至少有四个时,接受了肺炎的诊断(IE。> 50%)诊断标准组结果为阳性(表1⇓)。通过比较通过组织学数据获得的结果来验证这种诊断方法的准确性。在以前的出版物中,组织学结果被认为是肺炎验证的黄金标准15.那16.。
程序
计算机断层摄影(CT)成像(Aquilion 16; Toshiba America,Inc。,纽约,NY,美国)在静脉内氯胺酮 - 木嗪麻醉和24,48,72和96时进行〜10分钟进行〜10 min的机械通气 h after inoculation. The width of the slices was 0.5 mm. CT scans were performed during breath-hold (inspiratory phase) and always before bronchoalveolar lavage (BAL) in order to avoid the possible appearance of artefacts caused by any lavage fluid remaining.
BAL是根据先前公布的儿科医生的建议进行的19.。简而言之,每次CT扫描在氯胺酮 - 木嗪麻醉下立即进行BAL。在所有操纵期间使用无菌技术。通过使用最多五个不同的8ml等分试样为0.9%氯化钠(38℃)来收集BAL流体(BALF)。当返回5ml流体时被认为是完整的。获得的BALF标本在5分钟内转移到实验室以进行微生物和细胞评估。使用Millipore滤光器(Millipore Corp.,Bedford,Ma,USA)和细胞引诱量分离BALF中的细胞。使用ABX PENTRA 120血液分析仪(Horiba Abx,Montpellier,法国)确定BALF中的细胞计数和分布。
对于BALF的微生物评估,标本在生理盐水中顺序稀释,然后在胰蛋白酶大豆琼脂平板上涂抹,每平方根和每块稀释板两板20.。在含有5%绵羊血液和Macconkey II琼脂平板的胰蛋白酶大豆琼脂平板上,灌洗样品也被划分,用于培养分离。将所有平板在37℃的5%CO中孵育过夜2。使用标准微生物方法鉴定所有分离物21.。S.肺炎鉴定基于含有5%绵羊血液的胰蛋白酶大豆琼脂平板上的α溶血的存在,并将抑制区域≥14mm对5-μg乙基氢碳碱椎间盘(Optochin试验; BBL; BBL; BBL; BBL; BBON DICKINSON,SPARKS,MD, 美国)。
为了确定总血细胞计数和动脉血气水平,在接种后,在初始导管和24,48,72和96小时内从动脉导管获得1ml血液。使用ABX PENTRA 120血液分析仪和AVL OMNI模块化系统(AVL医疗器械; Roche Omni Systems,Indianapolis,Indianapolis,Indus,USA),在样品收集后立即进行总细胞计数和动脉血气分析。根据目前的临床标准收集并分析所有血液样品24.。
在每个动物死亡或安乐死时采集肺组织标本。执行安乐死通过静脉内施用兽医安乐死解决方案(致命加上vortech Pharmaceuticals,Dearborn,Mi,USA)。进行尸检,使肺部无菌地除去。对于每个肺叶,使用得分网格注意到宏观方面7.基于人体形态学发现(表2⇓)。将整体宏观评分作为所有瓣膜宏观评分的总和计算,在胸腔积液的情况下加2点(范围0-29)。这种方法已经成功地用于肺炎的兔子模型7.那8.。当一个叶中的分数> 2时,肺炎的宏观诊断被定义为正阳性。
每种叶片的两部分具有最大宏观病变的无菌地收获(一个用于定量培养物,一个用于组织学研究),以便比较组织学和细菌发现。对于病理研究,根据标准方法,在缓冲福尔马林中固定标本。兽医病理学家,尚未了解动物和细菌数据,评估了标本。病变分为五类:水肿,肺泡炎,支气管炎/支气管内,坏死和纤维蛋白血管炎。只接受了支气管炎/支气管炎和坏死作为肺炎的组织学确认与先前的研究一致18.。
对于标本的细菌学加工,无菌在尸检上拍摄的组织样品迅速发出,以除去任何表面污染物,然后放入预先称重的Stomacher 80袋(Seward,伦敦,英国)并称重以确定组织重量。将生理盐水加入到斯普尔赫赫袋中,并以正常速度将组织混合在狭口80实验室混合器中。所得溶液连续稀释,并如前所述进行定量板计数和培养分离20.那21.。使用标准微生物方法鉴定所有分离物。S.肺炎鉴定基于含有5%绵羊血液的胰蛋白酶大豆琼脂平板上的α溶血的存在,并将抑制区域≥14mm抵抗5-μg乙基氢COLKEINE盘(Optochin试验)。
结果
基于目前的诊断方法,18 of 24(75%)接种的动物开发S.肺炎肺炎。对照组没有发现肺炎的迹象。临床,放射,实验室,微生物学,宏观和显微疾病症状的临床剂量和分布,导致肺炎患者确认⇓。观察到大多数兔子在接种剂量时发育肺炎S.肺炎≥4.60日志10.CFU,暗示在当前模型中,这种接种水平代表了使肺炎最发作最可预测的临界值。为了统计测试这种假设,将所有接种的动物分为两个亚组:具有<4.60日志的接种剂量的那些10.CFU,以及剂量≥4.60日志的CFU10.cfu。在第一亚组中,5只家兔中只有1只(20%)发生肺炎,而在第二亚组中,19只家兔中有17只(89.5%)肺炎阳性。经Fisher精确检验,两组间发病率差异有统计学意义(p = 0.0021)。为了确认诊断方法的准确性,这两个亚组之间的差异被测试使用事后剖析肺组织组织病理学发现,被认为是最可靠的呼吸机相关肺炎的最可靠标准之一15.。微观评估显示,当接种剂量<4.60对数时,五种动物中的一只发生了肺炎10.当接种剂量≥4.60原木时,CFU和19个中的17个阳性是肺炎10.CFU(表3⇓)。通过Fisher精确测试测量的这两个亚组之间的差异也很显着(P <0.05)。
日志之间的重要关系10.使用Logistic回归和探测分析观察肺炎发作的剂量和概率(P <0.05;图1⇓)。计算编辑50.使用Reed-Muench方法得到的值是4.67 log10.CFU在目前的兔子模型中。通过逻辑回归和探测分析验证了这种近似,显示了ed50.是4。32和4。38的对数10.CFU分别(图1⇓)。
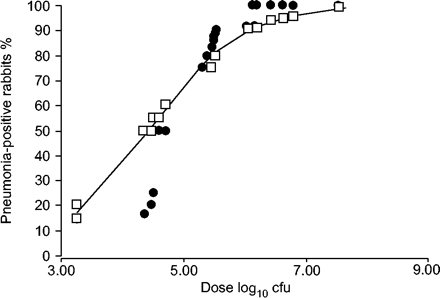
用芦苇 - 麦克风(•),探测(□)和物流回归(----)分析,肺炎发病的概率作为剂量的函数。CFU:形成殖民地的单位。
根据表3所示数据⇑,根据Sackett测试了肺炎患者确认不同诊断标准的敏感性,特异性,正负预测值和准确性等。24.。在本研究中,CT、显微和宏观形态征象三个标准的可靠性最高(表4)⇓)。红色充血是生病动物中最常见的宏观病变(16个,共18个(89%))。在所有生病的兔子中观察到肺炎的组织学表现。胸部CT扫描在本研究中具有高度敏感和特异性。当代高分辨率断层扫描的使用表明,兔肺的渗透性相对较小,具有明显的传统胸部射线照相诊断优势,出于解剖学原因,在兔子中非常复杂。CT扫描的代表性图像,肺炎阳性兔的宏观和组织学变化如图2所示⇓-⇓⇓5.⇓。
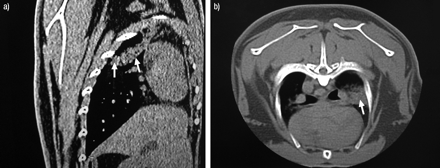
在右上叶(箭头)的兔子胸部的兔胸部的层压扫描(箭头):a)横向位置和b)横截面图像。
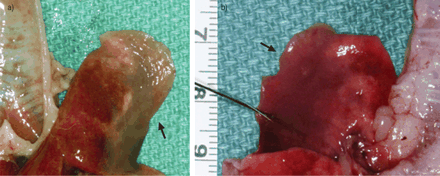
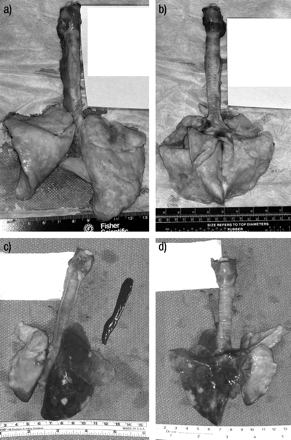
兔肺从与计算的断层摄影成像相同的动物裂隙(见图2⇑)在右上凸起(箭头)中显示肺炎:a)前视图,b)后视图。
A,B)正常兔肺:a)后视图和b)前视图。心脏,血管和食道被烧蚀;气管没有纵向解剖。C,d)右上型,中叶(红色血管)的梗塞肺炎(红色充血)样品:c)后视图和d)前视图。气管的后壁是解剖沿中间线的宽度。脓性痰存在于气管的上三分之一。脾脏的形状和尺寸正常。
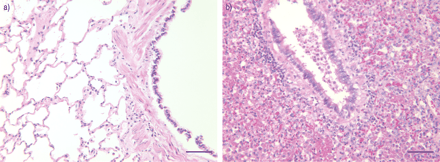
兔肺组织学:a)正常肺和b)支气管内黄酮,具有内含内炎性细胞和碎片,血浆螺旋炎炎症细胞和粒子充满纤维蛋白。血红素和曙红染色;内部尺度条=35μm。
讨论
目前的一项研究表明了关系S.肺炎接种剂量和肺炎的发育。当接种剂量超过4.60日志时,肺炎发病的概率显着增加10.cfu。低于该水平的剂量未能在大多数(80%)的健康新西兰白兔中引起疾病。根据芦苇和后勤回归方法,在目前的实验条件下,ED50.估计为〜4.32-4.67日志10.CFU为此兔子模型。在本研究中还测试了一种新的肺炎肺炎肺验证的新诊断方法,似乎是可接受的。
这些观察结果使人们有可能推测实验的发展S.肺炎大多数健康新西兰白兔的肺炎可能需要阈值剂量。在本研究中,剂量> 7.56日志10.没有使用Cfu,因为它们在动物中已经显示出100%的发病率和100%的死亡率7.那8.那17.。本发明的组织学数据类似于兔子中观察到100%致死剂量的兔肺组织样本的描述S.肺炎7.。
本研究中用于肺炎确诊的诊断方法采用了临床实践中常用的几个标准。在以往的研究中,任何单独用于诊断呼吸机相关性肺炎的标准,如BAL、胸片、肺组织细菌定量培养,甚至组织学表现,都不是高度敏感和特异性的诊断工具25.。在没有普遍认可的诊断金标准18.,对实验性肺炎的各种诊断程序的真正准确性仍然未知。肺炎的组织学体征通常被认为是最可靠的18.那25.,但最常使用事后剖析肺炎确认。因此,需要更好的肺炎患者肺炎诊断方法。在目前的兔模型中,假设是肺炎的几种不同标准将增加诊断的可靠性。因此,本诊断方法似乎对兔子肺炎确认敏感和可接受,并且应该适应其他实验模型。在使用的标准中,发现高分辨率CT扫描是兔子肺炎患者中最可靠的,具有与组织学数据类似的敏感性和特异性,但具有允许在活动物诊断的优势。
成人兔似乎是肺炎球菌肺炎的研究。新西兰白兔天然不易受到影响S.肺炎感染7.那26.,保证观察到的病理因实验操作诱导。此外,所用兔子的尺寸(4.75±0.5千克)允许使用用于临床小儿实践的设备,仪器和技术,并且兔子容忍每日BAL和血液采样。与之前的报告相反27.那28.,本研究使用免疫活性的动物,使肺炎发育更加自然。伤害S.肺炎在本研究中使用的是临床分离物,其具有常见的血清型,并且在相对长的时间(接种后高达96小时高达96小时)观察接种的兔子。此外,本模型通过自然气道接种到支气管,这具有其他优点。它比气溶胶滴注更可重复7.那29.而且比经皮气管内注射或经胸注射创伤小7.那31.。因此,据信,目前的兔模型是人类肺炎的良好模仿。
本模型的一个重要特征是它能够接近严重的人类下呼吸道炎症,特别是术后肺炎。本病常因病原微生物从上呼吸道脱位至气管所致。同样,本模型也直接从入侵阶段开始。因此,目前的实验模型也应该与呼吸机相关肺炎相关,其中主要的微生物入侵途径是通过气管内管32.。
微生物和宿主之间的成功生物平衡是正常肺部通常的情况,但这种关系可以在各种条件下容易地破坏,例如快速和大规模的细菌入侵,使得预先存在的主体防御不足,因此,允许疾病。更好地了解动物模型中正常肺部的局部防御应该导致对侵入微生物的治疗改善。因此,本研究支持该假设,即接种剂量应包括作为肺炎发育的危险因素。确认此假设的其他研究似乎有保证。
致谢
作者要感谢F.Quance-Fitch for组织学评估,以及A. Delgado,S. Alexander和D. Hardin,在实验室研究和动物护理中得到帮助。作者还要感谢J. Ward在统计分析中提供帮助。
- 已收到2004年8月3日。
- 公认2004年11月10日。
- ©ers Journals Ltd