摘要
粘液纤毛清除率受损是囊性纤维化(CF)的标志。早期形态改变首先出现在小气道。采用颗粒沉积法对11例轻中度肺疾病的年轻CF成人进行了肺清除率的研究。
放射性标记的Teflon颗粒(6μm)吸入极其缓慢的吸入流量,0.05 L·S.-1.在吸入后立即测量肺保留,并在四次最多21天进行测量。将结果与来自健康受试者的数据进行比较。
在CF患者中,24小时的肺保留量为67%(95%置信区间58-76),而健康受试者为48%(42-53)。CF患者在第1-7天的清除较大,22%(15-29)与健康受试者相比,14%(12-16)。在第7天至第21天的CF患者和缓慢间隙阶段的健康受试者之间没有观察到差异,代表小气道清除。CF患者的粘膜膜受损导致24小时保留增加和延长的快速间隙阶段。
这项研究的结果并不支持当前作者的假设,即囊性纤维化患者的小气道清除速度比健康受试者要慢。此外,数据表明粘液纤毛运输不是主要的清除机制在小气道。
气道表面液体的睫状活性和流变学决定了粘液间隙(MCC)。MCC是肺中的主要防御机制之一,以除去不溶性沉积材料。这种间隙机制迅速,导致吸入小时内的较大气道的间隙,并且认为在健康受试者的24小时内完成。24小时后静置的任何颗粒代表肺泡沉积1那2.然而,之前使用浅丸技术对健康受试者的研究以及使用极慢吸入流量(0.05 L·s-1)和6µm颗粒,导致颗粒沉积在小气道内,表明24 h后可能有相当一部分颗粒残留3.-5.这些研究提供了一种证据,即气管支出区域中的快速间隙阶段之后是秒,较慢的间隙阶段,但仍然比肺泡间隙更快。该中间间隙阶段提出代表沉积在支气管区域中的颗粒的间隙,已被列入人类呼吸道的修订剂量模型,由国际放射保护(ICRP)通过6..
囊性纤维化(CF)是一种遗传性疾病,其特征是由于离子在呼吸道上皮细胞中的运输缺陷,在气道中产生和积累大量黏度增加的粘液。这导致MCC受损,伴有复发性细菌感染、慢性炎症、支气管扩张和气道损伤。最终导致呼吸衰竭和过早死亡。CF的早期形态学改变首先见于终末细支气管7..
在CF患者中研究MCC最广泛使用的方法是使用用伽马相机技术检测的放射性标记颗粒。肺中吸入的放射性标记气溶胶的去除率可以通过串行伽马相机图像确定高达24小时。这些研究表明,MCC在中央和周边地区都受损8.那9..MCC受损也是原发性纤毛运动障碍(也称为静止纤毛综合征)患者和慢性支气管炎患者的特征。在这些组中,咳嗽能有效地清除集中沉积的颗粒。24 h的保留部分(Ret24)甚至可能比健康人还小10那11.然而,当粒子沉积在小型气道中时,与健康受试者相比,在这些患者组中,72和96小时的保留级分在这些患者组中显着较大12那13.
目前的研究采用一种主要在小气道内沉积颗粒的方法,研究了年轻成人CF的肺清除。根据Weibel模型A定义小气道14,为第9-15代,对应细支气管,有纤毛上皮,直径<2毫米。本研究的目的是:1)检验24 h的颗粒保留分数(Ret24)更大;2)与健康受试者相比,CF患者的一天和第21天之间的间隙较慢。它也是假设RET24随着肺部疾病的严重程度的增加和第1天到第21天之间的清除率下降。
材料和方法
主题
11名患者(四名男性)参加斯德哥尔摩CF中心,年龄18.7±2.5(平均值±sd)YRS,具有轻度至中度的肺病,满足了纳入标准和自愿进行研究。纳入标准是:1)诊断儿童时期的CF与症状的CF和阳性汗液试验(> 80 cl−更易·L-1)15;2)年龄≥15岁;3)临床病情稳定;4)无器官移植史;而且没有怀孕。人体测量数据,基因型和Bhalla评分16.以及目前的细菌培养和炎症参数(免疫球蛋白G)以及在研究开始时拍摄的肺功能数据如表1所示⇓.所有患者都检测了32种常见CF突变,包括瑞典最常见的3种,ΔF508, 3659delC和394delTT。3例患者被认为是长期单独殖民金黄色葡萄球菌还有7个病人假单胞菌铜绿假单胞菌其中两个也曾被殖民金黄色葡萄球菌在他们的下气道。当同一病原体定期从痰或鼻咽拭子中分离并连续6个月时,该患者被认为是慢性定植。所有患者均接受口服溶黏剂(溴己新和乙酰半胱氨酸)和每日1 - 2次吸入沙丁胺醇和乙酰半胱氨酸,并将黏液动员和疏散运动作为日常物理治疗的一部分。所有患者均未开系统性糖皮质激素或接受雾化rhDNase或雾化抗生素治疗。尽管临床情况稳定,但有3例CF患者(No。6、9和11)c反应蛋白略有升高;6在一个注射。在轻微的低度感染迹象时开始抗生素治疗17.2例中度肺部疾病患者在暴露期间自发咳嗽,并在21天的研究期间报告了自发咳嗽。其他CF患者仅在日常理疗时主动咳嗽。他们的咳嗽没有经过时间的详细监测。
通过强制呼气图评估肺功能(肺功能实验室2100;SensorMedics,阿纳海姆,加利福尼亚州,美国)。同样的技术助理指导每个CF患者。气道阻力(R.aw),使用呼吸技术在全身体积描记器内测量(transmurural Body Box 2800;SensorMedics)。所有肺功能参数均按全杰尔提出的标准确定等等。18.在间隙之前,评估数据,并根据其肺功能进行分类,一组具有轻度肺病(强迫呼气量(一秒钟)(FEV)1预测的70%;n = 6),一组有中度至重度肺部疾病(FEV)1<70%pred;n = 5)。
这项研究得到了卡罗林斯卡大学医院人类研究伦理委员会和卡罗林斯卡医院同位素委员会的批准。向所有患者和健康受试者提供有关该研究的书面信息,并告知肺部受到的放射性照射低于常规胸片的辐射剂量。所有患者和健康受试者均给予参与研究的书面知情同意。年龄小于18岁的患者获得了父母的同意。
研究设计
基于汇集的可变性数据的样本量计算sd在先前的一项研究中,比较了健康受试者和慢性支气管炎患者之间的清除率19,在每组中显示了12个个人的需求,以检测一个差异sd功率为80%。作者终于能够招募11名CF患者。CF患者和健康受试者吸入6μm单分散的Teflon颗粒标记111吸入流量极慢的铟,0.05 L·S.-1,沉积主要在小气道。在吸入测试颗粒后,立即测量了口腔、喉咙、肺部和胃部的放射性。在吸入后24小时、第7天、第14天和第21天测量肺潴留。对放射性核素的本底活动和物理衰变进行了修正。区域沉积数据是用卡罗林斯卡研究所开发的一个模型估计的。在数据评价中,研究期间分为两个阶段。第一个快速清除阶段定义为0 ~ 24 h之间的清除,主要代表大型和中型气道,第二个缓慢清除阶段定义为第1天到第21天之间的清除,主要代表小型气道。
出于伦理原因,目前的数据与当前作者先前研究中年龄相近的健康受试者的数据进行了比较。他们是非吸烟者,非哮喘患者,肺功能正常。健康受试者和CF患者均使用相同的设备进行颗粒生产和吸入。在整个研究过程中,两组患者使用了相同的吸入模式,并使用相同的检测器在肺部测量了放射性5.那20.那21.平均拟人化和肺功能数据(平均值±sd)健康受试者的情况见表1⇑.
吸入测试粒子和测量放射性
制造并标记的Teflon颗粒111在(半衰期68小时)通过旋转圆盘技术22.平均空气动力直径为6.2µm20..受试者戴着鼻夹,以坐姿吸入这些颗粒。受试者首先在房间外做一个中等深度的呼气,然后从房间里尽可能深地吸气。使用放置在气溶胶室和吹口之间的气速计监测流量,并以图形方式记录。在每次吸入室内粒子之间,受试者在室内吸入和呼出数次。平均吸入流量为0.045±0.003 L·s-1.早前已显示呼出的放射性为0-2%23.暴露的持续时间为6.3±2分钟,每次吸入的持续时间约为30秒。
紧接着吸入24小时后,用两个配备准直器的127×51 mm NaI晶体测量放射性。肺内平均放射性沉积为0.1 MBq。作者认为,热点沉积可能受到限制,因为粒子主要是通过沉降而不是碰撞沉降。瑞典辐射防护研究所(Swedish Radiation Protection Institute)还在吸入后24小时和第7天使用带有三个大型NaI探测器的全身扫描仪测量了放射性20.那24.在第7天、第14天和第21天,当胃肠道的放射性与肺部的放射性相比不显著时,受试者仰卧位使用更敏感的肺部计数器。
肺沉积的理论计算
利用卡罗林斯卡研究所开发的ki模型对理论沉积数据进行了检验,ki模型基于来自肺动力学工作组模型的撞击和沉积方程25,以及由Weibel提出的人类气道模型A(包括0-23代,其中0-16代是纤毛的)14.在KI模型中,吸入参数,如气道尺寸,潮气量,吸气流动,吸气后暂停和呼气时间可以在宽范围内更改。几代0-23的直径由相同的因子改变,并且每代计算沉积。选择该因素,使其提供了计算的气道阻力(使用Poiseuille Lave),其与测试受试者中测量的耐测定值相同,减去0.05kPa·s·l-1,代表口腔、喉咙和喉部的气道阻力。ki -模型被证明是高度可重复性的,当将ki -模型的预测与其他更精细的模型进行比较时,没有重大差异,如在ICRP 66出版物中修改的人类呼吸道模型和萨尔茨堡大学模型(USBG)使用蒙特卡罗粒子输运和沉积代码(IDEAL)24.两个CF组和健康受试者平均R.aw分别为0.228、0.242、0.155 kPa·s·L-1,分别。维度因子分别为0.56、0.55和0.65,用于模拟吸入流量为0.045 L·s的气道阻力-1,暂停2 s,分别为1.25,1.04和1.50升的潮量。
统计分析
描述性数据用平均值±表示sd并将结果作为平均值(95%置信区间(CI))。采用非参数秩和检验评价组间差异和Spearman相关系数;P <0.05被认为是显著的。在第2周和第3周,测量值通过插值调整到第14天和第21天,在少数情况下,当测量点相差1天时。
结果
意味着FEV1CF患者为2.4 L(1.7-3.4)对应72±17%的pred,而健康受试者为4.2 L(3.2-5.9)对应105±13%的pred。中重度肺病变的CF患者出现生长P.铜绿假单胞菌在其痰液中,在研究开始时拍摄,与肺病中的CF组中没有比较(表1⇑),尽管后一组的病人被认为是慢性殖民P.铜绿假单胞菌在他们的下气道。
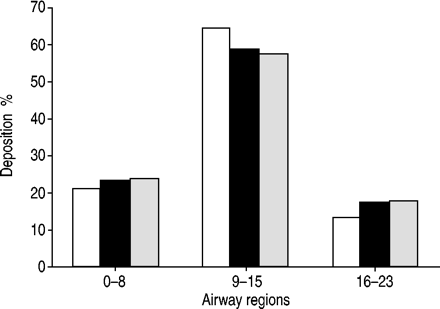
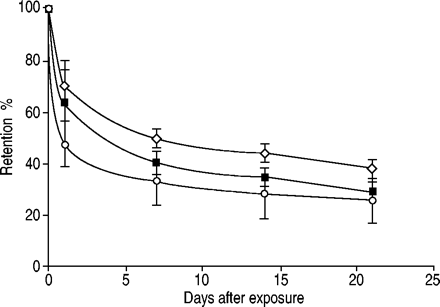
根据理论模型计算的不同气道区域沉积显示,主要沉积在小导气管内(9 ~ 15代)。沉积模式在健康受试者和CF患者之间没有差异,也没有根据肺部疾病在两组CF之间有差异(图1)⇓).受潮湿腐烂24CF患者中显着高(P <0.001),与健康受试者相比,67%(95%CI 58-76),48%(95%CI 42-53)。随着时间的推移肺保留的差异在第21天,34%(95%CI 30-38)和26%(95%CI 21-31)(P <0.01)时仍然更高图2⇓).CF患者第1天到第7天的清除分数更高,为22% (95% CI 15-29),而健康受试者为14% (95% CI 12-16) (p<0.05)。
计算区域沉积,大气道(代表0-8代)、小气道(代表9-15代)和肺泡区(代表16-23代)以极慢的吸入流速吸入6-µm颗粒(0.05 L·s)占肺沉积总量的百分比-1)的平均气道阻力在健康受试者(□)和两个囊性纤维化(CF)组(■:囊性纤维化伴轻度肺部疾病;烧嘴句子:CF伴中度肺疾病),视其肺功能而定。
使用极慢吸入流量(0.05 L·s-1)比较囊性纤维化患者与轻度(>70% 1秒用力呼气量(FEV)1) pred;▪)和中等(<70% FEV1pred;⋄)健康受试者的肺部疾病(〇)。
所有受试者在24小时后均有显著的清除。健康受试者和CF患者在21天内显示清除分数为55%,Ret为50%24,分别。第7天与第21天的斜率线性回归无统计学差异。第7天、第14天和第21天肺潴留,百分比为Ret24,健康受试者和两个CF组之间相似(图3⇓).Ret有轻微的差异,但变化更大24在两个CF组之间,63.8±16.4%(平均值±sd)肺病患者患者,患有中度严重肺病的患者的70.8±5.9%相比,(p = 0.4)。在24小时后,第7天和第14天和21天之间的保留在两个CF基团之间不同(P <0.01)。患有轻度肺病的CF组中的第2患者的患者患有RET2488%,但1周后,保留的分数达到与同一组中其他患者相同的水平。另一位患者(6号),ONI.v..抗生素(研究7天后结束治疗),以及有生化恶化体征的患者(9号),清除活性与其他患者无差异。如。不在外部范围内。
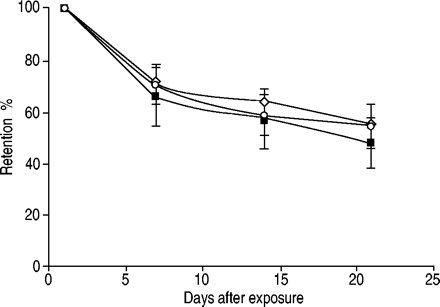
缓慢的清除阶段使用极慢的吸入流量(0.05 L·s-1).清除作为时间的函数在24小时后正常化到滞留,比较囊性纤维化患者轻度(>70%一秒用力呼气量(FEV)1) pred;▪)和中等(<70% FEV1pred;⋄)健康受试者的肺部疾病(〇)。24小时标准化是省略第一个快速清除阶段的标准程序。
讨论
本研究的目的是调查CF患者小气道的长期清除情况。最重要和意外的发现是,从第7天到最后一个测量点第21天,CF患者和健康受试者的清除情况相似。此外,与健康受试者相比,CF患者在24小时时发现颗粒保留比例增加。
吸入颗粒的估计肺部沉积在很大程度上沉积在小型气道中,并且计算出的区域沉积在CF患者(无论肺病)和健康受试者之间预测了非常小的差异。大ret.24(CF患者中67%的患者在健康受试者中的48%相比)还表明小型气道中的沉积较大,而不是使用正常吸入流动的沉积。如果粒子的粒子部分沉积在肺中,则为RET24CF患者可能比健康受试者小26,由于CF患者可能通过他们的日常物理治疗和自愿咳嗽更快地清除中央气道。如果在肺泡区沉积颗粒的级分,则24小时后的间隙比目前研究中测量的间隙慢得多27.在哮喘、慢性支气管炎或CF患者中,气道可能会因支气管痉挛、水肿或粘液分泌而变窄,导致湍流,增加大气道的嵌塞,从而减少对小气道的穿透。相比之下,在小气道中,气流的速度较慢,这是由于大的总截面积和颗粒沉积在气道表面的重力作用。通过使用极慢吸入流(ESI)和相当大的颗粒,沉积在小气道的部分通过沉降增加。即使FEV有差异1在CF患者和健康受试者之间,ESI被证明是强健的,对气道阻塞和通气不均匀相当不敏感28.
更大的遗憾24CF患者与健康受试者的比较是预期的。Ret的变化也更大24在所有时间点与健康受试者进行比较。此外,Ret之间的差异更大24并在CF患者的第7天保持颗粒。作者的解释是,他们的快速许可阶段未在24小时内完成,但在第一天之前的某个时间续,可能在某些时候完成。在第1天的患者中,24小时的较大保留部分也可能导致第1天的速度更快消除 -7。在健康的受试者中,快速的间隙(从前24小时到前24小时)主要受粘膜和纤毛活性的粘蛋白自动血清的主导。在CF患者中,这种间隙机制受到干扰,并且CF患者可能会通过更不可预测的咳嗽清除来弥补其受损的MCC。咳嗽可能对从实现必要气流速度的较大气道的间隙产生更大的影响,从而允许对快速间隙相的影响。患者(第3号),谁有RET2488%,然后在第7天清除50%的残留部分到下一个测量点,这可能是这种咳嗽清除作为MCC受损的代偿机制的一个例证。
缓慢清除阶段,从第7天开始测量,Ret的百分比24,在CF患者和健康受试者中相似。所有受试者继续以相同的速度清理气道,24小时后平均清除50%的滞留颗粒。CF患者和健康受试者之间的相似性可能是由于动力不足。为了增加CF患者和健康受试者之间差异的力量,他们也进行了独立的t检验,结果相同。MCC可能不是小气道清除率的主要决定因素。虽然咳嗽作为一种机械力可能会影响其他次级清除机制,但咳嗽对小气道清除的作用可能有限。在一项采用与当前研究类似的方法的研究中,研究人员对杜氏肌营养不良儿童的细支气管清除进行了长达72小时的研究,这些儿童肺部健康,但肌肉力量严重减弱。与持续气道正压治疗的对照实验相比,72 h时的滞留量显著降低(但24或48 h后不是如此),这表明机械力可以影响小气道的长期清除29.其他清除机制,如肺泡巨噬细胞的吞噬作用、测试颗粒通过上皮细胞的穿透或颗粒在一定时间内重新转移到凝胶层,也可能有助于缓慢清除阶段的清除30..
一些因素可能与肺清除率有关,如年龄、性别、BMI、肺功能和气道阻力。CF和健康受试者的年龄和性别相似,尽管他们不是单独匹配的。BMI有所不同,但这一因素被作为营养状况的标志,作为CF疾病的结果,而不是作为一个与肺潴留相关的因素。然而,仍然有可能BMI本身,独立于CF疾病的因果关系,具有独立的影响,可能影响了观察结果。然而,目前的作者没有发现健康受试者的BMI和肺潴留之间的任何相关性。
FEV1慢性阻塞性肺疾病患者与健康对照者的气道阻力也有显著差异。如前所述,这些因素对沉积的影响有限。然而,FEV1%pred作为预测肺部间隙的单个因素,是不确定的,方形相关系数(r2FEV之间)1% pred和Ret24是0.27。根据其肺功能,将CF患者分为两种亚组,测量为FEV1%预测在组水平上是否更严重的肺部疾病与更高的肺潴留相关。目前的细菌气道定植显示与FEV降低有关1% pred。CF组伴有中重度肺疾病(FEV1<70%的pred)具有更高的负担P.铜绿假单胞菌在他们的气管里,这与之前的发现一致31.Ret差异无统计学意义24在两个CF组之间。这可能是由于快速间隙阶段的巨大变化(反射来自大气道的清除)。在后面的测量时间点,这种差异变得显着,具有较大的肺保留,在患有中度严重肺病的CF患者中的沉积%。似乎在前24小时期间,在前24小时期间较慢的患者可以由于第一周的空间越来越多,但肺病的程度会影响快速清除阶段(第一周)的肺部潴留。肺病患者更严重的肺部疾病较长的吸入材料。延长的快速间隙阶段是由气道中的细菌定植引起的,或者如果较慢的间隙主要与疾病相关,则必须确认CF。具有已知对短期MCC的刺激作用的支气管扩张剂Terbutaline可能影响了快速间隙阶段的结果,但不应影响来自小型气道的缓慢间隙32.
早期的清关研究,大多是伽马摄像机研究,在CF患者上使用了正常的吸入流动。当正常吸入流(> 0.2 L·S.-1),颗粒主要沉积在较大的气道或肺泡区,仅在较小的气道中有很小的程度,与颗粒大小无关24.呼吸模式和使用的颗粒大小高度影响肺内沉积的位置。沉积可能是测量MCC最重要的决定因素26那33.因此,难以评估对MCC的不同研究,其中沉积的部位可能具有变化。据作者所知,这是第一次参见CF患者长期间隙的研究。
结论
与健康受试者相比,CF患者在24小时的沉积中沉积中沉积的颗粒的保留较大。CF患者显示出比第1天和第7天之间的健康受试者更快的间隙,表明咳嗽补偿后的快速间隙阶段仍在继续,以完成大于中等尺寸的气道的清理。CF患者和健康受试者均在第7天和第21天显示出显着的间隙,主要从小气道代表间隙。CF患者和健康受试者之间的这种慢间隙阶段没有差异。CF患者可能具有改变的粘液流变学,可以影响粘液运输,但这种机制似乎不是来自小型气道的关键的关键机制。肺病的严重程度似乎影响了快速的间隙,而不是缓慢的间隙阶段,其24小时后的较大保留级分的趋势较大1% pred。
具有极高的吸入流动,6μm粒子可以瞄准小型气道。这种吸入方法可以是临床效用,用于选择性地瞄准用于沉积治疗药物如抗生素或基因治疗的小型气道。需要进一步的研究来确认除了在小气道中的粘蛋白间隙以外的机制。类似于目前研究睫状体活性患者小型气道的长期间隙的研究可能有助于阐明清除机制。
致谢
这项研究得到了瑞典心肺基金会、欧洲委员会的资助。FIS5-1999-00214, BIODOSE)、卡罗林斯卡研究所基金会和斯德哥尔摩儿童福利基金会的Free Mason。作者要感谢L-L。Söderström,临床科室。生理、南斯德哥尔摩总医院、I. Östergren、瑞典辐射防护局(SSI)、U. Bergsten、秘书、M. Lundberg、卡罗林斯卡研究所环境医学研究所、放射性测量指导。
- 收到了2003年10月27日。
- 公认2004年10月10日。
- ©ers Journals Ltd