摘要
最近的一项研究表明,阻塞性睡眠呼吸暂停/低通气综合征(OSAHS)患者的日间心率变异性降低。在本研究中,假设OSAHS患者呼吸暂停/低通气和夜间自主活动周围的交感神经平衡发生改变。
频率和时域分析的RR间期监测交感迷走神经活动无创。14名未经治疗的OSAHS患者和7名健康受试者接受了夜间多导睡眠描图检查。
低(LF)和总(TF)频率功率在呼吸暂停/低呼吸结束前后增加2 min (LF 229±38 ms)2,tf345±45 太太2)与未受干扰的睡眠相比(LF106±18 太太2,tf203±23 太太2).高频功率增加不显著。与未受干扰睡眠(lfn52±2单位,HFn 48±2单位)相比,LF增加比例高于HF增加(正常LF (LFn) 67±1单位,正常HF (HFn) 33±1单位)。呼吸暂停/低通气前后RR持续时间无变化(RR 904±28 ms)。在唤醒诱导前后(lf260±45 ms),低频和低频功率增加较大2, TF 390±65ms2)与自终止(LF 161±31)相比 太太2,tf249±40 太太2)呼吸暂停/低通气;与未受干扰睡眠相比,两组的LF和LFn增加显著,HF功率差异不显著。自终止呼吸暂停/低通气前后的RR间期较长(RR 914±29 与未受干扰的睡眠相比,差异不显著。RR间期频谱功率不受事件类型的影响。RR持续时间缩短(912±28) LF、HF和TF功率增加(lf111±16) 太太2, HF 62±6ms2,tf173±21 太太2(RR 1138±91 ms, lf57±3 ms)2,hf 35±3 ms2,tf91±6 太太2).LFN和HFN没有显着变化。
呼吸暂停/低通气时交感神经活动增加。交感神经-卵磷脂平衡的反复夜间波动和夜间自主活动的总体增加可能对睡眠呼吸暂停患者心血管疾病的发展具有重要意义。
K.Dingli得到了欧洲呼吸学会的研究奖学金的支持。188bet官网地址
心率变异性(HRV)是RR间期的变化,可通过RR间期的功率谱分析检测。该方法已在生理和病理条件下得到广泛验证,并用作个体内部和个体之间自主心脏控制的无创测量1,2。该检测主要基于RR间期的低频(LF)和高频(HF)频带内的频谱功率变化。在不同条件下,已证明传出心交感神经流量与低频频带功率增加的相关性1,2这些研究表明,LF带功率的变化反映了交感神经心脏的激活,而HF带功率的变化反映了副交感神经、迷走神经的流出。健康受试者的RR谱与他们的外周交感神经活动进行了比较,在从腓神经经皮穿刺3.肌肉交感神经活动(MSNA)。虽然RR间期低频功率振荡的起源尚不清楚,但有人认为这些反映了脑干激活条件下的中枢紧张兴奋性交感神经输入4.这可能解释了在某些条件下(如呼吸暂停或过度通气)RR谱功率、RR持续时间与MSNA之间的解离现象5,并可反映呼吸和心脏自主调制的常见中枢控制机制。
高血压6与心肌梗死7导致HRV降低,即。LF的增加和总功率的减少。这些病症与阻塞性睡眠呼吸暂停/低尿布综合征(Osahs)的患病率有关8,9与健康受试者相比,OSAHS患者日间HRV降低10可能与这些患者心血管疾病的发展有关。
本研究通过监测RR间隔振荡和RR持续时间来调查OSAHS患者的夜间HRV。研究假设是呼吸症/低钠症与同性化变化有关。将Apnoeas / hypopnoeas周围的HRV特性与基线进行比较,对患者的无限睡眠时间。将患者的RR间隔谱振荡和RR持续时间与匹配的正常对照进行比较。
方法
主题
14例OSAHS患者的多导睡眠图(平均值±标准差),年龄51±9岁 年,体重指数(BMI)29±2 千克·米−2, 7名健康受试者,年龄50±10岁,BMI 28±2 kg·m−2进行了分析。诊断基于临床症状和多导睡眠图结果。对照组的年龄和体重指数相匹配。所有受试者在其他方面都是健康的;两名患者正在服用抗高血压药硝苯地平。这项研究得到了机构伦理委员会的批准。
多导睡眠图
多导睡眠图包括脑电图(EEG)、眼电图、颏下和胫骨肌电图、心电图(ECG)、两条压电带、热敏电阻、数字麦克风和脉搏血氧仪。
评分/定义
根据rechtschaffen和Kales的标准评分睡眠11.呼吸暂停定义为口鼻气流持续停止≥10 s。低通气被定义为在前2分钟内,与10‐s峰值相比,气流>降低50%,持续≥10 s,并与氧饱和度≥3%或觉醒有关12. 唤醒评分基于美国睡眠障碍协会(ASDA)的定义13修改持续时间阈值,设置为1秒。每小时睡眠中与呼吸暂停-低呼吸相关的脑电图唤醒次数为呼吸唤醒指数(RAI)。在所有数据中,12%的数据由于人为因素或R波形态异常而被排除在外。
第一次分析分析
根据RR间期分析,无创监测呼吸暂停/低通气结束时的自主活动1. 使用快速傅里叶变换(FFT)算法进行频域分析。在时域中,评估平均RR间期持续时间。
呼吸暂停/低通气的结束被确定为气流增加/恢复。为了评估呼吸暂停/低呼吸引起的RR间隔频谱功率的波动,我们在以呼吸暂停/低呼吸结束为中心的2分钟窗内,与未受干扰睡眠的2分钟时间段进行了比较。为了避免相邻呼吸暂停/低呼吸暂停或唤醒对RR间隔功率谱的影响,只有当2分钟窗与任何进一步的呼吸事件、唤醒或唤醒时间不重叠时,才选择事件进行分析(图1)⇓).窗的选择是根据频域RR区间分析的建议1,以最大限度地检测与呼吸暂停/低通气相关的功率变化,并保持信号平稳。2分钟段被视为准确分析0.04–0.40的下限 赫兹频带功率1. 一个值得关注的问题是呼吸振荡对2分钟窗口内RR功率谱(呼吸窦性心律失常)的影响14.
信号处理
HRV参数根据欧洲心脏病学会和北美起搏和电生理学会工作组的建议进行计算1.所有数据均由自定义信号处理框架中的程序模块处理,该框架使用C语言编写,适用于Unix/Linux操作系统。
仔细编辑和目视检查心电图信号,以100%采样 Hz,有助于消除由缺失QRS波群或虚假RR间期引起的误差源。RR间期估计是通过使用“阈值二阶导数”方法获得的。作为此时间序列(转速图)是数量的函数,而不是时间的函数,RR间隔序列通过均匀间隔采样(4)转换为平滑的心率时间序列 赫兹(ΔT=0.25s)15. 为了检查心率序列的平稳性,计算每个记录中所有选定心率段的平均值和标准差。同一记录各节段的平均值变化<1计算sd,即。所选分段均满足固定要求。
频域分析
对于每个2 min段,功率谱密度(ms2·赫兹−1),即。应用韦尔奇方程计算相应心率时间序列的功率(能量)分布16方法,在移除直流分量后。该方法基于重叠加窗傅里叶变换(滑动窗口)的平均值。为了尽量减少泄漏,使用了一个50%重叠的滑动汉明窗,有128个点。2分钟心率序列的长度为480个样本,零填充用于添加n=512个样本,并划分为偶数重叠的帧。光谱分辨率和统计方差的权衡是周期图方法固有的。也就是说,通过增加汉明窗的长度,从而提高光谱分辨率,要平均的帧数减少,因此估计的统计方差恶化。或者,如果通过形成较短的帧来增加要平均的帧的数目,则光谱分辨率恶化。本研究中的汉明窗和2分钟分析窗的长度是频率分辨率和信号平稳性之间的折衷。分离峰的分辨率为0.0078 赫兹,导致0.0156 Hz区分振幅不等的相邻频率分量。FFT频带宽度为0.03125 赫兹。
权力
通过高斯集成相应的功率谱密度函数,计算LF和HF频带的电力,并以MS表示2(图。 2.⇓).在分析中不考虑低于0.04 Hz的频率,因为这些频率需要更长的数据序列来进行准确的功率估计。LF功率和HF功率分别用归一化单位(LFn和HFn)表示,计算每个频带功率相对于其总和的百分比1,2.正常化权力强调自主神经系统的两个分支的控制和平衡行为,增加敏感性1以及与伴随的MSNA变化的相关性3..归一化将总功率变化对低频和高频分量值的影响降至最低1.
时域分析
在2分钟的段期间计算原始停滞的平均RR持续时间。RR持续时间的降低是一定程度的中央介导的心脏激活1,3..
评估了皮质唤醒和事件类型对这些标志物的影响。为了评估RR持续时间和溶光电在Osahs患者中发现的变化的重要性,将这些与健康受试者进行比较。在患者的整个夜间录制之间进行了比较相对健康对照,基于在整个睡眠期间不重叠2分钟滑动窗的分析;觉醒时期被排除在外。对每个受试者进行了至少1.5小时的分析。每个受试者贡献一个数据点对每个自主标记的平均值。
统计分析
对患者内部比较进行配对t检验。未配对t检验评估患者与健康对照组之间的差异。接收机工作特性(ROC)曲线17评估自主神经标记物区分每位患者呼吸暂停/低通气和未受干扰睡眠的能力。为了评估再现视觉评分的准确性,计算每个标记物和多导睡眠图的真阳性(TP)、真阴性(TN)、假阳性(FP)和假阴性(FN)读数、敏感性TP/(TP+FN)和特异性TN/(TN+FP)。ROC曲线是通过逐步改变研究参数的正常和病理状态的决定阈值来创建的。计算曲线下面积(最小值0.5表示无差别,最大值1.0表示完全差别)及其se18.曲线下的区域表示随机选择的ECG间隔的概率,以区分apnoeas /低钠缺失从未受干扰的睡眠。使用跨越21个受试者的2分钟轧制窗口的平均值,通过判决阈值的逐步改变构建ROC曲线,以证明标记物能力区分Osahs患者和健康受试者的能力。P <0.05考虑了显着性。值显示为平均值±SEM。
后果
患者的平均睡眠效率为睡眠时间(SPT)的88±2%。健康受试者的平均睡眠效率为SPT的92±3%(表1) 1.⇓).共对2288例呼吸暂停/低通气患者进行评分。在14名患者中,87±3%的呼吸暂停/低通气发生在非快速眼动(NREM)睡眠第1和第2阶段,6±2%发生在慢波睡眠(SWS)阶段,10±2%发生在快速眼动(REM)睡眠阶段。在四名患者中,SWS期间未对呼吸暂停/低通气进行评分,在两名患者中,REM睡眠期间未对呼吸暂停/低通气进行评分。平均呼吸暂停/低通气持续时间为25±2 s在评分事件中,48%为呼吸暂停,52%为低通气。患者的平均呼吸暂停/低通气指数为29·h−1(范围10-55·H睡觉−1),平均rai20·h−1(范围7-47·H睡觉−1); 32%的呼吸暂停/低通气通过视觉无法检测的方式终止。
跨患者比较
在2288例评分为呼吸暂停/低通气的患者中,214例(平均值±sem 15±2)符合“非重叠”标准,并被选择用于分析。这些事件与541例(39±8)非发作期(基线睡眠)进行比较。在14例患者中,77±4%的分析呼吸暂停/低通气发生在NREM第1和第2阶段(12±1),13±3%发生在SWS(2±1)8名患者在SWS期间未分析呼吸暂停/低通气,3名患者在REM睡眠期间未分析呼吸暂停/低通气。平均呼吸暂停/低通气持续时间为26±4 s
LFn增加,HFn功率降低2 与未受干扰睡眠相比,事件终止前后的分钟数(p<0.001)。绝对低频功率的增加(p=0.002)与总功率的增加相关(p=0.01);绝对高频功率没有显著增加(p=0.3)。与未受干扰的睡眠相比,患者呼吸暂停/低通气前后的平均RR持续时间没有变化(p=0.9;表1) 2.⇓).
基于LFn和HFn功率值的ROC曲线显示,这些自主活动的光谱功率标记物可以很好地区分呼吸暂停/低呼吸和未受干扰的睡眠,曲线下面积在0.74-1.00之间(p<0.03), se在0.0001-0.09之间(表3)⇓).ROC曲线对于自主活动的措施是相同的,因为它们的计算基于每个频带功率相对于其总和的百分比:
 高se值反映了某些患者呼吸暂停/低通气值与基线睡眠之间的差异。某些曲线中使用的少量样本可能导致se增加。
高se值反映了某些患者呼吸暂停/低通气值与基线睡眠之间的差异。某些曲线中使用的少量样本可能导致se增加。
皮质微觉醒,呼吸暂停相对低通气
在14名患者中分析的214例APNOEAS /低钠癌,154名(11±1),即。72%的患者因可见皮质唤醒而终止,60例(4±1),即。28%,是诱导爆发症/低钠症。与自我终止ApnoeAs /低okeAs相比,LF,TF和LFN功率较高(P <0.05),RR持续时间和HFN功率降低(P <0.05),与自我终止APNOEAS /低钠等相比(表4⇓).两组中,与基线睡眠相比,LF和LFn功率增加(p<0.02), HFn降低(p<0.001)。TF功率在唤醒-诱导前后显著增加(p=0.01),而在自我终止呼吸暂停/低呼吸前后显著降低(p=0.1);两组患者的高频功率与基线睡眠无显著差异(p>0.1;表5⇓).
其中139起,,即。65%为低通气(10±1)和75(5±1),即。35%为呼吸暂停综合征。呼吸暂停综合征和低通气综合征在任何自主神经标记物方面均无显著差异(p>0.6;表1) 4.⇓).与基线睡眠相比,呼吸暂停和低通气时的LF、TF、LFn和HFn功率存在显著差异(p<0.04;表1) 5.⇓).
患者相对健康受试者
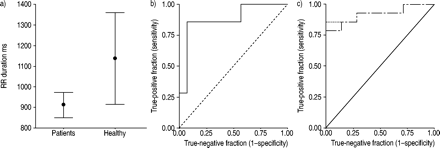
根据整个睡眠期的2分钟分析,患者的所有绝对功率值均较高(p<0.03)。与健康对照组相比,患者的LFn和HFn无显著差异(p=0.5;表1) 6.⇓).患者的平均RR持续时间下降(p=0.04;图。 3a⇓)为了评估测量参数区分患者与健康人群的可能性,根据时域和频域分析结果构建ROC曲线。每个受试者为每条曲线贡献一个数据点。RR持续时间曲线下的面积为0.88(se 0.08,p=0.006;图。 3b⇓).绝对LF和HF功率曲线下的面积相同,为0.91(se 0.06,p=0.002),表明患者和健康对照组之间的LF:HF比率相似。21名受试者的TF功率曲线下的面积为0.93(se 0.06,p=0.002)(图。 3c⇓).
讨论
这项研究的新发现是,无论觉醒可见度或呼吸事件类型如何,呼吸暂停/低通气周围的低频功率增加。基于2分钟滚动窗口的整个睡眠期RR间期分析显示,与年龄和BMI匹配的健康受试者相比,OSAHS患者的RR间期缩短,LF、HF和总功率增加。
本研究精心设计,以维持分析要求,同时能够检测呼吸暂停/低通气期间及其终止后的自主活动变化。为确保结果准确,仅对9%的评分事件进行了分析,即在终止后1分钟半径范围内与进一步事件、觉醒或觉醒事件不相邻的事件。频域分析结果表明,与未受干扰睡眠相比,呼吸暂停/低通气期间和之后交感神经活动显著增加。这种差异无法在同一节段的时域分析中得到证实,因为分析的节段包括事件期间的心动过缓和结束后的心动过速,与未受干扰的睡眠相比,事件前后的平均RR持续时间总体不变。这些发现证明了频域分析在检测由呼吸暂停/低通气引起的自主活动变化方面的优越性。
RR持续时间受压力反射环路的影响,反映相性交感神经活动,并与呼吸暂停或过度换气期间的功率振荡相互作用5.LFn功率的增加表明中枢紧张交感神经激活5,19.这与呼吸努力的增加有关,这是由于对阻塞/狭窄的气道进行吸气尝试以及在呼吸暂停/低通气结束时逐渐升高胸内负压所致。血流动力学后果是增加右心室的静脉回流,同时增加心肌收缩呼吸异常期间的心壁跨壁压和负变时态度。在呼吸后/低通气后恢复期,胸内压向零下降,导致跨壁心肌压降低,具有正变时效应。这种异常呼吸模式与ed伴随交感神经活动的增加,表现为呼吸暂停/低通气前后RR间期LF功率的增加以及呼吸后心率和血压的增加20.
目前的研究表明,呼吸暂停/低通气前后的LF功率增加与事件类型或觉醒诱导无关。这与先前观察到的在没有觉醒的情况下呼吸暂停后心率和血压增加一致21. 目前的研究发现,在觉醒诱导的呼吸暂停/低通气周围,LF功率增加更大。这与总功率增加和RR持续时间下降有关。高频功率的变化虽然不显著,但可能是由呼吸暂停/低通气和觉醒相关的呼吸振荡引起的。与基线睡眠相比,在觉醒诱导和自我终止呼吸暂停/低通气时,交感神经活动均较高。
目前的结果没有在MSNA或血压上得到验证,因为他们的监测会扰乱睡眠,影响自主活动,并不一定反映窦房结上的中枢强直交感神经交通5,19.一些建模研究表明,爆发/低钠癌对外周MSNA的影响可能与中央介导的交感神经活动不同。与基线呼吸相比,MSNA在呼吸症后直接增加和减少,平行于同情介导的中枢1920秒期间健康清醒受试者的血压和心率增加22.另一项对健康受试者的模型研究表明,与安静、有节奏的呼吸相比,在自愿呼吸暂停和过度通气期间,中枢和外周交感神经活动之间存在分离活动模式5.渡边等等。23研究OSAHS患者睡眠期间,发现MSNA增加,呼吸暂停期间血压下降,呼吸暂停后即刻MSNA和血压进一步增加。与安静睡眠相比,在呼吸暂停/低呼吸时LF功率增加,这与Keyl的结果一致等等。24,基于20分钟的窗口。
目前的研究发现,与年龄和BMI匹配的对照组相比,OSAHS患者的RR持续时间与睡眠相关减少,LF、HF和TF功率增加。RR持续时间的下降可能代表交感神经激活。这与之前使用不同标记物(如OSAHS治疗前后的血压和MSNA)对交感神经活动的评估一致,并与健康对照组进行了比较25与健康受试者相比,OSAHS患者的日间HRV降低10.在这些患者中,自主神经活动的夜间和日间变化可能导致昼夜交感迷走平衡紊乱。这与格罗特的调查结果一致等等。26世卫组织证明对α-β的血管反应降低2‐与对照组相比,OSAHS患者的受体刺激,这是与慢性昼夜过度刺激相关的外周血管受体下调的结果。
在频域分析中,本研究发现患者的总功率、低频功率和高频功率总体增加;夜间HRV的增加与交感神经和副交感神经活动的增加有关。与健康对照组相比,患者自主神经活动的两个分支均不占优势。这可能是由于在分析中使用了2‐min窗口,允许OSAHS患者的呼吸模式影响RR间隔功率谱。棕色(的)等等。14呼吸频率和潮气量对RR间隔高频功率有较强的影响,但对RR持续时间无明显影响。根据这些发现,目前检测到的患者高频功率的增加可能是分析窗口期间呼吸模式周期性异常的结果。与健康对照组相比,患者RR持续时间的平行显著下降支持了这一观点,反映了交感神经活动的总体增加,而在频域分析中对交感神经活动的检测受到呼吸模式的影响。这一因素的重要性可以通过从RR速图中消除呼吸振荡来评估,但在本研究中没有这样做。如果使用较短的分析窗口来将呼吸模式对RR间隔功率谱的影响降到最低,这些将不会基于功率谱分析的标准1并且需要针对自主活动的客观标记进行验证,如MSNA。
该研究的潜在局限性包括定义、分析的呼吸暂停/低通气的数量以及研究对象的数量。目前使用的呼吸暂停定义符合ASDA建议11.与其他定义相比,在定义中包含唤醒可能会导致与唤醒更大的联系,即。仅基于胸腹运动或鼻压。为了避免相邻的呼吸暂停/低通气、觉醒或觉醒期对RR间期功率谱的影响,仅分析了9%的评分呼吸暂停/低通气。分析的事件分布代表了总事件得分、它们在睡眠状态中的分布、引起觉醒事件的比例以及事件类型。因此,所分析的呼吸暂停/低通气周围的RR功率变化代表了整晚的呼吸暂停/低通气评分。根据ROC曲线下的面积,14名轻度至重度OSAHS患者的呼吸暂停/低通气和无干扰睡眠之间的差异是一致的。根据患者的症状和多导睡眠描记图(该综合征的典型表现)随机选择患者。因此,结果可能是稳健的,代表临床上重要的差异。
基于目前的发现,作者推测交感神经增强是由睡眠中的呼吸暂停/低呼吸引起的。这反映了大脑形态底物在调节睡眠和自主心肺功能中的功能重叠4.Zinkovska和Kirby支持假设27谁阻止了中枢交感神经介导的血管阻力的增加19针对气道阻塞,通过向猪脑室注射普萘洛尔来阻断自主神经对呼吸暂停的反应。在观察自主神经系统功能障碍和同时存在睡眠呼吸暂停的患者期间,提供了进一步的证据;“脱钩”记录呼吸周期的心率变化28.目前的研究发现,在其他健康的阻塞性睡眠呼吸暂停/低通气综合征患者中,围绕呼吸暂停/低通气的夜间交感神经活动增加可能与中枢紧张性传出神经流量增加有关。这表明,对神经调节输入的反应,夜间窦房结活动总体增加。这是支持阻塞性睡眠呼吸暂停综合征/低通气综合征患者夜间RR持续时间的缩短可能会导致夜间交感神经波动,这可能是先前证实的日间自主神经活动变化的原因10.这些观察结果可能对未经治疗的阻塞性睡眠呼吸暂停/低通气综合征患者发生心血管疾病具有病因和预后重要性。
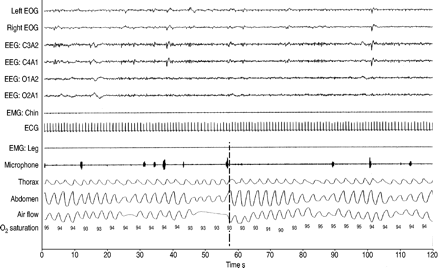
两分钟窗口(1 前一分钟和后一分钟 呼吸暂停(垂直虚线)结束后(分钟后)。在此窗口期间计算RR间期的频谱功率及其平均持续时间,并与2分钟无干扰睡眠窗口进行比较。眼电图;脑电图:脑电图;心电图:心电图;肌电图:肌电图。
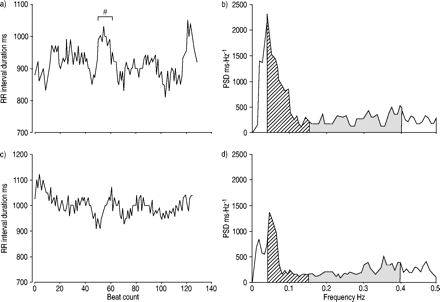
a) RR间隔时间序列(行车记录仪)2 图中呼吸暂停结束时的最小值 1.⇑RR间期数为128,平均持续时间为917.46 ms和方差2175.68 太太2.#:a.b)相同间隔的功率谱密度(PSD)曲线,使用非参数快速傅里叶变换算法计算。计算低频段(LF)的功率;└) 介于0.04到0.15之间 赫兹(峰值0.047 赫兹),功率82.56 太太2,以及高频波段(HF; )介于0.15到0.4之间 赫兹(峰值0.398 功率为60.76赫兹 太太2.c)来自同一多导睡眠图的2分钟无干扰睡眠的间隔速度图。RR间期数为126,平均持续时间为1001.2 ms和方差1481.61 太太2.d)相同睡眠周期基线PSD曲线。低频峰值功率和峰值频率为47.09 ms2和0.047 高频峰值功率和峰值频率分别为54.97 太太2和0.359 赫兹,分别。
)介于0.15到0.4之间 赫兹(峰值0.398 功率为60.76赫兹 太太2.c)来自同一多导睡眠图的2分钟无干扰睡眠的间隔速度图。RR间期数为126,平均持续时间为1001.2 ms和方差1481.61 太太2.d)相同睡眠周期基线PSD曲线。低频峰值功率和峰值频率为47.09 ms2和0.047 高频峰值功率和峰值频率分别为54.97 太太2和0.359 赫兹,分别。
a)患者(n=14)和健康对照组(n=7) RR持续时间的均值和95%置信区间。这些值用于构建b)中的受试者工作特征(receiver-operating characteristic, ROC)曲线。b)基于14名患者和7名健康对照者在2‐min睡眠相关摇窗期间的平均RR持续时间的ROC曲线。即。曲线由21分组成。曲线下的区域为0.88(SE 0.08,P = 0.006)。在此时间窗口期间的平均持续时间可以区分阻塞性睡眠呼吸暂停症/低通症综合征(OSAHS)患者和健康对照。c)RR间隔绝对低(LF)和高(HF)频率值( - - - )的ROC曲线产生0.91(SE 0.06,P = 0.002)的面积,总(TF = LF + HF)功率(═)在21个受试者中产生0.93(SE 0.05,P = 0.002)的面积。所有三个绝对功率值均匀地差异化奥沙斯患者和健康对照。固体表示参考。
致谢
作者要感谢E.Dolan提供的秘书协助。
脚注
↵编辑意见见第870页。
- 收到了2002年10月24日。
- 接受2003年8月28日。
- ©ERS期刊有限公司