摘要
1996/1997年冬季,在德国埃尔福特对53名成人哮喘患者进行的一项小组研究中,评估了微粒空气污染与哮喘药物使用和症状之间的关系。
超细颗粒的数量浓度,0.01-0.1µm直径(NC0.01 - -0.1),意思是17300厘米−3粒径为0.01 ~ 2.5 μ m (MC)的细颗粒质量浓度0.01 - -2.5),平均为30.3µg·m−3,同时测量。相关性不高(r=0.45)。环境粒子浓度与吸入β患病率之间的关系2用logistic回归模型分别分析-激动剂、皮质类固醇使用和哮喘症状,并对趋势、温度、周末、假期和误差的一阶自相关进行调整。
超过14天的超细和细颗粒累积暴露与皮质类固醇的使用有关。β2-激动剂使用与5天平均NC相关0.01 - -0.1和MC.0.01 - -2.5。哮喘症状的患病率与环境颗粒物浓度有关。结果表明,报告的哮喘药物使用和症状增加与颗粒物空气污染和二氧化氮等气体污染物有关。
本研究由GSF资助、HEI资助合同95/10和欧盟资助ENV4-CT960205资助。
在流行病学研究中,在当前浓度下一直观察到颗粒空气污染对健康的不利影响,例如死亡率和发病率的增加1,2.在基于面板的时间序列分析中,哮喘患者被认为是易感人群。在大多数研究中,在哮喘成人和儿童中观察到呼吸道症状轻微但持续的增加和肺功能下降3.- - - - - -8.相比之下,一项大型的欧洲多中心研究(污染对欧洲哮喘儿童的影响(PEACE))却显示出了负面结果9.据报道,哮喘药物的使用与空气颗粒物污染有关5,10- - - - - -12.
在德国东部,自1990年统一以来,空气污染排放已经发生了很大变化。家用煤炭供暖被天然气或石油的可控燃烧所取代。工业活动减少,机动车辆引擎得到改进。德国东部埃尔福特的粒度组成自1991年以来一直在监测。连续测量空气动力学直径<10 μ m的环境颗粒物10)、空气动力学直径<2.5µm的细颗粒(PM2.5),粒径分布在0.01–2.5之间 已进行µm和气体测试。在过去十年中,颗粒物质量和二氧化硫(SO2),但超细颗粒的数量浓度一直很高13.
美国和欧盟现行的空气颗粒物污染法规旨在减少颗粒物2.5和点10浓度。这些颗粒被吸入,流行病学研究表明会对健康造成不利影响1,2.此外,在埃尔福特哮喘成人的小组研究中,超细颗粒(直径<0.1µm)数量浓度与呼气峰值流量(PEF)的下降有关14和芬兰15埃尔福特的症状也在增加14.此外,死亡率的增加与超细颗粒(NC)的数量浓度有关0.01 - -0.1)16.这些超细颗粒数量大,但质量贡献小,不受现行规定的控制。
目前的研究旨在验证彼得斯观察到的结果等14在一个更大的哮喘成人小组,并扩大分析污染物和健康终点的数量。具体研究了环境空气污染对药物使用增加的作用。假设细颗粒物质量浓度和细颗粒物数量的增加与哮喘药物使用患病率的增加有关。特别是,它被假设粒子可能影响需求药物。此外,本研究还调查了哮喘药物是否会阻止哮喘和其他哮喘症状的报告。
材料和方法
研究设计
1996年9月至1997年3月在德国东部城市埃尔福特进行了一项小组研究,该城市有20万居民。这座城市位于图林根森林环绕的山谷中。在冬季,逆温可能会反复将空气困在山谷中。环境空气污染的主要来源是发电厂、车辆交通和家庭供暖16.
在研究期间,对空气污染物的日浓度和气象数据进行了评估。同时,研究参与者记录了他们的健康状况和药物使用情况。
专门小组研究
从1996年9月到11月,14名医生招募了67名埃尔福特的哮喘成人居民。呼吸系统疾病被医生记录在一份简短的问卷中。符合条件的参与者必须在前一年接受哮喘药物治疗,并且必须是非吸烟者。获得了所有参与者的书面同意。
在欧洲共同体(欧共体)呼吸健康调查的基础上,通过问卷调查获得了研究对象的健康和吸烟状况以及社会人口学指标的详细信息17,18.
哮喘被定义为存在,如果咨询医生诊断出哮喘,或者在最初的问卷调查中,受试者自己报告了在过去12个月内的哮喘诊断和哮喘症状。哮喘的症状包括喘息、休息时呼吸短促、醒来时出现呼吸问题或咳嗽,但没有感冒。
哮喘药物包括吸入短效β2-吸入长效β受体激动剂2-激动剂、吸入皮质类固醇、克罗摩钠、茶碱、口服皮质类固醇和N乙酰半胱氨酸。
在研究期间,参与者每天晚上在日记中记下症状的严重程度(无、轻微、严重或非常严重)和用药情况(药物名称和服用单位数)。需要记下的症状有:喘息,呼吸短促,呼吸短促伴喘息发作,醒来时呼吸困难,有痰和咳嗽。本研究详细报道了哮鸣作为一种与哮喘相关的主要下呼吸道症状;介绍了其他症状的主要结果。
研究参与者还记录了他们在研究区域之外的时间。这些日记每两周被送到研究中心,在那里检查是否可信和缺失的值。
参与时间小于30天(n=3)、报告值不可信(n=1)、发现为活跃吸烟者(n=7)或慢性阻塞性肺疾病(COPD)患者(n=3)的人被排除在统计分析之外。
曝光
埃尔福特每天测量空气污染物和天气数据。测量场地位于市区(背景场地),距离车辆交通50m14,19.用移动气溶胶光谱仪(MAS)每隔10分钟测量0.01-2.5µm直径颗粒的数量浓度19,20..MAS由两个仪器组成。第一个是差分迁移率分析仪(DMA,型号3071;TSI,亚琛,德国)和冷凝粒子计数器(CPC,型号3760;TSI,亚琛,德国),粒径范围为0.01-0.5µm;第二个是激光气溶胶光谱仪(lasx模型;PMS, Leonberg,德国),表征颗粒大小在0.1-2.5µm之间。MAS提供数量浓度数据作为颗粒直径的函数。质量分布是在体积分布的基础上估算的,假设粒子为球形,平均密度为1530 kg·m−3.
计算数浓度的日平均值。在回归分析中,选择粒径在0.01-0.1µm的超细颗粒、粒径在0.1-0.5µm的堆积模式颗粒和粒径在0.5-2.5µm的颗粒14.细颗粒(直径<2.5µm、MC)的质量浓度0.01 - -2.5)和累积模式粒子(直径0.1–0.5 μm,MC0.1 - -0.5)是根据上述数浓度计算的。
点10和点2.5哈佛影响者每天进行24小时测量。粗颗粒质量分数(PM-10 - 2.5)计算为这两个测量值的差值。点2.5日数值与计算出的MC高度相关0.01 - -2.524小时平均值(r=0.97),因此没有报告。
SO的测量2(所以2-根据紫外荧光原理,在同一地点同时进行温度和环境湿度监测。由“Thüringer Landesanstalt für Umwelt”(图林根州环境研究所)运行的监测站提供了二氧化氮每日浓度的数据(否)2) (通过化学发光)和一氧化碳(CO)(红外线吸收原理)是在距离国立环境保健研究中心(GSF)测量站2公里的城市背景站测量的。
统计分析
使用Logistic回归模型来估计日常用药流行率以及症状和控制随时间变化的混杂因素的颗粒物空气污染之间的关系。
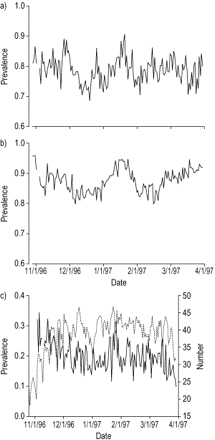
哮喘药物类别“吸入短效β”2形成和“吸入的皮质类固醇”(包括Cromolyn钠)并编码为0(不使用药物)或1(使用药物)。在研究期间,在研究期间,曾经报告使用这种药物,在参与者的亚组中计算了药物的日常患病。严重或非常严重的症状被归类为当天对各自主题的积极响应。根据所有参与者计算每个症状的日常患病率。在研究区外花费> 8小时的参与者被排除在一天的流行计算之外。50%的药物使用或症状数据的日子被排除在分析之外,以避免招聘期的效果。Figure 1⇓显示在分析中使用的三个各自的流行率时间序列。在统计分析中,可使用的天数在131-148天之间,这是由于结果、暴露和混杂变量中缺失了几天。
1996年10月25日至1997年3月30日用药和喘息患病率的时间序列,其中>为50%。一)短效β2-激动剂使用,b)皮质类固醇使用,c)喘息(-),参与者填写日记(长短不等)。
混杂因素的选择分阶段进行21.趋势被认为是一个线性、二次或三次函数,以控制总体的增加或减少,或药物使用或症状流行的季节变化。此外,采用非参数方法评估趋势的非线性。考虑了相对湿度和温度等气象因子的短期效应(线性和二次项),并检验了两者的1天滞后。非常寒冷的天气(< - 10°C)还使用分段线性项进行了调整。包括星期几的虚拟变量。区分工作日和周末的另一种方法。对每个月、圣诞节假期和流感流行期间的虚拟变量进行了测试。在使用自回归模型进行分析时,考虑到由于对每个受试者重复测量而导致的独立性不足22- - - - - -24.该模型基于广义估计方程,并控制了速率的异方差25.检测到一阶自回归结构。最终的模型,最初选择吸入短效β2-激动剂作为结果变量,控制一阶自回归、趋势(立方)、温度、周末和圣诞节假期,对分析中考虑的其他结果进行验证。采用拟合优度和估计值变化准则的组合逐步选择模型,并以线性趋势函数作为强制变量。
由于污染数据往往是连续相关的,而且由于存在滞后或累积效应的可能性,因此使用无约束滞后模型来评估滞后结构26。在最终模型中使用了移动平均值,这些模型是从同一天和前几天计算得出的。计算基于至少三分之二的非排放污染物测量值。因为可以获得2 在分析期前几周,与同一天的暴露测量相比,该程序没有增加缺失值的数量。
计算了细颗粒物(MC)的双污染物模型0.01 - -2.5)和超细颗粒(NC0.01 - -0.1),以及气体NO2,所以2由于质量浓度的测量具有很高的相关性,因此没有足够的能力来区分它们。相关系数的截止点设置为0.8,以避免极端的共线性,这将导致不成比例的偏倚效应估计。
结果
最终分析共纳入53名受试者,其中33名女性,平均年龄59.0岁;范围为37-77岁(表1)⇓).
所有53名研究参与者在研究期间都收到了哮喘药物处方。任何药物使用的平均流行率为95.2%,最低为89.5%,最高为100%。大多数哮喘患者采用吸入皮质类固醇(n=44)联合茶碱和/或吸入短效β2- 一个角度(n = 42)。五个受试者只吸入皮质类固醇或茶碱或吸入的短作用β2受体激动剂,分别;其中3例联合服用茶碱和吸入短效β2受体激动剂。总共有42名受试者报告使用了吸入短效β2角度(表1和2)。Figure 1⇑呈现研究期间吸入药物使用流行率的时间序列。
平均而言,20%的成年参与者在任何一天都报告有喘息(表2)⇓).每日哮喘患病率在10-34%之间(图1)⇑).表2.⇓显示其他症状的流行分布。
受试者参与研究的平均天数为147天(最少45天,最多188天)。排除在研究区域外的天数后,对研究的平均贡献为122天(最少25天,最多187天),相当于41份日记,平均每天在研究区域内完成。
空气污染物
所有粒子的质量浓度以及SO2在1996年12月至1997年1月期间上升(图2⇓).2天,这是美国总理的标准10(150µg·m−3)超过了。点10平均浓度为45.4µg·m−3(表2⇑).观测到的最大细颗粒质量浓度(MC0.01 - -2.5)为133.8µg·m−3,平均为30.3µg·m−3(表2⇑).累积模式粒子MC0.1 - -0.5平均质量浓度为24.8µg·m−3,占所有细颗粒物的82%(表2)⇑).超细颗粒的数量浓度平均为17,300个颗粒·厘米−3,并且范围从3,272-46,195粒子·cm−3在研究期间。12月和1月的气温经常<0°C(图2)⇓).12月底是一段温度< - 10°C的极冷时期。
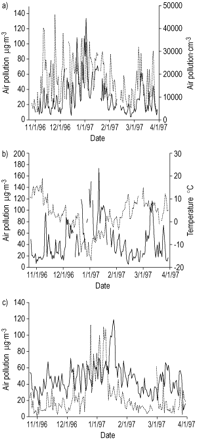
1996-1997年冬季德国埃尔福特的空气污染和温度。a)粒径为0.01-0.1µm的超细颗粒的数量浓度(NC0.01 - -0.1): ═; 细颗粒的质量浓度0.01–2.5 直径为µm(MC0.01 - -2.5):——b)空气动力学直径<10µm的颗粒物:——;温度:短键长的c)二氧化氮(NO2短时间的二氧化硫(SO2):——
颗粒质量浓度与颗粒数浓度>0.1µm处高度相关(表3)⇓).细颗粒质量与累积模式颗粒质量的时间过程基本一致(r=0.997)。超细颗粒数浓度与细颗粒质量浓度相关性中等(r=0.45),与PM相关性中等(r=0.45)10所以2(表3⇓)超细颗粒与CO和NO的相关性2强(r = 0.66)。温度与各污染物呈负相关,相对湿度与各污染物呈正相关。
空气污染物与健康结果之间的关系
对环境污染的延迟响应进行了研究,并在无约束滞后模型中发现了证据。这些模型建议考虑吸入短效β在一段~ 5天的时间内累积效应2吸入皮质类固醇的-激动剂使用≥10天(图3)⇓).为了解释这一点,在最终的模型中使用了5- 10和14天的运行方式。10天的结果并没有显示出来,因为它们与14天的平均值非常相似。
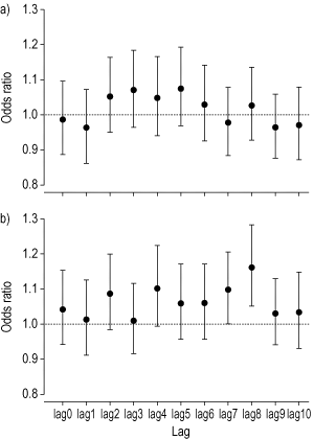
报告的药物使用与超微颗粒(直径0.01-0.1µm)数量浓度之间的关联的无约束滞后模型(NC0.01 - -0.1),滞后0-10,根据立方趋势、温度、周末、圣诞节假期和一阶自相关(在四分位数范围内计算增加的比值比)进行调整。一)短效β2-激动剂使用和b)皮质类固醇使用。
多元模型中混杂因素影响估计的一个例子如下:当包括14天超细颗粒移动平均值时,皮质类固醇的使用随温度下降而增加(>−10°C: 1.06(95%置信区间(CI): 1.00-1.12)),皮质类固醇的使用随温度下降而增加(当>−10°C: 1.06时,5°C下降的比值比(OR))。<−10°C (OR 0.83;95% CI 0.68-1.02, for如。−12 -−17°C)。周末的药物使用率与工作日相似(OR 1.01;95% CI 0.93-1.10),以及圣诞节假期(OR 1.05;95%可信区间0.89 - -1.25)。
表4⇓总结了短效β流行的结果2受体激动剂。所有污染物的同一天值与短效β患病率没有关联2-激动剂。几乎所有颗粒亚组分的5天运行平均值都存在关联。只有CO和粗颗粒分数(PM)-10 - 2.5)没有达到统计学意义。14天的污染物均值大多较低,且往往没有统计上显著的影响估计。
在双污染物模型中,5天平均超微粒子数浓度和超微粒子质量浓度似乎对吸入短效β的使用有独立的影响2受体激动剂(表5⇓)不2似乎是最好的预测者。
吸入皮质类固醇使用的回归结果见表6⇓.吸入皮质激素与同一天暴露于超细颗粒数浓度、细颗粒数浓度和气体NO之间的正统计学显著相关2在5天的运行中,发现了对颗粒组分和气体的显著影响。与14天平均颗粒物空气污染物相关的影响显著更高。所以2也显示出类似的,但并非同等强烈的长期累积效应趋势。公司也没有25天平均效果高于14天平均效果。吸入皮质类固醇与细颗粒物或超细颗粒物的关联程度相似。
在两种污染物模型中,14天的平均值为NC0.01 - -0.1显示出比MC弱的效果0.01 - -2.5(表5⇑).MC0.01 - -2.5与CO和NO相比,与吸入皮质类固醇使用的相关性更强2.
喘息回归结果如表7所示⇓.几乎没有证据表明,当天的污染物测量与哮喘患病率之间存在关联。超细颗粒、CO和NO的5天平均数量浓度之间有统计学意义的相关性2观察哮喘的发生率。与质量浓度呈正相关,但相关性较弱。考虑14天平均值,超细颗粒浓度和积累模式数浓度的影响增大,但对颗粒质量、CO和NO的影响不大2.
双污染物模型考虑了污染物的5天均值,支持超细颗粒对喘息流行率的强烈影响(表5)⇑).超细颗粒与CO和NO气体竞争这一效应2,而细颗粒质量效应的证据仍然很差。在以14天为平均值的双污染物模型中,有更有力的证据表明,超细颗粒与哮鸣患病率之间存在关联。
表8⇓显示其他症状的主要结果。呼吸短促及其与喘息的结合都显示出与喘息相似的模式,而对于“呼吸问题醒来”,另外5天的平均PM2.5效果和立即否定2影响被发现。咳嗽和痰与超细颗粒物、细颗粒物以及NO存在一致且显著的相关性2.5天和14天跑步的效果是相似的。
讨论
总结的结果
在目前的研究中,吸入哮喘药物使用的增加和哮喘症状(如喘息)与空气颗粒物污染有关。
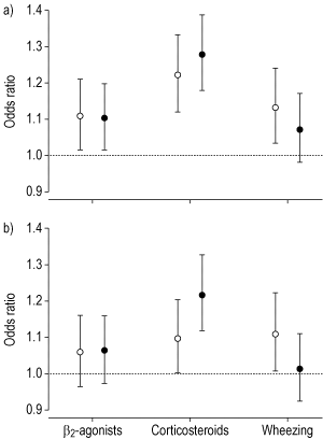
短效β2-激动剂的使用与污染物的5天平均水平相关。几乎所有的污染物都显示出类似程度的显著关联。在两种污染物模型中,超细颗粒数浓度和细颗粒质量浓度的效应估计具有可比性(图4)⇓).相反,吸入皮质类固醇的使用与14天的细颗粒和超细颗粒跑步密切相关。在双污染物模型中,细颗粒质量浓度比超细颗粒数浓度的影响更大。
比较a)单一和b)两种污染物模型中细(•)和超细(〇)颗粒5天平均值对吸入短效β流行率的影响估计值2-激动剂使用,皮质类固醇使用和喘息。
5天和14天的超细颗粒平均浓度与哮喘患病率有关。没有证据表明会立即产生影响。细颗粒的质量或数量浓度没有显著的相关性。气体CO和NO2与哮喘患病率呈正相关双污染物模型强调了超细颗粒的影响。其他哮喘症状表现出一致的效果。
药物的使用
观察到的颗粒物质量浓度和吸入短效β之间的关联2- Aganist使用与其他研究一致,在儿童或成人中进行呼吸系统症状或哮喘7,8,27- - - - - -31.已经发现空气污染对药物使用的累积影响的证据7,8,28- - - - - -31.然而,有研究报道称,β之间没有观察到关联2-激动剂使用和PM1032,33.吸入皮质类固醇的使用以前被分析为“维持药物”的一个类别。7,27,28或“哮喘药物”(包括吸入β2受体激动剂和糖皮质激素)5,其中只有两项与PM有关105,27.在一项针对成人哮喘的研究中,几乎没有证据表明吸入皮质类固醇(作为单独的类别)与PM有关联10观察到有黑烟29。对此的解释可能是,本研究在夏季进行,与本研究相比,随访期更短,污染浓度更低。
吸入糖皮质激素不是一种按需药物吸入短效β2-激动剂,应定期使用。因此,在完全依从性的情况下,空气污染和吸入皮质激素之间的关联是不可能的。据推测,空气微粒污染可能特别影响按需药物的使用。相反,皮质类固醇的使用有相当大的变化;使用糖皮质激素对环境颗粒物空气污染的影响高于吸入β2-激动剂,并在较长时间内积累。观察到的不满意的依从性可能是造成这种现象的原因;患者可能会在不感到不适时停止用药,而在由于外部压力因素(例如长时间的高空气污染水平)而感到不适时重新开始吸入。
无约束滞后模型显示,>前10天的暴露对皮质类固醇使用的流行率有贡献,对短效β有较短的累积效应2-激动剂的使用(图3⇑).值得注意的是,由于个别滞后之间的高度相关性,这些模型中的个别估计不容易被解释。为了克服这一限制,目前的作者考虑了移动平均,在最终模型中为每个滞后分配相同的权重26.对喘息和使用皮质类固醇的最大影响估计是在14天的跑步方式中看到的。这可能是由于暴露于累积的超细颗粒数量浓度引起的炎症反应。这和Neukirch是一致的等34他发现空气污染对症状的影响会在暴露后持续数天,并提出气道炎症过程是导致这一现象的原因。
这项研究与以往大多数调查的一个关键区别是,目前的研究考察了滞后时间≤14天的空气污染的影响,而不是仅仅几天。如果该研究仅在同一天或前几天进行,所看到的影响就会弱得多。考虑趋势的非参数滞后函数时,结果得到了验证。因此,这项研究的一个关键发现是需要研究更长的滞后。
喘息
有几项研究分析了颗粒物和其他空气污染物对“下呼吸道症状”类喘息的影响。与PM升高有关10在有症状的儿童中观察到浓度4,5,28,31.然而,在最近的其他研究中,PM10没有对成人呼吸道症状的影响无效32和孩子9,33,35(和平研究)。在和平研究中,由于随访时间短,很难控制季节或其他时间趋势。本研究随访时间较长,在这方面难度较小。
PM的显著影响10,所以2也没有2哮喘成人患病率作为单独的结果进行了观察34.关联的点10,所以2在儿童中发现了伴有喘息的黑烟7.其他研究没有观察到喘息和颗粒物(PM)之间的显著关联10下午,2.5)27,30.,或气体(NO2,所以2)30..
只有一项研究考虑了细颗粒物浓度和颗粒物浓度,在哮喘症状类别中,哮鸣与呼吸困难合并在一起2.5和点10随着曝光15.这项在芬兰进行的研究显示,超细颗粒对呼气峰值流量(PEF)有影响,但与目前的研究相反,对症状(包括喘息)没有影响。
在这里,对哮喘症状进行了专门讨论,但也检测到对其他哮喘症状的显著一致影响。
哮喘症状和药物治疗
哮喘药物治疗可能是空气污染与哮喘关系的混杂物或效应调节剂。在一项针对严重哮喘患者的流行病学研究中,当颗粒物暴露水平升高时,肺功能增加10.这被解释为药物混淆。在哮喘儿童中,症状与空气颗粒物污染之间的关联通过药物治疗得到改善11.在对哮喘成人的分层分析中,定期吸入短效β的亚组2-激动剂,显示没有效果,而不同药物的受试者显示了有害的健康影响的污染物34.最近的研究表明,空气微粒污染对儿童的不良影响无法通过药物预防11,12,31在本研究中,虽然吸入短效β-干扰素的使用增加,但观察到超细颗粒与哮喘症状之间存在关联2超细颗粒数浓度升高的-激动剂和皮质类固醇。因此,空气微粒污染对喘息等的影响估计可能被低估了。细颗粒质量对喘息的影响是无法检测到的,因为它可能已经被吸入的皮质类固醇有效地补偿了。
关于空气污染物结果的解释
颗粒物燃烧排放物的大小与空气中的细颗粒物相同,而较大的颗粒物(也称为粗颗粒物)大多来源于地质,因此毒性可能较小2,36,37.最近的研究假设,超细颗粒可能有独立的影响14,38.在成人哮喘中,与PM相比,PEF与超细颗粒数浓度的关系更大2.5或点1013- - - - - -15.相比之下,对有哮喘症状的儿童进行的两项研究表明,超细颗粒物的影响并不比其他颗粒物更强39,40.目前的研究发现了细颗粒和超细颗粒独立作用的证据。
气体没有2和CO与超细颗粒高度相关,在大多数分析中显示出与超细颗粒相似的结果。所以2与细颗粒质量高度相关,结果与细粒质量相对应。这与超细颗粒不一致,没有2CO主要是由车辆排放的,而SO只占一小部分2集中就是从这个源头来的。
限制
用几种方法研究了结果的敏感性。单一协变量的消除基本上没有改变污染物的影响。对样本组成的修改,排除了在各自药物的使用上没有变化的参与者(一半),导致了更高的效果估计。将吸烟者纳入回归分析中,导致的影响略有降低。为了考虑较长时间的温度模式,模型中包含了3天运行的温度均值,而不是日温度项。这些效果估计与这里提出的是可比较的。当将趋势视为非参数而非三次函数时,空气污染模型的回归结果没有显著变化。
在诊断方面,研究人群并不一致。这不太可能引入混淆,因为参与者在统计分析中作为自己的对照。鉴于小组是异质性的,在su中检查了与超细粒子浓度和细粒子质量浓度的关联b医生诊断为哮喘的受试者组(n=37)。结果显示吸入短效β的效果较低2-激动剂和吸入性皮质激素的更高效应。这可能是由于这个亚组包括了更严重的哮喘患者,他们可能更容易开始使用他们的抗炎药物。健康的参与者可能倾向于改变吸入短效β2- 以较高的空气污染水平结合使用。在哮喘诊断的参与者中,空气污染对症状喘息的影响比仅报告哮喘症状的参与者更高。关于空气污染的哮喘患者易感性的证据并不一致。在和平研究中9,不同健康状况的儿童在空气污染对呼吸道健康的影响上没有差异。另一方面,Boezen等41报告空气污染对血清免疫球蛋白E水平升高和支气管高反应性儿童的影响高于无此情况的儿童。彼得斯等11在接受药物治疗的儿童中PEF的下降比未接受药物治疗的儿童更明显。
短效β的发生率2-激动剂和皮质类固醇的使用进行了分析。因为每天的发病率非常低(图1)⇑),没有检测到任何影响。目前的作者得出的结论是,影响是长期和额外的药物摄入的组合。
假设个人暴露可以用一个固定测量点的测量值来描述。由于暴露的错误分类是独立于药物使用的,它很可能是无差异的,因此它可能导致了对效果的低估。我们假设,至少整个城市在时间上的变化是可比较的,这在PM中已经显示出来2.5对于超细颗粒来说也是如此42.
为了避免对暴露情况进行错误分类,将居住在城市以外的人排除在分析之外。没有评估在其他任何一天可能影响个人接触的污染源。这可能导致低估了影响。
治疗和空气污染之间的关系需要谨慎看待,因为药物记录是不准确的。很有可能,参与者在他们的常规夜间用药记录和剂量上犯了错误。这似乎不太可能与污染物有关,但随机的错误分类导致低估可能已经发生。
由于由不同来源和气象学引起的颗粒的组成,并且由于区域依赖性哮喘诊断和治疗,因此可以限于ERFURT的范围。
结论
结果表明,德国埃尔福特的成年人报告的吸入哮喘药物使用和哮喘症状增加与超细和细颗粒物空气污染以及二氧化氮等气体污染物有关。
- 收到了2001年8月21日。
- 接受2002年4月2日。
- ©ERS期刊有限公司