摘要
近年来,哮喘,特别是特应性哮喘的患病率显著增加。越来越多的证据表明,在婴儿和儿童早期,与过敏致敏和暴露于微生物刺激相关的环境因素与发病率的这些变化有关。然而,围绕微生物制剂的作用存在相当大的争议,因为已经有证据表明在这一背景下既有积极的影响,也有消极的影响。
以下审查重点介绍了婴儿期间免疫能力之间的相互作用,T-Helper(Th)1-极化的发展相对对吸入性过敏原的th2极化记忆,以及对病毒感染的敏感性。特别是,最近的发现强调了Th1功能的产后成熟延迟与出生后早期吸入性过敏原致敏的风险增加有关,也与婴儿时期病毒性毛细支气管炎的风险增加有关。
T-helper 1功能出生后成熟动力学的变化可能部分归因于CD14基因的多态性,其影响宿主对细菌和病毒刺激的反应性。
从不同地理区域进行的各种研究中明显是明显的,即过敏性疾病的患病率,特别是特应性哮喘,在过去的2-3几十年中已经显着增加。此外,在幼儿期间连续的出生队列中,增加变得明显。还普遍认为“诊断转移”不是这些变化中的重要因素。因此,考虑到发生变化的时间框架,负责因子必须是环境的,可能是与一种或多种易感基因相互作用。
对相关遗传和环境因素的研究仍在继续,并已确定了各种可能的候选基因。其中最突出的是与呼吸道感染有关的因素,特别是发生在儿童时期的呼吸道感染。矛盾的是,这些感染被认为是与哮喘/过敏发展相关的潜在保护因素,也是特应性哮喘患者哮喘加重的诱因。这些效应可能被调节的机制尚未被完全理解;然而,最近的发现提出了一些有趣的新可能性,这篇综述将对此进行讨论。
吸入剂的T细胞免疫转化剂:成年人群中响应者表型变异的基础
上呼吸道的上皮表面连续地暴露于致病和非致病空气中抗原的阵列,并且局部T细胞免疫的诱导和局部表达必须紧密控制,以避免慢性的病理后果T细胞驱动的炎症。虽然对空气传播的抗性是高度合理的,但是抗血液速度的直接函数,局部先天和适应性免疫机制的表达强度,逆转情况似乎更复杂。特别是,目前尚不清楚免疫系统如何避免不断应对空气抗原,例如花粉,这是本质上是不管的,而在自然环境中高度免疫原性和普遍存在。
对这种区别的经典解释设想了粘膜免疫系统对这种抗原的局部分泌性免疫球蛋白(Ig)A反应。这种IgA“毯”被认为是一种保护性排斥屏障,最大限度地减少上皮下惰性抗原的渗透,从而防止免疫系统的有效系统致敏。然而,将T细胞克隆技术引入该领域所产生的研究结果要求对这些观点进行彻底的修改。值得注意的是,现在很清楚,对常见非致病性空气传播抗原的主动T细胞免疫在成年人群中基本上是普遍存在的,这些免疫反应的定性方面决定了相关的临床结果(如果有的话)。
因此,大多数人的外周血中都含有识别花粉抗原的循环记忆T细胞(以及室内外灰尘中存在的许多其他此类蛋白质),在这样做的过程中触发释放低水平的细胞因子,如干扰素(IFN) γ,哪些是T细胞免疫辅助T细胞(Th)1模式的特征1.,2..这些受试者仅产生低水平的过敏原特异性IgG抗体,并在暴露时表现出临床症状。相比之下,少数受试者含有T-内存细胞,其响应相同的抗原通过释放Th2相关细胞因子,如白细胞介素(IL)-4,IL-5和IL-131.,2.,通常与IFN-γ相结合(即th0-like;3.,4.)。
二分性细胞因子分泌模式最初是在小鼠系统中定义的5.,这个Th1 / Th2范例的外推到人体系统并未普遍接受。特别地,已经指出,小鼠中Th1免疫的标志是延迟的超敏反应(DTH),但没有证据表明过敏原特异性DTH在过硬含有TH1-偏振的过敏原特定的TH记忆单元6..关于这一辩论,作者最近使用了T细胞免疫力的替代措施,分析了对人类过敏原的记忆的定性方面。作者已经证明了7.在抗原特异性重新激活的初始阶段期间,Th存储器单元表现出转录因子(TF)的表达的特征模式,该表达的表达(TF)镜像在幼稚细胞的细胞因子驱动的偏振中观察到的TH1或TH2分化途径。值得注意的是,Th2分化与TF GATA-3的表达的上调相关,而TH1分化与GATA-3基因的活跃下调的往复模式相关。当刺激来自Atopics和非储物学的外周血CD4 + T细胞时,可以看到GATA-3表达模式中相同的二分。体外用常见的吸入剂过敏原,如房子尘螨7.,提供独立确认Th1 / Th2范例对人类的适用性。
关于Atopic哮喘的缓解学,核心问题是:这些二分的几个内存模式如何编程?
儿童期过敏原特异性T辅助记忆编程
各种证据表明,初始免疫系统对吸入性过敏原的启动发生在生命早期,在许多情况下发生在妊娠晚期。这一结论是基于独立实验室的一系列研究得出的8.–12.展示脐带血单核(CBMC)样本中细胞的存在,其响应过敏原而增殖。另外,涉及来自这些培养物的T细胞克隆的脱氧核糖核酸基因分型的作者组最近已经证实了遗传细胞的胎儿13..
从这些研究中尚不清楚是否发生初始的Th细胞灌注通过与本土过敏原接触,围绕胎盘运输或通过交叉反应抗原刺激。然而,在多个实验室进行的一系列横断面和前瞻性研究中追踪这些出生后反应(例如14.–16.)揭示了“反应成熟”的特征模式,其从非储物学中分离出的情况。作者实验室最近的结果证明了一个明确的例子。首先,这些表明CBMC中的初始低水平响应由TH2细胞因子主导13.,但随后在婴儿期和幼儿期进行修改。因此,Th2反应性在进展到早期表现特应性症状的儿童中稳步增强14.和/或皮肤刺的吸入剂测试阳性17.,18.;然而,在非特应性反应中,这些反应转向(“免疫偏离”)为th1样模式。在许多个体中,Th记忆生成过程似乎在学龄前或早期学校生活结束时完成,潜在地将个体锁定在过敏原反应的终生模式中。然而,正如后面讨论的,这种记忆生成过程并不是临床反应表型的唯一决定因素,特别是在哮喘方面,因为只有一部分儿童对吸入性过敏原敏感,进而发展为持续性哮鸣19..
遗传相对过敏性敏化的环境决定因素:生命早期微生物暴露的意义
过敏性呼吸系统疾病易感性的遗传基础是国际上研究的热点。众所周知,多种基因可能与这种高度复杂的疾病有关。然而,从特应性和非特应性的Th1/Th2反应性相关问题的研究中,可以推断出这一过程中的一些关键因素。
20世纪70年代的文献主要涉及儿童期严重特应性疾病(特别是特应性皮炎)的表达,其中包含一系列独立报告,表明与健康老年对照组相比,受影响受试者的适应性免疫功能各方面都存在缺陷。最近,作者的实验室试图将这些发现推广到一般的过敏性疾病。基于大量分离克隆的定量T细胞克隆研究和细胞因子分析的关键发现表明,遗传易感性的一个重要因素是Th1功能的出生后成熟延迟20..本作者表明,相对于其低风险(LR)对应物,降低了对特性高风险(HR)产生Th1和Th2细胞因子的CD4 + Th细胞的容量;然而,IFN-γ的还原是最大的,导致人力资源儿童响应性的相对Th2“偏斜”。这些结果以来已扩展到一系列独立实验室的确认研究中的CBMC21.–26..
目前对这些发现的解释27.基于免疫学的相关文献怀孕,是过程涉及的正常过渡从胎儿Th2-polarized适应性免疫功能状态,更加平衡但Th1-dominant国家成熟的免疫系统的特点,进行人力资源的更慢比LR的孩子。此外,我们可以假设,由于这种延迟,HR儿童在免疫偏离过程中偶尔“失败”的风险将增加,这是新生儿对变应原的th2偏斜反应向非特应性特征的Th1模式复极化的基础27..
出生后Th1功能成熟的精确动力学和机制的本质尚不完全清楚,但最近在几个领域的发现为这一过程提供了新的线索。首先,小鼠模型的实验研究证明了启动子甲基化在Th2细胞中IFN‐γ基因沉默中的重要作用27.,以及作者实验室最近的研究(P.G.Holt,西澳大利亚州珀斯TVW Telethon儿童健康研究所,个人通讯)表明,人类胎儿原始CD4+T细胞中类似机制的过度活跃可能是其转录IFN-γ基因能力降低的原因,相对于成人CD4+对应物。第二,其他以前的研究来自动物模型28.表明哺乳动物中免疫功能的后期成熟是通过与胎儿寿命通常不遇到的微生物刺激的接触驱动,并且该刺激的重要部分是选择性地朝向TH1功能的选择性引导29..因此,作者提出Th1成熟过程动力学差异的潜在因素之一可能涉及基因决定的在生命早期对这些微生物刺激的反应能力的变化26..其中一个例子可能是白川的发现的基础等30.,这表明未能在婴儿期间响应Bacille Calmette-guérin免疫,未能产生长期Th1-极化记忆,与随后的特性和哮喘发育的风险有关。
在这种情况下可能具有重要意义的途径的第二实例涉及编码细菌脂多糖(LPS)的高亲和力受体的CD14基因。凭借其刺激Th1-营养的IL-12生产的能力,它很可能是LPS通过可溶性CD14依赖机制,在第1个功能的后上调中起关键作用,作者假设正常的胃肠细菌菌群可能在这个过程中发挥关键作用31..最近的Matricardi发现等32.建议胃肠道病原体可能发挥类似的效果。
本作者还与Baldini合作等33.在鉴定CD14基因中的多态性,这与血清中可溶性CD14的水平降低,降低了Th1的功能,以及增加的特征致敏强度。鉴于最近的报告证明CD14介导对呼吸道合胞病毒(RSV)的先天免疫应答的关键作用,这种多态性可能具有额外的影响。34..与微生物(特别是病毒)刺激识别相关的基因的进一步多态性有待发现,这是可行的。
在这方面,值得注意的是,最近的报告表明,儿童时期接触空气粉尘中的LPS似乎与吸入性过敏原的致敏性呈负相关35.,36.. 这些发现的一个潜在解释涉及已知的LPS对气道粘膜树突状细胞(DC)群的刺激作用(稍后讨论)。
呼吸道感染对哮喘和过敏的表观二元效应
呼吸道病毒感染在学校儿童中的研究很清楚,呼吸道病毒感染是哮喘恶化的有效触发,特别是在特应性哮喘中37..还显然,婴儿期间的呼吸道感染较低,特别是那些在足以引发喘息的严重程度上发生的那些,与随后的持久气道高反应性的风险增加(AHR;38.,39.). 关于急性加重,虽然确切的机制仍有待确定,但喘息的发生可能至少部分是由于宿主对感染的反应导致气道组织损伤的总和,以及持续的Th2介导的对吸入性过敏原的免疫炎症反应。
呼吸道感染与儿童哮喘之间关系的混淆有显着贡献的一个因素是儿童哮喘缺乏明显的表型描述。旧格言“所有那些喘息不是哮喘”几乎肯定适用于此。在儿童中,至少有三种不同的喘息综合征,每个危险因素都具有不同的危险因素,并且可能具有不同的预后意义。这些综合征被各种名称调用,但似乎围绕“瞬态婴儿喘息喘息”,“病毒相关的喘息”和“特应性哮喘”形成共识。这三种条件是单一疾病谱的不同部分,或者代表不同的疾病仍有待建立。
在出生后的第一年,有30%的婴儿在某些系列中至少出现过一次喘息40.瞬态婴儿嘶嘶声描述了第一年或两两个婴儿喘息的条件,而不是稍后。这种综合征似乎在吸烟和年轻母亲的母亲出生的婴儿中更常见,并且与生活后面的土木患病率没有增加。在学前教育和早期学年的幼儿中,病毒相关的喘息非常普遍。许多研究表明,在婴儿的RSV感染后儿童时期喘息增加了,但没有表现出这些儿童的特性的患病率。最近,斯坦伊坦等41.已经证明,RSV感染是6岁以下儿童喘息的一个危险因素,但这种风险已经降低了13% 同样,该研究中早期感染呼吸道合胞病毒的儿童在13岁时的特应性疾病患病率没有增加 病毒相关性喘息可能是幼儿喘息发作的主要原因,也可能是该年龄组医生诊断哮喘的主要原因。如果这是Stein描述的同一综合征等41.,这也可能是人们普遍认为许多儿童“长大后”不再患哮喘的原因。
关于婴儿期发生的感染的长期影响有关,已经假设了在快速肺生长的这种关键阶段的严重气道炎症可以在随后的生长和分化期间引发气道组织中的表型变化,最终导致最终引起的AHR.38.,39..它还已经假设,某些病毒,特别是RSV,有可能选择性地刺激“旁观者”TH2响应42.,43.,从而放大了针对吸入性过敏原的Th2极化免疫记忆的发展。然而,鉴于最近一项长期随访研究的结果,这些影响可能是暂时的,该研究未能发现早期呼吸道合胞病毒感染与特应性疾病长期表达之间的联系41..
相反,还提出了其他呼吸道感染,是由于它们发生或其特殊定位和/或严重程度的时间,可能具有相反的长期影响,而是防止过敏性敏感和/或哮喘发育44.–47..例如,美国儿童在3年龄之前开发出一个以上的非全腹部呼吸道感染,显示出特性患病率的显着减少48.,爱沙尼亚学童的过敏发生率很低,但与过敏经常发生的西欧儿童相比,他们的呼吸道感染时间更长、更严重49.. 这种效应的一个可能机制涉及感染介导的气道粘膜DC群刺激,其调节对吸入抗原的免疫反应中的Th1/Th2平衡50..这些DC绝对依赖于接收到适当的炎症细胞因子信号,和/或从微生物产品(例如LPS或病毒核酸)的刺激,以便上调它们的IL-12的产生,它们利用驱动Th细胞的反应th1差异途径51..在具有免疫能力的成年实验动物中,气道DC网络对病毒/细菌刺激具有高度反应性52.,但这一功能和相关的T细胞调节功能在婴儿动物中减弱53.,54.需要长时间的刺激以促进功能成熟。最近的一项研究表明,人类气道DC群体在婴儿期通常处于类似的低基线活动状态,并且在严重感染时可能会显著上调55..此外,这可能代表一种机制,通过它的早期生命中某些感染可以有助于提示对TH1的发展平衡,而不是对无处不在的空气过滤器的免疫力。这种模型的一种预测是这种潜在的“保护性”感染可能仅限于局部局限于上气道的粘膜的那些,这代表了用于沉积吸入过敏原的主要位点。
目前,这些相互冲突的概念似乎难以调和。然而,许多作者认为,早期感染与哮喘/特应性疾病之间关系的性质可能比以前认为的更为复杂。例如,有人提出,RSV诱导的婴儿喘息可能是一种预先存在的特应性倾向的标志物,而不是Th2分化的刺激物50..与早期生命中的RSV有关的研究的最新结果开始澄清这个问题,这些问题在本综述结束时讨论。
哮喘和儿童感染与过敏性致敏的相互作用:原因/效果关系解剖
如前所述,需要进一步澄清的一个关键问题涉及下呼吸道感染短期和长期后遗症的性质,特别是特应性/哮喘之间因果关系的性质。
稍后提到的方案和详细说明1⇓说明了哮喘病因学中的潜在因果途径,代表了作者目前对该领域有争议的文献中有很大一部分可以调和的观点。以下主要观察结果支持该方案的特应性部分。1) 过敏原特异性Th细胞启动发生在围产期8.–13.,这些早期的免疫应答在学龄前儿年内被分别为Th1或Th2-偏振记忆14.–18.. 2) 儿童期对吸入剂致敏的症状通常不会超过间歇性喘息,严重的长期后遗症似乎仅限于一部分过敏19.表现出高水平的Th2介导的炎症56.–58.以及随后的气道重塑57.,58..3)过度的气道炎症表明存在额外的“促炎”的宿主和环境辅助因素;这可能包括与气道黏膜内免疫控制机制失调相关的遗传因素和一系列环境因素58..4)较早的认为,Th2-偏振记忆对吸入剂过敏原的发展,越严重是与AHR相关的长期后果59.,60.,暗示在快速肺生长期间的呼吸道炎症的重复循环可以建立某种形式的“基质”,用于开发与气道重塑相关的后续变化。5)特性的遗传风险与自适应免疫功能的缓慢产后成熟有关,特别是Th1功能20.,27..
关于该方案中的感染组分,相关最近的观察结果如下:1)据报道,Atopate的遗传风险与严重RSV感染和支气管炎的易感性增加有关61.; 儿童的过敏症也与麻疹、腮腺炎和风疹的易感性增加有关62.以及频繁的上呼吸道感染63.;2)外周血单核细胞中的IFN-γ反应在开发支气管炎的儿童急性RSV感染期间衰减59.–69.,表明下调的Th1功能可能与发病机制有关;3)在婴儿期间对急性RSV支气管炎发育的敏感性与脐带血中的IL-12水平降低有关,相对于不开发支气管炎的受试者70,暗示本集团在TH1功能中的预先存在的缺陷;4)非植物喘息的儿童,喘息的主要刺激是病毒感染本质上,也表现出IFN-γ响应的表现减少71.;5)作者组最近的一项关于婴儿的预期队列的一项研究表明,在观察期间,在观察期间向RSV(作为RSV感染的替代标志物)的T细胞记忆的发展与动力学相反IFN-γ响应的产后成熟72..
总的来说,这些发现表明,与Th1功能的延迟后成熟有关的可比遗传缺陷可能使易感性敏感性敏感性和严重呼吸道病毒感染的发育,以及它们的扩散到下呼吸道。这种感染在短期内引发喘息,并且在很大一部分的情况下,它们可能具有足够严重的严重程度,以对肺部肺生长和分化进行充分损害,从而引发变化,随后与气道炎症的后期剧集产生的那些促成的变化其他刺激如过敏原。
目前的计划不能考虑病毒感染在哮喘病学中的所有潜在作用,特别是与成人发病的非植物哮喘相关的那些,尽管水蛭的发现等71.可能与此问题相关。然而,该方案确实为未来的系统研究提供了一个合理的框架,进入这种复杂问题。
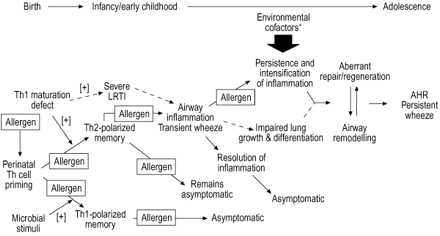
一种多级模型,用于哮喘病学中感染与特性的相互作用。LRTI:降低呼吸道感染;AHR:Airway HyperResponsience;TH:T-辅助细胞;[+]:刺激或倾向于。*:包括病毒感染,环境刺激剂,过敏原载荷/类型,等等.有关这些途径的构建的背景参考文献见正文。
脚注
↵本系列以前的文章:否。 1.: Pilette C, ouadriri Y, Godding V, Vaerman J‐P, Sibille Y.肺黏膜免疫:免疫球蛋白A再次访问。欧元和J2001;18: 571 - 588。2号:Lambrecht BN,原装J-B,Hoogsteden HC。肺树突细胞和宿主免疫感染。欧元和J2001;18:692-704。3号: Moore BB, Moore TA, Toews GB。T淋巴细胞和B淋巴细胞在肺宿主防御中的作用。欧元和J2001;18:846-856。4号:消息SD,Johnston SL。哮喘病毒感染的免疫学。欧元和J2001;18:1013-1025。5号: Crameri R, Blaser K.真菌感染和定植的过敏和免疫。欧元和J2002; 19: 151–157.6号:De Rose V.气道炎症的机制和标记囊性纤维化。欧元和J2002; 19: 333–340.
- 已收到2001年3月22日。
- 认可的2001年5月8日。
- ©ERS期刊有限公司














