摘要
此前提前报道了脑内脑内肠毒素-B(SEB)诱导的自身免疫性小鼠诱导间质肺炎(IP)的肿瘤内滴注。SEB-反应性T细胞批判性地参与IP在该模型中的IP。对肺损伤和纤维化过程中的活性氧物质(ROS)和反应性氮物质(RNS)的危害产生了担忧。
因此,一氧化氮(NO)和超氧阴离子(O2-)的发病机制,在这种自身免疫倾向模型已进行了研究。
支气管肺泡灌洗(BAL)流体和来自SEB注射小鼠的血清的亚硝酸盐/硝酸盐水平增加。No-(n-(二硫代羧)sarcosine的信号)2菲2+采用电子顺磁共振(EPR)技术检测seb注射肺和全血中络合物的含量。氨基胍(AG)处理显著降低NO产量。肺、BAL液和血浆中的黄嘌呤氧化酶(XO)活性随着SEB灌注而增加,4 -氨基- 6 -羟基吡唑罗(3,4 - d) -嘧啶(AHPP)显著抑制XO活性。此外,在seb注射的肺中,AG和AHPP均显著降低促炎细胞因子的产生、BAL液中浸润细胞的数量和增厚的肺泡间隔面积。
总之,一氧化氮和超氧阴离子的过量产生与间质性肺炎的发病机制有关,诱导型一氧化氮合酶和黄嘌呤氧化酶抑制剂在该模型中对间质性肺炎具有保护作用。
这项工作得到了日本厚生劳动省对间质性肺病的资助。
几种类型的间质性肺炎(IP)与自身免疫性疾病相关1- - - - - -3..虽然自身免疫性疾病的发病机制尚不清楚,但遗传和环境因素是已知的促成因素4.目前关于IP发病机制的理论强调肺泡炎的作用。自身免疫性疾病中与IP相关的肺泡炎以中性粒细胞和肺泡巨噬细胞增加为特征5.
细菌超级抗原,如葡萄球菌肠毒素B (SEB),一旦与特定的T细胞受体(TCR) Vß链结合,就会触发T细胞活化,而不考虑TCR α链伴侣或TCR特异性6.与传统抗原相比,对超级抗原有反应的T细胞比例要大得多。MRL-+/+鼠系携带野生型Fas基因,发展为系统性红斑狼疮样疾病7.作者以前曾报道过这些小鼠在服用SEB后肺部受累8.气管内灌注SEB对自身免疫倾向的MRL-+/+小鼠比自身免疫不倾向的小鼠诱导更严重的IP。这些结果支持了seb诱导的IP是在宿主免疫系统被激活时触发的观点,最近的研究表明,在这种自身免疫倾向模型中,支气管肺泡腔中的seb反应性T细胞触发了IP的发展9.支气管肺泡灌洗液中淋巴细胞、肺泡巨噬细胞和中性粒细胞增多。
近年来,大量论文认为活性氧(ROS)和活性氮(RNS)都参与了肺损伤和纤维化的发病机制。一氧化氮(NO)是一种气体自由基,由分子氧和l‐精氨酸的胍氮在NO合酶(NOS)催化的反应中生成。10..至少有3个NOS基因被克隆:一个神经元NOS (nNOS),一个诱导NOS (iNOS)和一个内皮NOS (eNOS)。iNOS在巨噬细胞、成纤维细胞、T‐helper 1淋巴细胞(Th1)和中性粒细胞中不正常表达。然而,当这些细胞被特定的细胞因子激活时,iNOS上调10.,11..早期研究表明,小鼠巨噬细胞可产生NO,提示NO可能在免疫中起重要作用12..大量的环境证据表明,在自身免疫性疾病中,NO可以作为组织损伤的中介物13.,14..例如,MRL-lpr/lpr小鼠自发发展狼疮样综合征,一种iNOS抑制剂阻止了肾小球肾炎的发展,并降低了炎症性关节炎的强度14..
关于NO对SEB诱导的冲击的影响达到了相互矛盾的结论。沙拉马等等。15.结果表明,iNOS抑制剂氨基胍(AG)对seb诱导的淋巴细胞性脉络丛脑膜炎病毒感染小鼠的休克具有保护作用。恰恰相反,弗洛坎等等。16.报道了SEB给药后产生的内源性NO具有保护作用,因为用iNOS抑制剂治疗显著增加了BALB/c小鼠的死亡率。
作者假设与自身免疫性疾病相关的IP特征的肺泡上皮细胞损伤可能至少部分是由氧化和亚硝化应激增强所致,这些应激可能存在于下呼吸道。因此,我们评估了iNOS和黄嘌呤氧化酶(XO)抑制剂对seb诱导的MRL-+/+小鼠IP的影响。结果表明,NO和超氧阴离子(O2-),并且在该模型中,iNOS和XO抑制剂对IP的发展具有保护作用。这些结果表明NO和O的升高2-产生在自身免疫相关IP的疾病表现和阻断NO或O的产生的治疗中是重要的2-可能有临床价值。
材料和方法
葡萄球菌肠毒素B应承担的管理
如前所述,将SEB (Sigma Chemical Co., St Louis, MO, USA)注入12周龄特异性无病原体MRL-+/+小鼠(Japan SLC, Shizuoka, Japan)的气管中8.简而言之,在每只小鼠麻醉后,将气管暴露,40μL的40μlPBS中的SEB,或单独滴加40μl磷酸盐缓冲盐水(PBS)。
用黄嘌呤氧化酶或诱导型一氧化氮合酶抑制剂处理Stapylocal Enterotoxin-B滴注小鼠
seb灌注小鼠口服4‐氨基‐6‐羟基吡唑(3,4‐d)-嘧啶(AHPP: Acros Organics, Geel, Belgium) 1.0 mg·小鼠−1在0.2 mL 0.1 M NaOH中,从SEB给药前一天开始每天注射,并持续整个实验过程。对照组小鼠口服0.2 mL 0.1 M NaOH。在另一项实验中,给小鼠注射i.p。100 mg·kg−1在施用AHPP的同一时间点,每天两次,在0.2ml盐水中。给予Ag处理的对照组0.2ml盐水i.p。一天两次。
定量组织病理学
气管内灌注SEB 2µg,固定充气至20 cmH后7天取肺组织2氧压力6%福尔马林。固定后,从中心矢状切开所有肺叶。组织切片用苏木精-伊红或氮赞染色。肺泡间隔增厚,间质炎症和成纤维细胞增生是该模型的病理特征之一8.用NIH图像测量各叶总面积与增厚、炎症组织面积的比值,计算病变面积。肺泡间隔增厚的区域以百分比表示。
血清和支气管肺泡灌洗液中亚硝酸盐/硝酸盐的测定
脱蛋白血清和BAL液中的亚硝酸盐/硝酸盐浓度用自动分析仪系统(TCI-NOX 1000;东京化学工业,东京,日本)通过检测在流动反应器中形成的重氮化合物与格里斯试剂,如前所述17..
用电子顺磁共振波谱法测量一氧化氮生成
通过分析NO-(N‐(Dithiocarboxy) sarcos (DTCS))来测定小鼠肺和全血中NO的产生。2菲2+复合生产(日本熊本Dojindo实验室)。(转轨国家)2菲2+复杂的形成新创dcs和FeSO给药后的组织中4在老鼠身上。电子顺磁复核(EPR)谱学如前所述进行18..注射SEB后第3天,FeSO4小鼠皮下注射dtci.p。,分别于取血浆、肺、全血30 min前进行EPR测定。将保存在液氮中的样品用X波段EPR光谱仪(ESP380E;Bruker Instrument Inc., Rheinstetten, Germany)价格为110 K。NO-信号高度的绝对浓度(DTCS)2菲2+采用1.0 mM Tempol溶液作为EPR光谱的主要标准溶液。对每个NO-(DTCS)的EPR信号强度进行评估2- - - - - -菲2+通过测量信号从基线到场槽的高度g=2.025。一般情况下,EPR谱的信号高度严格反映各自由基的浓度,如。形成的no -铁配合物。
免疫组织化学
气管内灌注SEB 40µg,固定充气至20 cmH后3天,取小鼠肺组织2氧压力6%福尔马林。脱水后,切割3μm厚的石蜡切片,脱碱化并进行免疫染色。然后用1:500稀释或抗硝基葡萄酒抗体(Upstate Biotechnology,Ny,USA)在1:100稀释,检测是间接的用过氧化物酶标记的抗兔免疫球蛋白(DAKO,GLOSTRUP,丹麦)稀释1:100的免疫氧化酶方法。通过使用3,3'-二氨基苯胺作为基质,可视化过氧化物酶活性。
黄嘌呤氧化酶和黄嘌呤脱氢酶活性的测定
通过先前描述的荧光法测定XO和黄嘌呤脱氢酶(XD)活性19..然后将样品与荧光测定法进行荧光测定,用Pterine(Sigma Chemical Co.)作为底物作为底物进行XO / XD活性。异甲肝(Aldrich Chemical Co.,Milwaukee,Wi,USA),一种反应产物,用光谱荧光仪(F-4500;日本,日本,日本,日本)以345纳米和390nm发射。该活性表示为Nmol异雄醇·min−1·毫升−1血浆、BAL液上清(s‐BAL)或全肺匀浆。
支气管肺泡灌洗细胞诱导型一氧化氮合酶和黄嘌呤氧化酶/黄嘌呤脱氢酶信使核糖核酸水平的评价
采用半定量逆转录聚合酶链反应(RT-PCR)检测iNOS和XO/XD信使核糖核酸(mRNA)表达。用Micro-FastTrack提取mRNATM2.0套件(Invitrogen公司,Carlsbad, CA, USA),根据制造商的说明。用逆转录酶法合成第一链互补脱氧核糖核酸(cDNA)。
用特定合成的引物(Gibco-BRL,Life Technologies,Rockville,MD,USA)进行PCR扩增。每个循环在94℃下在94℃下在54℃下在54℃下进行1分钟,用于退火,72℃下3分钟进行延伸。在热循环之前,PCR反应在95℃下在95℃下孵育10分钟,分别在72℃下孵育5分钟。对于内部对照,扩增β-肌动蛋白以使每个样品的CDNA的起始量标准化。使用以下引物:INOS,5'-CCCTTCCGAAGTTTCGCAGCAGCGGC-3'(SENSE)和5'-GGCTGTCAGAGCCCTCGTGGCTTGG-3'(反义);xo / xd,5'-cagggtcttggtcttttcac-3'(sense)和5'-cgtggtttcagcgtcagga-3'(反义);和β-actin,5'-agggtgtgtgatggtgggaatg-3'(Sense)和5'-ggctggggtgttgaaggtctc-3'(反义)。用于β-肌动蛋白的二十八个循环,使用38个循环用于InOS和XO / XD。频带强度由NIH图像测定,并计算inoS或XO / Xd至β-肌动蛋白比(INOS或XO / XD mRNA水平的密度比率)。
一氧化氮合酶诱导活性的定量分析
用克雷布斯-林格磷酸盐缓冲液(pH 7.4)进行BAL。如前所述,通过刺激小鼠巨噬细胞RAW 264 (American Type Culture Collection, Rockville, MD, USA)培养,检测小鼠s‐BAL液诱导inos的能力20..具体地,将来自用或许没有SEB处理的小鼠的250,100或50μL的S-BAL流体加入到24个骨板中的原料264的培养物中,最终体积为500μL的Dulbecco改良的Eagle媒体F:12(DMEM / F12:Gibco-BRL)和10%胎牛血清。刺激后48小时获得培养上清液,并先前描述了亚硝酸盐/硝酸盐测定。
支气管肺泡灌洗液中的肿瘤坏死因子-α,白细胞介素-1β和干扰素-γ水平
使用市场上可用的TNF - α、IL - 1β或IFN - γ酶联免疫吸附试验(ELISA)系统(BioSource International Inc., Camarillo, CA, USA)测定s - BAL液中的肿瘤坏死因子- α (TNF - α)、白细胞介素- 1β (IL - 1β)和干扰素- γ (IFN - γ)水平。
统计分析
数值报告为平均值±sem。采用未配对t检验分析组间差异。p<0.05时认为差异显著。
结果
氨基胍和4 -氨基- 6 -羟基吡唑啉(3,4 - d)嘧啶对注射的葡萄球菌肠毒素B肺病理变化的影响
评估NO和O的参与2-在SEB-灌注的MRL - + / +小鼠中IP的发病机制中,Ag(InOS抑制剂)和AHPP(XO抑制剂)用作潜在的治疗剂。
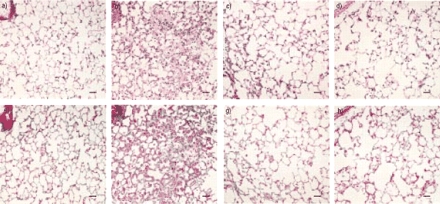
AG和AHPP处理后,肺泡间隔壁细胞浸润和肺胶原纤维合成均减少(图1)⇓).AG和AHPP处理后,肺泡隔区炎性细胞增厚,成纤维细胞减少(图2e)⇓).
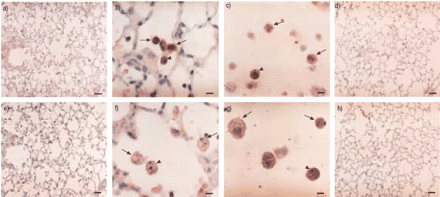
不同处理下对照小鼠和注射了葡萄球菌肠毒素B (SEB)小鼠的肺切片。第7天从磷酸盐缓冲盐水(PBS)灌注小鼠(a, e)和seb灌注小鼠(盐水/NaOH处理(b, f)、氨基胍(AG)处理(c, g)和4‐氨基6‐羟基吡唑-(3,4‐d)-嘧啶(AHPP)处理(d, h)获得肺组织。组织用苏木精伊红(a-d)和氮杂赞(e-h)染色。seb注射小鼠肺组织中肺泡间隔壁可见明显的炎症细胞浸润和胶原纤维合成(b, f)。AG和AHPP治疗后,炎症细胞浸润和胶原纤维合成减少(c, g和d, h)。内部标度条=50µm。
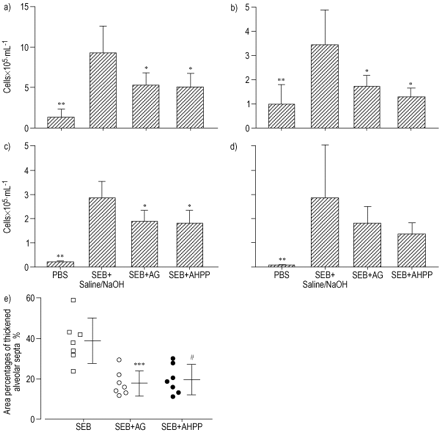
a)的数量,b)巨噬细胞,c)淋巴细胞和d)在滴注后3天的小鼠从小鼠的支气管肺泡灌洗液中的中性粒细胞3天(SEB),(SEB)的平均值±SEM是八个每组小鼠)。e)用盐水/ NaOH(ε),氨基胍(Ag;○)和4-氨基-6-羟基吡唑(3,4-D)-Pyrimidine(AHPP;•)处理的SEB-灌输小鼠的肺炎区域。值是肺泡隔膜面积百分比的平均值±SEM,其在每组中七只小鼠的间质炎症和成纤维细胞增稠增厚。PBS:磷酸盐缓冲盐水。*:P <0.05;* *: p < 0.01;***:P <0.001;#: p < 0.005。
在注射SEB的小鼠之间,BAL液中总细胞显著增加(9.2×105毫升−1)和对照组小鼠(1.20×105毫升−1(图2a, p⇑< 0.001)。用AG和AHPP处理seb灌注小鼠BAL液中总细胞、巨噬细胞和淋巴细胞的数量也降低。这些发现表明NO和O2-在seb灌注MRL-+/+小鼠的IP发病机制中起关键作用。此外,NO和O的抑制剂2-可能是治疗IP的潜在药物。为了确定这种治疗保护是否可行,研究了NO和O的产生2-并考察了抑制剂对该产物的影响。
葡萄球菌肠毒素B注入小鼠体内一氧化氮的释放
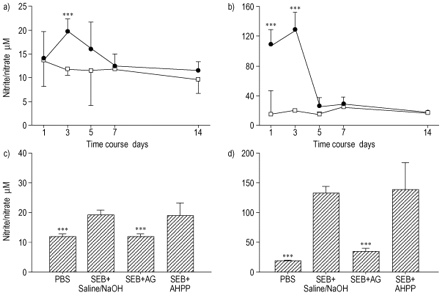
为了评价NO参与seb诱导的IP模型,采用Griess法和EPR法测定NO产量。seb灌注小鼠BAL液和血清中NO代谢物(亚硝酸盐/硝酸盐)产生的时间过程如图3a和b所示⇓.总的来说,seb灌注小鼠的s - BAL液和血清中亚硝酸盐/硝酸盐的含量增加。SEB灌注后3天,BAL液中亚硝酸盐/硝酸盐水平达到峰值(19.27±0.74µM),显著高于pbs灌注小鼠的峰值(11.84±1.70µM;p < 0.001)。同样,seb灌注小鼠的血清亚硝酸盐/硝酸盐水平在第3天达到峰值,显著高于对照组(131.55±14.8µM)与19.8±2.81µM;p < 0.001)。
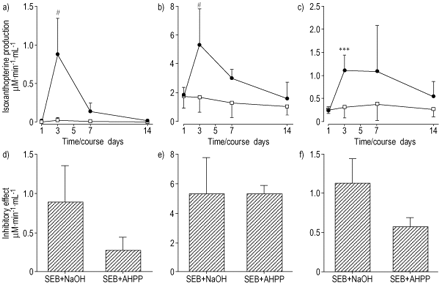
亚硝酸盐/硝酸盐产生的时间过程A)支气管肺泡灌洗液(BAL)和B)血清。与磷酸盐缓冲的盐水(PBS;□)相比,在葡萄球菌肠毒素-B(SEB;•)注射后第3天(PBS-Itserled小鼠:N = 6; SEB-Itserled小鼠:N = 6),亚硝酸盐/硝酸盐形成增加).氨基胍(Ag)和4-氨基-6-羟基吡唑(3,4-D)-Pyrimidine(AHPP)对C)BAL流体中亚硝酸盐/硝酸盐形成的甲嘧啶(AHPP)的抑制作用在SEB给药后第3天血清。与盐水/ NaOH和AHPP相比,AG抑制SEB灌注小鼠的BAL流体和血清中的亚硝酸盐/硝酸盐(盐水/ NaOH处理的小鼠:N = 6; Ag处理的小鼠:N = 6; AHPP处理的小鼠:N =6.值表示为平均值±SEM。***:P <0.001。
在给AG时,seb灌注小鼠BAL液和血清中的亚硝酸盐/硝酸盐水平(p<0.001)与对照组没有差异,给AHPP对亚硝酸盐/硝酸盐的产生没有抑制作用(图)。3 c和d⇑).
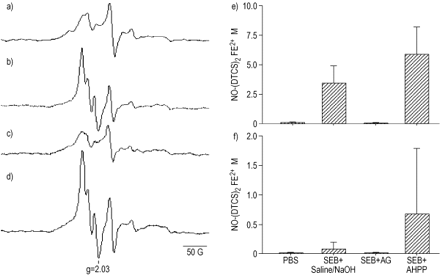
采用EPR光谱技术,检测seb灌注小鼠肺和全血样本中no -血红蛋白和no -血红蛋白复合物的特征超微结构信号(数据未显示)。增加灵敏度(DTCS)2菲2+配合物用作自旋诱捕剂检测NO(图4)⇓).经DTCS和FeSO处理后4,强烈的EPR信号显示NO-(DTCS)2菲2+在注入SEB的小鼠的肺和全血中检测到复合物(图4b)⇓).与此相反,pbs注射的对照组小鼠在给予DTCS和FeSO后,肺内未观察到明显的EPR信号4(图4⇓).NO-的EPR信号(DTCS)2菲2+AG处理后复合物被还原。NO-的EPR信号(DTCS)2菲2+在全血和肺组织中复合物在AHPP治疗后增加(图)。4 e和f⇓).采用AHPP处理后NO产量的增加反映了O的含量2-和过氧化物(Onoo-),因为阿2-与NO快速反应生成ONOO-几乎以扩散速度。相反,在Griess测定中,AHPP并没有增加亚硝酸盐/硝酸盐的含量(如图。3 c和d⇑)因为ONOO的数量-已被计算为硝酸盐,ONOO-.
体内NO-(N‐(二硫代羧基)肌氨酸)的自旋捕获2菲2+(没有投票权)2菲2+)复合物在注射了SEB的小鼠肺中形成,通过电子顺磁共振(EPR)波谱分析。小鼠肺注射了a)磷酸盐缓冲盐水(PBS), b)盐水/NaOH处理SEB, c)氨基胍(AG)和d) 4 -氨基- 6 -羟基吡唑(3,4 - d) -嘧啶(AHPP)处理后,观察到EPR谱。地理的浓度没有投票权)2菲2+在pbs或seb灌注小鼠肺和全血中加入生理盐水/NaOH、AG和AHPP。与生理盐水/NaOH和AHPP相比,AG抑制了NO-(DTCS)的浓度。2菲2+seb灌注小鼠全血和肺中g: g量阀;G:高斯。所有数据均显示为平均值±扫描电镜(生理盐水/NaOH处理小鼠:n=3;AG处理小鼠:n=3;AHPP治疗小鼠:n=3)。
葡萄球菌肠毒素B注入小鼠肺和支气管肺泡灌洗细胞的免疫组化
用抗iNOS抗体免疫组化检测seb注射后3天肺和BAL细胞中iNOS蛋白的诱导。在注射SEB的肺中,巨噬细胞和中性粒细胞浸润肺泡和肺泡间隔壁,可见iNOS染色(图)。5 a和b⇓).在注入SEB的小鼠BAL细胞的巨噬细胞和中性粒细胞中也观察到iNOS的阳性染色(图5c)⇓).在pbs注射的对照组肺中观察到很少的染色(图5d)⇓).核实ONOO在当地的生产情况-在seb灌注小鼠的肺和BAL细胞中,硝基酪氨酸的形成,众所周知的ONOO的生物标志物-免疫组织化学评价。肺巨噬细胞和中性粒细胞硝基酪氨酸染色明显阳性(图。5 e和f⇓)和BAL细胞(图5g⇓).抗酪氨酸抗体的染色模式与抗inos抗体的染色模式相似,这一点非常重要,因为这表明了inos衍生的NO可能转化为ONOO-在肺发炎的部位。
注射葡萄球菌肠毒素B (SEB) 3天后小鼠肺和支气管肺泡灌洗(BAL)细胞免疫组化;特异性抗诱导型一氧化氮合酶(iNOS) (a-d)和硝基酪氨酸(e-h)。在SEB注射的肺中,巨噬细胞(箭头)和中性粒细胞(箭头)浸润肺泡和肺泡间隔壁,可见强烈的inos染色(a和b)。在注射SEB的小鼠BAL细胞的巨噬细胞(箭头)和中性粒细胞(箭头)中观察到阳性的抗inos抗体反应(c)。pbs注射的肺用抗inos抗体染色(d)。用抗硝基酪氨酸抗体(e-h)染色也得到相同结果。内部尺度条:a、d、e、h=50µm, b、c、f、g=10µm。
诱导黄嘌呤氧化酶/黄嘌呤脱氢酶活性在葡萄球菌肠毒素-B滴注小鼠中
O.2-评估了该SEB诱导的IP模型中的产量,分析了AHPP的治疗机制。在SEB或PBS(控制)滴注后的各个时间点的小鼠肺,S-BAL流体和等离子体中的XO / XD活性如图6所示⇓.在SEB注入的小鼠中,在滴注后3天观察到S-BAL流体和肺中的最大XO / XD活性。S-BAL流体中的XO / XD活性和SEB灌注小鼠的血浆明显大于第3天对照小鼠(P <0.05),肺中XO / XD活性的增加更大,更大没有统计学上,而不是对照小鼠。通过使用AHPP的治疗与第3天相比,通过用AHPP治疗显着降低了来自小鼠S-BAL流体和血浆的XO / XD活性(图6⇓, p < 0.05)。在肺中的XO/XD活性方面,AHPP处理与对照之间没有显著差异,可能是因为肺中存在抑制化合物,这种活性难以测量。
黄嘌呤氧化酶/黄嘌呤脱氢酶(XO/XD)活性在a)支气管肺泡灌洗液(BAL)、b)肺和c)葡萄球菌肠毒素b (SEB)灌注小鼠血浆中的时间进程。与磷酸盐缓冲盐水(□)相比,SEB(•)在注射SEB后第3天增加了XO/XD活性。4‐氨基‐6‐羟基吡唑(3,4‐d)-嘧啶(AHPP)在第3天对XO/XD活性的抑制作用(d) BAL液,e)肺和f)血浆。平均±sem值,每组至少5只小鼠。***:P <0.001;#: p < 0.005。
B型葡萄球菌肠毒素小鼠支气管肺泡灌洗细胞诱导型一氧化氮合酶和黄嘌呤氧化酶/黄嘌呤脱氢酶信使核糖核酸水平的时间进程
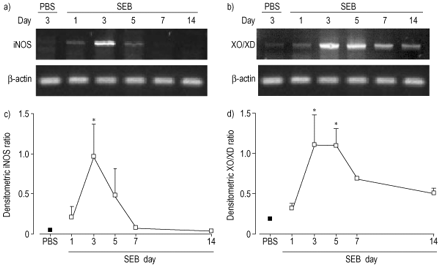
没有和o的过量生产2-被确认通过在分子水平上诱导iNOS和XO/XD。采用RT-PCR方法测量SEB给药后1、3、5、7和14天BAL细胞内iNOS和XO/XD mRNA水平,并与pbs灌注小鼠进行比较(图7)⇓).seb灌注小鼠iNOS和XO/XD mRNA水平均升高,并在第3天达到峰值。第3天seb灌注组与pbs灌注组差异显著(p<0.05)。
用SEB (staphylococcal enterotoxin‐B, SEB)灌注小鼠的支气管肺泡灌洗(BAL)细胞中信使核糖核酸(mRNA)的水平:a)诱导型一氧化氮合酶(iNOS);b)黄嘌呤氧化酶/黄嘌呤脱氢酶(XO/XD)。3只小鼠在PBS (phosphate-buffered saline)灌注后第3天或SEB灌注后第1、3、5、7、14天获得BAL细胞。时间过程c) iNOS和d) XO/XD。iNOS和XO/XD mRNA水平的密度比表示为平均值±SEM水平相对于β‐actin mRNA水平的每个样品。*: p < 0.05。
葡萄球菌肠毒素B注入小鼠支气管肺泡灌洗液中诱导型一氧化氮合酶诱导活性和细胞因子的产生
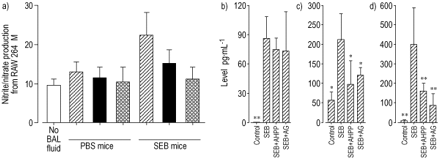
为了评估INOS诱导活性,分析了来自SEB注射的小鼠的BAL流体在原始264细胞的细胞培养基中诱导亚硝酸盐/硝酸盐产生的BAL流体。第3天的BAL流体注射SEB刺激的原始264细胞以产生亚硝酸盐/硝酸盐,并且在来自PBS灌注对照的BAL流体中未观察到这一点(图8A⇓).在图8B-D中示出了在第3天第3天在第3天在S-BAL流体中对促炎细胞因子水平的影响⇓.与pbs灌注对照组相比,SEB灌注显著增加s‐BAL液中TNF‐α、IL‐1β和IFN‐γ的水平。AG和AHPP可显著抑制SEB灌注小鼠s‐BAL液中IL‐1β的水平,分别为50.4%和38.3%。同样,AG和AHPP处理显著抑制SEB注射小鼠s‐BAL液中的IFN‐γ水平,分别降低78.6%和59.9%。尽管没有统计学意义,AG和AHPP治疗也抑制TNF - α水平。
a)培养的RAW 264细胞的支气管肺泡灌洗液(BAL)一氧化氮合酶(NOS)诱导活性。通过测量连续稀释s‐BAL液刺激培养后释放的亚硝酸盐/硝酸盐来评估诱导性NOS的诱导(└1×2;▪:1×5; : 1×10)。平均值±sem (n=5)值显示。b)肿瘤坏死因子(TNF)‐α;c)白介素- 1β应承担(IL 1β)应承担的;d)交互一些γ干扰素(干扰素γ应承担的)。酶联免疫吸附法检测BAL液中细胞因子浓度。小鼠注射磷酸盐缓冲盐水(PBS)或葡萄球菌肠毒素B (SEB),并在注射后用盐水/NaOH、氨基胍(AG)或4‐氨基‐6‐羟基吡唑(3,4‐d)嘧啶(AHPP)处理3天,获得BAL液体样本。每组至少6只小鼠的平均值±sem值。* *: p < 0.01;*: p < 0.05与单独注射SEB的小鼠
: 1×10)。平均值±sem (n=5)值显示。b)肿瘤坏死因子(TNF)‐α;c)白介素- 1β应承担(IL 1β)应承担的;d)交互一些γ干扰素(干扰素γ应承担的)。酶联免疫吸附法检测BAL液中细胞因子浓度。小鼠注射磷酸盐缓冲盐水(PBS)或葡萄球菌肠毒素B (SEB),并在注射后用盐水/NaOH、氨基胍(AG)或4‐氨基‐6‐羟基吡唑(3,4‐d)嘧啶(AHPP)处理3天,获得BAL液体样本。每组至少6只小鼠的平均值±sem值。* *: p < 0.01;*: p < 0.05与单独注射SEB的小鼠
这些结果表明,NO和O2-可能参与了促炎细胞因子的表达,AG和AHPP都可能通过抑制促炎细胞因子的产生而起到抗炎作用。
讨论
在本研究中,NO和O的产生增加2-在找到自动免疫相关IP的鼠标模型中。没有和o的过量生产2-与BAL流体中的TNF-α,IL-1β和IFN-γ的高级别产生密切相关。抑制不和o2-通过AG和AHPP(INOS和XO抑制剂分别)生产抑制了促炎细胞因子的产生并防止了IP的发展。这些结果在理解知识产权机制方面非常重要,并且可以为自身免疫疾病相关IP提供新的治疗方法。
seb注射小鼠BAL液和血清中亚硝酸盐/硝酸盐产量增加,并通过EPR光谱直接检测NO的生成。同样,在seb注射的肺中,XO/XD活性被高度上调,蛋白和mRNA水平增加,并释放到肺泡空间。有报道称NO在调节细胞功能中发挥重要作用,并在肺损伤中具有抗炎作用21,22.然而,在肺部的炎症部位,高浓度的O2O2-快速将NO转换为RNS,如ONOO-二氧化氮(NO2).RNS被认为是肺部炎症的重要介质,对肺细胞具有高度毒性20..体内检测ONOO-由于其半衰期短,反应活性高,不易降解。然而,NO-(DTCS)的增加2菲2+复合物在AHPP处理后,由于抑制O2-生产,是ONOO的间接证据-在肺中形成SEB。此外,ONOO的本地生产-使用抗酪氨酸抗体的免疫组化方法对炎症部位进行了验证。AG和AHPP均可降低BAL液中巨噬细胞、淋巴细胞和中性粒细胞的数量,从而减少病理性肺组织损伤面积。这些结果支持ONOO的观点-介导肺损伤,是seb诱导的IP发病机制中的一个因素。
seb注射小鼠的BAL液诱导RAW 264细胞iNOS活性。几种促炎细胞因子与巨噬细胞诱导的iNOS表达有关。此外,XO/XD的表达受到IL - 1β等促炎细胞因子的调控。XD(低O2-生成活性)转化为XO(高氧2-产生活性)的过程,包括硫醇氧化和/或蛋白质水解。事实上,seb注射小鼠BAL液中细胞因子(IFN‐γ、IL‐1β和TNF‐α)的水平明显高于对照组小鼠。这些发现表明,seb激活的Th1细胞产生的IFN‐γ或seb激活的炎症细胞产生的IL‐1β和TNF‐α刺激肺泡渗出巨噬细胞诱导iNOS基因表达。此外,AG和AHPP抑制促炎细胞因子的产生表明NO和O2-上调这些细胞因子的表达。推测iNOS、XO和细胞因子诱导之间存在正反馈回路,导致seb注射小鼠肺中RNS和ROS的过量产生。
转录因子核因子κB (NF - κB)和活化蛋白1 (AP - 1)诱导基因表达,介导免疫反应、应激反应、细胞生长和细胞存活。NF - κB和/或AP - 1的激活在活的有机体内肺炎症中早期反应细胞因子如TNF - α、IL - 1β、iNOS和IFN - γ的产生是否必要23,24.NF - κB和AP - 1是已知的氧化还原敏感转录因子,可被ROS和RNS激活。关于ROS和rns介导的NF-κB和AP - 1通路的激活机制已经进行了各种研究。细胞因子的信号沿着信号转导途径,从上游蛋白激酶级联到下游转录因子。ROS和RNS直接激活细胞因子受体通过受体二聚或受体酪氨酸激酶(RTK)的激活,它激活一个蛋白激酶级联,如MAP激酶(MAPK)和IκB激酶(IKK)25.许多论文认为抗氧化剂抑制细胞因子基因的诱导通过抑制NF-κB和/或AP‐1的激活26.因此,作者认为AG或AHPP治疗seb诱导的肺炎症和纤维化的有效性在于这些药物能够抑制NF-κB和AP‐1的激活,从而抑制促炎细胞因子的产生。本研究结果表明,对NO和O的抑制作用2-AG和AHPP的产生不仅降低了自由基的直接毒性,还减少了自由基介导的细胞因子的产生。
先前对人类和小鼠巨噬细胞的研究表明,NO在TNF - α和IL - 1β的产生中起调节作用20.,27,28.据报道,内源性NO在U937细胞中上调TNF-α产生28和肺泡巨噬细胞27.但在一定条件下,NO可下调细胞因子的产生20.,29.这些研究之间的差异仍然没有得到解释。NO对NF - κB调节的浓度依赖性已被报道30..低水平的没有激活NF-κB途径通过IKKs的激活。相反,高水平的NO部分抑制NF - κB通过年代亚硝基化等62p50亚基的Cys,消除NF-κB dna结合能力。越来越多的证据表明,RNS,如ONOO-或没有2,可能激活NF-κB。因此,不是所有的,但许多NO的细胞毒性效应可能是由ONOO介导的-,而不是它本身。因此,NO在细胞因子诱导活性中的双刃剑作用可能取决于NO的来源和水平、细胞类型、氧化还原状态以及ROS的细胞内外状态。因此,鉴定NO在seb诱导的组织损伤中的作用将有助于了解这一微妙的平衡。
综上所述,超级抗原作用于Vβ8+在小鼠自身免疫相关性间质性肺炎模型中,T细胞上调炎症部位一氧化氮和超氧阴离子的生成以及促炎细胞因子的生成。一氧化氮与超氧阴离子相互作用生成过氧亚硝酸盐,是本模型中肺部炎症的重要介质。内源性一氧化氮和超氧阴离子或其反应产物过氧亚硝酸盐调控促炎细胞因子的产生,在本模型中可能参与了间质性肺炎的损伤过程。此外,诱导型一氧化氮合酶和黄嘌呤氧化酶抑制剂可能是治疗肺泡炎和/或间质性肺炎纤维化的潜在药物。
- 收到了2001年7月31日。
- 接受2001年11月29日。
- ©ERS期刊有限公司