⇓本欧洲呼吸学会/美国胸科学会(ERS/A188bet官网地址TS)工作组立场文件的目的是定义介入肺学领域,并描述在方法和后勤方面的最低要求,每种介入手术的适应症、禁禁症、结果和培训要求。这份立场文件是由一组欧洲和北美专家编写的。
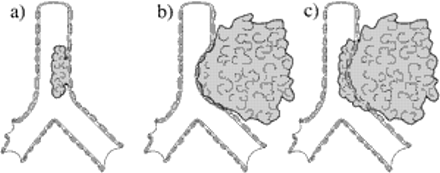
三种主要类型(a-c)在气管水平的恶性中央气道梗阻的示意图,具有相同程度的管腔狭窄。1)管腔内的;b) extraluminal;C)混合阻塞。
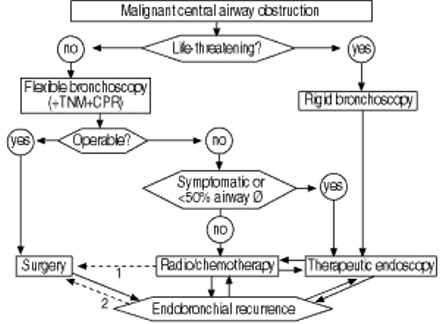
恶性中央气道梗阻的处理算法。六角形框中的术语是条件;矩形框中的项是过程。双向箭头指示支气管内肿瘤复发的趋势和反复需要多方式治疗。间断箭头:1:最初不能手术的肺癌,在初次治疗性支气管镜检查后可继发手术,通常随后进行新辅助治疗;2:手术后肺癌的罕见病例,最初表现为中央气道梗阻,经过仔细的支气管内复发再行手术后仍可手术。TNM:肿瘤分期,包括组织学;CPR:病人的心肺储备。转载须获授权81.
介入肺科学可以被定义为“与诊断和侵入性治疗程序相关的医学艺术和科学,这些程序需要额外的培训和专业知识,超出标准肺部医学培训计划的要求”。本学科所涉及的疾病过程包括复杂的气道管理问题、良性和恶性中央气道阻塞、胸膜疾病和肺血管手术。与这些领域相关的诊断和治疗程序包括但不限于:刚性支气管镜、经支气管针吸、自体荧光支气管镜、支气管超声、经胸支气管针吸和活检、激光支气管镜、支气管电手术、氩等离子凝固、冷冻疗法、气道支架植入、球囊支气管成形和扩张技术、支气管辐射(近距离治疗)、光动力疗法、经皮扩张性气管切开术,经气管置氧管,医学胸腔镜和影像学引导胸廓介入。后两个主题在本文中没有涉及,因为它们最近在本刊的其他地方已经被广泛的评论覆盖了1,2.
设施、人员、程序前调查和监测
为了进行介入手术,必须有设备齐全的设施、训练有素的人员、术前评估和监测。
设施
病房内应能放置担架或床,检查台应能从四面八方进入。调暗日光是必要的。套件的大小和设备的放置应考虑到支气管镜医师、麻醉师和护理人员之间的最小干扰。为加强合作,建议在录像观察下进行手术。某些手术可能必须在手术室进行(见下文)。病房应配备心肺监护和复苏设备。患者应在单独的房间进行准备和恢复,并配备氧气供应、真空吸入和充分的监护。
人员
支气管镜医师、麻醉师和护理人员应接受手术前的适当培训。麻醉师应精通常规、喷射和单肺通气。所有人员应经常执行这些程序,以保持其能力。对于介入手术,至少需要一到两名护理助理。如果手术是在全身麻醉下进行的,则需要增加一名麻醉师和专科护士。
Preprocedure评价
在进行任何手术之前,必须了解病人的病史,并进行彻底的身体检查。为了选择合适的患者,医生必须了解以前的治疗方法和当前的表现状况。实验室测试(如。推荐全血计数、电解质、凝血谱、心电图、胸片)。额外的研究,如计算机断层扫描(CT),肺功能测试,和动脉血气评估可能需要取决于程序的性质。
内镜治疗的适应症主要是晚期癌灶的姑息,但也越来越多地用于早期肺癌的治愈。前者主要用于缓解中央气道梗阻引起的呼吸困难,术前评估理想情况下应确定梗阻以外的肺是可行的,且呼吸困难与梗阻有效相关。图1⇑图示恶性气道阻塞的三种主要类型。早期肺癌的治疗是一个完全发展的领域,在这个阶段还不能给出明确的指导方针。为了澄清该领域的术语,将内镜下从正常组织到浸润性癌的各种可见病变定义如下:1)正常组织:正常上皮,无明显组织学改变;2)炎症:以急性和慢性炎症细胞明显浸润为特征,无明显异型性/异常增生;3)化生/增生:粘液细胞增生,基底细胞增生,无异型性(最多2 ~ 3层);4)轻度异型/发育不良:基底细胞增生伴核异型,三层或三层以上局限于层下三分之一,核轻微增大,罕见有丝分裂象;5)中度异型/发育不良(异常/癌前改变):基底细胞增生伴核异型,基底细胞延伸至地层下三分之二,核轻度增大,极性丧失,偶见核分裂象;6)严重异型/发育不良(异常/癌前改变):基底细胞增生伴核异型,基底细胞延伸至层厚三分之一以上,核增大,极性丧失,染色质分配不均,有丝分裂象频繁,角化;7)癌原位(异常/癌前病变):多面体细胞,核大小不等,极性丧失,染色质分配不均,有丝分裂象频繁,角化;8)微浸润性癌(异常/癌前病变):支气管黏膜内有癌浸润,但未向支气管壁深入;9)浸润性癌(异常/癌前病变):癌细胞浸润到支气管软骨和支气管壁。
监控
连续脉搏血氧测量和其他监测程序必须根据当地有意识镇静指南进行。虽然在局麻和清醒镇静的情况下可以通过柔性支气管镜进行一些手术,但如果情况需要,介入支气管镜医生应该准备转换为全身麻醉。
硬质支气管镜检查
刚性支气管镜是指在各种光源、望远镜和辅助仪器的辅助下,经口或经腹切开术通过刚性仪器进行诊断或治疗。
设备
刚性支气管镜检查可能需要以下四种设备中的任何一种:1)经典通气支气管镜:远端有斜角的开口管,通常在近端包含几个用于导光镜、望远镜、器械引入和辅助通气的端口;2)用于气管疾病的刚性内窥镜仪器:无侧孔的实心管;3)用于远端气道内窥镜的支气管镜:带侧孔的气管,以维持双侧通气;或者4)各种角度的望远镜,可以连接到摄像机,以提供良好的气道可视化和记录。
人员
因为刚性支气管镜检查通常是在全身麻醉下进行的,麻醉医师、护士和其他熟悉手术过程的助手必须协助支气管镜检查医生。
麻醉
全身麻醉可通过静脉注射或吸入进行。目前,静脉麻醉是首选。可采用的通气技术有:自发通气、自发辅助通气、文丘里射流控制通气、高频通气或闭路正压通气。
技术
麻醉诱导后,患者头部部分伸出,支气管镜插入中线,斜面朝前。操作者的手指或塑料牙齿保护器可以保护上面的牙齿。支气管镜进入会厌并通过然后旋转90°,所以它可以无痛地通过声带。一旦气管进入,支气管镜向后旋转90°,并向下气道前进。为了检查其中一个支气管,支气管镜医生将患者的头部向对侧肩部旋转。
在插管患者中,支气管镜沿气管内管推进至声带水平。然后取出气管内管,支气管镜进入气管。另一种插管技术是使用喉镜将会厌向前抬高,并允许支气管镜通过声带。此时,操作者通过支气管镜观察并引导它穿过声带。通过支气管镜使用望远镜以充分显示节段气道的水平。许多诊断和治疗程序可以通过刚性支气管镜进行。
迹象
刚性支气管镜的主要适应证是:大咯血的处理、气管支气管狭窄的治疗、异物清除、肿瘤切除和支气管深壁活检。治疗程序,如机械切除和扩张,可以完成仅与瞄准镜的桶。激光纤维、冷冻治疗和电灼探针、球囊扩张器、支架、吸管和各种活检和取钳等工具可以通过刚性支气管镜的筒体插入。
刚性支气管镜检查的禁忌症包括:颈椎不稳定,严重的颌面创伤或畸形,或阻塞性口腔或喉部疾病。
培训要求
刚性支气管镜方面的培训应保留给在柔性支气管镜和气管插管方面有丰富经验的医生。受训者应首先在人体模型或动物模型上练习,并应在单独尝试此程序之前执行至少20个监督严格的支气管镜检查程序。为保持能力,该程序应至少执行10-15次·年−1.
经支气管针抽吸
经支气管针抽吸(TBNA)是一种对气道壁、肺实质和气管支气管树旁纵隔结构内的病变进行细胞学、组织学或微生物取样的技术。
设备
选择合适的针取决于适应症;除粘膜下病变取样外,所有诊断针应≥13毫米长。为了获得标本进行组织学检查,应使用19号或更大的针。用于细胞学检查的标本可使用22号或更大的针获得。对于纵隔和肺门病变,需要一根带硬导管的针。对于周围病变,应使用带较软导管的针。要抽吸纵隔囊肿或脓肿,应使用21号,15毫米长的针和更宽更硬的导管。为防止损伤柔性支气管镜的工作通道,所有针头都应采用可伸缩设计。除了支气管镜医生,这个过程还需要一个专门的助手。
技术
TBNA最常通过柔性支气管镜进行。在择期TBNA前应充分复查胸片和胸部CT,以准确定位病变。对于周围病变,TBNA应在透视引导下进行。肺癌分期时,应避免支气管分泌物污染样本。柔性支气管镜可引入支气管树,无需吸痰。覆盖在目标部位的气管支气管分泌物要洗掉。TBNA可在支气管内检查之前和获得任何支气管内标本之前进行。在TBNA导管近端使用注射器吸入,在针从气管支气管壁抽出之前应停止。在多个淋巴结受累的患者中,首先选取预后最差的淋巴结(N3)。每个目标部位应获得两个满意的标本。 Each disposable needle should be used in one patient only.
细胞学标本可以通过将样品喷在载玻片上进行现场检查或固定而立即制备。将样品冲洗到细胞块的防腐溶液中也是可以接受的,并且是组织学标本的首选方法。细胞学标本必须由有经验的细胞病理学家阅读。标本的快速现场评估提高了诊断率。每个标本应明确分为阳性、恶性或阴性。支气管癌的分期不应以肿瘤细胞数量少为依据。标本中大量淋巴细胞的存在说明它是足够的淋巴结样本。样本中的呼吸道上皮细胞应引起对可能污染的关注。一个真正的阳性样本显示大量的肿瘤细胞团块或腺体形成。真阴性标本应有大量淋巴细胞。 A negative TBNA does not rule out malignancy. Every positive result should be interpreted individually, using a team approach of the clinicians involved.
迹象
TBNA的主要应用是通过纵隔和肺门淋巴结的采样来诊断和分期支气管癌,以及诊断支气管周围/气管肿块、粘膜下疾病和肺周围结节。次要应用包括支气管内坏死性或出血性外生性病变的诊断,预测手术切除路线,小细胞癌或淋巴瘤的随访,纵隔囊肿和脓肿的诊断和引流。
结果
TBNA对肺癌分期的诊断率在15-83%之间,阳性预测值为90-100%。TBNA更有可能在以下情况下成功:使用组织学针;小细胞癌存在;隆突异常;放射学证据提示纵隔疾病;病灶位于右侧;淋巴结很大;或者病变在气管旁或隆突下。在评估周围肺结节时,TBNA通过促进钳或刷子无法触及的病变取样,使柔性支气管镜的诊断率提高20-25%。在获得性免疫缺陷综合征(AIDS)患者的粘膜下疾病、结节病和纵隔淋巴结病的评估中,TBNA也被证明可以提高产量。
并发症
严重并发症很少发生。自限性小出血、气胸、纵隔气肿或相邻结构的无意穿刺可以通过适当的纵隔解剖知识以及胸部CT的全面复查来避免。TBNA中对柔性支气管镜的损伤是一个真正值得关注的问题,可以通过严格遵循最佳程序来避免。
自体荧光支气管镜检查
自体荧光支气管镜(AFB)使用检测正常和异常组织荧光的设备来检查气管支气管树,以确定癌前和恶性粘膜异常。
迹象
荧光支气管镜系统可帮助定位常规白光支气管镜无法识别的恶性和癌前黏膜区域。初步研究表明,荧光支气管镜可提高支气管粘膜异常(如发育不良和癌)的敏感性和定位原位.这项新技术的应用目前正在进行评估,用于筛查有发展支气管癌风险的患者。
禁忌症
除了常规白光支气管镜外,使用荧光支气管镜没有已知的禁忌症。
结果
AFB用于鉴别常规白光支气管镜未见的粘膜异常时,可能以降低特异性为代价提高敏感性。需要进一步的研究来确定这些设备在支气管癌高危患者的管理中的适当使用。
并发症
除柔性支气管镜外,荧光支气管镜未见并发症报告。
支气管内超声
支气管内超声(EBUS)是一种可视化气管支气管壁及其周围结构的诊断技术。超声波被传送到解剖结构,反射的回声被转换成电信号。
设备
超声探头有两种类型:1)7.5 MHz的扇形换能器,安装在专门设计的7毫米柔性支气管镜的尖端;2) 2.8-3.2 mm的气球头微型探针,带有12 mhz和20 mhz传感器,可通过常规柔性或刚性支气管镜的工作通道插入。此外,还需要一个驱动装置来旋转微型探测器,以及一个超声波处理器,用于产生超声波并生成图像。
技术
超声探头轻轻按在支气管壁上,并沿着被研究的结构通过。对于圆形视图,仪器必须围绕其轴旋转360°。在目标位置,用蒸馏水使气球膨胀,直到实现紧密的圆形接触,并且可以看到墙壁和周围的结构。这些图像存储在视频和照片上。如果病人服用镇定剂或全身麻醉,并且预充氧足够,则可以对气管进行短时间检查。该探测可以传递到所有感兴趣的区域。
迹象
EBUS用于评估支气管癌淋巴结累及的区域延伸(分期),在诊断或治疗干预前识别和定位气管附近的纵隔结构(纵隔肿瘤、心脏、食管和大血管),定位肺组织中的固体结构进行活检,并分期肿瘤侵入支气管壁的深度。在这些情况下,EBUS可以作为CT的补充。
禁忌症
除柔性支气管镜外,EBUS无禁忌症。
结果
与已建立的放射诊断程序相比,EBUS的作用尚未通过前瞻性多中心研究进行评估。
并发症
具体到EBUS的并发症尚未报道。
经胸穿刺活检
经胸穿刺/活检(TTNA/B)是指对胸壁、肺实质和纵隔的病变进行经皮取样,用于细胞学、组织病理学或微生物学检查。
设备及人员
以下是执行此取样程序所需的设备和人员清单:1)适当长度的吸针,规格(18-25)和设计(切割)与非切割)根据所需样品;2) x线片或超声引导定位病灶,引导置针;3)准备试样的用品;4)气胸引流管;5)心脏氧饱和度监测仪;6)训练有素的助理。
技术
针穿的深度、角度和位置应事先估计。在提供局部麻醉后,针或套管针可在透视、CT或超声引导下以无菌方式引入。然后可以将标本喷洒到载玻片或溶液中,并使用标准的细胞学技术进行处理。
迹象
TTNA/B的适应症包括诊断肺周围结节或浸润、胸膜肿块、选择性空腔病变、纵隔肿块和其他可及的胸部病变通过经皮的方法。
禁忌症
TTNA/B的禁忌症是不可纠正的凝血功能障碍,不可纠正的低氧血症,血流动力学不稳定,肺动脉高压,大疱性肺气肿,病变太接近血管结构。相对禁忌症为既往行过肺切除术,用力呼气量< 1l。
结果
TTNA/B对所有大小病变的总体诊断敏感性为68-96%,特异性为⪕100%,准确性为74-96%。病变越小,诊断准确率越低。
并发症
气胸的发生率为~ 20 ~ 40%,其中50%的气胸患者需要放置胸管。自限性出血和咯血并不常见。
激光支气管镜检查
激光支气管镜是利用激光能量输送的通过标准支气管镜,以治疗各种支气管内疾病。
设备
只有波长可以通过光纤传输的激光才适合进行激光支气管镜检查。这些包括磷酸钛钾(KTP),氩染料,钇铝钙钛矿(YAP), Nd-YAG(钕钇铝石榴石)和二极管激光器。Nd-YAG激光目前是气道切除术的首选,因为它对活组织的影响是可预测的(即。光凝或汽化),取决于应用的能量。
人员
进行激光支气管镜检查的医生应该具备柔性和刚性支气管镜方面的专业知识,以及激光物理学的工作知识。可能需要机构激光委员会的认证。除了标准支气管镜检查通常需要的辅助人员外,还应有一名助理全权负责控制激光。因为在支气管外科中使用的大多数激光都有因反射能量而造成眼部损伤的风险,所以患者和激光团队都需要戴上防护眼镜。
技术
激光支气管镜可以用柔性或刚性支气管镜进行。大多数专家倾向于采用刚性支气管镜技术,原因有四:1)全身麻醉的使用对患者和医生来说更舒适;2)开口管可同时使用激光纤维、吸管和镊子;3)使用刚性支气管镜更易控制通气和出血过多;4)支气管镜可进行扩张和机械切除,缩短手术时间,减少激光照射量,更彻底地缓解梗阻。此外,如果有指示,硅胶支架放置也可以在同一过程中进行。刚性技术的相对缺点包括手术费用的增加,这是由于需要全身麻醉,手术室时间和人员,以及上肺叶病变不容易治疗的事实。在需要增加机动性的情况下,可通过刚性支气管镜使用柔性支气管镜。
安全的激光切除术依赖于维持通气、预防出血和尽量减少激光照射。必须经常检查未阻塞的气道,并清除碎片、血块和血性分泌物。为减少出血的危险,使用低功率激光凝固病灶是很重要的(如。30-45瓦(W),脉冲持续时间为1秒,纤维距离为1厘米)。如果光纤太接近目标(如。在3毫米内),组织将被烧焦和汽化。在可能的情况下,应通过机械切除尽量减少激光照射。建议持续抽吸以消除烟雾。氧饱和度应持续监测。吸入氧浓度不应为>40%,以尽量减少点燃易燃装置的风险(如。吸入导管,激光纤维,柔性内窥镜)。
迹象
中央气道管腔内的任何梗阻(即。对影响通气并产生明显症状的气管、左右主干支气管、支气管中间和肺叶孔)可考虑进行激光切除术。最常见的指征是不能手术的癌症,无论是原发性肺癌还是支气管内转移。激光切除可联合放疗或化疗。与冷冻疗法或近距离疗法相比,激光疗法具有立竿见影的效果。
其他适应症包括预后不确定的肿瘤(腺样囊性癌,类癌肿瘤),良性支气管内肿瘤,以及气管或主支气管的医源性或感染后瘢痕性狭窄。通常需要机械扩张和假体支架的联合治疗。
禁忌症
激光支气管镜的绝对禁忌症是孤立的气道外源性压迫(图1⇑).
结果
激光治疗恶性疾病的主要目的是提高生活质量,这是在大多数治疗患者中实现的。危重气道梗阻患者生存率提高。气管和主支气管病变缓解恶性梗阻的成功率为> ~ 90%,但远端病变则降低至60 ~ 70%。良性瘢痕性狭窄成功率高(>90%),但可能需要重复治疗和/或支架置入。
手术最常见的并发症是出血、低氧血症、穿孔和心脏事件。并发症发生率应<5%。
支气管电手术和氩-血浆凝固
支气管内电手术(EES)(同义词:电灼或透热)被定义为高频(HF)电流的应用通过使组织凝固或汽化的探针。氩等离子体凝固(APC)是非接触模式的单极电凝固;采用氩气作为导电介质。
设备
EES和APC所需的设备如下:1)高频发电机;2)绝缘探头(刚性,柔性),将电流传递到目标组织(探头类型为单极和双极;单极探针可以是刚性或环形,钳子或柔性陷阱,切割或凝固);3)中性板完成电路,如果使用单极探头;4)如果使用柔性支气管镜进行检查,则需要绝缘仪器以防止电流泄漏;除发电机外,APC内还装有氩气(带流量计的油箱)和同时输送气体和电流的微电极导管。
技术
电手术和APC都使用电产生的热量来破坏组织。根据所使用的能量,可以引起凝固或汽化。由于其非接触性质和较低的能量密度,APC产生更均匀但表面的热效应。对于较大、体积较大的病变,首选使用刚性器械;而柔性支气管镜适用于浅表小病变。APC是止血的首选模式,也可能适用于覆盖面积较大的病变。电手术探针与目标组织直接或密切接触,以传递电流,直到看到所需的效果。在靶向肿瘤组织本身之前,可以先在正常支气管黏膜的一个小点上测试能量设置(通常为25-50 W)。重要的是要持续抽吸,以保持目标区域没有血液和粘液,并将烟雾排出。能量设置可以根据可见的组织效果而改变。
迹象
EES的适应症与激光手术基本相同,包括支气管内外生性病变的姑息性消肿,以及良性支气管内肿瘤和医源性或感染后瘢痕狭窄的治疗。EES的另一个适应症是可见浅表肺癌(严重发育不良到微浸润癌)的潜在治愈。APC的适应症包括内窥镜下可见来源的出血凝固和气道肉芽肿病变的治疗(如。病变在气道支架附近)。EES和APC产生立竿见影的效果。
禁忌症
绝对禁忌症是存在易受电干扰的起搏器或气道排他性腔外梗阻(见图1)⇑).一个相对禁忌症是金属物体的存在,在接近任何一个电极。
结果
治疗效果与其他使用热能的技术相当(如。激光、冷冻疗法)。潜在的并发症包括出血、火灾、气道穿孔和狭窄。
支气管冷冻疗法
冷冻疗法是用极冷的方法局部破坏活体组织。与激光或电手术相比,冷冻破坏是延迟的,在应用后的几个小时到几天内发生。
设备
冷冻治疗可以通过刚性或柔性支气管镜进行,需要刚性或柔性冷冻探头。常用的低温剂是氧化亚氮(N2O)和液氮(N2).
技术
冷冻疗法利用液态气体快速膨胀引起的冷却来冷却冷冻探头的尖端(焦耳-汤普森原理)。探针的尖端被冷却到- 40°C的工作温度,这足以破坏活组织。将冷冻探针放置或插入病变2-3次,在同一位置反复冷冻和解冻,然后移动到邻近部位。冻结/解冻循环的效果可以通过视觉或阻抗测量进行监测。冷冻时间在30-60秒之间。解冻时间取决于探针的类型,从刚性探针的几秒钟到柔性探针的⪕60秒不等。通常在1周内进行重复支气管镜检查,以清除粘液组织,必要时重复治疗。冷冻疗法可以在高氧环境中安全地进行。
迹象
冷冻治疗主要用于缓解非危重的支气管内外植性梗阻性病变和清除异物和血栓。其他适应症包括治疗低度恶性病变(如。腺样囊性癌)及早期癌症(如。癌原位).
禁忌症
禁忌症为气管腔外梗阻或抗低温组织梗阻(如。纤维组织或软骨)。
结果
治疗结果与其他使用热效应的技术(如。激光、电外科学);治疗效果不是立竿见影的,而是在几天后才能看到。清洁支气管镜检查可能是必要的,以清除碎片。
并发症
并发症的发生率低于5%。包括出血和肿瘤充血导致的短暂性气道阻塞增加。
气道支架
气道支架或气管支气管内假体是用于重建气道开放的空心假体装置,用于支持狭窄或软化的气管支气管壁或封闭气道瘘。
设备
表1描述了各种类型的支架⇓.大多数支架有各种形状(直型、y型、j型)、直径和长度。支架由聚合物、金属或两者的组合(混合)制成。输送装置包括刚性支气管镜及其附件、专门设计的刚性支架引入器系统(一般用于聚合物支架)、柔性支气管镜及其附件、专门设计的柔性支架引入器系统(一般用于金属支架和混合型支架)。在某些情况下(即。狭窄,曲线狭窄),透视引导可能是必要的。
技术
首先是狭窄的类型、长度和直径(图1)⇑)进行支气管镜检查。其他资料可透过CT (如。局部解剖,气道远端狭窄,肺动脉开放)。在引入支气管镜之前,需要建立一定程度的气道通畅。可选择的方法包括扩张外部压迫的气道或切除腔内病变。支架的最佳长度应超过狭窄的边缘;外径应略大于受累气道的正常直径。特定支架的选择取决于狭窄的类型。内窥镜和x光片确认支架位置和通畅是必要的。
迹象
气道支架植入术的适应证为:1)因恶性或良性疾病导致的中心气道外源性狭窄伴或不伴腔内成分;2)复杂、不能手术的气管支气管狭窄;3)气管支气管软化;4)缓解腔内肿瘤复发性生长;5)中央气道瘘(食管、纵隔、胸膜)。
禁忌症
当组织长入(肿瘤、肉芽)可能导致阻塞时,如果预期要移除支架,应避免使用未遮盖的金属支架。一般情况下,如果在梗阻之外存在无法存活的肺,应避免放置支架。每种类型的支架都有独特的禁忌症(表1⇑).
结果和并发症
大多数患者症状缓解,生活质量和肺功能改善。迄今为止,长期随访仅适用于Dumon硅胶假体(Endoxane®,Novatech SA, Grasse, France)。一般而言,可预期并发症在⪕占所有病例的20%(表2⇓).
支气管内近距离放射疗法
“Brachy”是一个希腊语词根,意思是短或近;因此,近距离放疗允许局部肿瘤照射。近距离放射治疗的模式包括直接在肿瘤间质中植入放射性粒子,使用注射器系统和柔性支气管镜植入源,经皮ct引导的源放置,以及最常用的通过支气管镜腔内插入导管的方法。
人员及设备
近距离放射治疗需要专门的人员和设备。人员包括但不限于放射肿瘤学家、支气管镜医师和适当的支持人员。该设备包括一个带有适当屏蔽的独立房间,以及在高剂量率(HDR)处理的情况下,一个远程后加载装置。铱192 (192I)是目前首选的辐射源。
技术
后置导管插入通过柔性支气管镜。如果支气管被完全阻塞,最初的消肿可以用各种设备来完成。导管通过支气管镜的工作通道向前移动,直到到达所需的位置。固定导管,并将假源装入导管中,以指导放射肿瘤学家计算剂量。导管的位置可以通过透视或胸片确认。然后患者可以被运送到合适的位置进行插入192我的来源。对于最佳剂量和分馏频率尚无共识。低剂量率任意设定为1-2灰(Gy)·h−130-72小时。中、中剂量率为2 ~ 10 Gy·h−110小时。HDR定义为>10 Gy·h−11小时内送达。
迹象
近距离放射治疗的主要指征是缓解恶性气道阻塞引起的症状,如咳嗽、咯血和呼吸困难。近距离放射治疗也可能对某些非常早期的浅表癌症(不扩散到支气管壁以外的癌症)有治疗潜力。近距离放射治疗被认为是安全的患者谁接受了之前的外束放射治疗。
禁忌症
不能进行常规支气管镜检查或在6个月内曾在同一部位接受过支气管内放疗的患者禁用近距离放疗。
结果
近距离放射治疗可长期缓解50%的患者的症状。在⪕90%的病例中,咯血得到改善。增加激光切除术可改善对近距离治疗的反应。据报道,联合治疗可延长生存期,改善生活质量。
并发症
与支气管镜检查和后负荷置管相关的并发症包括气胸、出血、感染、咳嗽、导管移位、心脏心律失常和支气管痉挛很少见(0.5%)。放射治疗的并发症包括致命出血、气管食管瘘、气管血管瘘、软组织坏死、放射性支气管炎和支气管狭窄。这种情况发生在5-15%的患者中。
光动力治疗
光动力疗法(PDT)涉及静脉注射的光敏剂,当暴露在适当波长的光和氧气存在时,会导致细胞死亡。
人员及设备
使用PDT的医生必须同时了解激光技术和光敏剂。Photofrin II®(二血卟啉酯;Quadra-Logic Technologies Inc., Vancouver, Canada)是迄今为止唯一获得广泛批准用于肺癌治疗的光敏剂。该化合物由波长为630 nm的激光光源激活。用于传输光的处理纤维是石英纤维,用于圆柱形或间质处理区域的扩散器,或用于聚焦表面处理的微透镜。光剂量测定是复杂的,需要训练有素的人员。
技术
在注射光敏剂后的推荐等待期后,患者接受支气管镜检查,可以用适当波长的光照亮异常区域。根据需要,光可以以浅表或间质方式(探针插入肿瘤)传输到目标组织。PDT的作用不是立竿见影的,而是在48小时内发生。因此,对于有梗阻性病变的患者,需要进行清扫性支气管镜检查。如有必要,可提供重复照明。
迹象
PDT已在美国、日本和几个欧洲国家获得批准,用于治疗不延伸到气道壁以外的浅表癌症,不适用于手术或外束放射治疗的患者,以及作为晚期癌症导致支气管梗阻导致肺部症状的姑息治疗。PDT反应不依赖于肿瘤的细胞类型。
禁忌症
PDT禁忌用于对血卟啉成分过敏的患者和有卟啉症、严重中央气道梗阻的患者,或侵袭主要血管或食管的肿瘤患者。
结果
PDT在60-80%的早期粘膜癌中产生完全缓解率。对于梗阻性病变,PDT已被证明可以缓解80%患者的气道阻塞。
并发症
PDT的主要并发症是皮肤光敏,可在注射后4-6周发生。局部气道水肿、肿瘤坏死和迟发性狭窄可引起气道阻塞。肿瘤溶解可导致出血和瘘管穿孔。
经皮扩张气管切开术
经皮扩张性气管造口术(PT)是一种床边技术,包括经皮针穿刺气管,然后逐步或一次性扩张和放置气管造口管。
人员及设备
操作人员(外科医生、重症专科医生或肺科医生)需要一名助手给病人注射镇静剂,监测生命体征,并处理气管插管。建议在支气管镜医师的陪同下评估气管插管的正确位置、气管中线穿刺、导丝和扩张器的正确推进。各种PT套件都可以在市场上买到所有必要的设备和用品。
技术
PT在重症监护室进行,患者需仰卧、麻醉、通气,颈部伸直。甲状腺和冷冻软骨被识别。手术区域已经准备好,同时病人接受100%的氧气。在内窥镜观察下,气管内管被收回,使其泄气袖口刚好在声带下方。如有需要,可进行局部麻醉。然后在第一或第二气管间隙上做一个1.5-2.0厘米长的水平切口。将一根12或15号针插入气管中线,并通过它引入导丝。取针后,可以使用Ciaglia或Griggs/Schachner技术。
Ciaglia技术
通过导丝将8-French (F)引导导管引入气管。气管造口部位通过使用12-F-36-F润滑扩张器在这个双导轨上逐步扩张来准备。装有适当大小扩张器的润滑气管造口管(如。然后将24f扩张器(用于8毫米气管造口管)引入气管。听诊和支气管镜确认气管造口管定位正确后,取出气管内管。较新的套件包含一个单锥形扩张器,其中气管造口可以创建一个插入。
开发/ Schachner技术
专用的经皮气管造口工具(由一个斜角的金属圆锥组成,在中心裂开,连接到一对关键的手柄),在金属丝上引导,通过气管前壁牢固地引入,并打开以扩张气管造口部位。取出导丝,在直接观察下,将气管造瘘套管放置在舒适的塑料套管针上(带一个泄气的袖口)。套管针被取出,袖带充气,气管内管被取出,气管造口套管被固定。
迹象
PT的适应症与常规气管造口术相同。
禁忌症
相对禁忌症包括紧急情况、儿童年龄、解剖畸形、明显肥胖或凝血功能障碍。PT的绝对禁忌症是皮肤感染和以前的重大颈部手术。
结果和并发症
随机临床试验表明,早期和晚期并发症(狭窄)的发生率与外科气管造口术一样低或更低,并且具有更好的美容效果。PT可以在更短的时间内进行,比传统的气管切开术更具成本效益。PT的死亡率很低(0.2%),主要并发症的发生率<1.5%。气管撕裂伤、假通道插入和出血是最常见的并发症。
经气管氧疗
经气管氧疗(TTOT)是一种将导管通过气管皮道插入气管,进行长期连续氧输送的方法。
迹象
任何需要持续、长期氧疗的患者都是TTOT的潜在候选者。对于难治性低氧血症,需氧量> 3-4 L·min的患者,建议采用TTOT−1不耐受鼻插管(鼻出血,局部刺激或过敏),自愿或非自愿不服从(美容原因,夜间脱位),需要通过减少氧气流量来改善活动能力,嗅觉丧失。
禁忌症
禁忌症为插入部位胸膜突出(肺气肿性泡)、凝血功能障碍、严重共病或绝症、咳嗽反射障碍、缺乏意愿、能力或家庭支持照顾导管、无法沟通、上呼吸道梗阻。
设备
有多种TTOT导管可供选择。文献倾向于使用多步手术工具包(SCOOP, Transtracheal Systems, Denver, CO, USA)来促进技术的标准化,提高患者的适应性,并最大限度地减少并发症。用于大流量氧疗(>4 L·min−1),首选多孔永久导管。这减少了背压和无意中断开氧气管。导管直径应≥3mm,长度应足够长,使远端尖端高于隆突2-3厘米。
技术
适当的患者和家庭教育是必需的在tott手术之前。必须确定患者或家属对导管的护理能力。多步TTOT手术包括使用Seldinger技术在局部麻醉下将无菌导管插入气管。在插入后的第一周,初始导管允许尿道形成。在此期间没有氧气输送。最初的导管被替换为更柔软的单端口导管供氧。这将留在原地8周,并进行清洁而不移除。最后一步是用较软的开孔导管替换第二根导管,患者可通过成熟的气管皮瘘进行更换和清洗。
第一周提倡使用抗生素、止咳药和止痛药。必须在每次就诊时评估患者的能力,在插入TTOT后的第一年至少每3个月评估一次。应根据制造商的建议更换TTOT导管。
结果
在休息和运动时,TTOT产生的血氧含量比其他供氧系统所需的血流速率低(39-72%)。微小的通风和呼吸的工作减少。呼出的微小通气和动脉血液中的二氧化碳压力(P,有限公司2)不变。吸气肌和隔膜的代谢工作也减少了。通过12分钟步行来评估运动耐力,TTOT比吸氧更好通过鼻插管。与鼻插管氧疗相比,TTOT可能会带来更大的生存益处,并且通过对呼吸困难、嗅觉、口腔摄入、体重增加和因美容因素而产生的整体幸福感、独立感以及减少抑郁和提高士气的趋势产生显著的主观改善,从而提高生活质量。
并发症
最重要的并发症是导管周围形成粘液球,这可能导致上气道阻塞,需要拔除导管。轻微的并发症与手术有关(如。头导管移位和皮下肺气肿)或早期,通常是短暂性的问题,如咳嗽和痰量增加。
气管支气管病变的综合治疗
多模式治疗是指多种内镜技术的结合或内镜与非内镜方式的结合来治疗气管支气管病变。
基本原理
各种内窥镜治疗方式是相当新的,许多治疗内窥镜医生只熟悉其中的几个。因此,比较各种内镜技术用于相同适应症的报道很少。其中一些技术几乎完全是竞争性的,如激光和支气管内电手术;因此,大多数专家将使用其中之一或另一个。有些技术是互补的(如。支架和激光或支架和支气管内电手术);典型的混合病变合并(图1)⇑),具有腔内成分(可切除)和腔外成分(需扩张和置入支架以维持气道通畅)。每种技术对某一类型气道病变的相对值列于表3⇓,为选择治疗组合提供指导。
一个尚未被广泛研究的主题是内窥镜与非内窥镜治疗方式的结合。这种联合疗法主要用于中央气道不能手术的恶性肿瘤的治疗。实际上,在这些情况下,多模式治疗意味着放化疗与一种或多种内镜治疗方式的结合。肿瘤学家使用的术语“多模式”通常只指放疗和/或化疗以及手术。本工作组认为,这一术语应扩大到包括内窥镜治疗。
决定在什么情况下使用何种治疗形式是非常重要的。图2⇑显示了最近提出的管理恶性中央气道阻塞的算法。最初治疗的选择在很大程度上取决于情况的紧急程度以及以前的治疗。在气管、主隆突或双主支气管水平的高级阻塞通常必须通过紧急内镜治疗来缓解,以保证生存。为了评估内镜治疗的技术可行性和计划治疗,必须进行诊断性支气管镜检查,大多数情况下(在非重要情况下)使用柔性支气管镜。如果病变是可以切除的,就像大多数良性病变一样,手术是治疗的选择。对于引起症状或气道直径缩小50%的不可切除的中央气道病变(通常定义为叶前水平),许多内窥镜医生倾向于在进行非内窥镜治疗之前先用内窥镜治疗缓解梗阻。>50%的气道阻塞似乎是进行内镜治疗的合理指征,因为这种程度的气道阻塞患者通常有症状或在非内镜治疗时可出现症状(如。放射治疗)导致组织肿胀。选择内镜治疗的决定总是要因人而异。在恶性肿瘤中,也取决于组织诊断。小细胞癌和淋巴瘤是化学敏感的,所以即使它们造成50%的梗阻,也可以在非内镜下治疗。然而,在现实中,大多数恶性疾病患者被转介到内镜治疗已经用尽了所有的非内镜选择。
内镜治疗效果评估
肺部介入治疗的结果评估是比较诊断结果(如。准确性)或治疗结果(如。治疗,生存,生活质量),数据来自研究人员,科学协会或政府机构发布的建议,指南,一般规则或标准。
仪器
所有相关数据应存储在传统或数字文档系统中。介入性手术尤其应记录在录像和摄影胶片上。
评估数据
数据应包括患者病史、介入前和介入后的临床和实验室调查结果、治疗指征、知情同意、手术本身、监测、手术结果、副作用和并发症。
结果评估的目的
诊断程序的目的是发现或排除和分类病理过程,作为治疗的基础。理想情况下,每个适应症在流程图上都应该有一个明确定义的位置。对于治疗程序,通常评估主要终点和次要终点。在姑息治疗中,症状缓解程度和生活质量是主要标准,生存是次要结果。对于治愈性治疗,还必须在长期随访中记录确切的愈合和生存时间。
变量
对于诊断程序,敏感性、特异性和诊断准确性必须与竞争对手的方法进行比较。对于治疗程序,定期进行与呼吸困难程度、肺功能检查(流量/容量循环)、胸片和性能相关的常规非侵入性测量。受累气道横截面积的定量测量可通过目测或激光或超高速CT(如果有的话)进行。
副作用和并发症
应报告所有副作用和并发症。这些副作用包括:轻微副作用(如。不需要治疗的心律失常);支架内轻度感染;近距离放疗、电灼或PDT时粘膜肿胀;轻微的出血;在活检过程中不需要引流的咳嗽或气胸;还有气管穿刺。此外,严重的并发症包括大量出血、窒息、穿孔、坏死、瘘管和脓肿形成、支架移位、复发性梗阻和激光灼伤。
患者接受度和成本效益
与手术相关的患者接受度以及其他与治疗相关的因素,如等待时间、环境和工作人员的态度,直到最近才引起人们的关注。相比之下,有关设备、人力和其他资源的费用的详细分析已成为人们更关心的问题,特别是在退还费用、购置仪器和安排工作时间方面。
- ©ERS期刊有限公司