摘要
气道炎症现在被认为是囊性纤维化(CF)肺部疾病发病的一个主要因素。其最典型的特征是中性粒细胞显著而持续地流入气道,中性粒细胞通过释放活性氧和蛋白水解酶等有害介质而损害肺。
最近的研究表明,炎症很早就发生,甚至可能在没有感染的情况下发生。此外,假设CF跨膜电导调节功能障碍与感染和炎症之间存在联系;细胞因子产生失调和上皮细胞宿主防御异常被认为是持续炎症的原因。
支气管肺泡灌洗和中性粒细胞和炎症介质的评估提供了最准确的气道炎症图像。然而,常规支气管镜与支气管肺泡灌洗对患者来说是不愉快的,通常对个别病例的管理没有立即的好处。
因此,通过无创方法收集替代标记物对囊性纤维化患者的随访有很大帮助。在囊性纤维化患者的痰、血清和尿液中检测了几种与气道炎症程度相关的标志物。需要长期的研究来证实它们潜在的临床效用和特异性,并确定哪些可用于临床监测疾病结局和治疗效果。
囊性纤维化(CF)是高加索人群中最常见的缩短寿命的常染色体隐性疾病。它是由位于7号染色体长臂上的单个基因突变引起的,该基因编码1480个跨膜糖蛋白残基。这是CF跨膜电导调节器(CFTR)1,在上皮细胞的顶端膜上起环腺苷单磷酸调控氯通道的作用。最近的数据表明CFTR还参与调控其他离子通道(刺激其他氯离子通道或抑制上皮钠通道)、核内体融合和囊泡内运输2.CFTR在CF中存在缺陷、定位错误或缺失1,导致盐和水通过上皮屏障的运输受到干扰。CF的特点是临床表现的广泛变异性;外分泌腺导管中的粘液分泌物脱水和堵塞易导致多器官临床表现,特别是在胃肠道、肝胆、生殖道和呼吸道。主要临床表现为慢性阻塞性肺疾病、外分泌胰腺功能不全、钠含量高+和Cl−在出汗,和男性不育症。
以特定菌群慢性气道感染为特征的进行性肺部疾病是CF患者发病和死亡的主要原因1.尽管最近在理解CF的细胞和分子基础方面取得了进展,但导致不可逆肺损伤的事件顺序仍然不明确。然而,气道炎症现在被认为是一个主要因素3.,4.传统观念认为,原发性遗传缺陷导致氯化物分泌缺陷和钠重吸收增加,导致气道内高黏性分泌物,从而损害粘液纤毛清除。慢性细菌感染更容易引起异常和持续的炎症。然而,最近的研究表明,炎症是一种非常早期的事件,甚至可能在没有感染的情况下发生。事实上,CFTR缺陷与感染和炎症之间可能存在直接联系3..无论它们的时间关系如何,感染和炎症在疾病发展的早期就密切相关,彼此加剧对方。因此,形成了感染和炎症的恶性循环,这主要是渐进性和不可逆的肺损伤的原因。本文将重点介绍CF肺病中炎症的发生和病因,其在肺损伤中的作用及其与气道感染的关系方面的最新进展。CF中的炎症反应标志物也将被描述。
囊性纤维化肺病
CF肺部疾病的主要临床特征是慢性气道感染和反复急性加重,具有独特的菌群,导致不可逆的肺损伤。CF肺正常在子宫内在出生后的头几个月,除了气管粘膜下腺轻微扩张5,6.然而,许多病人在出生后不久就被细菌感染,并出现气道炎症。早期表现以异常黏液堵塞小气道最为突出,伴粘膜及黏膜下层炎性浸润。随着时间的推移,过多的粘液产生、气道阻塞、气道慢性感染和气道慢性炎症导致严重的支气管扩张和呼吸衰竭。
囊性纤维化患者气道感染的微生物
虽然许多微生物都能感染CF肺,但主要的病原体是长期感染气道的细菌:金黄色葡萄球菌,流感嗜血杆菌,铜绿假单胞菌.金黄色葡萄球菌而且流感嗜血杆菌早期,通常在临床症状出现之前就已出现CF气道,而感染铜绿假单胞菌几乎所有病原体都会跟着其他病原体7,8.CF和之间有一种特殊的联系铜绿假单胞菌;气道慢性感染这种微生物,特别是粘液菌株,与进行性肺恶化密切相关,尽管进展速度是高度可变的。大多数患者在学龄或青春期早期被慢性感染。非粘液类菌株的早期定植有时可以被根除,但菌株往往会持续存在并改变其表型。产生藻酸盐的粘液变异体的出现,是CF的高度特征,与肺功能的更快下降有关。一旦在CF气道内建立,铜绿假单胞菌是出了名的对化疗有抗药性1,8- - - - - -10.它长期在支气管腔内定植,几乎从不突破上皮屏障。
在过去的十年里,感染着伯克不过的问题日益引起人们的关注。这种多重耐药生物菌株也可感染CF气道,有些菌株表现为患者之间的直接交叉感染。慢性不过感染通常伴有不良的临床病程(20-30%的感染患者病情迅速恶化,并伴有菌血症和死亡)。8,10.
囊性纤维化患者气道感染的易感性
CF中基本缺陷与气道感染易感性之间的因果关系是一个及时但极具争议的研究领域。没有系统免疫缺陷可以解释CF患者对特定菌群感染的特殊易感性已被记录。尚未观察到呼吸道外感染增加。细菌主要存在于支气管内,不会引起免疫功能低下的宿主所注意到的侵袭性或播散性感染1,4,10.这些临床数据表明,CF肺部疾病是由气道的宿主防御系统被破坏引起的,并由无法有效清除感染而传播。已经提出了许多假说来解释CFTR功能障碍如何导致CF患者对气道感染的易感性。利用新切除支气管标本培养的上皮细胞,松井et al。11发现Na+和Cl−在正常和CF培养中,表面液的浓度和渗透压不同。然而,CF上皮显示加速等渗液体吸收,耗尽气道表面液体量,导致粘液纤毛清除受损和粘液增厚。这些发现支持了传统观点,即CF的主要缺陷是粘液脱水,损害粘液纤毛清除,有利于CF相关病原体的气道感染。对CF患者粘液的研究显示了一系列的流变学异常12,而在活的有机体内粘液纤毛清除研究尚无定论13,14.此外,CF和原发性纤毛运动障碍综合征之间的临床过程和粘液纤毛清除障碍的比较强烈地表明,清除缺陷不足以解释CF中观察到的感染易感增加和进行性阻塞性肺病。在原发性纤毛运动障碍综合征中,粘液纤毛清除比CF更严重,而肺部疾病和慢性气道感染的严重程度要低得多铜绿假单胞菌在病程中发生较晚且频率较低15.
相反,另一种假说认为CFTR缺陷导致盐浓度升高,从而损害CF气道表面液(ASF)内的先天防御机制。ASF含有多种相互作用的抗菌因子,包括抗菌肽和β-防御素1和2,它们可以杀死细菌铜绿假单胞菌还有其他物种16- - - - - -18.这些肽的活性对盐敏感,在CF患者气道上皮细胞培养的ASF中显著降低。降低盐浓度可恢复CF ASF的抑菌活性在体外.这表明防御系统的组成部分是完整的,但无法在CF患者气道内异常高浓度的NaCl中正常发挥作用16.这一理论的核心是CF ASF中NaCl含量的升高,这一观察结果是有争议的19.进一步的研究和技术的发展,以提供准确的测量CF ASF的电解质组成在体外而且在活的有机体内可以证实这个假设。
最近的证据表明,CFTR功能障碍导致CF中气道上皮细胞和细菌之间的相互作用受损。因此,这些异常可能直接干扰宿主的防御。
在体外研究表明铜绿假单胞菌粘附于CF患者的呼吸道上皮细胞,特别是受损和再生细胞,而不是对照细胞20.,21.这被认为是由于受体数量的改变铜绿假单胞菌粘附素在细胞表面,这反过来是受CFTR的影响。的确,P。绿脓杆菌皮林,受体负责铜绿假单胞菌结合,识别和结合到细胞表面糖脂asialo神经节苷M1 (aGM1),但不是唾液化的同系物。aG)M1CFTR功能障碍导致CF气道上皮细胞水平升高20..
CFTR也与摄取有关铜绿假单胞菌通过培养人气道上皮细胞。已有研究表明,表达CFTR ΔF508等位基因的细胞在细菌摄取方面存在缺陷22.尽管这与临床相关在体外虽然观察结果尚不清楚,但这种机制可能进一步导致CF中微生物清除能力受损。综上所述,这些观察结果表明CFTR的主要缺陷与CF中局部宿主防御能力受损之间存在直接联系。
不管感染的起始机制是什么,一旦感染,就是慢性的铜绿假单胞菌在大多数CF患者中,感染对于加速肺部疾病的进展至关重要。尽管宿主有强烈的反应,但细菌仍然存在于气道中,这反映在对许多细菌产生抗体上铜绿假单胞菌抗原和免疫复合物的形成4,23.表现型转换铜绿假单胞菌大菌落中的黏液生长抑制吞噬作用,被认为是主要的持续机制。高抗原性的粘液样胞外多糖铜绿假单胞菌导致免疫复合物的形成原位,从而进一步刺激炎症反应。这种炎症反应阻止了感染的全身扩散,但未能从气道中根除它,最终对气道和肺实质造成不可逆的损伤4,23.
囊性纤维化的炎症
气道炎症的特点
CF患者气道炎症最典型的特征是宿主和细菌趋化剂吸引多形核中性粒细胞进入气道腔内。CF肺中导致慢性中性粒细胞流入的化学引诱剂包括可溶性细菌产物、补体第五组分的片段,如C5a和C5adesArg,以及细胞产物,如白介素(IL)-8和白三烯(LT) B43.,4,23.IL-8是主要的中性粒细胞趋化肽,由包括中性粒细胞在内的多种细胞类型产生。即使在稳定的临床情况下,CF患者的痰液、支气管肺泡灌洗液(BALF)和血清中的IL-8水平也会升高24,25.这些介质水平与BALF中中性粒细胞的数量相关。Di芒果et al。26有没有显示出绑定的铜绿假单胞菌致总检察长M1受体在CF气道上皮细胞上的水平较高,可诱导核因子(NF)-κB的活化,从而诱导IL-8的表达。铜绿假单胞菌产品也增加了气道上皮细胞产生IL-827.因此,炎症细胞和微生物维持CF气道中的IL-8水平,并维持一个放大炎症反应的正反馈循环。此外,最近的研究表明CFTR功能障碍可能是CF气道中IL-8水平升高的初始原因(见后文)。在CF痰和BALF中检测到其他促炎细胞因子,即IL-1、肿瘤坏死因子-α和IL-6的浓度升高,已知这些细胞因子可放大气道炎症25,28.
高水平的趋化剂和促炎细胞因子确保激活的中性粒细胞继续积聚在气道中,其分解是脱氧核糖核酸(DNA)的主要来源,这使得CF痰如此顽强。肺部感染的加重伴随着痰中DNA含量的增加。这主要是源于人类,而不是细菌29.中性粒细胞还释放一系列潜在的有害介质,如活性氧(ROS)和蛋白水解酶,它们可能损害周围组织(见后文)。
气道炎症的发生和机制
支气管肺泡灌洗(BAL)的使用使得对CF肺炎症过程的理解取得了重大进展。对CF婴儿和轻度肺部疾病患者的BAL研究为CF肺部疾病的发病时间和气道感染与炎症之间的关系提供了深入的了解。这些研究表明,炎症是一种非常早期的事件,发生在轻度疾病患者以及稳定的临床条件下30.- - - - - -32.Konstanet al。30.发现中性粒细胞主导的气道炎症在12岁的CF患者中始终存在,即使是那些病情轻微或临床症状远未加重的患者,气道中也有大量的中性粒细胞和活跃的弹性蛋白酶。
汗et al。31和阿姆斯特朗et al。32研究表明40%的婴幼儿存在气道炎症。这是在肺部疾病临床表现明显之前通过新生儿筛查发现的。令人惊讶的是,在一些没有明显感染迹象的婴儿的BALF中,中性粒细胞为主的炎症和IL-8水平升高。其他研究证实了气道中性粒细胞的存在,尽管通常的cf相关病原体培养呈阴性,这表明炎症甚至可能先于感染33.此外,Muhlebachet al。34最近报道,感染CF儿童的BALF中IL-8和中性粒细胞含量明显高于感染其他呼吸道疾病儿童的BALF。此外,即使将细菌数量考虑在内,CF患儿的炎症反应也高于对照组34.因此,CF肺的过度炎症可能与炎症反应调节的构成性异常有关,与感染刺激无关。两者都有在活的有机体内而且在体外CFTR功能缺陷可能与炎症加剧直接相关。
在无病原体条件下饲养的CF小鼠与野生型同窝小鼠相比,观察到气道黏膜下层炎症细胞数量增加35.此外,它已被证明在活的有机体内而且在体外ΔF508 CF支气管粘膜下腺上皮细胞在IL-8的产生中表现出选择性上调36在细胞外低渗、等渗和高渗NaCl含量下观察到,NF-κ b和高IκB激酶α水平与组成性活化有关37.CF支气管腺细胞的构成性和/或IL-8的过量产生,代表了CFTR在人类气道中的主要表达位点,可能涉及这些细胞促进CF患者气道炎症相关的中性粒细胞募集。相反,与对照细胞相比,CF支气管上皮细胞产生的抗炎细胞因子IL-10水平降低。在成年CF患者的BALF中也检测到较低水平的IL-1038.这些观察结果进一步支持了CFTR功能障碍与炎症反应失调有关的观点,并且异常的炎症控制机制有利于CF肺中的促炎细胞因子平衡。也有证据表明,这种功能障碍可能与CF气道中的氧化剂/抗氧化剂失衡有关(见下文)。
据报道,髓过氧化物酶依赖的氧化剂活性和氯胺释放在CF患者中高于对照组,并用阿米洛利或胆碱缓冲液治疗CF中性粒细胞后两者都被抑制39.这些数据表明,细胞内pH值或离子浓度可能与CF中性粒细胞髓过氧化物酶活性的改变有关。CF基因在中性粒细胞中的表达已被报道40CFTR与细胞内细胞器的pH调节有关,因此,这种基本的遗传缺陷可能导致CF气道内产生过多的氧化剂。CFTR还涉及调节谷胱甘肽的水平41它是一种重要的呼吸道抗氧化剂,其功能障碍也可能是CF患者报告的水平降低的原因42.最后,CFTR突变可能导致上皮细胞和白细胞的异常凋亡43.这可能是CF炎症反应增强的另一种机制在活的有机体内而且在体外因此,研究结果支持了CF的基本遗传缺陷导致气道内明显和持续炎症的论点。然而,还需要进一步的研究来确定炎症是否先于感染,并确定导致CF肺病的确切事件顺序。
炎症过程在肺损伤中的作用
不管炎症过程是如何开始的,以及CF中感染和炎症之间的时间关系,气道中持续的炎症反应在肺损伤的进展中起着核心作用,这是毫无疑问的。炎症反应不仅不能根除引发炎症的有机体,而且越来越多的证据表明,炎症反应实际上会导致局部宿主防御功能受损,从而干扰炎症的根除。因此,形成感染和炎症的恶性循环,导致肺组织的结构性损伤(图1)⇓).
慢性气道感染和高水平的化学引诱剂和炎症介质确保激活的中性粒细胞继续积聚在气道中。除了产生趋化因子和促炎细胞因子(两者都能放大和延续炎症细胞的招募),这些细胞还释放出一系列可能损害周围组织的有害介质。中性粒细胞弹性蛋白酶是这些介质之一,在CF慢性炎症的病理生理学中起着重要作用。它通过降解弹性蛋白、胶原蛋白和蛋白聚糖等结构蛋白直接导致组织损伤44,并在CF气道中有许多其他有害的生物活动。它是一种有效的促分泌剂,增强浆液腺细胞的大分子分泌45.它还促进粘液分泌器的肥大和增生,并抑制睫状体跳动在体外46,47.综上所述,这些影响可能进一步损害粘液纤毛清除,加剧CF患者的气道阻塞。中性粒细胞弹性蛋白酶还通过在吞噬细胞表面切割免疫球蛋白、补体成分和补体受体(补体受体(CR) 1)等调节受体,促进感染的持续,从而对调理吞噬作用具有重要影响48- - - - - -50.此外,分泌物中的中性粒细胞弹性蛋白酶本身可能通过诱导上皮细胞产生IL-8而吸引更多的中性粒细胞进入气道腔内51.
CF患者气道内游离弹性蛋白酶增多与中性粒细胞增多和蛋白酶两种主要生理抑制剂α的失活有关1抗胰蛋白酶(α1-AT)和分泌性白蛋白蛋白酶抑制剂。两种主要机制使α失活1CF肺中的at: 1)复合抑制剂被过量的、未复合的酶和/或假单胞菌蛋白酶切割,对其抑制活性不敏感;2)中性粒细胞激活时释放的ROS导致的失活4,23.CF痰免疫印迹显示少量α1-AT以高分子量复合物的形式与蛋白酶迁移,而抑制剂的大部分以低分子量降解产物的形式存在52.
由于过度的中性粒细胞为主的炎症,在CF患者的呼吸道中也有ROS的慢性负担。虽然ROS在CF肺病中作为组织损伤介质的作用尚未明确,但大量的间接证据支持其参与53.在CF患者中检测到痰液中细胞外髓过氧化物酶水平高,髓过氧化物酶是一种多形核中性粒细胞(PMN)衍生酶,可将过氧化氢转化为高活性氧代谢物,且与肺功能呈负相关54.据报道,与对照组相比,CF患者血浆中氧化产物浓度更高55.此外,肺中主要的局部抗氧化剂谷胱甘肽的水平在CF患者的上皮内膜液和血浆中都降低了42;这种缺乏症易使CF患者发生氧化组织损伤42.此外,最近有报道称,CF患者嗜酸性粒细胞释放细胞毒蛋白的倾向增加,这表明这些细胞及其介质可能导致CF的进行性组织损伤56.
总之,在CF肺部疾病的早期,感染和炎症形成了一个自我延续的恶性循环。过度的炎症反应不仅不能清除感染,而且导致其持续存在,是导致肺损伤和CF肺病进展的主要原因。
囊性纤维化中的炎症反应标志物
最近认识到气道炎症在CF进行性肺损伤中起着至关重要的作用,这鼓励了对其严重程度的可靠标志物的研究。BAL,连同中性粒细胞数量和炎症介质水平的评估,提供了最准确的气道炎症图像。然而,BAL的常规支气管镜检查对患者来说是不愉快的,通常对个别病例的管理没有立即的好处。因此,通过非侵入性程序收集的替代标记将有很大的帮助。
已经在CF患者的痰中评估了几种与炎症严重程度相关的标记物。在临床稳定的CF患者中,活性弹性蛋白酶痰液水平随着肺部受累程度的增加而增加57.相反,在一项前瞻性研究中,Suteret al。58发现抗生素治疗后这些水平显著下降。据报道,CF痰中存在高水平的其他中性粒细胞蛋白酶,如活性胶原酶,且与疾病严重程度呈负相关59.其他中性粒细胞介质,如氧化剂(氯胺、牛磺酸和髓过氧化物酶)54,趋化剂(LTB4)60还有一些促炎细胞因子25,已在CF痰中检测到数量增加。然而,尽管痰很容易收集,但这只能在年龄大到可以咳痰的人身上进行。此外,其中一些介质的痰液检测是不可重复的。
最近有报道称,与呼出的一氧化氮相比,CF患者呼吸凝析液中的亚硝酸盐水平升高,而一氧化氮是正常的,甚至很低61,62.这是一个潜在的标记,以跟踪炎症过程,需要进一步的长期研究。
作为潜在炎症标志物的众多血清和血浆分析中,没有一项被证明能高度预测急性变化。c反应蛋白和弹性蛋白酶α1-抗蛋白酶复合体经常在病情加重时增加,在抗生素治疗后下降。然而,在长期研究中观察到患者内部和患者之间存在广泛的变异性63.尿液中的两种炎症标志物,LTE4肌氨酸(一种弹性蛋白的分解产物)一直被提倡作为替代标记,但在长期研究中,它们的可变性也很高64,65.对临床稳定的CF患者血清中白细胞内皮粘附分子可溶性形式的评估表明,与健康对照相比,可溶性细胞内粘附分子(sICAM)-1和可溶性e-选择素(sE-selectin),但不含可溶性血管细胞粘附分子(sVCAM)-1显著升高。sICAM-1水平与疾病严重程度相关。一些患者在临床稳定时,以及在抗生素治疗肺加重前后都进行了一系列可溶性黏附分子的测量。有趣的是,与临床情况稳定时相比,所有患者在病情加重时血清sICAM-1和se -选择素水平均有所升高,并在静脉抗生素治疗2周后显著降低66.
血清和其他体液中可溶性黏附分子水平的增加已在几种炎症性疾病中得到证实。有人认为,它们的测量可能有助于监测炎症/免疫疾病。在目前的CF患者中观察到的增加可能反映了血管内皮细胞上这些分子的上调,这可能在CF肺部炎症的发病机制中发挥重要作用,并可能是其严重程度和持久性的指示。此外,作者的观察表明,它们的测量可以帮助CF患者的随访和监测抗生素治疗。需要长期的研究来证实这些标记物的临床潜力。
结论
明显的持续性炎症过程发生在CF肺部疾病的早期,即使在轻度、稳定的疾病中也存在。越来越多的证据表明,CFTR功能障碍与气道中发生的异常炎症反应之间存在联系。
认识到气道炎症是肺损伤的主要原因,为开发新的治疗策略控制其提供了理论依据。虽然基因替代疗法最终可能成为囊性纤维化患者的治疗选择,但目前,减少与气道炎症相关的肺损伤可能对疾病进展有最大的影响。更好地理解炎症机制和囊性纤维化感染炎症反应的动态是必要的。此外,现在还需要仔细对照的研究来确定炎症过程活动的最佳生物学指标,并为患者的临床随访和监测治疗效果确定简单可靠的标记物。
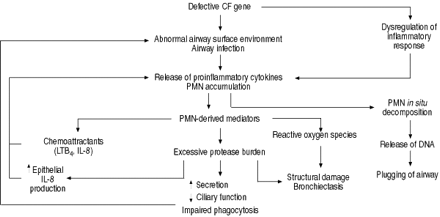
囊性纤维化(CF)肺的炎症反应。CF中过度的炎症反应在肺损伤中起主要作用。一个基本的遗传缺陷导致气道感染和炎症反应失调,这两者都有助于持续的多形核中性粒细胞(PMN)流入。此外,PMN自身释放的趋化剂和气道中高水平弹性蛋白酶诱导的白介素(IL)-8的产生维持了慢性PMN招募。这些细胞释放出一系列有害介质,如活性氧和蛋白水解酶,这些介质会导致结构损伤。过多的蛋白酶负担也会损害吞噬作用,促进感染的持续。因此,感染和炎症形成了一个自我延续的恶性循环,导致不可逆的肺损伤。LTB4:白三烯B4;DNA:脱氧核糖核酸。
脚注
↵本系列以前的文章:第1篇: Pilette C, Ouadrhiri Y, Godding V, Vaerman J-P, Sibille Y.肺黏膜免疫:免疫球蛋白a重述。呼吸呼吸J2001;18: 571 - 588。2号: Lambrecht BN, Prins J-B, Hoogsteden HC。肺树突状细胞与宿主感染免疫呼吸呼吸J2001;18: 692 - 704。3号: Moore BB, Moore TA, Toews GB。T和b淋巴细胞在肺宿主防御中的作用。呼吸呼吸J2001;18: 846 - 856。4号:消息SD,庄士敦SL.哮喘病毒感染的免疫学。呼吸呼吸J2001;18: 1013 - 1025。5号: Crameri R, Blaser K.对真菌感染和定植的过敏和免疫。呼吸呼吸J2002;19日:151 - 157。
- 收到了2001年3月22日。
- 接受2001年5月8日
- ©ERS期刊有限公司