摘要
白介素-12 (IL-12)被证明是一种有效和成功的辅助标准抗结核药物在患者患有进行性临床结核病(TB)。
IL-12是干扰素-γ产生的有效增强剂,是杀死细胞内细菌如分枝杆菌所必需的。该患者的结核病是进行性的,尽管对一线抗结核药物敏感,并在超过8个月的时间内直接观察药物治疗。IL-12辅助治疗3个月后,疗效明显改善。
本病例是文献中首次描述辅助白介素-12治疗结核病的病例,相信对更系统的辅助白介素-12治疗研究具有重要意义。
干扰素-γ (IFN-γ)在感染吞噬细胞的位置是杀死细胞内细菌(如分枝杆菌)的先决条件1。在结核病(TB)患者中,外周血单个核细胞(PBMC)的IFN-γ生产缺陷已被证实2和Sodhi等。3.描述了人类免疫缺陷病毒(HIV)阳性和阴性患者肺结核与肺外疾病的螺栓放射学程度和低IFN-γ产生之间的密切相关性。预激活t细胞中IFN-γ释放最有效的增强剂是白细胞介素(IL)-124。从最近的数据可以得知,结核病患者血清中的IL-12水平与疾病活动性不相对应5。对支气管肺泡灌洗液的分析显示,活动性肺结核患者表达IL-12受体β1和β2亚基信使核糖核酸(mRNA)的细胞增加6。用于其他部位的结核病即。结核性胸膜炎或淋巴结炎IL-12、受体-β2 mRNA表达升高在活的有机体内导致IFN-γ的产生增加7。
病例报告
一名24岁男性(167厘米,50.1公斤),出生于缅甸,1995年以来居住在德国,1998年4月因怀疑结核病住院。患者HIV 1/2血清阴性,既往无结核病史。诊断为肺结核伴粟粒性传播及结核累及颈部淋巴结。隔离的结核分枝杆菌对所有一线抗结核药物都敏感。联合异烟肼(0.3 g)、利拉平(RMP;0.45 g), eltambutyol (EMB;l.0 g)和吡嗪酰胺(PZA;1.5 g)启动。治疗方法为直接观察口服治疗(DOT),在抗结核药物吸收不良时,当疾病有临床进展时,再进行静脉注射。然而,在接下来的几周内,症状(发烧,咳嗽)在静脉治疗中有所进展,并重新开始口服DOT。患者在不同部位出现颈椎和纵隔脓肿,需要重复手术切口。结核分枝杆菌在脓肿的脓液中发现了相同的药物敏感性模式。肺部病变好转,最新分离结核分枝杆菌1998年10月被培养出来,仍然对所使用的药物敏感。然而,持续发烧,进一步发生颈部脓肿,从计算机断层扫描(CT)怀疑脾脏和腹部淋巴结受累。患者于1998年10月中旬转至Borstel医院(胸片见图1a⇓).在这里,DOT继续使用异烟肼(INH), EMB, RMP和PZA,直到1998年11月,由于肝酶的增加,RMP被利福布汀取代结核分枝杆菌菌株对这种药物敏感。12月用链霉素(SM)代替PZA,并给予30 g的累积剂量。肺受累进一步改善,但在颅骨中发现骨缺损,新的颈椎(图1b⇓),腹部及纵隔出现脓肿,其中一个位于左肺动脉附近。新发展的前足病变的脓液涂片阳性抗酸杆菌和脱氧核糖核酸(DNA)M.tuberculosis核酸扩增技术检测到-复合物,培养阴性。没有共存疾病,通过监测INH和RMP血清水平排除药物吸收不足。在辅助细胞因子治疗前,荧光激活细胞分选仪(FACS)分析了外周血中的细胞差异,显示活化t细胞(CD25+, CD38+)计数升高。IFN-γ释放在体外然而,稀释全血(DWB)和PBMC的刺激培养显著受损。患者知情同意细胞因子治疗,皮下注射IFN-γ(每日1次1.5×106U IFN-γ lb, Imukin®,勃林格殷格翰,德国)除上述结核药物。体外-在体外在后续研究中,受刺激的IFN-γ释放增加(见图2)⇓),但在4个月的治疗期间,患者的临床病程并没有如预期的改善,并出现了新的宫颈脓肿。停用IFN-γ处方。作为在体外添加IL-12可增加IFN-γ细胞的产量8在IL-12存在的刺激下,患者的PBMC是否会表现出增强的IFN-γ反应在体外进行了测试。
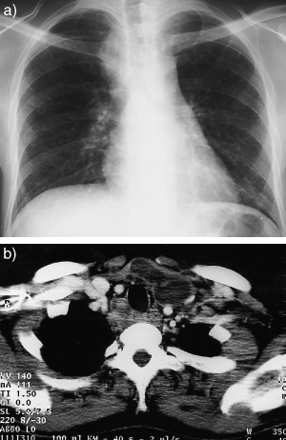
a) 1998年10月胸片显示右侧气管旁纵隔肿大。b)颈部电脑断层扫描显示颈椎脓肿(1998年12月)。
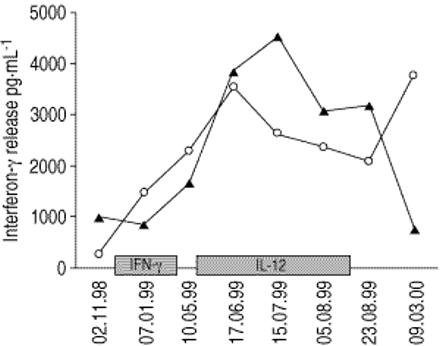
患者细胞培养上清中干扰素(IFN -γ)浓度。细胞作为外周血单个核细胞培养,用纯化蛋白衍生物(〇)或抗cd3(▴)刺激。灰色条形显示细胞因子名称,标记辅助细胞因子治疗的时间。il - 12: interleukin-12。
结果发现,IL-12的加入恢复了纯化蛋白衍生物(PPD)的抗原刺激以及植物血凝(PHA)和抗cd3单克隆抗体的多克隆刺激中受损的IFN-γ释放。然而,在未受刺激的PBMC中,IL-12没有诱导IFN-γ释放(图3⇓).因此,得出的结论是,患者t细胞IFN-γ释放能力受损不是由于主要的IL-12受体缺陷。因此,我们期望用IL-12治疗患者可以增强分枝杆菌特异性记忆t辅助细胞在感染部位的IFN-γ释放,从而增强t细胞和单核/巨噬细胞的局部抗真菌活性。以该细胞因子开始辅助治疗3个月(300 ng·kg体重)−1皮下注射,每周两次,重组IL-12,遗传学研究所,美国)。IL-12治疗事先获得了患者和当地伦理委员会的同意。在使用额外细胞因子治疗的同时,采用INH利福宾和EMB三联药物治疗。IL-12治疗最初导致培养的PBMC和DWB的PPD-IFN-γ释放正常化(图2⇑),最重要的是,显著改善了患者的临床病程:没有新的脓肿发生,纵隔脓肿减少,颅骨异常也减少了。胸片恢复正常,但脾脏仍有异常。细胞因子治疗的唯一副作用是药物注射后发烧和轻微虚弱。

在体外1999年1月,稀释的全血或外周血单个核细胞(PBMC)释放干扰素γ。用纯化蛋白衍生物(PPD)或抗cd3刺激培养,加入或不加入浓度为1 ng·mL的白细胞介素-12孵育−1或10 ng·mL−1。□:控制;░:用1 ng·mL孵育−1; : 10 ng·mL−1。
: 10 ng·mL−1。
停止IL-12治疗6个月后随访检查,不同部位淋巴结大小仅发生微小变化,但颈部出现直径2cm并有引流窦的淋巴结。患者继续按先前讨论的方法接受三联药物治疗。由于缺乏IL-12的可用性,IFN-γ治疗重新开始了4周,没有任何临床获益。重新应用IL-12 3周后,宫颈病变愈合,淋巴结大小减小到1厘米。IL-12治疗联合三联药物治疗,进一步治疗5个月。
讨论
提出的是一个不寻常的情况下,患者播散结核病和肺部和肺外反应之间的差异治疗。虽然证明了对标准抗结核药物的敏感性,但肺部受累有所改善,而肺外表现恶化。
通过与不同数量的IL-12共孵育,PPD或抗cd3刺激的IFN-γ释放增强,但未刺激的PBMC没有在体外只有在治疗方案中添加IL-12才能令人信服地改善患者的临床和实验室参数。全身应用IFN-γ无临床益处。的在体外在本试验中,检测患者PBMC中IFN-γ释放增强IL-12能力的能力至关重要,因为通过这种方法,遗传性IL-12受体缺陷已在一些分枝杆菌免疫受损患者的病例中被描述9,可以排除。8月5日,患者接受IL-12治疗时INF-γ释放数据显示在体外与7月15日应用相同治疗方案时相比,受刺激的IFN-γ释放减少,尽管浓度仍显著高于细胞因子治疗前的测量值。在分离的PBMC培养中,这似乎部分是由于8月5日PBMC中非b淋巴细胞的比例比7月15日相对较小,因为当与等量的非b细胞相关时,IFN-γ释放的减少被取消。
关于抗结核治疗肺部和肺外改善之间的差异,有实验数据表明脾肿大与淋巴组织结构破坏和凋亡增加有关,这可能是对抗分枝杆菌诱导的免疫病理无效免疫反应的重要组成部分10。这组数据与1例播散性结核在脾切除术前对化疗无反应的临床观察一致11。在病人脾肿大与持续病理改变脾脏ct扫描被记录。
据信,由于感染部位的细胞因子浓度不足,IFN-γ的应用不如白细胞介素-12有效(使用的剂量受到副作用的限制,即。发热等)。相比之下,添加白介素-12是一种更耐受的预刺激细胞兴奋剂。这一结果鼓励人们在更系统的基础上研究白细胞介素-12在结核病患者中的作用。
致谢
作者感谢德国慕尼黑遗传学研究所提供重组细胞因子白细胞介素-12和患者保险。
- 收到了2000年5月29日。
- 接受2000年10月13日。
- ©ERS期刊有限公司














