摘要
背景肺动脉高压(PAH)和肺静脉闭塞性疾病/肺毛细血管瘤病(PVOD/PCH)的遗传形式因肺组织病理学病变、临床和半临床表现、其责任基因和传播方式而异。自鉴定之始BMPR2在多环芳烃影响的家族中,已经发现了两种形式的其他几个基因突变。这些新基因的突变情况还不为人所知。
方法我们建立了下一代基于测序的靶向测序基因面板,可以同时分析PAH和PVOD/PCH的已知基因.对263例PAH和PVOD/PCH患者(成人和儿科病例)进行了前瞻性遗传分析。
结果19.5%的散发性PAH患者(n=180)、54.5%的家族性PAH患者和13.3%的PVOD/PCH患者中发现了致病突变。BMPR2突变频率最高的基因是TBX4在儿科和成人多环芳烃中BMP9在1.2%的成人多环芳烃病例中发现了突变。EIF2AK4双等位基因突变仅限于PVOD/PCH。在中还鉴定出截断突变和预测的功能丧失变异BMP102例重度散发PAH女性患者。
结论我们的研究结果证实了在基因之外也发现了突变BMPR2在遗传性多环芳烃中,强调TBX4而且BMP9,并指定BMP10作为一种新的多环芳烃基因
摘要
基因组测序揭示了肺高压在成人和儿科病例的遗传结构,强调的重要性BMPR2,EIF2AK4,BMP9而且TBX4突变,并提出BMP10作为疾病的新基因http://ow.ly/Oxes30mXnrI
简介
肺动脉高压(PAH)是一种罕见的严重的小肺动脉疾病,其特征是肺血管阻力的进行性增加,导致右心室衰竭,最终在没有治疗或移植的情况下死亡。当没有已知的危险因素或相关疾病被证实时,可诊断为特发性多环芳烃(IPAH) [1].除了特发性形式,遗传性形式的疾病占PAH病例的约30%(遗传性PAH (HPAH)),这一类别包括家族性形式(家族性PAH (FPAH)),有或没有确定的突变,以及携带突变的散发性形式[1].HPAH是一种遗传异质性疾病,是一种不完全外显的常染色体显性疾病。参与HPAH突变的主要基因是BMPR2(骨形态发生蛋白受体2型),是一种编码BMP信号通路2型受体的基因[2].BMPR280%的PAH和~ 15%的散发性PAH均有突变[3.,4].BMPR2基因突变携带者发病的男性为~ 14%,女性为~ 42%,尽管这一比例在不同家庭间差异很大[5].同一途径的其他基因突变,ACVRL1(激活素A受体样1型)和在极少数情况下英格(endoglin),可能导致PAH与遗传性出血性毛细血管扩张症(HHT)相关[6,7].突变的SMAD9,编码BMP信号转导的重要下游介质转录因子Smad8BMP9(别名GDF2(生长与分化因子2)),编码的配体ACVRL1,已在PAH [8,9].其他与BMP信号通路无关的基因突变也已被发现。突变KCNK3(钾通道双孔域亚家族K成员3;别名TASK1(twik相关酸敏K+通道1)),编码电压敏感的钾通道,已在一些多环芳烃家族中被发现,并证明了识别错义突变的功能后果在体外[10].一个纯合子KCNK3功能丧失(LOF)变体随后在一个近亲家庭的严重多环芳烃儿科病例中被描述[11].只有三个突变CAV1编码洞穴蛋白-1的基因目前已经被鉴定出来:其中一个基因属于多环芳烃的大家族,另一个基因属于多环芳烃新创在一个年幼儿童中发生突变,第三个与先天性全身性脂肪营养不良有关[12,13].
TBX4(T-box 4)突变已被识别为PAH的起源,通过重叠染色体缺失TBX4以及导致儿童多环芳烃,以及骨骼异常,这促使研究人员寻找突变TBX4其他儿科多环芳烃病例的基因[14].TBX4杂合失活突变是导致小髌骨综合征(也称为髋臼髌综合征)的原因,它在不同程度上与髌骨、骨盆、足部和股骨的骨骼异常有关。此前有报道称,携带aTBX4突变在儿科病例中较高,高于成人病例,这表明该基因突变在儿童中具有特定的影响[15,16].
肺静脉闭塞性疾病(PVOD)和肺毛细血管瘤病(PCH)均以小静脉和间隔静脉弥漫性重塑为特征,并伴有斑块状毛细血管增生和不同程度的动脉病变。的双等位突变EIF2AK4(真核翻译起始因子2α激酶4)已被证明是PVOD和PCH作为隐性疾病传播的遗传形式的原因[17,18].遗传性PVOD和PCH(在这里都被进一步称为PVOD)具有相同的临床表现,预后差,即使组织学肺病变可能不同(主要是由于毛细血管增生的重要性),也被认为是相同的实体。
本研究的目的是描述可以在前瞻性收集的一系列散在或fppah或PVOD患者中发现的突变,并推断每个已知的负责基因在成人和儿童形式的肺动脉高压中的各自位置。我们报告了大量PAH或PVOD患者的基因型和表型特征,通过基因组测序,允许检测单核苷酸变异(SNVs)和拷贝数变异(CNVs)。
患者与方法
病人
这项研究包括法国肺动脉高压调查中心的263名患者,这些中心包括法国肺动脉高压转诊中心(Hôpital Bicêtre, Université Paris-Sud, Le Kremlin-Bicêtre, France)和相关专家中心。所有病例均经专家中心临床诊断为散发性或PVOD、药物和毒素性PAH或散发性PVOD。根据先前描述的方案,在本研究纳入的所有患者右心导管插入术期间,通过血流动力学测量来诊断毛细血管前肺动脉高压[19].在临床、生物学和遗传学调查排除了所有已知病因后,散发的PAH患者被进一步称为IPAH [20.].当家族中至少有两例病例延伸至三级亲属时,病例被认为是fpha。经医院调查诊断为相关PAH的患者(特别是结缔组织疾病和艾滋病毒感染)不包括在内。
儿科病例的诊断年龄<18岁。
确诊或极有可能PVOD的诊断依据先前描述的标准[17,21],由于纳入期重叠,在之前的一篇文章中纳入了少数PVOD患者[22].本研究中所有PVOD患者均为散发病例。
PAH诊断时的临床特征存储在法国肺动脉高压登记处。该登记处是根据法国生物伦理学法律(国家信息委员会Libertés)建立的,患者同意纳入[23].超过90%的患者为白种人欧洲血统。本研究纳入的所有患者均接受遗传咨询并签署书面知情同意书。
本研究纳入的所有病例均为2014 - 2017年前瞻性收集的肺动脉高压发病指数病例,除8例既往为阴性的患者外,均在纳入期间诊断时进行DNA测序分析BMPR2而且ACVRL1都被提到了新创用基因板分析。
捕捉设计
我们设计了一个针对所有外显子的定制基因面板,包括侧翼50 bp的内含子序列和每个感兴趣基因上下游1 kb的区域。该小组包括9个用于肺动脉高压分子诊断的基因(BMPR2,TBX4,EIF2AK4,CAV1,KCNK3,SMAD9,ACVRL1,英格而且BMP9).的BMP10基因,BMP9旁白,也被包括在捕捉设计中。该下一代测序(NGS)组还包括与肺动脉高压和其他遗传性血管疾病(HHT,毛细血管和动静脉畸形)相关的额外基因,以临床诊断和研究为目标,占总目标序列的79%。
目标捕获测序法
文库使用1 μg基因组DNA,按照KAPA样品制备方案(KAPA Biosystems, Wilmington, MA, USA)制备。在进行适当的质量控制后,按照制造商的协议,使用SeqCap EZ Choice Library (Roche/NimbleGen, Madison, WI, USA)收集样本库(12个样本库)。使用MiSeq系统(Illumina, San Diego, CA, USA)对捕获的两个库(24个样本)进行测序,生成2×150 bp对端reads。
数据分析
质量控制、处理和变异检测由GenoDiag(巴黎,法国)提供服务。简单地说,FASTQ序列文件用BWA 7.12版本(http://bio-bwa.sourceforge.net),并使用SAMtools版本1.1 (www.htslib.org).SNV和插入/删除(indel)调用使用GATK 3.5版本执行(https://software.broadinstitute.org/gatk).基因变异由GenoDiag专有脚本检测。检测是基于每个外显子的覆盖范围。为了根据样本之间的变化去除覆盖率偏差,应用了归一化。然后用归一化的覆盖率来计算z分数。计算另外两个参数,即。覆盖离散度和覆盖率,用以衡量测序质量和缺失或重复显著性。这三个值用于过滤假阳性结果并设置事件置信度。每个碱基必须被至少40次读取才能被验证。该方法在23个主要基因上含有snv或cnv的样本上进行了验证(BMPR2,EIF2AK4而且ACVRL1).
对误义变异的假定功能影响进行了评估在网上利用SIFT、PolyPhen-2、Combined Annotation Dependent Depletion (CADD) Phred评分和等位基因频率在基因组聚合数据库gnomAD [24- - - - - -26].所有数据库和软件均使用Alamut 2.7.1版本查询(www.interactive-biosoftware.com/alamut-visual),除了CADD Phred评分是通过Ensembl网站上的变异效应预测工具获得的(http://grch37.ensembl.org/Homo_sapiens/Tools/VEP?db=core).根据美国医学遗传学和基因组学学院(ACMG)的标准对每种变体进行分类[27].任何潜在的致病变异均通过Sanger测序(点突变)和多重连接依赖探针扩增(MLPA) (MRC-Holland, Amsterdam, Netherlands)或定量PCR (qPCR)分析(大规模重排)确认。
统计分析
数据以均值和标准差表示。由于数据不遵循正态分布,在适当的情况下使用非参数Mann-Whitney检验或Fisher精确分析进行比较,使用XLStat 2014 (www.xlstat.com).使用Benjamini-Hochberg校正对多重检验的显著性阈值(p<0.05)进行校正。
为了评估的关联BMP10多环芳烃的变异,我们比较的频率BMP10polyphen2预测的可能具有损害作用的错义变异,SIFT预测的可能具有有害作用的CADD评分>20 (n=32), gnomAD中报告的LOF变异(n=3),频率为BMP10在我们的队列中检测到具有相似特征的变异(n=2)。统计学比较采用卡方分析。
结果
序列分析和质量控制
设计捕获板富集目标DNA,该捕获板由150 071 bp组成,覆盖289个捕获区域。我们的设计和测序方案通过筛选23例患者进行了验证,这些患者之前已通过Sanger测序和MLPA进行了分析。所有之前鉴定的突变(n=16) (SNVs和indes)和CNVs (n=4)均通过NGS分析检测。相反,在3例患者中证实了突变检测的缺失。
本研究共分析了29个不同的测序序列。均值±sdQ30质量评分为91.5±3.8%。所有分析样本的平均覆盖率为1106±353倍。95.6±3.4%的reads位于感兴趣区域,2.6±2.2%的reads位于感兴趣区域外,1.8±1.6%的reads未映射到人类基因组。
检测肺动脉高压基因突变
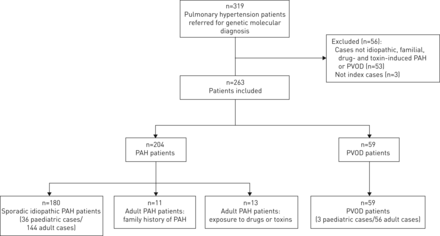
经谱系分析和临床检查,初步诊断为散发性PAH 180例,FPAH 11例(仅包括指标病例),药物和毒素性PAH 13例,散发性PVOD 59例(图1).在263例被分析的患者中,有49例被鉴定出突变。双等位基因的鉴定EIF2AK4一名最初疑似PAH病例的突变导致我们将该患者重新分类为PVOD。因此,在散发性PAH患者中鉴定出35个突变(占散发性PAH的19.5%),在FPAH患者中鉴定出6个突变(占FPAH的54.5%),在PVOD患者中鉴定出8个突变(占PVOD的13.3%)(表1).
本研究分析的患者流程图。PAH:肺动脉高压;PVOD:肺静脉闭塞性疾病。所指示的诊断是由分子诊断请求提供的诊断。
31BMPR2突变(散发性PAH 25例,FPAH 6例),5例TBX4突变(5个散发PAH), 2个ACVRL1(2例散发PAH), 2例BMP9(2例散发IPAH), 1例SMAD9(1例散发PAH)和8例双等位EIF2AK4基因突变(8个PVOD)表1).大部分的BMPR2突变是截断突变,即。中断基因功能的终止密码子(n=11)或插入密码子(n=1)补充表S1).鉴定出三种不同的错义突变:其中两种是以前描述过的,第三种(p.A373V)是新的。这种突变位于BMPR2的激酶结构域,改变了一个保守的残基,并被预测是有害的在网上工具(参见数据分析)。根据ACMG标准[27],这种突变被归类为可能致病。发现了三个剪接突变:两个影响一致剪接位点,一个位于内含子7内的c.968-12位置,预计会影响接下来的剪接在网上分析。利用从突变载体的循环血细胞中提取的RNA进行的逆转录PCR实验证实,mRNA剪接存在缺陷,导致在成熟mRNA中添加内含子序列并产生移码(补充图S1).
剩下的6个BMPR2突变是由NGS检测到并经MLPA证实的CNVs。另外两个CNVs也被检测到:一个在SMAD9还有一个TBX4.qPCR分析证实均为阳性。所有EIF2AK4所鉴定的突变为双等位:5个为纯合子状态,3个为复合杂合子状态。
中仅发现截断突变TBX4而且BMP9(停止密码子n=2, indel n=4, CNV n=1),而先前描述的两个错义突变在ACVRL1.HHT症状在成人病例中出现ACVRL1突变携带者,而儿科病例在诊断时没有HHT迹象,被实验室称为散发性PAH。
的BMP10基因也被包括在基因面板中,之后的描述BMP9由于两个基因之间的密切相似性(蛋白质水平上65%的序列相同)。在一名年轻女性患者中发现了位于编码成熟BMP10肽区域上游的截断突变(c.370C>T, p.Arg124*),该患者在11岁时被诊断为散发性PAH,并出现严重进化(表2这名年轻患者有一个小的房间隔缺损和一个小的限制性室间隔缺损,在2岁时自发闭合。一个预测BMP10LOF突变(c.1057C>T, p.Arg353Cys)在另一名28岁诊断为散发性PAH的患者中被发现,该患者临床情况严重,35岁时被移植(表2Arginine 353位于BMP10的生长因子片段中,在种与整体之间高度保守(补充表S2)在网上对该变异的分析与有害影响一致(表4).计算LOF不耐受的概率BMP10并被发现为0.72,这个值接近不耐受阈值0.9,LOF突变可能是有害的,而对于LOF突变的不耐受阈值为0.09BMP9[24].根据联合生物信息学预测工具(见数据分析),在可能有害变异的频率与截断突变之间发现了高度显著的差异BMP10在gnomAD数据库中列出,以及我们肺动脉高压队列中LOF的频率(246000个等位基因中40个等位基因上有35个不同的变异)与536个被测等位基因中有2个LOF变异;p < 0.0001)。
转诊患者在诊断时年龄各异,从新生儿到老年人(> ~ 80岁)。为了准确了解在成人和儿科病例中发现的突变的遗传格局,对18岁以下和18岁以上的患者进行了单独的分析(表3).分析了35例儿科和168例成人PAH病例。成人和儿童PAH病例的突变率无显著差异(分别为19%和26%)。BMPR2突变在两个年龄组中都是最常见的(在成人和儿科组中分别有75%和77%的已鉴定突变)。TBX4在成人和儿科病例中检测到的突变频率相似(分别占每组中已识别突变的12.5%和11%)。
在一个病例临床上称为新生儿多环芳烃,双等位基因突变EIF2AK4,导致重新分类为未识别的PVOD。相比之下,在最初诊断为PVOD的其他3例儿科病例中未发现突变。在成人PVOD患者中,只有双等位基因EIF2AK4发现了突变(12.5%的病例检测呈阳性)。
确定了意义不确定的变异
根据ACMG标准[27],在被调查的基因中发现了14个不确定意义的变异(VUS)。在网上的VUS分析表4.未发现致病突变KCNK3而且CAV1但在这些基因中发现了两个VUS。的误义变体KCNK3被发现位于该通道的细胞外区域,这一位置类似于先前在PAH中涉及该基因的第一项研究中显示的改变通道功能的错义突变。在框架内的一个氨基酸缺失被鉴定CAV1也应被视为VUS。
两个BMPR2确定了gnomAD数据库中未描述的启动子变体。两个错义EIF2AK4在同一个体中发现了变异,但它们在两个不同等位基因上的位置无法确定。
诊断时的临床状况
比较突变携带者和非携带者在诊断时的临床表现表5成人多环芳烃病例、儿童多环芳烃病例及成人PVOD病例。在成人PAH和PVOD中,突变携带者的诊断年龄明显低于非携带者,但在儿科PAH中没有。在成人多环芳烃中观察到的性别分布(女性多2- 3倍)与先前分析的各种队列中描述的相似[5,28].在多环芳烃儿科病例中也观察到类似的趋势。非携带者PVOD的性别分布显示,男性在PVOD病例中占不显著优势,这与PAH形成对比(p<0.0001;表3),而在EIF2AK4突变携带者(表3而且5).
即使成人PAH只有平均肺动脉压达到统计学意义,但突变携带者的血流动力学参数往往更差。
在成人和儿科PAH病例中,急性血管扩张剂应答者的比例往往高于非携带者,即使没有达到统计学意义(表5).
讨论
大规模并行测序(即。NGS)彻底改变了遗传性疾病的分子遗传学,使新的致病基因得以识别,并使临床分子诊断效率大幅提高[29].针对一组已知的疾病基因的NGS是一种有效的方法,可以对潜在的负责基因进行广泛的、经济上可接受的调查。
在这项前瞻性的事件病例研究中,我们对因PAH或PVOD转诊到参考实验室的患者使用了NGS小组方法。基因组包括通过以前的出版物建立的基因,以及基于生理功能和以前可用数据的研究基因。使用这种NGS靶向捕获方法,可以通过单一技术检测不同类型的突变(SNVs、CNVs和indes),从而节省成本和时间。
BMPR2是成人(家族性和散发性)多环芳烃的主要基因,如在儿科形式。在FPAH病例中,只有突变BMPR2发现,可能是因为它的显性频率,但更具体的原因可能涉及与外显率和临床演变相关的突变基因。这些结果与先前发表的结果一致[30.,31].
在本研究中,TBX4突变是其后发现的第二常见突变BMPR2在成人和儿科多环芳烃病例中。我们之前观察到经常发生TBX4儿科多环芳烃基因突变[15],最近另一项基因研究证实了这一结果[16].的显著频率TBX4本研究在成人病例中发现突变,与先前报道的结果形成对比[16],可能是由于随机差异以及患者收集模式的差异(流行和存档患者与事故情况下)。
BMP信号通路的其他基因突变被发现(BMP9而且SMAD9),这使得这些基因在多环芳烃中的意义得以证实,因为文献中只描述了罕见的病例。的确,最初的描述BMP9突变与一种特殊形式的HHT相关,随后描述了一个与双等位LOF相关的严重PAH病例[32,33].罕见的杂合的BMP9最近通过全基因组测序在一大批患者中发现了突变[9].在我们的研究中,BMP9是成人多环芳烃病例中第三大突变基因(1.2%的多环芳烃病例,6.3%的已鉴定突变),表明该基因与多环芳烃有显著相关性。具有杂合子的小鼠遗传模型BMPR2LOF显示BMP9输注可改善缺氧诱导的多环芳烃,这一结果进一步支持了该基因参与多环芳烃(虽然是间接的)[34].在研究工作的框架内,我们进行了调查BMP10的近景BMP9它编码ALK1 (ACVRL1)的激活配体,并且在血管生成的实验模型中显示出与BMP9相同的作用,因为它可以替代BMP9BMP9敲除小鼠[35,36].最近也有研究表明,BMP9-BMP10异源二聚体在人血浆中循环,是主要的生物受体激活复合物,尽管这种异源二聚体的附加功能尚未确定[37].我们发现了一个BMP10杂合截断突变和一种在网上预测两例年轻女性严重PAH患者的LOF错义变异。两名患者中有一名患者表现为小的心房左向右分流和小的高度限制性室间隔缺损,无肺溢流,在2岁前自发闭合,而PAH在11岁时被诊断出来。根据2013年先心病相关多环芳烃的分类,该病例的临床表现不允许将其归类为偶发病例或术后病例[1],但提出了一个问题的关系BMP10杂合子LOF,心脏发育和多环芳烃,自Bmp10-缺陷小鼠胚胎很早就死亡,在胚胎9.5天至10.5天之间,心脏和血管发育有重大缺陷[38,39].识别两个LOF变体BMP10由于该基因的生理作用,其LOF不耐受的概率评分,以及患者与未选择人群之间LOF变异频率的高度显著差异,该基因在PAH中的作用是高度提示的。BMP10PAH相关易感性似乎与不完全外显的常染色体显性遗传相容,但也可能与其他因素联合作为易感性因素。的确,有些误解BMP10根据生物信息学预测工具,可能致病的变异在gnomAD数据库中以极低的频率被发现,其他多环芳烃基因也被观察到。进一步的研究将允许的作用BMP10有待定义的突变。无致病性突变CAV1在本研究中发现,与之前的报道和对大量患者的研究一致[9,30.],总的来说,这些结果表明该基因在多环芳烃易感性中的作用非常有限。
双等位的比率EIF2AK4在成人散发性PVOD病例中发现的LOF突变(12.5%)与我们之前发表的散发性PVOD病例的结果一致[22],但低于已报道的系列[39].这种差异可能是由于有限病例数量和患者收集特异性所支持的随机变化。唯一的双等位基因EIF2AK4在儿科形式的PVOD中发现的突变是在一名最初由早期心肺衰竭提示的PAH分子诊断的新生儿病例中发现的[22].这个案例强调了…的重要性EIF2AK4为了建立诊断,在所有假定的病例中进行检测,因为临床图像可能会产生误导,而能够最好地区分PAH和PVOD(高分辨率计算机断层扫描和肺对一氧化碳的扩散能力)的调查可能没有明确区分或遗漏,甚至是禁忌(肺活检)[22,30.,31].EIF2AK4通过临床基因检测进行突变鉴定对于遗传性PVOD的高外显率和疾病严重程度,以及对批准的PAH治疗反应的肺水肿风险特别重要,因为它允许遗传咨询和适应的随访,包括及时转诊肺移植。EIF2AK4突变的解释通常是直截了当的,但在一种情况下,有两种误解EIF2AK4在PVOD患者中发现了突变,两者都被认为是在网上是良性的,在gnomAD数据库中发现频率很高。如果找到的话,可以推测它携带了两种误义变体在反式,可能会导致这种疾病,但这一假设需要进一步调查。
在进行遗传分析的各种患者类别中,发病年龄和性别差异是遗传类型(外显率是决定这些参数的主要因素)和非遗传类型(环境因素占主导地位)混合的结果。在PAH中观察到的性别比例与之前在不同队列中发现的值一致,包括突变携带者和非携带者[5].在成人中EIF2AK4突变载体组,性别比分析受到受试者数量的限制,但似乎是平衡的。的确,有很强的外显力EIF2AK4两性的突变可能解释了平衡的性别比例,正如常染色体隐性疾病所预期的那样。
如先前报道的,突变携带者多环芳烃组的诊断年龄也较年轻BMPR2突变携带者[28].在成人PVOD组中,突变携带者和非携带者的发病年龄有很大差异,我们小组已经报道了这一观察结果[17,22].明确的环境因素在非遗传性PVOD中已有文献记载,这可能解释了遗传性PVOD与其他PVOD发病年龄的巨大差异(34.4与61.2年;p < 0.0001)。
迄今为止,我们报告的全部描述基因序列分析的数据仍然有很大比例的病例未得到解决,特别是儿科和家族病例。识别和解释已知责任基因(包括非编码区域)中所有变异的功能影响仍然是一个重大的实际挑战,需要进一步的努力和知识,但这将阐明大量案例[29].例如,在我们的研究中,我们发现了一个位于非一致剪接位点(内含子位置−12)的变体,并通过cDNA分析证明它改变了mRNA剪接。我们还在BMPR2启动子和功能的研究是必要的,以评估这些变异对基因调控的病理影响。
许多患者的功能数据参数缺失限制了本研究在基因型-表型关系方面的影响,尽管这方面超出了本研究的范围。
通过大系列不相关病例的全外显子组测序和全基因组测序,或在有多例肺动脉高压病例的家族中,可以发现额外基因的突变。事实上,最近通过全基因组测序方法在大量PAH病例中发现了以前未描述基因的罕见变异[9,并通过全外显子组测序来寻找新创儿科病例的突变[16].这些新发现的基因可以很容易地添加到靶板中进行进一步评价和临床分子诊断。由于经济和技术上的原因,靶向捕获面板方法是目前最有效的临床分子诊断的第一步。
一个主要的挑战将是阐明各种基因是否通过一种共同的机制倾向于PAH或PVOD的发展,就像可以提出的属于BMP信号通路的基因一样,或通过不同的机制。例如,BMP通路在胚胎发生过程中对中胚层和间充质细胞的发育很重要,TBX4在发育过程中驱动间充质祖细胞入侵肺也是如此[40].BMP4也显示出诱导作用TBX4培养的人肺成纤维细胞的表达[41].EIF2AK4和BMP信号通路之间的调控联系最近在果蝇,但观察到BMP信号激活增加Eif2ak4果蝇orthologue失活不符合BMPR2缺陷的预期影响[42].
我们对已知肺动脉高压基因数据的总体分析似乎证实了之前描述的所有主要基因的参与,如果不仅考虑到LOF突变,而且还考虑到在各种基因上发现的错义变异。事实上,将多环芳烃的致病作用归咎于杂合突变是毫无疑问的主要基因,如BMPR2而且TBX4,但对于其他基因来说可能更困难,因为关于多环芳烃的数据较少。我们的数据的一个兴趣是刺激分析BMP9而且BMP10多环芳烃的临床分子诊断基因,允许来自多个中心或大型多中心研究的结果在未来共享。
补充材料
确认
我们感谢Anne Leroy和Marie-Christine Waill (Département de Génétique, Hôpital Pitié-Salpêtrière, AP-HP,巴黎,法国)的专家技术援助。我们感谢来自法国肺动脉高压网络的患者、他们的家人和医疗保健提供者,以及法国患者协会HTAP。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:M. Eyries报告了在研究进行期间罗氏诊断法国公司的个人费用。
利益冲突:D. Montani报告了Actelion, GSK, MSD和辉瑞的个人费用,在提交的工作之外。
利益冲突:S. Nadaud没有什么可透露的。
利益冲突:B. Girerd没有什么可透露的。
利益冲突:M. Levy没有什么可透露的。
利益冲突:A. Bourdin报告了在提交的工作之外,来自GSK的演讲和非金融支持的赠款、个人费用,来自阿斯利康和勃林格殷格翰的演讲和咨询委员会工作的赠款、个人费用,来自诺华的演讲和咨询委员会工作的个人费用,来自MSD的赠款,来自Actelion的演讲和个人费用,以及来自Chiesi pharmaceuticals的演讲和非金融支持的个人费用。
利益冲突:R. Trésorier没有什么可披露的。
利益冲突:A. Chaouat没有什么可透露的。
利益冲突:V. Cottin报告了Actelion和Roche的咨询、讲座和医疗会议差旅费的个人费用,Boehringer Ingelheim的教育演示、咨询、讲座和医疗会议差旅费的个人费用,拜耳的个人咨询费,吉利德的裁决委员会工作的个人费用,MSD的咨询和医疗会议差旅费的个人费用,诺华和赛诺菲的咨询和讲座的个人费用,来自勃林格殷格翰(Boehringer Ingelheim)和罗氏(Roche)的机构资助,来自Promedior和Celgene的数据和安全监测委员会工作的个人费用,以及来自加拉帕戈斯群岛(Galapagos)的咨询和数据和安全监测委员会工作的个人费用。
利益冲突:C. Sanfiorenzo没什么可透露的。
利益冲突:G. Prevot没有什么可透露的。
利益冲突:M. Reynaud-Gaubert没有什么可透露的。
利益冲突:C. Dromer没有什么可透露的。
利益冲突:A. Houeijeh没有什么可透露的。
利益冲突:阮k没有什么可透露的。
利益冲突:F. Coulet没有什么可透露的。
利益冲突:D. Bonnet报告了Actelion制药公司、拜耳医疗保健公司和诺华公司咨询委员会工作的个人费用,这些费用超出了提交的工作。
利益冲突:M. Humbert报告了Actelion、拜耳、GSK、强生、默克和联合治疗公司在提交工作之外的个人费用。
利益冲突:F. Soubrier没有什么可透露的。
支持声明:本作品由Legs Poix (Chancellerie des Universités de Paris)支持。本文的资助信息已存入交叉参考基金注册.
- 收到了2018年4月25日。
- 接受2018年11月23日。
- 版权所有©ERS 2019