抽象的
Covid-19中的Hyperytopopiny Immune失调称为细胞因子风暴综合征。白细胞介素-6级别≥80pg×ml-1预测呼吸衰竭和死亡的风险增加,免疫调节治疗是一种紧急调查的领域
Covid-19相关细胞因子风暴综合征(Covid-CSS)的概念在严重的急性呼吸综合征冠状病毒2(SARS-COV-2)大流行中出现,解释为什么暴露于该病毒的一些患者与急性呼吸窘迫综合征均危重生病,多器官失败和死亡。来自武汉的一项精神研究报告,与患有较高疾病的患者需要关键护理的患者血清浓度高,提交人假定“细胞因子风暴与疾病严重有关”[1].Covid-19 Hypercytokinemia最初邀请对其他呼吸道病毒感染的比较,导致失调的免疫反应,即严重的急性呼吸综合征(SARS)和中东呼吸综合征(MERS)。随后,Covid-CSS与其他细胞因子风暴综合征之间的相似性,例如血糖淋巴管肾小球菌(HLH)[2[自身炎症综合征,嵌合抗原T细胞治疗细胞因子释放综合征(汽车T细胞CRS)变得明显[3.-5.].Hypercytokinemia在某些Covid-19催化患者中病理到免疫调节和细胞因子抑制剂治疗的患者病态的命题。然而,评论家争辩说,CSS是Covid-19的误导性概念框架,两个突出的社论对Covid-CSS提出了重大怀疑[6.那7.]. 简言之,这些作者主张:
1) 细胞因子风暴综合征尚无定义;
2)Covid-19中位IL-6水平相对较低;
3) 新冠病毒-19应被描述为低炎症性血管病,而不是高炎症性高细胞因子血症综合征;
4)因此,免疫调节治疗可能在Covid-19的治疗中起很少或没有作用。
在这方面,我们解决了这些争议,并证明细胞因子风暴综合征可能在严重的呼吸衰竭和由Covid-19引起的死亡中发挥重要作用。
细胞因子风暴综合征的定义
Covid-CSS概念的批评者已声称“细胞因子风暴没有定义”[6.],并且没有“没有证据表明Covid患者发展细胞因子风暴”[7.].事实上,专家将细胞因子风暴综合征定义为[临床表型8.]:
以淋巴细胞和巨噬细胞持续激活为特征的免疫失调
导致大量细胞因子分泌
导致严重的全身炎症和多器官衰竭,死亡率高。
CSS术语首先是在移植物中描述患者的血糖血症相对异基因干细胞移植后的宿主病[9.]. 最近,CAR T细胞CRS表现出明显升高的白细胞介素(IL)-6水平,通常超过1000 pg·mL-1(正常<7 pg·mL-1),并响应IL-6封锁,已包含在伞期CSS中[3.].许多病毒、细菌和寄生虫感染都能导致CSS。传染性病原体如eb病毒(EBV)和结核分枝杆菌在遗传性和获得性免疫缺陷患者中,引起病理性免疫激活,其特征是细胞因子和细胞因子受体,如干扰素-γ (IFN-γ)和可溶性白细胞介素-2受体(sIL-2r)显著升高,导致噬血细胞淋巴组织细胞增多症(HLH)的临床综合征[10.那11.].
详细的免疫学研究明确表明,部分重症COVID-19患者确实符合细胞因子风暴综合征的一般标准,这与其他传染性CSS不同。最近一项纵向研究对中度相对严重的Covid-19在严重疾病中展示了3种不同签名的“免疫误解”[5.].患有中度疾病的患者(患者入院,患有ICU入院的医院)对炎性细胞因子的表达低,增加了组织重新生长因子,如表皮生长因子(EGF),血小板衍生的生长因子(PDGF)和血管内皮生长因子(VEGF)(无花果。1A). 相反,重症患者(死亡或需要ICU入院的患者)的促炎细胞因子(包括IL-1α、IL-1β、IL-6、IL-18和TNF-α)高度升高(无花果。1B.)[5.].另一项研究发现,虽然细菌败血症诱导的免疫分析是通过单核细胞缺乏和生产细胞因子,在严重的Covid-19中,外周血单核细胞(PBMC)具有LPS刺激的持续TNF-α和IL-6产生的细胞因子。离体并显着升高了IL-6和CRP浓度in-vivo.[4.].与其他呼吸病毒相比,如SARS-COV-1,MERS-COV和人对血管病毒和呼吸道合胞病毒,SARS-COV-2中的转录高炎反应是唯一的不平衡,具有低IFN-1和-III水平伴随通过非常高的炎性趋化因子和细胞因子(IL-1,IL-6)和严重淋巴细胞的表达,导致“高炎症,低先天抗病毒防御”状态[12.].
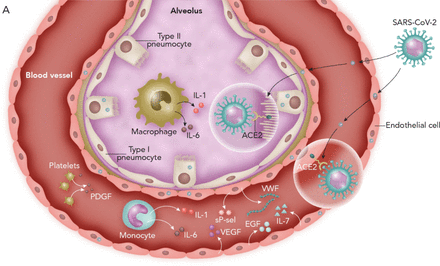
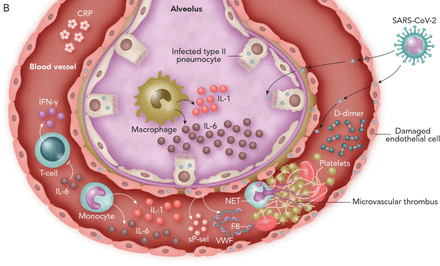
一种新的严重急性呼吸综合征冠状病毒2(SARS-COV-2)在一些患者中导致轻微疾病和他人的严重疾病的机制的示意图。在这两种情况下,病毒进入了人体细胞通过与血管紧张素转化酶2(ACE2)结合,跨膜受体广泛表达II型肺细胞,巨噬细胞,内皮和其他肺细胞[24.那25.].a)轻度疾病(低发生凝血病和血栓形成,较短的医院住宿,低危重疾病和死亡率):这些患者具有低血肿炎症细胞因子和高组织重复生长因子,如表皮生长因子(EGF),血小板衍生的生长因子(PDGF)和白细胞介素(IL)-7 [5.].b)严重疾病(微生物血管血栓形成的高发病率,较长的住院住宿,高临界疾病和死亡率):许多这些患者有细胞因子风暴,具有高血清炎症细胞因子(如IL-6,IL-1,IFN-γ)和内皮激活的标记,如von Willebrand因子(VWF),因子8凝结剂(F8)和可溶性p-选择素(SP-SEL),导致内皮炎和微血管血栓形成[5.那15.那27.].显着升高的IL-6导致淋巴细胞增长和免疫分析,其被IL-6阻断部分恢复[4.那32.].缩写:网:嗜中性粒细胞外壳;IFN-γ:干扰素-γ。
虽然COVID-CSS还没有标准的诊断标准,但这一术语通常用于指表现出过度免疫激活的患者子集,其特征是炎症标志物(如c -反应蛋白(CRP)、白细胞介素-6 (IL-6)和铁蛋白)显著升高,以及淋巴细胞减少和一系列末端器官损伤,从孤立的呼吸功能障碍到多器官衰竭。IL-6的临床测量目前还不广泛,但对许多临床实验室来说是一种相对简单和廉价的分析方法。在我们中心的COVID-19早期,当IL-6被用于研究目的而不是临床护理时,我们对COVID-CSS采用了以下标准:1)需要机械通气的COVID-19肺炎;2)发热(最高体温>38°C);3) CRP >100 mg·L-1;4)峰血清铁蛋白>1000μg·L.-1[13.].符合这些标准的患者显着提高了研究血清IL-6水平,中位数91 pg·ml-1,四分位间距(IQR)54–696 pg·mL-1(n = 15)。然而,IL-6并不总是对应于CRP(由肝细胞响应于IL-6的肝细胞产生)或铁蛋白(这是巨噬细胞活性的标志物)[14.].最近,至少两个大型研究表明,血清IL-6优于CRP,铁素,肝酶和其他简单的临床实验室标志物,用于预测临床结果,如呼吸衰竭和死亡,最佳截止值为80和86 pg·L.-1, 分别 [15.那16.]. 综上所述,这些数据表明IL-6阈值≥80 pg·mL-1在未来定义Covid-CSS中携带预后价值。最终,多变量预后模型包含简单,广泛的可用参数,如井子2/ fio.2、中性粒细胞/淋巴细胞比率、CRP和铁蛋白以及细胞因子/趋化因子如IL-1、IL-6、干扰素- γ诱导蛋白(IP)-10和IL-10可能导致预后评分系统,而不是HLH采用的二元“是/否”诊断模型[16.那17.].
白细胞介素-6和covid-css
在COVID-19早期研究中报告的血清IL-6适度升高被引用为反对CSS在该疾病中的相关性的论据[6.那7.].例如,中位数(7-45 pg·ml-1)和血清IL-6水平的IQR在四项针对轻至重COVID-19患者的大型研究中相对较低[6.].然而,中位数和IQR是中央趋势的估计,在细胞因子风暴中,利益群体在患者的顶部四分位数内。此外,这些研究中细胞因子分析的时间异质性可能错过了一些患者中细胞因子水平的快速增加。重要的是,细胞因子风暴与大多数展示的患者都不讨论生理对给定曝光的回应,而是患有患有的少数民族病态量的免疫激活或功能障碍。为了提供一些类比,仅暴露于EBV的少数比例的人发育HLH,不到15%的患者进行汽车T细胞疗法的患者开发严重的3-4级CR,要求IL-6阻断。同样,小但高度相关的那些暴露于Covid-19的比例开发CSS。
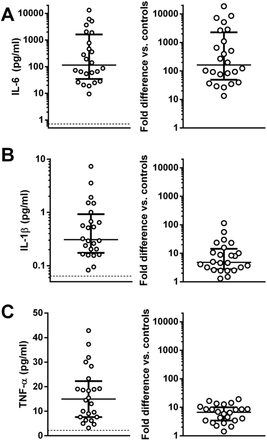
在Covid-CSS中,许多炎症细胞因子如IL-1,IL-10和肿瘤坏死因子(TNF)-α高于规范值的约2-100倍,而IL-6表现出更大的增加,在某些情况下超过1000倍正常。图2.24例重症COVID-19患者IL-1β、IL-6和TNF-α的炎症因子水平,包括绝对值和高于正常值的“fold elevation”。其他几项大型研究也报道了血清IL-6水平在100-10 000 pg·mL显著升高-1严重疾病患者的范围[12.那15.那17.那18.]. 这些显著升高的白介素-6水平在新冠病毒CSS中与严重的CAR T细胞CRS的程度相似[19.],并且高于其他Hyper-IL-6综合征,如多中心卡车疾病,其中IL-6升高,但通常<100pg·mL-1[3.那20.].HLH据说包含多种“具有共同终末途径但有不同致病根源的高铁血症高炎症综合征”[21.]. 类似地,在COVID-CSS中,免疫失调的不同“根”特征越来越可能导致共同的末端炎症途径,其特征是IL-6显著升高、严重T细胞淋巴细胞减少和呼吸衰竭[4.那5.那17.].
Hyperytokinemia,血管病变和内皮炎
有些作者提出,与中生中位IL-6水平相比,显着升高的D-二聚体水平和高血管血管血栓形成的高血管血管血栓形成,表示Covid-19病理生理后遗症与炎症性血管病相关,而不是炎症性细胞因子风暴[7.].受体血管紧张素转化酶-2(ACE2)在病毒细胞进入中的核心作用和在尸检研究中观察到的包括肠血管生成和弥漫性内皮膜破坏的复杂血管变化确实支持Covid相关发病率的血管病变的核心作用[22.]. 然而,最近的研究表明,高细胞因子血症和血管病变不是一个非此即彼的命题。肺血管系统是新冠病毒-19血管内凝血和血栓并发症的关键部位[23.那24.].早期的SARS-COV偶像蛋白对血管紧张素转换酶(ACE)2的研究表明,S蛋白与ACE2的结合导致产生炎性细胞因子,包括IL-1和IL-6 [25.那26.].
这种高炎性反应导致内皮屏障的破坏和高凝血性。弥漫性闭塞在肺血管床的微循环中可能导致肺动脉高压,增加死亡空间通风并最终进行右心力衰竭。血清内皮因子如可溶性血栓调节蛋白,可溶性p-选择素(SP-SEL)和von Willebrand因子(VWF)在疾病进展中发挥着重要作用,对急性呼吸窘迫综合征(ARDS)[27.].这些研究结果表明了一种模型,其中Covid-19最好被视为炎症内皮炎,具有肺细胞,内皮和上皮细胞的直接病毒感染,产生炎症细胞因子和免疫介导的血管系统和周围组织损伤[25.那27.](无花果。1B.)。
Covid-19中的细胞因子,呼吸衰竭和免疫调节治疗
CSS的批评者争夺Covid-19中的高胞肿瘤血症可能是病毒清除的必要生理反应,并警告在这种情况下使用免疫调节治疗[6.那7.]. 在更为成熟的CSS中,特定细胞因子的中心作用不仅通过将细胞因子升高与特征性器官损伤联系起来的研究来确定,而且还通过临床试验证明细胞因子阻断可带来临床益处。原发性HLH可能是该模型的范例,因为干扰素-γ/趋化因子配体(CXCL)-9轴是该疾病病理生理学的中心[28.]并用Emapalumab阻止这种轴产生深度和持续的剩余释放[29.].同样地,IL-1已被证明在自身炎症综合征和继发性HLH中起着类似的作用,并且患有胰岛素或加坎诺姆的阻断导致临床益处[30.那31.].
证据表明,IL-6驱动免疫功能测定和Covid-CSS中的呼吸衰竭迅速积累。升高的血清IL-6与淋巴细胞,淋巴细胞减损细胞毒性和内皮激活有关(无花果。1B.)。这些免疫缺陷可通过用IL-6阻断与TOCOLIZUAB的治疗部分恢复[4.那32.].德国研究证明IL-6> 80 pg·ml-1结合c反应蛋白>97 mg·L-1高度预示呼吸衰竭[15.].在我们自己的中心,发现IL-6与动脉氧张力与灵感氧气(PAO2 / FIO2)和静态肺顺从的比率相反相关[33.].此外,从大型前瞻性队列(n = 501)产生的多变量模型表明早期的全身炎症预测死亡率。在医院入院时测量的15个变量中,CRP在87.5 mg·L的截止值-1在86 pg·ml的截止下是最敏感的(0.97)和IL-6-1预测死亡是最具体的(0.89)[16.].
恢复试验证明死亡率从红塞米松6毫克每日治疗,特别是在严重疾病的患者中,是第一个随机对照试验(RCT),以明确地显示免疫调节治疗的益处[34.]. 尽管对细胞因子阻断(如Anakina和tocilizumab)和JAK抑制(如baricitinib)的众多回顾性研究显示了希望,但最终还是需要进行RCT。其中有几项研究正在进行中或最近完成,其结果令人翘首以待[3.].Covid-19患者证明CSS表型肯定是疾病谱的严重结束。因此,试验应旨在靶向患者的患者,以确定免疫调节疗法的真正疗效。2020年7月29日,Covacta RCT的新闻稿(nct04320615.)在新冠病毒-19中比较托昔单抗和安慰剂在主要转归(临床状况和死亡率)方面没有差异。然而,住院时间和无呼吸机天数有积极的趋势,由于未能达到主要终点,因此不被认为是显著的。COVACTA试验的纳入标准相当广泛,只需明确诊断血氧饱和度为93%或更低的COVID-19肺炎或SpO2/ fio.2<300 mmHg,没有提及全身炎症的标记,如CRP或IL-6。鉴于在恢复试验中患者在恢复试验中患者的较严重病人的患者中看到更多益处,Covatta试验中的亚组分析以及正在进行的免疫调节性RCT将具有极大的兴趣。
承认
作者感谢Catherine Biggs博士,为您对稿件的批判性审查。
脚注
贡献:所有作者都为文章的构思和起草做出了贡献,并为重要的知识内容和最终批准提供了批判性修订。
支持声明:陈博士由UBC血液学研究计划提供支持。Sekhon博士得到温哥华沿海卫生研究院临床医学家科学家奖的支持。惠灵顿博士得到加拿大卫生研究院,国家卫生研究院,威斯顿大脑研究所和治疗阿尔茨海默基金的支持。治疗阿尔茨海默氏症的基金;DOI:http://dx.doi.org/10.13039/100007625;温哥华沿海卫生研究所;DOI:http://dx.doi.org/10.13039/501100008002;NIH临床中心;DOI:http://dx.doi.org/10.13039/100000098;韦斯顿大脑研究所; DOI: http://dx.doi.org/10.13039/100012479; Canadian Institutes of Health Research; DOI: http://dx.doi.org/10.13039/501100000024.
利益冲突:陈博士没有披露。
利益冲突:霍伊兰博士没有什么可透露的。
兴趣冲突:斯塔努萨博士没有披露。
利益冲突:惠灵顿博士没有什么要披露的。
利益冲突:Sekhon博士无需披露。
- 收到了2020年8月2日。
- 公认2020年8月24日。
- 版权所有©ers 2020
本文是开放获取的,并根据知识共享188滚球软件署名非商业许可4.0的条款分发。