摘要
背景有一种新认识是,2019冠状病毒病(COVID-19)与纵隔气肿(PTM)发病率增加有关。我们的目的是确定其在英国COVID-19住院患者中的发生率,并描述与结果相关的因素。
方法2020年9月至2021年2月对PTM及其发病率进行了一项结构化调查。征集全英国的参与通过呼吸研究网络。确诊患者均为严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)感染和经放射证实的PTM。主要研究结果是确定COVID-19中PTM的发生率,并调查与患者死亡率相关的危险因素。
结果在研究期间,53家医院的58 484例COVID-19住院患者中发现377例PTM,发生率为0.64%。COVID-19 PTM患者120天总死亡率为195 / 377(51.7%)。COVID-19患者的PTM与机械通气率高相关。377例患者中有172例(45.6%)在诊断时采用机械通气。机械通气是COVID-19 PTM患者在诊断时及其后死亡率的最重要预测因素(p<0.001),以及年龄增长(p<0.01)和糖尿病(p=0.08)。在诊断为PTM后,将患者从持续气道正压支持切换到吸氧或高流量鼻氧与死亡率的差异无关。
结论PTM似乎是严重COVID-19肺炎的一个标志。大多数确诊为PTM的患者在诊断时未进行机械通气。
摘要
大约0.6%的COVID-19患者被确诊为纵隔气肿。这一发现与严重的COVID-19和高死亡率有关。https://bit.ly/3nXlaR5
简介
纵隔气肿(PTM)是指纵隔内空气或气体的异常存在。自发性PTM罕见,约在33 000名住院患者中出现1例[1].PTM在接受正压通气(PPV)的患者中发生率较高,特别是急性呼吸窘迫综合征(ARDS)患者[2,3.].
在2019冠状病毒病(COVID-19)大流行期间,接受PPV的患者数量显著增加,许多COVID-19肺炎患者符合ARDS标准[4,5].可在此背景下看待发表的几个病例报告和COVID-19患者的PTM小系列[5- - - - - -8].然而,也有一些报告称,在没有PPV的COVID-19肺炎中发生了PTM [9- - - - - -11].COVID-19中PTM的真实发病率及其与PPV的关系尚不清楚。此外,尚不清楚PTM识别后是否需要改变管理。
我们报告了2020年9月至2021年2月期间来自英国53家医院的377例COVID-19 PTM的多中心观察性研究(poem)。我们描述了COVID-19中与PTM相关的发病率和危险因素以及与死亡率的关系。
材料与方法
研究人群
诗意研究招募了全英国。这是广告通过国家和区域培训生研究网络,包括肺研究站点间矩阵(PRISM)和西北协同呼吸研究(NCORR)。
参与机构贡献了2020年9月1日至2021年1月31日期间确诊的COVID-19住院患者的PTM病例(补充表S2).PTM的诊断基于计算机断层扫描(CT)或胸部平片,COVID-19的诊断基于严重急性呼吸综合征冠状病毒2型(SARS-CoV-2) PCR阳性结果或CT图像上COVID-19肺炎的证据和明确的临床病史。所有参与机构都使用关键词“纵隔气肿”、“气胸”或“皮下肺气肿”搜索放射学报告,以及医疗、呼吸病房和重症监护病房的患者名单,以确保所有病例都得到确认。每个病例都收集了匿名数据。这些数据包括人口统计数据、既往病史、放射学检查结果、临床结果和PTM诊断前后所有呼吸支持系统的呼吸设置。所有患者均记录随访≥120天,并对所有医院间转移病例进行交叉检查,以确保无重复。为了准确估计发病率,我们收集了在此期间收治的PCR检测为sars - cov -2阳性的患者总数和各机构进行胸部CT成像的比例。
所有与吸入氧分数有关的数据(FIO2)在分析前归一化到统一的尺度(如。所有病人接受15升的氧气通过采用带储液器的非换气面罩FIO2的90%)。使用各种设备输送高流量鼻氧(HFNO)和持续气道正压(CPAP)。呼气末正压(PEEP)和呼气末正压FIO2基于呼吸技术与生理学协会(www.artp.org.uk COVID19).基于G形和Tobin[12].详情可参阅补充表S3a和b而且补充图S3c.
从牛津大学医院NHS基金会信托(英国)审计委员会获得了伦理批准,并在相关情况下获得了当地NHS信托的额外伦理批准。所有数据都是回顾性收集的,并由当地医生以匿名的方式输入,不与患者标识挂钩。
统计方法
分类数据以频率(百分比)表示,连续数据以平均值和标准差表示。如果数据不是正态分布,则给出中位数(四分位差)。分类数据的差异用卡方检验表示。对于连续正态分布数据的比较,采用双边独立t检验。所有引用的结果都是120天的结果。回归模型的变量输入是向后逐步执行的。使用SPSS 28版本(IBM, Armonk, NY, USA)进行分析。图是在R版本4.0.3中创建的(www.r-project.org).我们按照STROBE(加强流行病学观察研究报告)检查表提出了这篇文章。
结果
共检出PTM 377例,其中98.4% PCR阳性,其余临床诊断。318例(84.4%)经胸部CT检查确诊或证实为PTM。在318例经CT扫描诊断的病例中,有147例(46.2%)在之前的胸片上未发现PTM。获得所有纳入医院的所有患者的预后数据和发病率数据。所有参数的其他数据均≥95%完整。
发病率
2020年9月1日至2021年1月31日期间,53家参与医院共有58 484例聚合酶链反应阳性住院患者入院(平均±平均)sd每家医院新冠肺炎住院患者1103±611例)。PTM发生率为每例COVID-19住院患者0.64% (95% CI 0.58-0.71%),平均±sdPTM病例数为每家医院7.1±4.8例。58484例pcr阳性住院患者中,12703例(21.7%)入院时进行了胸部CT检查,平均±sd每所医院进行CT扫描的次数为240±200。住院总人数,胸部CT成像的使用和跨医院的PTM病例数之间的关系呈现在补充图S4.
人口统计资料
中位(IQR)年龄为60(52-78)岁。男性患者比例过高,为277例(73.5%)男性患者比100例(26.5%)女性患者。最常见的共患病是高血压(32.4%)、糖尿病(21.5%)、哮喘(19.4%)、肥胖(10.6%)、缺血性心脏病/左室收缩功能障碍(8.8%)和慢性肾病(4.5%)。三名患者怀孕。入院前症状的中位数(IQR)持续时间为7(5-10)天,而从入院到影像学确认PTM的中位数(IQR)持续时间为7(5-12.3)天。胸痛是11.9%患者主诉的一个特征。
377例患者中有315例(83.6%)认为有条件进行机械通气。是否适合机械通气是记录在笔记中的临床决定。其余62例患者的治疗仅限于必要时的CPAP支持。鉴于这两组之间的治疗差异,在我们的回归分析中分别考虑与患者预后相关的因素。
管理
315例(76.5%)符合升级到机械通气条件的患者中有241例(76.5%)在入院期间进行了机械通气。这241例患者中有172例(71.4%)在诊断为PTM之前进行了机械通气。241例患者中有38例(15.8%)在插管后24小时内检测到PTM。24 / 241(10.0%)患者继续接受体外膜氧合(ECMO)。377例符合条件接受CPAP治疗的患者中,377例患者中有256例(67.9%)在诊断为PTM之前接受过CPAP治疗。377例(2.4%)患者中有9例在入院时使用了有意识的无创双侧气道正压通气(BiPAP),而不是将其用于停止机械通气的患者。9例患者中有4例为2型呼吸衰竭。其他5例患者使用BiPAP的适应症尚不清楚。考虑到接受BiPAP治疗的患者很少,且其使用方法存在差异,我们将其排除在分析之外。
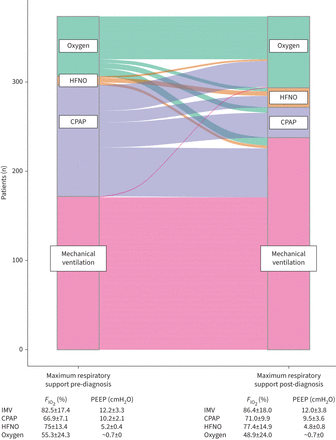
在PTM诊断前后,提供给所有患者的最大呼吸支持描述在图1.4名治疗仅限于无创呼吸支持的患者在诊断为PTM时从CPAP切换到氧气,作为开始姑息治疗的决定的一部分。两名患者全程在室内空气中接受治疗。
桑基图绘制了所有患者在诊断纵隔气肿(PTM)前4小时和诊断PTM后的最大呼吸支持(n=374)。均值±sd吸气氧分数(FIO2)和呼气末正压(PEEP)在这些水平的支持下给出了下表。HFNO:高流量鼻氧;CPAP:持续气道正压;有创机械通气。
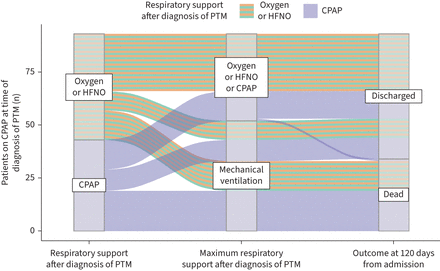
诊断时呼吸支持的改变见图1.在诊断为PTM后改变呼吸支持的患者大多使用CPAP。在诊断为PTM时,93例符合机械通气条件的患者使用了CPAP。50例(53.8%)患者在诊断为PTM后立即切换到吸氧或高流量鼻氧疗,形成了两个可分析的亚组:50例切换到吸氧或高流量鼻氧疗,43例继续使用CPAP。这两个亚组在诊断年龄上回顾性匹配良好(CPAP平均年龄57.0岁与氧或HFNO 55.6年;P =0.51),达到最大值FIO2他们接受了(CPAP平均值FIO266%与氧或HFNO 68%;p=0.15)或根据他们所接受的最大呼气末正压(CPAP平均呼气末正压10.4 cmH)2O与氧或HFNO 9.8 cmH2O;p = 0.19)。这两个子组的后续轨迹说明在图2.这些患者呼吸支持方式的改变与死亡率的相关性采用方差分析(ANOVA)进行检验。从CPAP切换到氧疗或高流量鼻氧疗对预后无显著的主要影响。然而,机械通气是两个亚组死亡率相关的主要影响因素(p<0.001)。
冲积图描述了93例符合机械通气条件的患者在诊断纵隔气肿(PTM)时一直处于持续气道正压(CPAP)状态。在诊断时,那些随后使用CPAP的患者与那些随后使用氧气或高流量鼻氧(HFNO)的患者在年龄、最大吸气氧分数或最大呼气末正压方面没有统计学差异。
并发气胸、皮下肺气肿及与PTM相关的并发症
377例患者中有154例(40.8%)并发气胸,其中154例(90.1%)中有139例(90.1%)并发皮下肺气肿。在377例(74.3%)患者中,共有280例出现皮下肺气肿。PTM合并气胸、皮下肺气肿、张力现象及肋间引流的使用表现在图3.插入肋间胸引流的次数和频率见补充图S5.在与皮下肺气肿相关的病例中,6例(1.6%)采用了皮下引流。在这6个病例中,有5个是对威胁或实际张力性皮下肺气肿进行了皮下引流。4例(1.1%)纵隔引流使用。在这四例中的一个病例中,插入纵隔引流作为疑似张力性PTM和张力性皮下肺气肿的紧急床边程序。另外四分之三的病例插入纵隔引流以消除可能的张力性PTM。这四个纵隔引流管是在四家不同医院的患者中插入的,每家医院都没有现场心胸外科服务。张力性气胸14例。在10例疑似张力现象的病例中,作为紧急程序插入双侧肋间引流管。这10例中有7例在术前没有气胸的影像学证据。
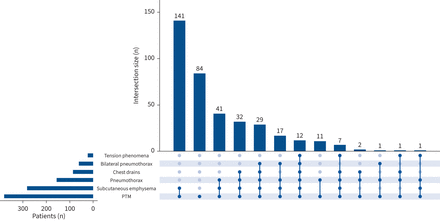
纵隔气肿(PTM)合并皮下肺气肿、气胸和紧张现象,并使用肋间胸引流(n=377)。交集大小是指只有这些特征的患者数量。双侧气胸是指在同一住院时间内发生两侧胸腔的气胸。
在我们的队列中,气胸的发生与死亡风险的增加无关(表1),包括16名在出现气胸前进行机械通气的患者(116名患者中有11名(9.5%)是随后死亡的患者,56名患者中有5名(8.9%)是出院的患者;p = 0.9)。气腹2例。这两例均为机械通气患者。
在8个病例中,PTM是在介入手术后出现的,这可能代表着一种单独的发生机制,如。气管造口术,这些病例都包括在最后的分析中。进行的分析排除了这些病例,与提出的结果没有任何统计上的显著偏差。
死亡率
入院后120天,377例患者中有175例(46.4%)出院,377例患者中有195例(51.7%)死亡。在住院120天的7名患者中,在撰写本文时,有1名患者在入院第162天死亡。3例患者在入院第131、146和150天仍保持机械通气。1例患者在入院第132天拔管,但仍在重症监护中。在所有结果分析中,这5名患者与120天内死亡的患者归为一类。其余两名患者在入院第137天和第149天的身体状况适宜出院到康复设施。在所有结果分析中,他们与120天出院的患者进行了分类。死亡率的细目载于补充表S6a和b根据患者是否符合机械通气条件或仅限于CPAP支持。
所有患者的表现因素和与结果的关系表1.在单变量分析中,所有与死亡率显著相关的因素都被输入二元回归预测模型,但ECMO除外,因为该变量的关联方向有利于出院而非死亡,因此将ECMO排除在外。当模型从诊断点进行时,排除了变量“PTM的影像学进展”。
中提出了一个回归模型,比较了从诊断点起120天内符合所有治疗条件的患者死亡率的变量的预测效用表2.进一步的模型着眼于相同变量在住院期间死亡率的预测效用,为符合条件的所有治疗的患者提出补充表S7对于那些只接受CPAP治疗的患者补充表S8.
讨论
这些数据构成了迄今为止关于COVID-19的最大的PTM系列数据。与其他系列相比,我们试图准确表示调查期间COVID-19中PTM的发生率,即。英国的“第二波”疫情。每个中心都系统地审查了医院记录和放射学报告。没有观察到PTM病例但提供准确发病率数据的医院也包括在内。但是,要求医院参与通过培训生研究网络,这可能导致了包容偏见。
我们对发病率的估计也受到诊断偏差的影响。我们通过放射科报告确定病例,这可能并不总是参考相关的发现。PTM的主要诊断模式是CT成像,各参与医院对CT的使用存在很大差异(补充图S4).许多胸部CT扫描是肺血管造影研究,以分析肺栓塞,而不是PTM。在胸部CT诊断为PTM的患者中,46.2%的患者在之前的胸片上无法看到PTM。我们共有58484例COVID-19 pcr阳性住院患者,其中只有21.7%的患者在入院期间进行了胸部CT成像,因此在我们的分母人群中可能有一些未被发现的PTM病例。这些未知病例的疾病轨迹可能比已查明的病例更为良性。
有了这些警告,这些数据显示,每住院患者中PTM的发生率为0.64%,每接受胸部CT的COVID-19住院患者中PTM的发生率为3.0%。这一发病率与巴西和罗马尼亚的另外两项关于COVID-19住院人群中PTM的研究报告的发生率相似,分别为0.51%和0.67% [13,14].在该队列中,COVID-19“自发”PTM的发生率,即。没有任何PPV通过机械通气(CPAP) 77例/ 58 484例(0.13%)。这远远高于非covid -19“自发”PTM的估计背景率。在定义分母人群的文献中,最大规模的非covid -19“自发”PTM研究发现,在过去16年的1824967例急诊科入院患者中,有41例为PTM (0.00002%) [15].
队列的平均年龄(59.1岁)与来自巴西、罗马尼亚、土耳其、巴基斯坦和美国的国际住院COVID-19 PTM队列一致[13,16- - - - - -19].根据最大的流行病学研究(70.4岁),这略低于英国普通COVID-19住院患者的平均年龄[20.].可能有病理生理原因导致发生PTM的COVID-19住院患者比医院人口平均水平更年轻(我们注意到,非COVID-19 PTM的背景率通常发生在年轻人中)[1,14,15].这可能反映出年轻患者倾向于更频繁的成像,他们通常符合所有治疗的条件,而在老年患者组中人为减少了PTM的识别。平均年龄较低也代表了英国“第二波”期间COVID-19住院患者的趋势[21].
气胸与PTM并存的病例占40.3%。相比之下,在其他10例以上患者的系列中,报告的发生率为20.0%至72.7% [6,13,16- - - - - -18,22].在这个队列中,没有发现对气胸死亡率的影响,也没有发现对那些发生气胸时进行机械通气的患者的影响。这与Marciniaket al。[23)的研究报告显示,在英国一个大型住院患者数据集中,COVID-19气胸的死亡风险增加hopraet al。[24他们发现,在美国的四个重症监护病房中,机械通气患者的死亡率增加了。由于M未报道并发PTMarciniaket al。[23与30%的Chopraet al。[24]研究中,尚不清楚这些患者组与我们的队列有多大可比性。气胸和PTM在多大程度上是COVID-19中由病理生理过程引起的气压创伤的表现,以及它们在多大程度上是不同的实体,仍有待确定。
77.9%的COVID-19 PTM患者出现皮下肺气肿(见CT图像)补充图S9).在其他COVID-19 PTM系列中,10名以上患者的皮下肺气肿发生率在63.6%至90.5%之间[13,16,17].这一结果与自发性非covid型PTM中皮下肺气肿高达100%的高报告率一致[1],并且皮下肺气肿与非covid -19气胸同时发生的较低发生率高达20% [25].这可能表明皮下肺气肿是与PTM密切相关的特征,而不是专门与COVID-19 PTM相关。然而,公认的是,皮下肺气肿和PTM的同时发生可能会导致诊断偏差,出现皮下肺气肿的患者更有可能通过CT成像诊断为PTM。
在这样的观察性研究中,不可能确定不同通气策略对结果的影响。然而,我们对那些在诊断为PTM时使用CPAP的符合机械通气条件的患者进行了检查。CPAP在PTM患者中的作用是一个临床重要问题:分析PTM诊断后呼吸支持的变化,可以探索医生对呼吸支持的偏好,并通过推断在PTM中使用PEEP。那些在诊断为PTM后立即继续使用CPAP的患者与那些立即使用吸氧或高流量鼻氧疗的患者的回顾性匹配程度最高FIO2和最大PEEP。这些亚组之间120天的存活率没有差异。因此,尽管我们承认潜在的混杂因素,但目前的数据不支持在诊断为PTM时停用CPAP的政策。
COVID-19 PTM患者的120天死亡率为51.7%,与其他COVID-19 PTM队列中报告的47.7-72.2%的死亡率一致[13,16,17].2019冠状病毒病的严重程度可从平均水平的高水平看出FIO2PTM诊断前后的PEEP (图1).只有2例患者(0.5%)在整个住院期间使用室内空气。与英国COVID-19住院患者机械通气的平均水平8.8%相比,在入院期间进行机械通气的患者数量为76.5%,非常显著[20.].机械通气在预后预测模型中是一个重要的预后因素和主导变量(表2).在有资格获得这种支持的病情恶化的患者中,这是一个普遍存在的事件。在我们的队列中,只有1例符合条件的患者在未进行机械通气的情况下死亡。
其他综合医院COVID-19住院患者研究报告了COVID-19患者机械通气的高比例[13,16].这可能反映了在高护理环境中,更严重的疾病与更高的CT扫描和检出率之间的混杂关系。这也可能提示机械通气在COVID-19 PTM发展中的重要作用。然而,该队列的大多数,377例患者中的205例(54.4%),在诊断PTM时未进行机械通气。因此,对于大多数患者来说,机械通气不是一种充分或必要的PTM机制。
文献中描述了不同的PTM机制,包括咳嗽引起的气管后膜病变或破裂[26].“麦克林效应”描述了继发于边缘肺泡破裂的PTM,这是由于肺泡和间质空间之间的压力梯度急剧增加[27].肺泡破裂后,空气沿支气管维管束鞘向心分离进入纵隔。根据体积和压力,空气可以沿着颈筋膜面减压进入胸壁、颈部或面部的皮下组织。空气可使相对较薄的纵隔胸膜破裂进入胸膜腔,引起单侧或双侧气胸和/或气心/气腹。米acklin和Macklin[27]认为,如果空气直接压缩心包或静脉回流(张力性PTM或气胸),这种影响可能是良性的,或导致循环衰竭。支气管-维管束中的空气还可能产生有害的夹板效应,导致恶性膨胀、血管压迫依从性低和气体交换不良,即“恶性间质性肺气肿”。“麦克林效应”的灵感来自于医生对1918-1920年流感大流行期间患有严重呼吸道疾病的患者出现“肺间质性肺气肿”的描述[28,29],其病理生理学可与COVID-19大流行相比较。
“麦克林效应”为COVID-19中的PTM提供了一种可能的机制,即肺炎为肺泡破裂和PTM的出现创造了一种改变的素质。队列研究支持COVID-19 PTM患者有严重肺炎的命题,这些队列研究描述了COVID-19 PTM患者肺炎的高放射学评分[10,16- - - - - -18].我们队列中高水平的呼吸支持(用于代表严重肺炎)、高发生率的皮下肺气肿、紧张现象发作和低发生率的胸痛(与自发性PTM相比)的补充发现支持“麦克林效应”作为COVID-19中PTM的可能机制。在2002-2004年的SARS疫情中,PTM病例报告也有所增加[30.这可能反映了相似的病理生理学。
未来对COVID-19机械通气患者的研究可能阐明改变跨肺泡压力的策略是否与PTM的发生或进展有关。我们注意到,与其他PTM患者相比,我们队列中377例(10.6%)肥胖患者中的40例死亡风险没有增加,并推测这是否与胸壁和/或腹部周围的肿块负荷与肺泡依从性和/或跨肺泡梯度降低有关。倾向匹配队列分析可以解决PTM的发展是否除了严重肺炎之外还增加了死亡风险,或者PTM的发展是否受到改善疾病的药物的影响,如地塞米松(我们队列的护理标准)或SARS-CoV-2的不同变体。
总之,本研究是COVID-19中报道的最大的PTM系列研究。PTM似乎是严重肺炎的标志,而不一定是使用PPV的结果。没有证据表明发生PTM的COVID-19患者持续CPAP会增加伤害。
补充材料
可共享的PDF
确认
我们要感谢Pallav Shah(英国伦敦国家心肺研究所皇家布朗普顿医院)、Lupei Cai和Muhammad Tariq(英国斯托克北部中部大学医院NHS信托医院皇家斯托克大学医院)、Benjamin Jones(英国威尔士卡迪夫大学医院和卡迪夫&瓦尔大学卫生委员会)和Emma Helm(英国考文垂大学医院和沃里克郡NHS信托大学医院大学医院)在数据收集方面的帮助;Maria Tsakok(英国牛津大学医院NHS信托基金会John Radcliffe医院)和Nick Tessier(英国沃特福德西赫特福德郡NHS信托医院沃特福德总医院)协助成像;和Simon Couillard (Faculté de Médecine et des Sciences de la Santé, Université de Sherbrooke, Sherbrooke, QC, Canada)和Sanjay Ramakrishnan(英国牛津大学约翰拉德克利夫医院纳菲尔德医学部)审阅手稿。
脚注
数据共享:研究中去身份识别的参与者数据将在非营利性基础上通过电子邮件请求通信作者的方式向医学研究人员提供,以用于倾向匹配或元分析。
作者贡献:J. Melhorn构思和设计研究,整理和分析数据,起草手稿。A. Achaiah和R.J. Hallifax贡献了数据,参与了研究设计和数据分析,并起草了手稿。F.M.康威、E.M.F.汤普森、E.W.斯基尔伯格、D.M.史密斯、P.纳兰、B.维贾阿库玛尔、M.J.泰特、C.A.多伊格、G.林奇、V.H.阿西姆巴、t.j.琼斯、A.奥贾耶布、B.R.H.欧文、A.J.E.哈里斯、V.卡鲁那尼提、E.W. Rowlands、A.Y.K.C. Ng、S.乌拉、M.S.斯图尔德、N.马德卡尔、P.J.埃文斯、M.纽金特、F.阿里、G.迪克森、M.巴特纳加、C.摩根、M.伊贾兹、M.P.布莱克本、N.A.哈桑、Y.马达尼、R.A.黑斯廷斯、H.R.贝伦伯格、A.阿扎姆、K.A.杰克逊、G.E.特里维良、i.a .扎基、D.M.史密斯、N.A.马赫迪、C.A.S.L. Khan, H. Iftikhar, J.H. Noble, h.h. Ellis, c.j. Chen, H. Lawrence, R.L. Saville, N.T. Johl, A.N. Grey, T.P. Sapkal, K.L. Bunclark, C. Rafique, B.J. Pippard, E.C. Barton, G. Warwick, r.j. Wollerton, R.S. Thorley, K.J. Millington, N.J. Budhram, V. Kumar, S. Naik, K. Savlani, M.A. Khan, A.I. Muhammad, Y. Maung Maung mung Myint, H. Ghani, B. Lara Gallego和A.J. Rostron贡献了数据并修改了重要知识内容的手稿。拉森(W. Lason)设计了数据并进行了统计分析,拉赫曼(N.M. Rahman)帮助设计了研究,并修改了重要的智力内容的手稿。J.梅尔霍恩是担保人,并对从开始到发表的文章的完整性负责。
利益冲突:作者声明没有利益冲突。
支持声明:该研究由国家卫生研究所(NIHR)牛津生物医学研究中心(BRC)资助。本文仅代表作者个人观点,并不代表国家卫生条例或卫生和社会福利部的观点。
- 收到了2021年9月19日。
- 接受2022年1月12日。
- 版权所有©作者2022。
此版本在知识共享授权许可4.0的条款下发布。