文摘
背景严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)呼吸系统感染可以进展到一个多系统疾病与异常炎症反应。细胞衰老促进慢性炎症,名叫senescence-associated分泌表型(SASP)。我们调查了冠状病毒是否疾病2019 (COVID-19)与细胞衰老和SASP相关联。
方法尸检肺组织样本11 COVID-19患者和43岁的同龄non-COVID-19控制SARS-CoV-2通过免疫组织化学方法分析类似的并发症,衰老的标志和关键SASP细胞因子。病毒诱导衰老功能完成在体外通过感染上皮Vero-E6肺泡ⅱ型细胞和一个三维的alveosphere系统(at₂)细胞SARS-CoV-2菌株隔绝COVID-19病人。
结果SARS-CoV-2检测主要通过免疫细胞化学和电子显微镜在at₂细胞。感染at₂细胞表达血管紧张素转换酶2和衰老增加(p16展出INK4A和SenTraGor积极性)和白介素(IL) 1β和IL - 6表达。在体外、感染与SARS-CoV-2 Vero-E6细胞诱导衰老(SenTraGor), DNA损伤(γ-H2AX)和增加细胞因子(CXCL8 IL-1β,il - 6)和载脂蛋白B mRNA-editing (APOBEC)酶表达。下一代测序分析获得的后代从感染/细胞衰老Vero-E6证明APOBEC-mediated SARS-CoV-2突变。传播SARS-CoV-2-infection和衰老证实肺外的网站(肾脏和肝脏)COVID-19病人。
结论我们证明严重COVID-19 at₂细胞感染SARS-CoV-2展览衰老和炎性表型。在体外,SARS-CoV-2感染诱发衰老和炎症。重要的是,被感染的衰老细胞可能充当SARS-CoV-2诱变源由APOBEC酶。因此,SARS-CoV-2-induced衰老可能是一个重要的分子机制严重COVID-19疾病持久性和诱变。
文摘
2型(at₂)严重COVID-19肺泡细胞感染SARS-CoV-2展览衰老伴随着炎性表型、持久性的分子机制可能是重要疾病(急性后遗症COVID-19)和诱变https://bit.ly/3fnopg9
介绍
严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)导致冠状病毒疾病2019 (COVID-19),它主要影响呼吸系统。临床课程范围从无症状到危及生命的呼吸衰竭伴有多系统炎性疾病(1,2]。系统性疾病可能发生在一个病毒介导炎症反应,由多种促炎细胞因子和趋化因子,包括白介素(IL) 1β,IL - 6、IL - 12, interferon-γ,肿瘤坏死因子(TNF) -αCXCL-8, CXCL-10 CCL-2 [3,4]。病毒感染的细胞之间的联系和发展严重肺部疾病和系统性表现仍知之甚少。病毒感染导致复杂的先天和适应性免疫反应的激活顺序编排,涉及多种细胞类型和炎症介质(5,6]。在细胞水平上,内在的防御机制被激活和结果从完全恢复到细胞死亡(7- - - - - -11]。一个“中间”被忽视和必要的细胞状态,由于缺乏有效的方法论工具,是细胞衰老12,13]。
细胞衰老是一种应激反应机制,保持体内平衡。衰老细胞的特点是长时间的,一般不可逆细胞循环逮捕和抗细胞凋亡(12,14]。此外,他们具有分泌功能,集体称为senescence-associated分泌表型(SASP) [12]。SASP包括多种细胞因子,趋化因子,生长因子、蛋白酶和其他分子,这取决于类型的衰老和细胞(12,15]。这些炎症蛋白被释放的可溶性细胞外空间因素,跨膜蛋白后ectodomain脱落或分子内吞噬细胞外囊泡(16- - - - - -18]。细胞衰老起着关键作用在一些肺部疾病,涉及几个细胞的衰老在肺19,20.]。在生理条件下,衰老和SASP期间短暂地激活介导免疫细胞衰老细胞间隙的招聘。此外,其他SASP因素促进组织再生和修复,全面确保细胞/组织内稳态。相比之下,持久性的衰老细胞产生有害属性促进组织功能障碍和慢性炎症的维护,通过旁分泌和系统性SASP [12,15]。
几乎没有证据表明病毒感染细胞衰老(发表21- - - - - -26]。鉴于炎症反应的含义COVID-19的恶化和SASP衰老细胞分泌,我们调查是否细胞衰老发生在COVID-19。因为单个标记不足够明确检测衰老,特别是在活的有机体内,因为他们也可能出现在nonsenescent条件,我们跟着在临床设置详细multimarker算法,我们和其他人最近发表和被批准的衰老社区(12,27]。我们是第一个提供证据证明COVID-19-infected衰老的肺组织通过应用该算法之前,预印本版本目前的手稿(28],它已经被其他人随后证实[29日]。这是最大的临床研究验证viral-induced衰老SARS-CoV-2感染与促炎的表型,这可能导致急性和慢性严重COVID-19临床表现。还重要的是,我们提供的新证据的生成病毒突变促进衰老细胞SARS-CoV-2持久性。
材料和方法
组织
Formalin-fixed和石蜡包埋尸检肺组织样本来自11个病人死于严重COVID-19(经逆转录(RT)定量(q) PCR) (表1和补充表S1a)。肺实质显示类似病变(肺不张、纤维化和由免疫细胞浸润)从43个年龄相似的并发症患者先前发表的队列(30.)和新情况下,切除COVID-19爆发前,被用于与COVID-19样本为所有实验详细(负控制)(此表1和补充表印地)。non-COVID群60与肺样本被用作验证生物-控制anti-SARS-CoV-2 (G2)单克隆抗体(补充材料)。此外,肾和肝组织的11 COVID-19病例和五non-COVID-19患者可以和分析存在的病毒和细胞衰老。临床样本收集和实验使用委员会批准Cantonale D 'ethique de la矫揉造作的(瑞士洛桑大学;2020 - 01257年)和生命伦理委员会雅典大学的医学院,希腊。
细胞和SARS-CoV-2文化
SARS-CoV-2(孤立30 - 287,B.1.222和(加入没有责任压力MT459880.1)是通过文化州立E6细胞(写明ATCC crl - 1586),从两个不同的感染(COVID-19)患者。病毒从鼻咽拭子中恢复,1毫升生理盐水冲洗,通过0.22纳米过滤器过滤两次。股票是由病毒感染完全汇合的Vero-E6细胞在DMEM, 10%胎牛血清和抗生素,在37°C和5%的二氧化碳。病毒接种后第4天股票收集,使用新一代测序序列(补充材料)和上层清液被冻结(−80°C),直到使用。感染进行了24-well盘子,使用SARS-CoV-2 0.01感染复数。细胞被固定用4%多聚甲醛或细胞溶解与NucleoZOL (Macherey-Nagel)感染后17天。政府的具体ataxia-telangiectasia-mutated (ATM)蛋白激酶抑制剂ku - 55933进行了描述(其他地方31日]。三个独立的实验进行。所有操作都进行三级生物安全水平的实验室设施。
SARS-CoV-2主要人类肺alveosphere系统
Formalin-fixed和石蜡包埋部分从三维alveosphere系统感染SARS-CoV-2和相应的控制(未感染)进行分析。alveospheres包括自我更新2型(at₂)肺泡细胞表达的at₂细胞标记htii - 280和表面活性剂蛋白质C,以及一些细胞表达AT1细胞标记HTI-56 [32]。Alveospheres轻轻打开使用移液允许感染,避免细胞应激(32]。
Anti-SARS-CoV-2 (G2)抗体的一代
小鼠免疫抗体集合,选择和特异性测定中描述补充材料。杂种细胞的转录组分析和氨基酸的测定选择克隆也提供。四个克隆(479 - s1, 480 - s2, 481 - 482 s3和s4)是根据专利申请(V.G. Gorgoulis, d . Vassilakos Kastrinakis。GR-patent应用:22 - 0003846810)。
蛋白分离和免疫印迹分析
蛋白分离和免疫印迹分析进行描述的其他地方(31日]。详情,请参考补充材料。辣根过氧化物酶抗体结合,anti-mouse anti-rabbit二级抗体(1:1000稀释)(细胞信号)。主要抗体anti-APOBEC(载脂蛋白B信使rna编辑酶,催化polypeptide-like) 3 g / A3G (Abcam ab109727和ab172694), anti-APOBEC3H (LSBio LS-C151868)和anti-glyceraldehyde 3 -磷酸脱氢酶(细胞信号)。
免疫细胞化学、免疫组织化学
免疫细胞化学、免疫组织化学进行根据出版协议(34]。一夜之间,以下主要抗体被应用在4°C: anti-SARS-CoV-2 (G2)单克隆抗体(稀释施用)anti-SARS-CoV-2单克隆抗体(1 a9克隆;Genetek), anti-angiotensin-converting酶(ACE) 2 (Abcam),甲状腺转录因子1 (TTF) (Dako) anti-surfactant蛋白(SP) - b (1 b9克隆;ζ公司),anti-p16INK4A(Santa Cruz), anti-IL-1β(Abcam) anti-IL-6(研发系统),anti-phospho-histone (Ser139年)H2AX(γΗ2ΑΧ)(细胞信号),anti-Ki67 (Abcam)和anti-p21Waf1 / Cip1(细胞信号)。
Senescence-SenTraGor (GL13)方法
SenTraGor GL13化合物(商标)染色和double-staining实验进行和评估如前所述27,35]。SenTraGor-positive肺泡细胞的平均比例≥10大功率领域(×400)/病人被量化。
电子显微镜
代表地区的苏木精和eosin-stained石蜡部分肺COVID-19患者的尸检和non-COVID-19控制是在光学显微镜下明显。石蜡包埋组织deparaffinised,水化和固定在2.5%戊二醛在PBS的24小时和你找找1%水锇。
生物信息学分析识别SARS-CoV-2基因组的突变特征
的详细描述补充材料,参加APOBEC脱氨基作用C→U SARS-CoV-2基因组的突变替换菌株中可用GISAID数据库(36,37),在细胞培养后获得感染,是检查和验证实验验证APOBEC主题(补充图S7)。
统计分析
数据意味着±sd。与未配对比较进行非参数Mann-Whitney u测验(比较两组)或克鲁斯卡尔-沃利斯检验Dunn的紧随其后事后分析对比三组)。Wilcoxon成对非参数测试是用来比较值受感染的细胞在体外。
结果
检测SARS-CoV-2肺细胞
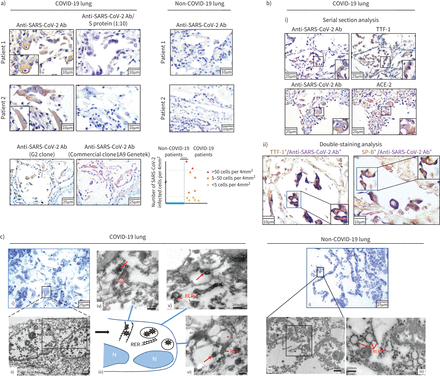
为了检测肺组织中的SARS-CoV-2我们发达单克隆抗体反应的受体结合域SARS-CoV-2和确定了高亲和性的突起蛋白抗体(G2),这是最近的有效性验证(38)(补充图S1,补充表S1)。SARS-CoV-2检测(使用我们的内部G2克隆和商用抗体从GeneTek)主要在at₂细胞,这是被TTF-1 SP-B积极性,在稀疏的炎症细胞(肺泡巨噬细胞和组织)在所有COVID-19病人,从< 5细胞/ 4毫米2组织> 50细胞每4毫米2组织(图1一个,补充表S1a)。表面上皮细胞在小外围航空染色也积极的在某些情况下(补充图S2)。偶尔SARS-CoV-2-infected at₂细胞大而出现孤立(剥蚀或合胞体)或集群(增生),表现出多种拓扑分布(图1一个)。这些细胞中的ACE2受体(图1 b),支持SARS-CoV-2感染ACE2受体介导的(39]。此外,电子显微镜分析代表COVID-19确诊病例at₂细胞内病毒的存在(图1 c)和高放大显示病毒粒子在内质网的距离,来显示他们可能装配和出芽,以及居住在胞质囊泡病毒粒子,这意味着他们的转移和释放到细胞外空间。
检测严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)从2019年死于冠状病毒疾病的患者肺细胞(COVID-19)。)代表的图像SARS-CoV-2 (G2 mAb)免疫组织化学染色在COVID-19尸检肺组织。与anti-peptide竞争(S蛋白)显示G2免疫染色的特异性。验证的G2 immunopositivity商业anti-S抗体(Ab) (clone1A9克隆;Genetek)。代表消极控制免疫染色non-COVID-19肺组织。图显示了肺部SARS-CoV-2染色样品的量化。b)检测SARS-CoV-2 2型(at₂)肺泡细胞(证实了积极甲状腺转录因子1 (TTF)和表面活性剂蛋白(SP) - b染色)和血管紧张素转换酶(ACE) 2-expressing细胞(我);(二)双SARS-CoV-2和TTF-1显示疣状。c)检测SARS-CoV-2通过透射电子显微镜(EM)代表COVID-19病人。 Presence of SARS-CoV-2 i, ii) within AT2 cells and of iii, iv) virions in the proximity of the endoplasmic reticulum, iii, v, vi) as well as in cytoplasmic vesicles. ****: p<0.0001.
SARS-CoV-2-infected细胞衰老
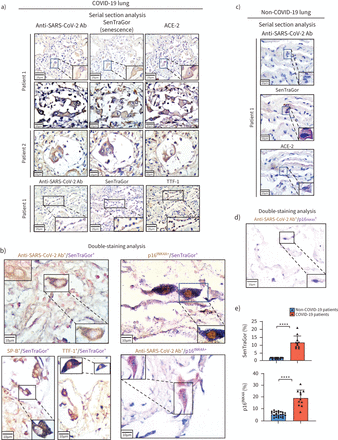
SARS-CoV-2-infected at₂细胞比例(8 - 21%范围)显示衰老表型,SenTraGor和p16阳性染色INK4A(图2一个- c,补充图S3)[12,29日,30.]。SenTraGor衰老的标志,检测衰老细胞的独特财产在任何设置,包括档案材料(formalin-fixed石蜡包埋组织)(12,27,35]。相比之下,肺组织出现纤维化肺不张及炎性浸润的同龄non-COVID-19例类似的并发症(表1,补充表S1),包括一个单独的控制群患者急性肺炎(吸入性肺炎),显示显著降低衰老(范围1 - 2%,p < 0.0001) (图2一个- c,补充图S4),这表明SARS-CoV-2感染可能引起衰老。
衰老在严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)来华的细胞。SARS-CoV-2)代表图像,SenTraGor(衰老)和血管紧张素转换酶(ACE)在串行部分染色冠状病毒病2019 (COVID-19)肺组织。b) Double-immunostaining分析SARS-CoV-2, SenTraGor(衰老),p16INK4A、甲状腺转录因子1 (TTF)和表面活性剂蛋白(SP) - b在COVID-19肺部组织。c)代表SARS-CoV-2连续染色结果,SenTraGor(衰老)和ACE2,和d) double-staining SARS-CoV-2和p16INK4A在non-COVID-19肺部组织。e)图表显示增加SenTraGor和p16的表达INK4A在COVID-19肺部组织。阿瑟:抗体。* * * *:p < 0.0001。
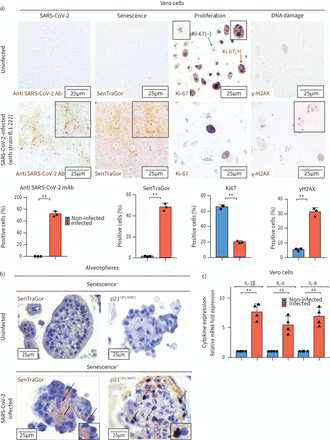
为了证明SARS-CoV-2可以诱导细胞衰老,我们维洛细胞感染病毒毒株COVID-19病人隔离。Vero-E6细胞为病毒传播和提供一个建立了单元系统的研究中,除了他们的高传染性SARS-CoV-2他们为数不多的细胞系展示SARS-CoV-2-mediated细胞病变效应,一个重要的方面在诊断(40,41]。感染进行了低感染复数模仿自然的冠状病毒感染(42]。符合我们的假设,浪潮过去感染细胞后,细胞死亡达成平衡展示清楚衰老(p21 SenTraGor积极性增加,增加的证据WAF1 / CIP1和减少ki - 67),比未感染控制细胞在感染后17天(图3,补充图S5a)。维洛细胞p16缺乏INK4A(43),最可能引发衰老的DNA损伤,先前报道(12,13]。DNA损伤衡量γ-H2AX疣状明显在SARS-CoV-2感染细胞(图3一)。治疗感染细胞的选择性ATM抑制剂(ku - 55933)显著下降衰老评估SenTraGor染色(补充图S6)。ATM先前报道的关键驱动因素NF-κB-dependent DNA-damage-induced衰老(44]。看来,基因毒性压力强加的结果从一个恶性循环病毒在宿主细胞劫持大多数细胞内蛋白质机械(11,45]。同样,细胞衰老被确认感染肺泡细胞/ alveospheres建立主肺肺泡的三维模型,证实了在活的有机体内观察和研究结果在维洛细胞(图3 b,补充图S5b)。
全身的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2) Vero-E6细胞衰老和alveospheres。SARS-CoV-2面前,衰老诱导、细胞增殖和DNA损伤激活,与相应的量化直方图,Vero-E6细胞有无SARS-CoV-2感染(17天postinfection)。b)衰老感应(p21 SenTraGor和评估WAF1 / CIP1肺泡细胞染色)(alveospheres)主肺肺泡SARS-CoV-2感染后三维模型(黑色箭头)相比nonsenescent(黄色箭头)。没有未感染肺泡细胞衰老中一览无遗。c)图显示诱导senescence-associated SARS-CoV-2感染后细胞因子分泌phenotype-related Vero-E6细胞(mRNA表达对β正常化2微球蛋白mRNA表达)。阿瑟:抗体;IL:白介素。* *:p < 0.01。
Senescence-associated分泌表型
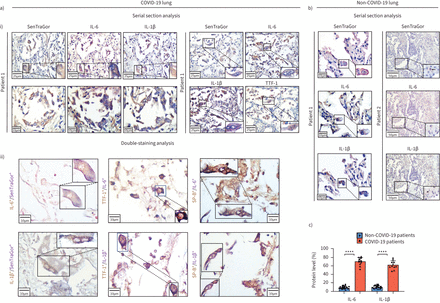
我们发现很高IL-1β和il - 6的表达衰老at₂COVID-19患者的肺细胞,而在non-COVID-19控制情况下,包括急性肺炎患者样本,表达很低的少数细胞衰老at₂检测肺组织纤维化,肺不张,炎性浸润(p < 0.0001) (图4一- c,补充表S1)。作为炎症反应的细胞因子都是关键的组件SARS-CoV-2,我们的研究结果表明,这种模式的炎症可能是由于SASP COVID-19患者由于细胞衰老。同样,SARS-CoV-2衰老维洛细胞显示SASP-related细胞因子的表达,作为衰老的评估我们的算法评估,支持我们在活的有机体内发现(图3 c)。
Senescence-associated分泌表型在冠状病毒疾病2019 (COVID-19)肺组织。)代表染色结果(SenTraGor在低和高放大倍数)、白介素6 (IL) IL-1β和甲状腺转录因子1 (TTF)和/或表面活性剂蛋白(SP) - b i)相应的串行部分和ii) double-immunostaining COVID-19肺组织的分析。原来放大:×400。b)代表缺席或最低级别的SenTraGor染色结果表明,il - 6和IL-1β年龄non-COVID-19控制样本。c)相应图表描绘量化的il - 6和IL-1βCOVID-19和non-COVID-19患者。* * * *:p < 0.0001。
SARS-CoV-2肺外的传播
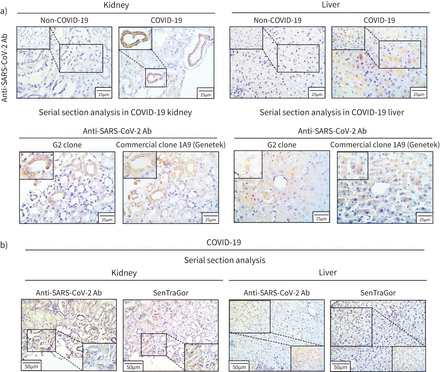
SARS-CoV-2免疫反应性是我们内部G2克隆另外被应用和商业从GeneTek串行部分可用的肾脏和肝脏组织从一个COVID-19病人(图5一个)。明显的胞质信号明显的肾小管以及肝实质的领域。相比之下,在组织non-COVID-19缺席情况下,信号,如预期(图5一个)。有趣的是,通过连续切片分析,区域窝藏病毒也表现出衰老(SenTraGor积极性),暗示SARS-CoV-2-induced衰老的发生肺外的网站(图5 b)。
严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)在肺外网站传播。)代表的染色结果SARS-CoV-2肾脏和肝脏的2019 (COVID-19)患者冠状病毒疾病。缺乏相应的组织的免疫组织化学信号明显代表non-COVID-19情况。b)的连续切片分析代表COVID-19案例(看到)描述并发SARS-CoV-2积极性和衰老标记(SenTraGor)在肝脏和肾脏的细胞。阿瑟:抗体。
受感染的衰老细胞和SARS-CoV-2诱变
最近,我们提出,衰老细胞可能代表SARS-CoV-2准物种来源的一代(46]。这种假设是基于事实,衰老细胞的凋亡宽容性质允许病毒被托管更长时间比其他细胞营业额较高的细胞(47,48),从而呈现SARS-CoV-2 virome更容易host-mediated编辑。APOBEC酶是众所周知的参与病毒基因组编辑(12,33,49]。值得注意的是,我们给这些酶在衰老细胞中表达的高度49]。
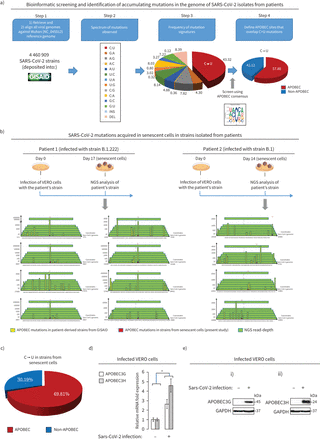
更新我们最初的生物信息学研究[46),我们筛选∼4 500 000 SARS-CoV-2菌株GISAID数据库(36,37]。这种分析主要表明SARS-CoV-2变异的主要特征是APOBEC-mediated (图6),符合最近的文献[50]。来验证我们的假设,我们进行细胞培养感染两种隔离病人和获得的后代从衰老细胞(图6 b)。下一代测序分析表明,收集到的病毒基因组获得突变。重要的是,主要的模式是APOBEC-driven,协议的生物信息学分析GISAID数据库。此外,符合我们的假设和先前的研究[49),演示的SARS-CoV-2-induced衰老细胞明显高于APOBEC mRNA和蛋白水平的酶,尤其是G和H (RNA编辑细胞质变种),据报道,发挥关键作用的病毒RNA编辑(12,33,49]。其他突变签名也发现在cell-culture-isolated virome基因组的菌株GISAID,也许氧化应激的结果出现在衰老细胞(51]。
衰老细胞感染作为一个公认的严重急性呼吸系统综合症冠状病毒来源2 (SARS-CoV-2)准物种变异的一代。)原理图的布局呈现载脂蛋白B的识别mRNA-editing (APOBEC)介导突变4 672 296 SARS-CoV-2菌株的基因组中可用GISAID数据库。算法评估看到补充图S7和补充材料和方法。b)识别SARS-CoV-2突变在衰老细胞在两株(B.1.222和责任)与两种不同的患者中,感染后细胞培养的时间(每天1和14)表示。黄色栏显示C→U替换的频率在GISAID数据库在下一代测序(上天)读计数(绿色限速)和红酒吧描述C→U突变频率观察感染后细胞在当前的研究中,在两个雇佣SARS-CoV-2菌株的基因组。这些网站是排名最高的相对C→U算得上观察到的GISAID数据库。每个C→U基因组序列侧翼也提出,而他们的坐标相对于叠加SARS-CoV-2基因组所示。总会在读取被证实在一式三份。c)更高频率的c→U替换在APOBEC共识(补充图S7)在隔离病毒的基因组Vero-E6细胞获得的后代。d)增加APOBEC3G和APOBEC3H mRNA水平Vero-E6感染细胞。e)增加APOBEC3G和APOBEC3H Vero-E6感染细胞中蛋白质含量。
讨论
我们演示了存在SARS-CoV-2 at₂细胞的患者死于COVID-19使用我们的小说,一个商业anti-SARS-CoV-2抗体对其峰值蛋白质和电子显微镜。我们展示了第一次后,senescence-detecting算法在活的有机体内占SARS-CoV-2-infected at₂细胞表现出细胞衰老的特征(如通过显著增加染色与p16的小说衰老标记SenTraGor也INK4A)[12,27,35]。在这方面,我们的调查包括连续切片分析和costaining首次展示在活的有机体内哪些细胞真正衰老和感染。发现在年龄non-COVID-19控制,包括肺组织样本一群患有急性肺炎,衰老细胞的比例要低得多(1 - 2%)比COVID-19病人(8 - 21%)强烈表明SARS-CoV-2触发衰老。确认SARS-CoV-2诱导细胞衰老本身,我们证明了SARS-CoV-2病毒感染上皮细胞(B.1.222应变)在体外增加SenTraGor染色和诱导的DNA损伤,以增加γ-H2AX表达式。ATM的重要的是,我们发现抑制顶端DNA损伤反应的协调器(DDR)途径,极大地降低了衰老在感染样本,表明SARS-CoV-2-induced衰老是由DNA损伤和DDR通路的激活。符合我们的在活的有机体内和在体外发现,SARS-CoV-2-induced衰老被确认在初选之前建立肺肺泡(三维模型32]。alveospheres这一事实进行了温和的机械操作不太可能是导致衰老的发生,鉴于此类干预措施经常应用于三维瀑样系统和没有报告衰老表型也明显从感染后细胞增殖率和文化52]。
此外,我们表明,高表达的细胞感染SARS-CoV-2展览IL-1β和il - 6,这两个组件SASP和涉及严重的系统性特征COVID-19 [3,4]。因此,我们的在体外和在活的有机体内研究结果表明,SARS-CoV-2高度at₂细胞通过ACE2感染这些细胞,通过激活DDR信号,诱导细胞衰老和相关的促炎的表现型(SASP)。符合我们的观察,Leeet al。(29日]表明SARS-CoV-2-induced衰老表现出增强γ-H2AX DNA损伤病灶废除的活性氧(ROS)清除剂n -乙酰半胱氨酸常暗示的含义ROS和氧化应激(补充图S8)。此外,感染细胞显示SASP-positive衰老由p53和注册会计师/刺信号通路的激活29日]。他们也证明了senolytics减少COVID-19肺部疾病和炎症感染的仓鼠和老鼠29日),进一步表明SASP作为病毒诱导衰老的结果。Camellet al。(53)报道,治疗senolytics老老鼠感染SARS-CoV-2-related鼠标β-coronavirus减少炎症。基于我们的研究结果和最近的证据,一个潜在的机械的场景可以如下(补充图S8)。在入口,病毒劫持某些能源消耗功能与RNA加工、翻译和内质网(11]。因此,发生能量转移,导致活性氧产量的增加,氧化应激和DNA损伤/ DDR途径激活。此外,DDR和随后的细胞周期阻滞可能由一个交互的冠状病毒nsp13蛋白质和DNA聚合酶δ(54)和SASP通过注册会计师/刺痛和其他DNA-damage-dependent通路(补充图S8)。因此,我们之前的工作表明,DNA损伤/ DDR的衰老意味着它的重要性是一个有效的诱导物的建立病毒诱导衰老表型(31日]。
衰老细胞的细胞周期阻滞,但保持新陈代谢活跃,分泌炎症蛋白质称为SASP的典型剖面。SASP组件包括促炎细胞因子IL-1β和il - 6,升高血浆的COVID-19病人急性呼吸窘迫综合征或系统性炎症特征。我们在COVID-19表明,衰老改变at₂的属性和功能的细胞,产生细胞因子,可以释放到体循环,放大和延续慢性炎症。当然,组织样本的可用性和更精致的COVID-19的缺失在体外和在活的有机体内模型很难得出可靠的结论。很可能SARS-CoV-2利差从上皮细胞下呼吸道感染at₂肺泡壁细胞,ACE2表达,导致当地的衰老和炎症通过SASP肺。符合这个概念,它之前已经报道过了在体外细胞衰老也作为一个天然抗病毒防御机制和SASP充当这个反应的主要因素,激活和招募免疫系统清除感染(21,22]。随后,其他细胞隔间(干/祖细胞,内皮细胞和炎症细胞)可能会受到影响通过不同的细胞和noncell-autonomous机制,导致异常的免疫反应,慢性炎症,组织功能障碍和/或纤维化,最终肺损伤和失败(26,55]。特别是,在干细胞/祖细胞衰老会损害肺再生能力。免疫衰老导致高架neutrophils-to-lymphocytes比率和高il - 6生产。此外,il - 1、il - 6、CXCL8 TNF-α可能是至关重要的维持慢性炎症,TGF-β、纤溶酶原激活物inhibitor-1基质金属蛋白酶可能支持纤维化通过纤维化的基因的表达(ACTA2、COL1A1 COL1A2和FN1)在周围的微环境。病毒可能会进入血液循环并衰老可能随后系统传播,影响其他器官(图5),导致multiorgan失败/ multimorbidity和死亡在急性期(1,25),或导致急性后遗症COVID-19 (PASC或长COVID),长期并发症的发展综合症(26,56]。通过这种方式,衰老也会使疾病严重程度根据SARS-CoV-2再次感染或由其他病毒感染,甚至产生负面影响疫苗效果,同样提出了老年个体(26]。
额外的含义与长期生存的衰老细胞感染病毒,因为衰老细胞抗凋亡和间隙efferocytosis [12,14]。这种情况下可以提供一段时间“窗口”病毒复制,因此暴露其基因组host-mediated编辑。沿着这个脉络我们表明,衰老细胞间充当“肥沃”环境突变病毒的进化,因为它是更容易APOBEC-3G和3 h RNA编辑(图6)[33,49]。当然,其他机制延长生存和复制SARS-CoV-2可能发生。冠状病毒代码的一种重要的多功能酶称为papain-like蛋白酶产生内在deubiquitinating和deISGylating活动。后者与干扰素刺激基因(研究小组)upregulation和可以与宿主的免疫反应,否则阻碍感染(57]。以这种方式,增加和长期病毒复制和曝光的基因组host-mediated编辑和准物种生成也可能发生。考虑到干扰素衰老抗病诱导剂,情况变得更加复杂,呈现很难区分ISG-mediated机制涉及到的那些病毒诱导衰老(58]。还需要更多的研究和指导算法的方法在活的有机体内衰老评估,然后在当前工作,预计澄清在未来很多悬而未决的问题在临床设置(12,27]。值得注意的是,在最近确认买卖(B.1.1.529) SARS-CoV-2变体/应变APOBEC签名被确认为主要突变概要文件(补充图S9)。为了更好的理解这个角色的APOBEC代病毒突变,抑制APOBEC蛋白质的RNA干扰将是有价值的。然而,这是非常具有挑战性的,因为APOBEC抑制诱发DNA损伤和tslp细胞应激死亡(59- - - - - -61年]。有趣的是,和符合我们概念连接细胞衰老与病毒突变,通过进行生物信息学分析,我们发现病毒绕过细胞衰老(致癌)表现出显著的低突变病毒诱导衰老(相比负担补充图S10)。鉴于突变会影响疫苗的有效性,我们的发现可能意味着病毒诱导衰老在疫苗接种战略的潜在含义。需要进一步的研究。
尽管至今这是最大的临床研究表明病毒诱导衰老SARS-CoV-2,限制我们的研究是相对比较小的样本的大小COVID-19肺尸检,由于访问这种稀有材料的难度,因为尸体解剖是有限的,只有在初始阶段的COVID-19爆发为了确定这个新实体的病理基础。另一个限制由于疾病,病理的本质特性,如肺细胞衰老,只能在惨白的调查材料,代表最严重的结果COVID-19谱的临床表现。因此,评价幅度较小的衰老状况目前不是可行的。此外,在我们的研究中,我们研究了18例吸入性肺炎,显示相似程度的衰老和其他未感染控制情况。这将是有趣的扩展这些研究其他类型的肺炎。然而,从患者急性材料,但不是COVID-19-related炎症反应是罕见的,因为这些病人通常恢复后罕见病例的治疗和致命的尸检结果很少执行。
总的来说,SARS-CoV-2-induced衰老证明的治疗应用senotherapeutics COVID-19患者的治疗和可能long-COVID综合症(56]。槲皮素是最近在两个随机临床试验测试与标准治疗(ClinicalTrials.gov标识符NCT04578158和NCT04861298)患者确诊SARS-CoV-2感染和轻度COVID-19-associated症状。在这两个试验,senolytic干预导致临床改善(62年,63年]。总的来说,这些数据暗示senolytics的有益作用在显著改善结果SARS-CoV-2感染。
补充材料
可共享的PDF
确认
我们要感谢Konstantinos Ntostoglou(分子致癌集团部门组织学和胚胎学,医学院,国家和大学Kapodistrian雅典,雅典,希腊)为他宝贵的帮助在准备材料。我们承认在RNA序列支持希腊个性化医学研究基础设施(pMED-GR) (MIS 5002802),这是实现作用下研究和创新基础设施的“强化”,由运营计划“竞争力、创业和创新”(NSRF 2014 - 2020)和希腊和欧盟联合(欧洲区域发展基金)。
脚注
作者的贡献:k Evangelou和d . Veroutis:免疫细胞化学,SenTraGor染色;k . Evangelou P.G. Foukas, c . Kittas l . de水平表示和V.G. Gorgoulis:染色的组织病理学检查和评估;m . Dimitriou和i Karakasiliotis:细胞培养、病毒操作;开国元勋之一B.R.安贝德卡对脱:3 d alveosphere系统和病毒操作;a . Kotsinas Papaspyropoulos: RNA和蛋白质提取、RT-qPCR,门店,免疫印迹;n Lagopati和美国Havaki:电子显微镜;o . Hazapis和Polyzou:统计分析、生物信息学分析和图表生成;d . Vassilakos: anti-SARS-CoV-2抗体生成;k . Evangelou A.G. Tzioufas, k . Paschalaki Tsiodras和V.G. Gorgoulis:数据分析和解释,手稿准备;s . Tsiodras a . Papantonis g . Blandino P.J.巴恩斯和V.G. Gorgoulis:实验设计、指导、手稿写作与输入从所有的合作者。
利益冲突:P.J.巴恩斯得到研究经费从阿斯利康和勃林格殷格翰集团和阿斯利康的科学顾问,勃林格殷格翰的发言,Epi-Endo,诺华,地区和梯瓦。其他作者希望宣布无利益冲突。
支持声明:这项工作得到了国家公共投资项目的发展和投资/总秘书处研究和技术框架的旗舰计划解决SARS-CoV-2Σe01300001 (2020);地平线2020玛丽·斯卡洛多斯卡·居里培训项目722729号(SYNTRAIN);福利社会和文化科学基础,雅典,希腊(KIKPE);h·帕帕斯捐赠;希腊的基础研究和创新(回报)授予数字775年和3782年;欧洲区域发展基金的欧盟和希腊国家基金通过操作项目的竞争力,创业与创新,在调用研究-创建创新(项目代码:t1edk - 02939)和NKUA-SARG格兰特70/3/8916。k . Paschalaki为国家心肺研究所资助,伦敦帝国理工学院和英国心脏基金会项目资助(PG / 19/75/34686)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2021年8月27日。
- 接受2021年12月24日。
- 版权©2022年作者。
这个版本分布在Creative Commons归因执照的条款4.0。