摘要
COPD患者因肺炎入院后的死亡率明显高于从常规临床实践中招募的急性加重入院后的死亡率。因此,COPD症状急性恶化时的正确诊断非常重要。https://bit.ly/3LyhnnC
致编辑:
慢性阻塞性肺病患者常出现病情加重和肺炎,有时病情严重,导致住院[1- - - - - -3.]。吸入糖皮质激素(ICS)治疗可进一步增加肺炎的风险[4- - - - - -6]。虽然可能很难区分[7],与这些事件相关的死亡风险可能存在差异,在规划管理和临床随访时需要考虑到这一点。Salford肺研究的建立是为了评估每日吸入一次糠酸氟替卡松和维兰特罗的有效性和安全性(FF/VI;在ELLIPTA干粉吸入器中)与现有的维持疗法(常规护理)相比,在正常护理条件下的大量真实世界COPD患者群体中[8]。该研究的优势包括相对未选择的患者群体,使用联合电子记录系统进行随访的完整性,以及所有患者在病情加重和入院期间都得到了通常标准的护理。我们使用这个研究数据库来检查重症加重或肺炎入院后的死亡率,以及这些事件分类的影响。
索尔福德肺研究共招募了2799名40岁或以上、全科医生诊断为COPD且过去3年COPD发作≥1次的全科患者[8]。所有患者均接受常规吸入器维持治疗。
该研究已在前面详细描述[8]。平均年龄67岁,平均FEV11.62 L,女性占49%。在本亚研究的分析中,我们汇集了所有ICS患者,以便能够联合分析足够数量的事件。我们回顾了研究期间所有因严重加重或肺炎入院的患者的死亡叙述以及所有可用的胸片。影像学检查由临床医生自行决定。在这项研究中,所有的x光片都是由三名专业放射科医生独立阅读的,他们不知道医生的诊断。如果有分歧,通过讨论达成一致意见。
为了确保事件发生后有足够的随访,我们纳入了随机分组后184天的事件,以便随访6个月。严重急性加重定义为住院和诊断为急性加重。根据主治医生作出的初步诊断,确诊为肺炎。对于我们的额外分类分析,我们根据放射科医生对胸片的评估进行了诊断,即。存在与没有新的肺浸润;肺炎与恶化。对于这两种情况,我们都采用了首次入院的方法。为此,我们获得了121张胸片,全部由三位放射科医生评估。
在接受随机分组的2799名患者中,111名患者因初步诊断为COPD加重而入院;86人住院,初步诊断为肺炎。入院患者年龄较大(肺炎:70.2岁;COPD加重:69.3年)比未入院者(66.4年)。与因慢性阻塞性肺病加重或未因两者入院的患者相比,因肺炎入院的患者多为男性,目前吸烟的患者较少。在收治的COPD患者中,60%患有严重或非常严重的COPD;47%的肺炎患者和27%的未入院患者都是如此。与肺炎患者(53%和42%)和未入院患者(48%和30%)相比,在随机分组前一年有>2加重史和心脏共病的COPD患者(77%和47%)更频繁。
在111例住院恶化患者中,有8例(7%)在6个月的随访中死亡,而86例肺炎入院患者中有14例(16%)死亡。在Cox回归模型中,以年龄、性别、加重史、进入研究时使用ICS、COPD评估测试评分和吸烟状况为协变量,入院后30天内死亡的危险比在加重住院和肺炎入院时分别为29.6 (95% CI 12.5-69.9)和176.8 (95% CI 102.6-304.7)。在一个分析入院后31-180天死亡率的类似模型中,风险比分别为0.85 (95% CI 0.1-6.2)和11.6 (95% CI 5.1-26.3)。因急性加重或肺炎死亡的患者入院前病情加重史无差异。
入院医生诊断为肺炎的事件与随后基于专科放射科医生对胸片的盲法评估而进行的事件分类之间存在很大差异。放射科医生认为只有61%的病例存在肺炎,10例临床分类为慢性阻塞性肺病急性加重的病例被重新分类为肺炎。放射科医师对有无肺炎的重新分类对出院后死亡风险有显著影响(图1).
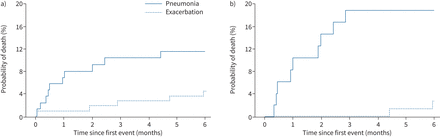
根据a)研究报告和b)放射科医生报告,因急性加重或肺炎入院诊断后的死亡时间。
入院后死亡率的解释是有警告的。许多死亡发生在指数住院后的几个月,这在以前的肺炎研究中是众所周知的。然而,死亡风险持续上升约3个月。我们进行了6个月的随访,更长的随访时间可能会增加额外的死亡。恶性肿瘤在这组患者中很常见,就像在一般的慢性阻塞性肺病中一样,我们不能排除一些肺炎是随后致命恶性肿瘤的首次影响的可能性。然而,值得注意的是,仅在独立放射学评估确诊为肺炎的患者中,才观察到30天后死亡风险持续升高。放射科医生对与肺炎一致的浸润的诊断对预后的影响是重要的。这对临床护理有影响,因为区分急性加重和肺炎的重要性很少被强调[1这对于解释过去和未来COPD背景下的肺炎研究来说是一个显著的教训。
在我们的亚研究中,由于研究设计的原因,大约90%的患者接受了ICS治疗[8]。因此,我们无法评估ICS带来的额外风险;然而,与ICS使用相关的肺炎风险是有据可稽的[9]。使用ICS治疗的目的是减少需要全身性皮质类固醇治疗的病情加重,这种治疗本身与严重肺炎风险增加有关[10]。这总是使临床医生对ICS的风险/收益评估复杂化。
我们的研究包括未选择的诊断为COPD的患者群体,可能占索尔福德所有COPD患者的50%。在务实的环境中,存在许多不确定性:诊断程序的不同使用,临床医生诊断评估的差异,后续再入院的影响,等。然而,这些真实世界的数据很重要,因为在随机对照试验中,对ICS治疗背景下与肺炎相关的风险的解释可能具有误导性,因为肺炎风险最高的患者(肺功能非常低,体重指数非常低,严重的合并症)通常被排除在外。我们的数据有力地表明,在未选择的COPD患者组中,在决定是否使用ICS时给予肺炎事件的权重可能在某些患者组中有所不同,特别是那些通常被排除在随机对照试验之外的患者。
可共享的PDF
确认
商标由葛兰素史克集团拥有或授权给该公司。
脚注
索尔福德肺研究试验注册号是NCT01551758。有关葛兰素史克的数据共享承诺和要求访问匿名参与者个人数据和相关文件的信息可在www.clinicalstudydatarequest.com
利益冲突:J. Vestbo从葛兰素史克公司收取个人费用。,Chiesi Pharmaceuticals, Boehringer Ingelheim, Novartis and AstraZeneca, congress attendance from Chiesi and holds a grant from Boehringer Ingelheim. G. Waterer received personal fees from GlaxoSmithKline plc. N. Diar Bakerly received grants and personal fees from GlaxoSmithKline plc., Novartis and Almirall/AstraZeneca, and congress attendance from Boehringer Ingelheim. I. Satia received personal fees from GlaxoSmithKline plc., consulting and speaker fees from AstraZeneca and Merck, grants from Merck, GlaxoSmithKline plc, fellowship from ERS Marie-Curie Award, E.J. Moran Campbell Early Career Award, Department of Medicine, McMaster, outside the submitted work. A. Woodcock received speaker fees and expenses from Boehringer Ingelheim, Chiesi, GlaxoSmithKline and Novartis; is chairman/shareholder of Reacta Healthcare and Axalbion, and Chairman of the Medicines Evaluation Unit. D. Leather, L. Frith, L. Jacques and C. Harvey are employees of GlaxoSmithKline plc. and hold shares in the company. C. Crim was an employee of GlaxoSmithKline plc. at the time of the study.
支持声明:该研究由葛兰素史克公司全额资助。(研究编号:HZC115151)。J. Vestbo, I. Satia和A. Woodcock得到了国家健康研究所曼彻斯特生物医学研究中心(NIHR Manchester BRC)的支持。本文的资助信息已存入交叉参考基金注册。
- 收到了2021年11月9日。
- 接受2022年2月6日。
- 版权所有©作者2022。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org















