文摘
背景慢性气道炎症是发病的主要原因在严重哮喘等呼吸系统疾病,慢性阻塞性肺疾病,囊性纤维化(CF)和支气管扩张。当气道炎症的常见病原体的作用被广泛认可,其他微生物群成员的影响还知之甚少。
方法我们提出,肺部微生物群包含细菌和免疫调节活动调节净重要呼吸道病原体的免疫激活水平。因此,我们评估了肺部微生物群的免疫调节效应的几个成员经常报道出现在CF下呼吸道样本。
结果我们表明,罗氏菌属mucilaginosa普通居民的口腔也经常检测下呼吸道慢性疾病,对病原菌有抑制作用,或者lipopolysaccharide-induced促炎症反应,在体外(三维细胞培养模型)在活的有机体内(小鼠模型)。此外,在一群成年人与支气管扩张,大量的罗思氏菌属物种是负相关的炎性标志物(白介素(IL) 8和IL-1β)和基质金属蛋白酶(MMP) 1, MMP-8 MMP-9痰。机械的研究显示,r . mucilaginosa抑制NF-κB途径激活的磷酸化通过减少IκBα因此NF-κB目标基因的表达。
结论这些发现表明的存在r . mucilaginosa在航空公司可能减轻炎症,这可能反过来影响慢性呼吸系统疾病的严重程度和进展。
文摘
一个共生的细菌的航空公司,罗氏菌属mucilaginosa由NF-κB通道失活,抑制炎症。r . mucilaginosa丰富反向与痰在慢性肺病、炎性标记表明了有益的作用。https://bit.ly/3lNT9th
介绍
持续或肺部炎症特异表达的一个特点严重慢性呼吸道疾病,如哮喘、慢性阻塞性肺疾病(COPD),囊性纤维化(CF)和支气管扩张1- - - - - -9]。在慢性呼吸道疾病患者,释放促炎细胞因子的细胞的肺粘膜反应外部触发器(病原微生物,香烟的烟雾,污染或过敏原)通常会导致先天免疫细胞如中性粒细胞和嗜酸性粒细胞的浸润,进一步加重肺部炎症(5- - - - - -7,10,11]。持续的炎症和组织损伤相关损害肺间隙和促进微生物的积累较低的航空公司。这些微生物代表认可的呼吸道病原体和口咽共生的类群,起源于上呼吸道(12]。
殖民的航空公司由特定细菌和真菌物种直接有助于炎症、组织损伤和肺疾病进展(13- - - - - -15]。这些物种包括铜绿假单胞菌和金黄色葡萄球菌CF患者(16- - - - - -18),流感嗜血杆菌和铜绿假单胞菌支气管扩张患者(19),流感嗜血杆菌中性粒细胞哮喘患者(20.),而莫拉克斯氏菌属复活在慢性阻塞性肺病患者21]。这些病原体的存在和丰富很大程度上被视为唯一的微生物气道疾病的决定因素。然而,除了这些病原体,降低气道的慢性肺部疾病患者也遭到更大的殖民微生物群,包括许多细菌类群不被认为是直接导致发病机理(12,14,22- - - - - -24]。
这种广泛的呼吸道微生物群与不同疾病的构成特点,严重程度和患者年龄(25- - - - - -27]。然而,微生物群成员的潜在影响疾病通过中介或调节炎性外部诱因的影响,包括呼吸道病原体,是知之甚少28- - - - - -30.]。
我们提出,肺部微生物群包含细菌和免疫调节活动调节免疫激活的净含量主要呼吸道病原体,如铜绿假单胞菌。因此,我们评估了肺部微生物群的免疫调节效应的几个成员经常报道出现在CF下呼吸道样本(21,31日,32]。这些物种代表认可病原体(金黄色葡萄球菌),较少恢复病原体(无色菌xylosoxidans和链球菌anginosus)和上呼吸道共生体广泛认为是不致病的在这种情况下(罗氏菌属mucilaginosa和Gemella haemolysans)。后者包括革兰氏阳性球菌r . mucilaginosa常见的口腔共生体,经常发现在肺部慢性肺部疾病患者的23,33- - - - - -36新陈代谢,已被证明是活跃和适应环境CF肺37]。我们发现r . mucilaginosa展品抗炎活性在体外。我们随后在动物模型上验证我们的发现一群患者的肺部炎症和中性气道疾病。最后,我们确定了主机通路r . mucilaginosa干扰发挥其抗炎作用。
方法
细菌种类和培养条件
六个细菌物种(表1)一般隔绝CF肺被选在这项研究中,包括两个病原体(铜绿假单胞菌和金黄色葡萄球菌),两个频率恢复病原体(美国anginosus和答:xylosoxidans)和两个细菌通常不认为是病原体(r . mucilaginosa和g . haemolysans)。选择性的媒体对这些物种之前开发的(38,39]。我们还包括额外的选择实验罗思氏菌属物种,例如罗氏菌属dentocariosa,罗氏菌属土,罗氏菌属amarae和罗氏菌属aeria。所有隔离在37°C在不断震动条件下培养(250 rpm)在脑心浸液肉汤(实验室M、埋葬、英国),直到固定相。大多数隔离在有氧条件下,除了培养美国anginosus和g . haemolysans在microaerobic培养条件(< 1%2)(Oxoid CampyGen紧凑;美国马热费希尔科学、沃尔瑟姆)。
三维肺上皮细胞培养模型
A549细胞株
以前开发的organotypic三维(3 d)细胞培养模型被用来研究对炎性刺激免疫反应(40- - - - - -43]。3 d在活的有机体内如肺上皮细胞培养模型系统反映家长组织的关键方面,包括3 d建筑,屏障功能,apical-basolateral极性和多细胞复杂性(40,42]。它已被证明铜绿假单胞菌附着力,以及host-secreted细胞因子资料,在三维细胞培养模型的肺上皮细胞更相似在活的有机体内比细胞生长情况单层塑料(41]。三维模型的人类肺腺癌肺泡上皮细胞系A549 (ccl写明ATCC - 185)生成GTSF-2中(美国UT HyClone, Logan)补充了1.5 g·L−1碳酸氢钠(Sigma-Aldrich,圣路易斯,密苏里州,美国),10%胎牛血清(的边后卫)(美国生活技术,卡尔斯巴德,CA), 2.5毫克·L−1胰岛素转铁蛋白亚硒酸钠(Lonza、巴塞尔、瑞士)和1%青霉素和链霉素(生命技术)在37°C下5%的股份有限公司2。3 d A549细胞被培养为11 - 14天,被转移到48-well盘子2.5×10的浓度5每口井的细胞含有新鲜血清GTSF-2介质当天感染。
IB-3和S9细胞系
前面提到的三维细胞培养模型优化使用IB-3和S9细胞系(44]。IB-3细胞系是支气管上皮细胞系的异构F508del (F508del / W1282X)。的S9细胞系来源于IB-3细胞系,并与野生型稳定转导CF跨膜电导调节器(雌性生殖道)。LHC-8介质没有庆大霉素(生命技术)补充5%的边后卫和1%青霉素和链霉素用于文化两个细胞系。IB-3的3 d模型和S9的3 d A549细胞生成的所述模型,除了一个细胞:使用珠4:1的比例(2:1的3 d A549模型)。
在体外感染的研究
之前感染,细菌培养是离心机和resuspended宿主细胞在无血清培养基。细胞被感染了单一细菌培养4 h在感染复数(MOI) 10:1,除非另有指示。此外,细胞被感染铜绿假单胞菌与每一个CF肺部微生物群成员在10:1比例为4 h,导致20:1的莫伊。时表示,3 d细胞总量受到其他炎性刺激,即:金黄色葡萄球菌(MOI 10:1),脂多糖(LPS)(µg·100毫升−1)(Sigma-Aldrich),鼠李糖脂(100µg·毫升−1)(Sigma-Aldrich)和H2O2(1毫米),一起r . mucilaginosa4 h。长期实验,3 d细胞总量受到µg·100毫升−1有限合伙人单独或结合r . mucilaginosa24 h的莫伊1:1。对颗粒的上层清液的实验r . mucilaginosa,文化是离心机和0.22μm宠物过滤膜过滤(美国通用电气医疗集团,芝加哥,IL)。获得细胞溶解细胞悬液,r . mucilaginosa文化受到冷/热循环两次(即。5分钟冰之后5分钟在85°C)。细胞溶解细胞的生存能力被镀在营养琼脂,检查确认没有可耕种的细菌。3 d A549细胞暴露4 h铜绿假单胞菌PAO1 (MOI 10:1)有或没有r . mucilaginosa上层清液(100µL浮在表面的游离和150µL GTSF-2细胞培养基的边后卫),细胞溶解细胞(100µL细胞溶解细胞悬液最初包含2.5×106细胞,相当于10:1的莫伊和150年µL细胞培养基)或活细胞如前所述(MOI 10:1)。
细胞毒性检测
在感染后3 d细胞的各种细菌或接触其他炎性刺激(有限合伙人,鼠李糖脂和H2O2),细胞生存能力评估使用膜联蛋白V / propidium碘(技术)和乳酸脱氢酶(Sigma-Aldrich)化验,根据制造商的指示。
细菌细胞的依从性分析
确定细菌粘附到宿主细胞如前所述[42]。以前开发的有选择性的媒体被宿主细胞co-exposed时使用铜绿假单胞菌和r . mucilaginosa,即。Luria-Bertani琼脂补充1.25毫克·毫升−1三氯生选择为铜绿假单胞菌和营养琼脂补充5 mg·毫升−1莫匹罗星和10 mg·毫升−1硫酸粘菌素选择r . mucilaginosa(38]。
评价interleukin-8退化
重组白介素8 (IL)标准(美国BioLegend,圣地亚哥,CA) 125 pg·毫升的浓度−1被添加到r . mucilaginosa文化GTSF-2介质没有血清(5×107CFU·毫升−1对应的莫伊10:1)或控制媒体。引发浓度测量0后,15、30、60和90分钟用ELISA中所描述的部分炎性指标量化。
在活的有机体内小鼠模型
12个月大的雌性BALB / c小鼠ByJRj (Janvier实验室、Le Genest-Saint-Isle、法国)管理按照欧洲指令所提供的实验动物保健(指令2010/63 /欧盟的欧洲议会)。实验动物伦理委员会大学的安特卫普(比利时安特卫普)授权和批准所有动物实验研究(文件2019 - 90)。气管内的管理r . mucilaginosa嵌入在海藻酸珠子在有限合伙人的存在与否是通过使用一个协议所描述的M奥泽等。(45),适应中描述补充材料。嵌入细菌藻酸盐技术发达保留足够的微生物负载在肺部一段时间没有免疫抑制(46]。在初步实验中使用r . mucilaginosa细胞悬液气管内的管理,无法取得一致的殖民统治(补充材料)。此外,对于r . mucilaginosa海藻酸,该方法用于准备珠子移除细菌团> 0.25毫米,从而限制阻止老鼠的航空公司的风险。因此,嵌入的r . mucilaginosa在海藻酸珠子用于所有实验。的准备r . mucilaginosa含海藻酸珠子,三个独立的文化汇集。老鼠灌输每50 10µgµL有限合伙人有或没有r . mucilaginosa(r . mucilaginosaDSM20746或CF隔离r . mucilaginosaB03V1S1C最大剂量,可以得到海藻酸的珠子,即。∼1×105每小鼠CFU)嵌入在海藻酸珠子48 h。小鼠观察在这48 h毛皮质量,姿势,活动和呼吸道症状,体重每24 h。老鼠被颈椎脱位48 h感染后实施安乐死。左肺单一化,用于测定微生物负载(通过平板计数)以及细胞因子量化。脾脏和内侧叶肝脏的收集和单一化检查灌输细菌的传播(通过平板计数)。正确的肺收集1毫升4% PFA进行组织学分析。组织学分析部分通过苏木精和伊红染色进行盲目和得分如前所述使用evo FL汽车显微镜(技术)47]。
量化的罗思氏菌属物种在呼吸道样本
存档,诱导痰液样本来自85名成年人确诊支气管扩张和历史的两个或两个以上的感染性急性加重(基于需求与细菌感染有关补充全身抗生素治疗)前,招募的祝福随机对照试验(48]。病人群的信息(包括包含/排除标准和痰诱导过程)的提供补充的方法。这项研究是通过母亲健康服务(南布里斯班,澳大利亚)人类研究伦理委员会和知情同意是获得所有的参与者。诱导痰液收集在基线,任何干预之前,所有患者痰中性粒细胞数量≥70%(占总痰细胞)。所有患者有慢性下呼吸道感染。的相对丰度罗思氏菌属物种在79年测量的85个样本使用16 s rRNA基因扩增子测序(49和详细补充的方法。序列数据是可得到的在国家生物技术信息中心序列读取档案加入SRA128000数量。r . mucilaginosa绝对丰度是衡量定量PCR (qPCR)在82年的85个样本使用微生物DNA qPCR测定试剂盒r . mucilaginosa(BPID00297A;试剂盒、希尔登,德国)。基因拷贝数测定标准曲线进行比较,如前所述[50]。
炎性指标量化
为在体外实验中,引发分泌测定细胞培养上清液中人类引发ELISA马克斯标准试验(BioLegend)。为在活的有机体内动物实验中,巨噬细胞炎性蛋白(MIP) 2分泌被MIP-2鼠标以肺匀浆酶联免疫试剂盒(LabNed Amstelveen,荷兰)。所有其他的细胞因子在体外细胞培养和在活的有机体内动物实验被Bioplex量化多路复用化验(Bio-Rad、大力神、钙、美国)。炎症标记物测定支气管扩张患者的痰液用ELISA(美国BD生物科学,圣何塞,CA)引发和IL-1β和使用磁Luminex性能分析多路复用设备(研发系统,明尼阿波利斯,美国)为基质金属蛋白酶(MMP) 1, MMP-8和MMP-9如前面所描述的51]。
定量反向transcriptase-PCR
3 d A549细胞被感染铜绿假单胞菌PAO1或组合铜绿假单胞菌PAO1和r . mucilaginosaDSM20746如前所述。感染后4 h、3 d A549细胞被洗了三次与汉克的平衡盐溶液和RNAprotect试剂(试剂盒)补充道。细胞总RNA提取使用金总RNA迷你包(Bio-Rad)和反向转录成cDNA使用iScript先进互补脱氧核糖核酸合成装备(Bio-Rad)。不同基因的表达参与炎症是量化使用“细菌感染在正常航空公司”PrimePCR面板(Bio-Rad)和SsoAdvanced SYBR绿色supermix (Bio-Rad)。qPCR实验进行Bio-Rad CFX96实时系统C1000热循环。真沸点,GAPDH和HPRT1被用作参考基因。基因的表达水平不足被排除在进一步分析。
分析NF-κB激活
一个3 d的上皮细胞模型NF-κB-luciferase-transfected A549细胞(BPS生物科学、圣地亚哥、钙、美国)开发3 d A549的描述模型。细胞暴露4 h单一或培养铜绿假单胞菌和r . mucilaginosa(或其浮在表面的游离)如前所述。同样,筛选NF-κB激活的有限合伙人(100µg·毫升−1)有或没有36代表五个不同的隔离罗思氏菌属物种(表1)执行。当表示,的影响罗思氏菌属物种(r . mucilaginosaDSM20146,r . dentocariosaHVOC18-02,r . aeriaHVOC13-01和r .土HVOC29-01) NF-κB途径激活的有限合伙人(100µg·毫升−1)是评价microaerobic条件下(3%啊2,5%的公司2和92% N2)在BACTROX-2缺氧室(替代高能激光实验室,科尼利厄斯,美国)。一步荧光素酶检测系统(BPS生物科学)是用来量化NF-κB通路激活和发光测量的设想光度计(美国PerkinElmer沃尔瑟姆,MA)。
免疫印迹分析
免疫印迹实验完成了如前所述[52]。鼠单克隆抗体,在浓度推荐的制造商,被用来检测表达A20(美国圣克鲁斯生物技术、达拉斯、TX), NF-κB p65(圣克鲁斯生物技术)和磷酸化(p) -IκBα(细胞信号技术,丹弗斯、马、美国)和一只山羊多克隆抗体被用来检测IκBα(圣克鲁斯生物技术)。作为anti-mouse二级抗体,免疫球蛋白辣根过氧化物酶(合)抗体与抗体(圣克鲁斯生物技术)或免疫球蛋白HRP-linked抗体(圣克鲁斯生物技术)使用。
统计分析
所有在体外实验进行了至少在生物一式三份(n≥3)。在体外感染实验包含两个技术复制的可行性评估,量化的CFU电镀和细胞因子的量化。动物实验、MIP-2 CFU、疾病症状的动物,殖民和传播为两个独立的实验测定r . mucilaginosaDSM20746。的验证在活的有机体内数据与另一个r . mucilaginosa应变(B03V1S1C)和其他细胞因子的量化以及组织学分析菌株的做了一个实验。
统计分析了使用SPSS 24.0版(美国、IBM、纽约Armonk)。Shapiro-Wilk测试用于评估数据的常态。对于正态分布数据,差异意味着评估通过独立样本t检验和方差分析Dunnett的紧随其后事后分析。非正态的分布式数据进一步分析了克鲁斯卡尔-沃利斯非参数检验或Mann-Whitney测试。假设统计学意义,p < 0.05。之间的相关性分析,罗思氏菌属物种丰度(相对或绝对)和细胞因子/ MMP的浓度,皮尔逊相关系数和假定值是由测试(r)的参数分布或枪兵的测试(r年代)非参数分布。
结果
r . mucilaginosa抑制促炎细胞因子的生产由肺上皮细胞在体外
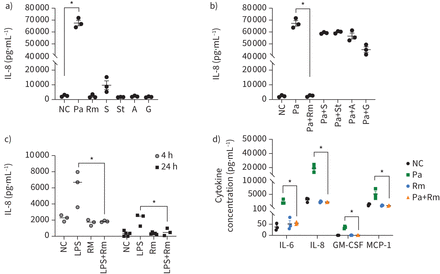
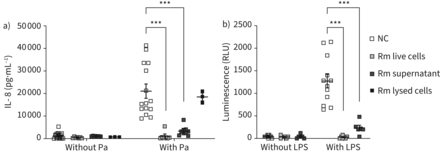
暴露的在活的有机体内式3 d肺泡上皮细胞模型铜绿假单胞菌PAO1 (MOI 30:1的)诱导高引发生产,而低或中度引发生产接触之后金黄色葡萄球菌SP123,美国anginosusLMG14696,答:xylosoxidansLMG26680,g . haemolysansLMG18984和罗氏菌属mucilaginosaDSM20746 (图1一个)。当3 d A549细胞被co-exposed铜绿假单胞菌五其他细菌物种之一,r . mucilaginosa完全废除了铜绿假单胞菌,诱导引发响应(图1 b)。r . mucilaginosa还降低了曝光引发反应引起的铜绿假单胞菌的莫伊100:1和10:1 (补充图S1a)。的影响r . mucilaginosaDSM20746上铜绿假单胞菌全身引发生产确认另外两株r . mucilaginosa(写明ATCC 49042和CF痰隔离B03V1S1C) (补充图印地)。这三个r . mucilaginosa压力也减少了由各种引发反应铜绿假单胞菌CF痰隔离(补充图印地)。减少引发反应r . mucilaginosa确认使用有限合伙人(100µg·毫升−1)作为炎性刺激,对短期(4 h)和长期(24小时)接触(图1 c)。在实验条件下测试,同样数量的r . mucilaginosa观察菌落之间最初的培养液(0 h)和总菌落与宿主细胞,存在于周围的液体在4和24 h,表明细菌仍然可行的在整个实验(补充图1 c)。总共4 h后,略有增加r . mucilaginosa观察菌落与培养液(补充图就是S1c)。
三维(3 d)肺上皮反应促炎症刺激的存在和没有肺部微生物群的成员:铜绿假单胞菌PAO1 (Pa),罗氏菌属mucilaginosaDSM20746 (Rm),金黄色葡萄球菌SP123 (S),链球菌anginosusLMG14696(圣),无色菌xylosoxidansLMG26680 (A)和Gemella haemolysansLMG18984 (G), a, b)白介素8 (IL)生产4 h后由3 d A549细胞接触)单一细菌培养或b)培养各种肺部微生物群成员铜绿假单胞菌PAO1的莫伊30:1。由3 d c)引发生产4或24 h后A549细胞暴露于μg·100毫升−1脂多糖(LPS)单独或与培养r . mucilaginosa在莫伊10:1 (4 h)或1:1(24小时)。d) il - 6、引发、集落刺激因子(gm - csf)和单核细胞化学引诱物蛋白(MCP) 1生产的3 d 4 h后A549细胞接触铜绿假单胞菌单独或在培养r . mucilaginosa莫伊的10:1。NC:负控制(未受感染的3 d上皮细胞在无血清培养基)。数据代表的意思是±扫描电镜或者是说,n≥3。*:p < 0.05;* *:p < 0.001。
r . mucilaginosa也显著降低引发水平提升的革兰氏阳性病原体金黄色葡萄球菌(MOI 10:1) 3 d A549细胞(补充图S1d)。的抗炎作用r . mucilaginosa被确认的3 d模型CF支气管上皮细胞(IB-3细胞株)和在雌性生殖道纠正控制(S9细胞株)(补充图S1e和f)。
此外,r . mucilaginosa降低水平的其他铜绿假单胞菌全身的促炎细胞因子(il - 6、引发、集落刺激因子(gm - csf)和单核细胞化学引诱物蛋白(MCP) (1) (图1 d)。暴露在铜绿假单胞菌,r . mucilaginosa或组合显示正常形态基于微观分析和细胞保留> 80%感染后的生存能力(补充图S2)。
r . mucilaginosa一个降低了LPS-induced炎性反应在活的有机体内小鼠模型
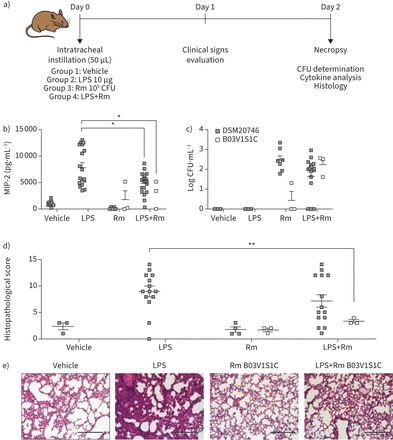
接下来,我们评估了在活的有机体内抗炎效果r . mucilaginosa通过测量小鼠肺部炎症细胞因子水平有限合伙人滴注法或有限合伙人r . mucilaginosa(无论是DSM20746和B03V1S1C菌株)一氧化碳暴露(图2一个)。一氧化碳暴露后48 h, LPS-induced MIP-2(人类引发的同系物)降低了40%应变DSM20746 (图2 b)。结果被验证使用另一个r . mucilaginosa应变(B03V1S1C),这表明减少LPS-induced MIP-2产量的70% (图2 b)。,il - 6水平的其他细胞因子(MCP-1 IL-1α,IL-5, il - 10和gm - csf)也显著降低小鼠暴露于有限合伙人r . mucilaginosa独自B03V1S1C相比,有限合伙人(补充图S3)。的肺r . mucilaginosa来华的老鼠包含同样数量的细菌(CFU·毫升−1)的存在和缺乏有限合伙人(图2 c)。未发现细菌在肝脏和脾脏,暗示没有传播,和老鼠显示整体正常毛皮质量、姿势、体重和在所有测试条件下无呼吸道症状。苏木精/ eosin-stained LPS-instilled小鼠的肺部分显示更明显的肺组织损伤与部分老鼠co-exposed有限合伙人和r . mucilaginosaB03V1S1C,同样的趋势r . mucilaginosaDSM20746观察(图2 d和e)。
的影响罗氏菌属mucilaginosa(Rm)在活的有机体内对脂多糖(LPS)。时间轴的动物感染和验尸,b)巨噬细胞炎性蛋白浓度(MIP) 2 (ELISA),和c) CFU·毫升数−1小鼠肺匀浆后48小时暴露在汽车(n = 7),有限合伙人(n = 18),r . mucilaginosa暂停(n = 9r . mucilaginosaDSM20746和n = 3r . mucilaginosaB03V1S1C)或有限合伙人+的组合r . mucilaginosa(n = 18r . mucilaginosaDSM20746和n = 3r . mucilaginosaB03V1S1C)。d)肺组织病理学评分的苏木精/ eosin-stained部分肺。e)肺苏木精/ eosin-stained部分车辆,有限合伙人,r . mucilaginosaB03V1S1C和有限合伙人+r . mucilaginosaB03V1S1C灌输老鼠。酒吧规模:200μm。车辆:无菌藻朊酸盐珠;有限合伙人:10每50μLμg。从两个独立的动物实验数据提出了应变应变B03V1S1C DSM20746和一个实验。数据代表的意思是±扫描电镜n≥3。*:p < 0.05;* *:p < 0.01。
罗思氏菌属物种在上皮细胞抑制NF-κB激活
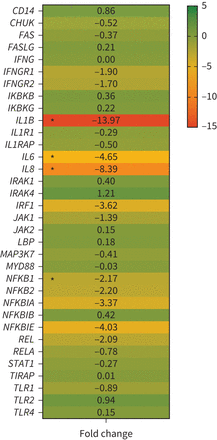
破译的行动方式r . mucilaginosa基因的表达,是主要的炎性通路的一部分在3 d A549细胞暴露评估铜绿假单胞菌或co-exposed铜绿假单胞菌和r . mucilaginosa。r . mucilaginosa一氧化碳暴露显著表达下调基因的表达编码引发(IL8)、il - 6 (白细胞介素6)和pro-IL-1β(IL1B)(图3)引起的铜绿假单胞菌。此外,r . mucilaginosa大幅下调NFKB1表达式(图3)。的监管NFKBIA,NFKBIE和REL基因表现出下降的趋势,进一步指示的作用r . mucilaginosaNF-κB通路。
差于炎症相关基因的表达三维(3 d) A549肺泡上皮细胞接触铜绿假单胞菌和铜绿假单胞菌结合罗氏菌属mucilaginosa。定量PCR分析显示平均折mRNA水平变化3 d A549细胞的刺激铜绿假单胞菌PAO1与的培养铜绿假单胞菌和r . mucilaginosa。n = 3。*:具有统计学意义(p < 0.05)褶皱变化。
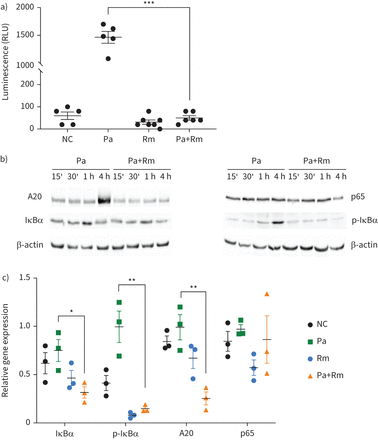
的影响r . mucilaginosaNF-κB通路的激活在NF-κB-luciferase记者证实3 d A549细胞模型,显示显著减少NF-κB培养活动r . mucilaginosa与铜绿假单胞菌相比之下,铜绿假单胞菌单曝光(图4一)。NF-κB通路的抑制r . mucilaginosa还显示使用有限合伙人作为观察炎性刺激和36隔离代表五个不同罗思氏菌属物种从临床和环境来源(补充图S4a和b)。不同的抗炎效果罗思氏菌属物种NF-κB途径激活microaerobic条件下有限合伙人也观察到(补充图自己),它可以被微生物遇到粘液的慢性肺部疾病的患者,如CF (53]。的最小有效剂量r . mucilaginosa抑制铜绿假单胞菌全身炎症的莫伊至少对所有剂量的5:1铜绿假单胞菌测试(MOI 100:1) (补充图S5a)。我们还测试了更高的剂量r . mucilaginosa(MOI 100:1和大展身手的地方)和抗炎效果确认(补充图S5b)。
的影响罗氏菌属mucilaginosa(Rm) NF-κB途径激活铜绿假单胞菌(Pa)。NF-κB通路的激活测量通过发光的三维(3 d) NF-κB记者A549细胞。3 d细胞暴露4 h铜绿假单胞菌PAO1单独或在培养r . mucilaginosaDSM20746。b)半定量的测定(通过免疫印迹)的蛋白质(即。样子,IκBαp65和磷酸化(p) -IκBα)由3 d A549细胞产生刺激铜绿假单胞菌PAO1有或没有r . mucilaginosaDSM20746 15分钟(15′),30分钟(30′),1 h和4 h。c)带强度的免疫印迹(正常化β-actin) 4 h 3 d A549细胞的刺激铜绿假单胞菌PAO1有或没有r . mucilaginosaDSM20746。RLU:相对光单位;NC:负控制(未受感染的3 d NF-κB记者A549细胞在无血清GTSF-2介质)。数据代表的意思是±扫描电镜,n = 3。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
我们随后进行免疫印迹分析调查阶段r . mucilaginosa影响NF-κB信号。后4 h共培养铜绿假单胞菌和r . mucilaginosa,r . mucilaginosa预防铜绿假单胞菌全身IκBα磷酸化(图4 b和c)。这表明r . mucilaginosa影响NF-κB上游信号或IκBα激酶水平的复杂(IKK)。符合这一点,IκBα和表达A20的表达两个NF-κB目标基因,大大降低了培养样本(图4 c)。
最后,我们排除了退化引发或抑制铜绿假单胞菌粘附到3 d A549上皮细胞r . mucilaginosa作为替代的解释观察到的抗炎效果(补充图S6)。
r . mucilaginosa上层清液能抑制引发生产和NF-κB通路激活炎性刺激3 d肺上皮细胞
曝光的3 d A549细胞铜绿假单胞菌PAO1 (MOI 10:1)的存在r . mucilaginosa浮在表面的游离,但不是细胞溶解细胞,引发强烈降低生产(图5一个)。我们确认r . mucilaginosaDSM20746浮在表面的游离完全废除LPS-stimulated NF-κB途径激活(图5 b)。
的抗炎作用罗氏菌属mucilaginosa(Rm)是由其浮在表面的游离。一)白介素8 (IL)生产三维(3 d)接触后A549上皮细胞铜绿假单胞菌PAO1 (Pa) 4 h,有或没有r . mucilaginosaDSM20746活细胞,细胞溶解细胞或浮在表面的游离。b)的量化NF-κB途径激活4 h后暴露在脂多糖(LPS)(μg·100毫升−1)有或没有r . mucilaginosaDSM20746浮在表面的游离。在所有实验感染的多重性是10:1。RLU:相对光单位;NC:消极的控制(未受感染的3 d上皮细胞)。数据代表的意思是±扫描电镜n≥3。* * *:p < 0.001。
气道炎症和逆关系罗思氏菌属物种中性气道疾病患者
两种文化无关的方法被应用于测量罗思氏菌属物种支气管扩张患者诱导痰液样本中,一种中性气道疾病。第一种方法(测量r . mucilaginosa绝对负荷)表示r . mucilaginosa引发负载水平显著负相关(图6)和IL-1β(图6 b),以及与金属蛋白酶- 1 (图6 c)和MMP-8 (图6 d)。之间没有明显的相关性r . mucilaginosa和MMP-9 (图6 e)或痰中性粒细胞百分比(图6 f)。在第二个方法中,我们确定的相对丰度罗思氏菌属和发现它还具有负相关性与水平的引发,IL-1β,金属蛋白酶- 1和MMP-8。之间的相关性罗思氏菌属相对丰度和MMP-9也是重要的。又没有相关性罗思氏菌属丰富和中性粒细胞百分比(补充图S7)。
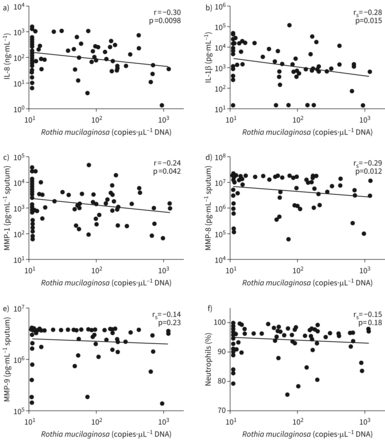
绝对负荷的相关性罗氏菌属mucilaginosa与促炎症诱导支气管扩张患者的痰样本参数:a)白介素8 (IL), b) IL-1β,c)基质金属蛋白酶(MMP) 1 d) MMP-8 e) MMP-9和f)中性粒细胞。数据点代表个人诱导痰液样本。相关系数和假定值计算排名当枪兵的测试使用(r值年代)。
讨论
我们报告常见肺癌属于属的微生物群的成员罗思氏菌属发挥抗炎作用在体外和至少一个(r . mucilaginosa这个效果也是明显的在活的有机体内。被经常口腔微生物群的一部分,很少引起肺部感染(54,55),r . mucilaginosa通常被认为是唾液污染的一部分样本较低的航空公司。然而,比较的口腔微生物组的肺微生物表明r . mucilaginosa不是一个污染物(37,56,57]。核心肺部微生物群落个人间变化罗思氏菌属检测到物种在COPD和哮喘病人,在儿科和成人患者CF (23,33,35,36,58),同时降低航空公司的健康个体(59]。然而,很少有人知道它的作用在慢性肺疾病(24,60]。
细菌的存在下呼吸道慢性肺部疾病病理生理学(通常被认为是作为一个因素13- - - - - -15]。结果在目前的研究强烈建议的存在r . mucilaginosa在航空公司是有益的,因为它不仅抑制生产铜绿假单胞菌全身的促炎细胞因子,它还显示引发反应的抑制作用引起的有限合伙人的另一个重要呼吸道病原体,金黄色葡萄球菌。抗炎效应被确认为一个大的集合罗思氏菌属物种和microaerobic条件下也被观察到。自罗思氏菌属物种是兼性厌氧菌,它很可能与低氧水平,这些微生物将殖民壁龛中发现慢性肺部疾病患者的肺粘液53]。然而,的最小剂量罗思氏菌属需要获得抗炎效果吗在体外所有剂量的铜绿假单胞菌测试,表明存在剂量依赖的相关性的影响。最常使用的剂量在我们的研究(MOI 10:1)是合理的慢性肺部疾病的患者,因为作为一个模型总细菌莫伊∼100:1已经报道了CF患者(61年),的相对丰度罗思氏菌属变化在1%和40%之间(62年,63年]。也在保佑队列,在我们的研究中,分析了均值的相对丰度罗思氏菌属为9%,支持使用的生理剂量的相关性。然而,我们也不能排除,在某种程度上,高负载罗思氏菌属可能导致净促炎效应在肺的环境中,不管其抗炎作用。高剂量的r . mucilaginosa(MOI大展身手的地方)仍然发挥抗炎作用在体外;因此,进一步的研究是需要评估的负载罗思氏菌属可以容忍的在活的有机体内不会造成不良影响。
r . mucilaginosa也能够减少LPS-triggered生产促炎细胞因子在小鼠肺匀浆,使用海藻酸珠模型。一些细胞因子的水平在老鼠暴露在空海藻酸珠子类似LPS-treated老鼠,在协议的一项研究报告在小鼠的肺部炎症反应与无菌藻朊酸盐珠滴剂后64年]。尽管如此,r . mucilaginosa引起的肺组织炎症反应明显衰退的刺激和抗炎效应的应变程度相关的。
有趣的是,先前的研究显示的相对丰度之间的负相关罗思氏菌属物种和痰中性粒细胞弹性蛋白酶等炎症标记物,引发和IL-1βCF患者(65年,66年]。最近的一份报告发现的相对丰度属罗思氏菌属在咯血痰积极预测患者的肺功能的CF (67年]。不仅我们能确认之间的负相关罗思氏菌属物种和炎症的祝福群的相对丰度水平,但我们也表明的绝对丰度r . mucilaginosa与炎症标记物负相关(基于引发和IL-1β水平)和介质的气道重构(金属蛋白酶- 1和MMP-8水平)。金属蛋白酶- 1的水平,MMP-8 MMP-9,降解细胞外基质蛋白(68年),增加患者的气道中性气道疾病,具有负相关性与肺功能(51),导致不可逆的气道损伤(68年]。我们没有找到之间的关联罗思氏菌属和中性粒细胞数量。这可能是由于相对较低的水平的变化之间的中性粒细胞百分比(≥70%)的患者。的评估罗思氏菌属丰度在其他群中性气道疾病需要确认可能的抗炎效果罗思氏菌属物种的病人和确定的程度这可能损害结构肺部疾病的进展。
虽然一些研究大量的增加有关罗思氏菌属与积极的健康结果,它最近被证明的相对丰度罗思氏菌属物种是在一群高一系列慢性肺部疾病患者(严重的哮喘,慢性阻塞性肺病、支气管扩张)69年),在结核病患者与健康人相比70年]。还有待决定是否增加罗思氏菌属相对丰度也意味着绝对的微生物负载的实际变化的物种或仅仅是反映了一种减少大量的其他物种(更占主导地位)。然而,研究H昂等。(70年)表明,r . mucilaginosa可以作为一个锚物种结核分枝杆菌和其他20个类群。可能是代谢槽可以改变其他的同现肺环境中致病或不致病的物种。为r . mucilaginosa,这是证明其代谢产品槽铜绿假单胞菌(71年]。虽然我们没有观察到r . mucilaginosa全身的增长铜绿假单胞菌在我们的研究中,长期的种间相互作用是值得探索进一步评估是否共餐的种类等r . mucilaginosa可能会影响整体社区组成,除了发挥抗炎活性。此外,是否改变罗思氏菌属丰富的描述和现在的研究是一个司机疾病/疾病标记或肺生理的改变的结果(如。由于改变气道间隙或微分的活性氧水平,促炎细胞因子或黏蛋白)仍然是一个问题完全解决。在动物身上获得的数据表明,补充罗思氏菌属在肺部可能减少对外部刺激做出的促炎症反应,进一步探索之间的因果关系罗思氏菌属丰富和炎症的病人是必要的。
的发现罗思氏菌属作为抗炎属肺微生物群引发了一个问题,是否其他非病原的同桌的呼吸道,特别是来自口腔,可能有免疫调节特性。最近的研究在动物72年]或在体外(73年支持这一假设。例如,肺吸入口腔人类共生的(普氏菌melaninogenica,韦永氏球菌属parvula和链球菌)在小鼠体内诱导辅助细胞类型17炎性表型,减少敏感性链球菌引起的肺炎。我们的数据对细胞因子的生产和NF-κB激活说明r . mucilaginosa防止NF-κB信号,可能在IKK激活。事实上,引发IL-1β,白介素和肿瘤坏死factor-α通过绑定其分子由NF-κB模式toll样受体(通常)[74年]。这是特别感兴趣的,因为NF-κB通路介导高架先天免疫反应在慢性肺部疾病患者75年- - - - - -84年]。浮在表面的游离表现出抗炎活性,表明r . mucilaginosa分泌(一)抗炎介质(s),直接妨碍了NF-κB通路或诱发主机解决炎症介质。因为抗炎活动观察使用纯TLR4配体有限合伙人以及不同微生物物种促炎症触发,我们可以排除的抗菌活性r . mucilaginosa造成的效果。研究确定免疫调节中介(s)将需要进一步的了解罗思氏菌属物种调节炎性反应。
理解的贡献可能有益的物种净炎症可以使我们能够更好的理解疾病严重程度的变化和慢性肺部疾病患者之间的进展。前瞻性研究来评估的临床效用r . mucilaginosa气道炎症的标志,在多大程度上它可能提供一个依据小说发展的治疗干预措施,现在需要。
补充材料
可共享的PDF
确认
我们谢谢凯瑟琳·格林(呼吸医学,皇家外科学院在爱尔兰,都柏林,爱尔兰)提供CF细胞系,马修Parsek(西雅图华盛顿大学微生物部门,佤邦,美国),Boo曾(生命科学学院,内华达大学拉斯维加斯,拉斯维加斯,NV,美国)提供铜绿假单胞菌CF127,琼娜Doci(药品微生物实验室,根特大学,根特,比利时)寻求帮助的实验。
脚注
作者的贡献:a .克拉布概念化的研究。克拉布,c . Rigauts和t . Coenye负责总体研究设计。郎j . Aizawa, c . Rigauts m . Govaerts和l . Ostyn进行动物实验。S.L.泰勒和s·西姆斯进行DNA测序,qPCR实验和数据分析。c . Rigauts和l . Ostyn执行在体外实验,c . Rigauts分析数据。l .毛刺和J.L.辛普森负责临床抽样。G.B.罗杰斯,p Cos, y Dondelinger, m . Sze l . Vereecke a . Bragonzi c . Cigana h . Van涡流和大肠Vandeplassche试验装置提供了重要的指导,分析和/或解释的结果。c . Rigauts a . Willems M.M. Tunney, G.B.罗杰斯和S.L.泰勒分离菌株用于这项研究。c . Rigauts a·克拉布G.B.罗杰斯S.L.郎泰勒和j . Aizawa写的手稿。t . Coenye p Cos M.M. Tunney, a . Willems y Dondelinger, l . Vereecke和c Cigana修订后的手稿。
利益冲突:c . Rigauts声明一个专利申请相关工作。
郎的利益冲突:j . Aizawa没有披露。
利益冲突:S.L.泰勒没有披露。
利益冲突:G.B.罗杰斯没有披露。
利益冲突:m . Govaerts没有披露。
利益冲突:p Cos没有披露。
利益冲突:l . Ostyn没有披露。
利益冲突:美国西姆斯没有透露。
利益冲突:大肠Vandeplassche没有披露。
利益冲突:m .施鹏翔没有披露。
利益冲突:y Dondelinger没有披露。
利益冲突:l . Vereecke没有披露。
利益冲突:h . Van Acker没有披露。
利益冲突:J.L.辛普森没有披露。
利益冲突:l .毛刺没有披露。
利益冲突:a . Willems没有披露。
利益冲突:M.M. Tunney没有披露。
利益冲突:c . Cigana没有披露。
利益冲突:a . Bragonzi没有披露。
利益冲突:t Coenye声明一个专利申请相关工作。
利益冲突:a .克拉布声明一个专利申请相关工作。
支持声明:这项工作是由研究基金会资助的弗兰德斯(FWO)。c . Rigauts是收件人的FWO-Strategic基础研究(某人)奖学金(1 s23117n)。a·克拉布是一个接受者的FWO奥德修斯格兰特(G.0.E53.14N), a和p Cos, t . Coenye和克拉布收到一封FWO科研补助金(G010119N)。郎j . Aizawa收到了来自欧盟的资助下地平线2020研究和创新计划玛丽Skłodowska-Curie格兰特(722467印救财团)。G.B.罗杰斯是由马修·弗林德斯研究奖学金和NHMRC高级研究奖学金。y Dondelinger支持的博士后奖学金FWO (12 t9118n)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2021年5月5日。
- 接受2021年9月10日。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org