摘要
伴有哮喘和慢性阻塞性肺疾病(COPD)的患者有沉重的疾病负担。
使用欧洲共同体呼吸健康调查前瞻性收集的数据,我们比较了哮喘+COPD (n=179)、既往(n=263)或当前(n=808)单独哮喘、单独COPD (n=111)或两者均无(n=3477)的中年受试者从成年早期到60多岁的危险因素、临床病史和肺功能轨迹。
访谈数据及支气管扩张前1 s用力呼气量(FEV)1)、用力肺活量(FVC)分别于1991-1993年、1999-2002年和2010-2013年进行3次临床检查。根据存在固定气流阻塞(支气管扩张剂后FEV),在2010-2013年进行疾病状态分类,受试者年龄40-68岁1/FVC低于正常下限),终生哮喘史和累积暴露于烟草或职业性吸入剂。评估了这些表型的既往肺功能轨迹、临床特征和危险因素。
哮喘+COPD患者报告母亲吸烟(28.2%)和儿童呼吸道感染(19.1%)的频率高于单独COPD患者(分别为20.9%和14.0%)。哮喘+慢性阻塞性肺病患者在20岁时肺功能受损,并持续到成年期,其中一半以上的人在儿童时期就患有哮喘。COPD患者终生暴露于吸烟和职业性吸入剂的风险最高,并且在成年期肺功能衰退加速。
与单独的COPD相比,哮喘和COPD的共存似乎有更早的起源。这些发现表明,预防这种在老年人中很常见的严重疾病应该从童年开始。
摘要
哮喘和慢性阻塞性肺病的共存通常在老年人中诊断出来。尽管如此,预防这种情况应该从童年开始。作为优先事项,应鼓励产妇和个人避免吸烟。https://bit.ly/3uQCmIX
介绍
哮喘和慢性阻塞性肺疾病(COPD)是普通人群中常见的慢性呼吸道疾病。区分这些疾病是有问题的,特别是在老年人中[1]。事实上,一些哮喘患者,特别是吸烟者,在老年时发展为固定气流阻塞和慢性阻塞性肺病[2]。一些COPD患者表现出哮喘患者常见的临床特征,如气道高反应性(AHR)、支气管扩张剂反应性(BDR)、血液和气道嗜酸性粒细胞增加[3.],尽管这些患者患哮喘的几率较低。
1995年,美国胸科学会(ATS)指南提出了非比例维恩图来描述慢性支气管炎、肺气肿和哮喘的重叠[4],后来的研究量化了重叠的扩展[5]。越来越多的共识认为,广泛使用的标签“哮喘-慢性阻塞性肺病重叠”包含异质性表型,而不是单独的疾病实体[6- - - - - -10]。2020年更新的全球慢性阻塞性肺疾病倡议(GOLD)指南不再使用哮喘- COPD重叠标签,全球哮喘倡议(GINA)指南将其替换为“哮喘+COPD”。2,3.]。
由于近几十年来哮喘发病率呈上升趋势[11以及全球预期寿命的增加,使得哮喘患者的年龄有所上升[1],同时患有哮喘和慢性阻塞性肺病的患者的临床表现一直在增加。根据最近的一项荟萃分析,尽管各研究之间存在很大的异质性,但哮喘+COPD的全球患病率估计为2.0%,而哮喘和COPD的相应数据分别为6.2%和4.9% [12]。哮喘+COPD患者的诊断和临床管理具有挑战性,因为对于如何定义这种疾病尚无共识[13],大多数关于治疗的证据都是从单独患有这两种疾病的患者的试验中推断出来的[7]。
了解哮喘+COPD的危险因素和临床特征在生命中何时发生,有助于确定易感窗期,从而更有效地预防[10]。另一个重要的问题是与这些表型相关的肺功能轨迹是否不同[7]。虽然临床指南指出,与单独患有COPD相比,哮喘+COPD患者的肺功能衰退加速[3.],但最近的一些研究对这一假设提出了质疑[14- - - - - -20.]。
鉴于上述知识差距,我们在欧洲共同体呼吸健康调查(ECRHS)第三波参与者中对40-68岁的单独哮喘、单独COPD和哮喘+COPD受试者进行了分类。我们估计了这些表型在20-68岁年龄段的危险因素、临床特征和肺功能轨迹。
方法
研究人群
该调查是一项国际队列研究,对象为1991-1993年入组时年龄在20-44岁的一般人群[21]。在ECRHS I中,从邮政筛查(第一阶段)的参与者中随机抽取20%的样本参加临床评估(第二阶段),并为有呼吸道症状的受试者提供丰富的样本。第二阶段的参加者于1999-2002年在ECRHS II再次接受调查[22]和2010-2013年的ECRHS III [23],中位随访时间分别为9年(4-12年)和20年(18-23年)。每个中心都获得了伦理批准,并获得了参与者的书面知情同意。
临床数据
每次检查时,受试者接受标准化访谈和支气管扩张剂前肺活量测定(附录E1).1 s内最大用力呼气量(FEV)1),用力肺活量(FVC)可重复至150 mL [24]。测定屋尘螨、草、猫变应原的血清总IgE和特异性IgE水平。在ECRHSⅰ和ⅱ中,进行了甲胆碱激发试验[25]。在ECRHS III时,使用200µg沙丁胺醇(2次,每次剂量100µg)进行支气管扩张剂后肺活量测定,并呼气一氧化氮(F伊诺)用电化学分析仪(NIOX - MINO;Aerocrine AB, Solna, Sweden),呼气流速为50 mL·s−1[26]。
定义
我们将哮喘的终生史定义为在ECRHSⅰ、ⅱ和/或ⅲ时自我报告的哮喘;或有AHR合并哮喘样症状,或在ECRHS I和/或II使用吸入或口服呼吸系统药物(补充表E1).我们重建了终身职业暴露于蒸汽,气体,粉尘或烟雾所描述的附录E1[27]。我们确定了以下gold定义的关键指标,以考虑在ecrs III中诊断COPD [3.1)基于任何时间点累积数据的终生暴露史(吸烟≥10包年或低强度职业性物质暴露≥5年);2) ecrs III的主要症状(慢性咳嗽、慢性产痰、剧烈活动后呼吸困难或呼吸短促);3)生命早期危险因素(5岁前呼吸道感染或父母患有慢性支气管炎、肺气肿或COPD)。
疾病分类
在最后一次检查(ECRHS III)中,当使用支气管扩张剂后的肺功能测量可用时,我们将受试者分为五个相互排斥的组(补充图E1).根据ECRHS III测量的数据(肺功能数据、症状)或累积/过去数据(暴露史、哮喘史、生命早期呼吸道感染),在ECRHS III时满足构成疾病定义的所有标准。疾病组分为:1)哮喘+COPD,定义为支气管扩张剂后FEV1/FVC<正常下限(LLN) [28+至少一项gold定义的COPD指标(终生暴露史、关键症状和/或早期生命危险因素)+终生哮喘史或明显的BDR (FEV增加)1>12%和>400 mL) [2];2)单纯COPD,定义为支气管扩张剂后FEV1/FVC
我们排除了18例支气管扩张剂后FEV患者1/FVC
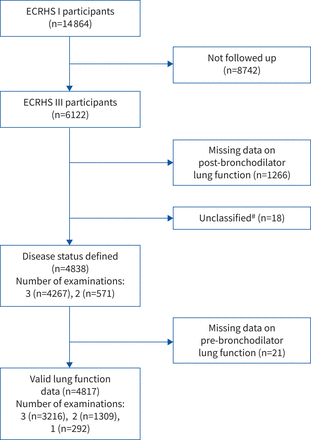
研究流程图。#支气管扩张剂后用力呼气量小于1 s/用力肺活量<欧洲共同体呼吸健康调查III正常下限,不能归类为任何疾病组(无慢性阻塞性肺疾病全球倡议定义指标,无哮喘史)的受试者。
统计分析
对于在ECRHS III中被划分为疾病组的受试者(年龄40-68岁),我们用mean±来描述特征的分布sd,中位数(Q1-Q3)或数字(%),并酌情使用Kruskal-Wallis或卡方/精确检验检验各组间的总体差异。然后,我们估计了这些表型的成人生活轨迹,从ECRHS I的最小年龄为20岁到ECRHS III的最大年龄为68岁。我们对所有三个时间点可用的指标进行建模,包括两个风险因素(暴露于主动或被动吸烟的比例),两个自我报告的结果(报告呼吸困难(曾经有过呼吸困难)的比例)或医学检查(在过去12个月内见过全科医生/专家),补充表E2));三个肺功能结果(平均FEV)1(L)、FVC (L)和% FEV1/ FVC)。我们使用广义估计方程与泊松结果分布和对数链接函数的二进制结果,或高斯结果分布和恒等链接函数的定量结果。该模型包括一个稳健方差估计器和以下自变量:性别、年龄、疾病状态、疾病status×age(相互作用项)、ECRHS样本(随机)与呼吸计类型(仅用于肺功能结果)和身高(仅用于FEV)1和FVC)。年龄2还有疾病status×age2如果它们改善了模型拟合(α=0.10),也会依次进行测试,并包括考虑轨迹中的非线性。我们设置了非结构化的主题内相关性来解释重复测量。我们按列表方式删除了调整变量的缺失数据。每个受试者都提供了任何时间点的可用信息。我们使用STATA软件,release 16.1 (StataCorp, College Station, TX, USA)。
敏感性分析
我们还估计了肺功能轨迹:1)模拟FEV1预测FVC %;2)仅考虑具有三项有效肺功能测量的受试者;3)排除支气管扩张剂后FEV受试者后1/FVC>LLN结合FEV1或FVC< ECRHS III的LLN,这是保存比率受损肺活量(PRISm)的指标(总肺活量和剩余肺活量的测量不可用)。此外,我们在应用基于GOLD持续梗阻(FEV)固定截止的疾病定义后重复了分析1/ FVC < 0.70) (附录E1).
结果
共有14 864、9251及6122名来自23个中心(补充表E3).ECRHSⅰ与ⅱ、ECRHSⅱ与ⅲ的中位时间间隔分别为8.8年(范围4.3 ~ 11.7年)和11.5年(范围8.5 ~ 15.6年)。与ECRHS I的参与者相比,在ECRHS III随访的受试者在基线时的平均年龄为34.3岁与33.6岁),受教育程度较低的可能性较小(12.4%)与15.8%),目前吸烟的可能性较低(20.5%)与23.4%), FEV较高1(99.6%与98.8%预测)补充表E4).4838人的疾病状态按ECRHS III分类(图1),其中4267人参加了所有三项检查,3216人在三个时间点进行了有效的肺功能测量。与更大样本的ECRHS III参与者相比,被分配到疾病组的受试者具有相似的特征(补充表E4).有295名受试者出现支气管扩张剂后FEV1/ FVC < LLN;其中,290例患者至少满足一项gold定义的COPD指标(补充表E5),其中5例仅为既往哮喘(n=1)或当前哮喘(n=4)。有哮喘史的1248例受试者,其中1045例在ECRHSⅰ、ⅱ和/或ⅲ期报告曾患哮喘。
参与者疾病分类特征(ECRHS III)
在ECRHS III中,哮喘+COPD组的女性比例与参照组相似(~ 50%),介于COPD(42.3%)和过去/当前哮喘(bbb60 %)之间(表1).低教育水平在哮喘+COPD组中更为常见。肥胖在单独患有哮喘(31.9%)和哮喘+COPD(27.7%)的受试者中比单独患有COPD(18.9%)的受试者更常见。哮喘+COPD患者的体力活动量与单独患有哮喘的患者相同(约43%),比COPD组(30.6%)更活跃。在不吸烟的,F伊诺哮喘+慢性阻塞性肺病患者的水平最高,而在吸烟者中,有哮喘病史的人的水平最高。哮喘+COPD患者中有177例(98.9%)报告有哮喘史。哮喘+COPD患者报告儿童期哮喘发作的可能性(53.4%)高于过去或目前仅患有哮喘的患者(分别为41.2%和38.4%),报告晚期哮喘发作的可能性较低(10.8%)与分别为12.1%和16.8%)。哮喘样症状和gold定义的关键COPD症状在哮喘+COPD受试者中比在单独COPD受试者中更常见。与单独COPD或对照受试者相比,哮喘表型受试者的过敏结局更常见,而哮喘+COPD组的血清总IgE水平最高。呼吸问题在哮喘+COPD患者中最常见。在ECRHS III中,哮喘+COPD患者报告使用吸入或口服呼吸药物的可能性(72.9%)高于当前哮喘(61.2%)或单独COPD(10.8%)的患者,但在其他检查(补充表E6).
参与者的童年和终身特征
哮喘+COPD患者最常报告母亲在儿童期吸烟(28.2%),其次是既往哮喘和当前哮喘(表2).哮喘+COPD受试者的父母在儿童期患有哮喘(25.3%)或呼吸道感染(19.1%)的可能性更高,父母患有COPD的可能性(28.7%)低于单独患有COPD的受试者(分别为20.8%、14.0%和34.3%)。哮喘+COPD患者的终身累积吸烟或职业性吸入物暴露低于单纯COPD患者。哮喘+COPD患者最可能有AHR病史(89.6%)和高血清总IgE(73.3%)。
成年生活轨迹
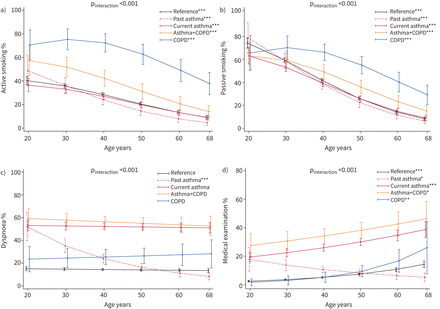
在哮喘+慢性阻塞性肺病组中,20岁至68岁的终身主动吸烟患病率介于慢性阻塞性肺病组和其他低暴露组之间(图2一个).我们估计,除慢性阻塞性肺病外,所有组的吸烟者比例都呈单调的年龄相关下降,在30岁左右达到最大,然后下降。在成年早期接触被动吸烟的受试者比例在疾病组之间相似(60-70%),然后遵循与老年主动吸烟相似的轨迹(图2 b).
报告a)主动吸烟,b)被动吸烟,c)呼吸困难或d)在过去12个月内被医生看过的受试者比例的预测轨迹作为疾病组和年龄的函数。提供数据的受试者数=4838。p交互由Wald检验获得(零假设:真实轨迹不随疾病组而变化)。垂直线代表95%的置信区间。定量/指标自变量设为等于所包括的一组受试者计算的平均值/比例。p值用于检验疾病组中与年龄相关的趋势的显著性(零假设:真实比例在各个年龄段都是恒定的)。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
随着年龄的增长,呼吸困难的患病率没有统计学意义上的显著变化,除了单纯有哮喘病史的受试者的患病率有所下降,这与他们在ECRHS III (图2 c).除既往哮喘患者外,所有组患者在过去12个月内接受医生诊治的比例均呈年龄相关增长,在仅患有慢性阻塞性肺病的组中,这一比例在50岁后变得更为陡峭。图2 d).
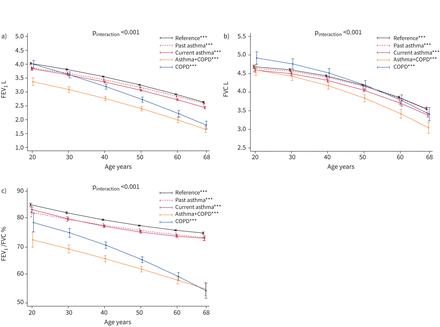
患有哮喘+慢性阻塞性肺病的受试者在年轻时肺功能较低,这种情况会持续到他们的成年生活。补充表E6和图3).他们的原始FEV1下降速度仅略快于当前哮喘单独组和参考组,而FEV的下降速度更快1%预测(补充图E3a);生植被(图3 b),预测FVC % (补充图E3b)和FEV1/ FVC (图3 c)的速度也加快了。
预测平均支气管扩张剂前1 s用力呼气量(FEV)的轨迹1), b)用力肺活量(FVC)和c) FEV1/FVC比值与疾病组和年龄的关系。提供数据的受试者数=4831 (FEV)1), 4822 (FVC)和4816 (FEV)1/ FVC)。p交互由Wald检验获得(零假设:真实轨迹不随疾病组而变化)。垂直线代表95%的置信区间。肺量计类型设置为NDD EasyOne;定量/指标自变量设为等于所包括的一组受试者计算的平均值/比例。***:疾病组中年龄相关趋势的显著性检验p<0.001(零假设:真实平均值在各个年龄之间是恒定的)。
我们观察到最快的FEV速率1慢性阻塞性肺病患者(图3一和补充图E3a).他们FEV1/FVC在成年早期介于哮喘+COPD组和其他组之间,但随后急剧下降,并在生命的第七个十年达到哮喘+COPD组的低水平(图3 c).
讨论
使用从人群样本中前瞻性收集的超过20年的数据,我们发现40-68岁同时患有哮喘和COPD的受试者在儿童期更有可能报告母亲吸烟和呼吸道感染,但与单独患有COPD的受试者相比,在成年期更不可能暴露于吸烟和职业性吸入剂。估计FEV过去的轨迹1FVC和FEV1/FVC比值表明,成年早期肺功能低下更常见于晚年同时患有哮喘和慢性阻塞性肺病的受试者,而不是单纯患有慢性阻塞性肺病的受试者。然而,肺功能急剧下降在随后被单独诊断为COPD的成年人中更为常见。我们假设早期生活风险因素在哮喘+COPD的发展中具有更突出的作用,而成年生活中的暴露可能是不具有哮喘特征的COPD发展的更强的风险因素。
疾病分类和社会人口统计学
在疾病分类时,我们研究的所有参与者年龄均≥40岁,在这个年龄,哮喘和COPD之间的重叠通常开始被视为潜在的诊断[8]。与哮喘+COPD的受试者数量相比,单独患有COPD的受试者数量相对较少,这可能是因为ECRHS III的年龄范围仍包括一小部分老年人,但也可能是因为ECRHS的设计,哮喘患者的比例过高[21]。哮喘+COPD组中女性的比例(49.7%)高于单纯COPD组(42.3%),这在一些研究中很常见[15,18,29,30.],这与欧洲女性患成人哮喘的风险较高以及男性吸烟的风险较高是一致的[31]。
至少有一个gold定义的COPD指标是哮喘+COPD和单独COPD的纳入标准[3.]。然而,四名受试者支气管扩张剂后FEV1/FVC 终生有哮喘史或明显的BDR (FEV升高)1>12%和>400 mL)是哮喘+COPD的附加纳入标准,但仅为COPD的排除标准[9,32]。尽管如此,10.2%的COPD患者单独出现BDR (FEV增加)1200-400 mL),而哮喘+COPD为24.3%。几乎所有哮喘+COPD患者都有哮喘史(98.9%),这意味着只有少数持续性气流阻塞患者仅根据明显的BDR归为这一组。明显的BDR与哮喘+COPD的诊断相关性较低,因为它不常见[33,34],它不能可靠地区分COPD伴哮喘和不伴哮喘[7],因为包括BDR在内的定义并不会随着时间的推移而稳定[19]。
哮喘+COPD疾病分型的临床特点
哮喘+COPD患者的哮喘样症状患病率(86.4%)和慢性咳嗽/产痰(35.8%)与单独患有哮喘的患者相似或更高(分别为89.2%和26.4%)。他们也更有可能报告去急诊室或住院,而且他们更频繁地使用呼吸系统药物。然而,哮喘+COPD受试者的体力活动与单独患有哮喘的个体一样,这表明他们的日常活动受到轻微损害。支气管炎症高度的支气管炎症,如F伊诺水平,可能与哮喘+COPD受试者的过度疾病负担有关[35,36]。高F伊诺水平是2型炎症的一个有用的标志,用于哮喘诊断、表型和监测,并有助于预测谁将从吸入皮质类固醇治疗中受益[37],但它们在COPD和哮喘+COPD中的临床意义尚不清楚。
哮喘+COPD的早期生命起源
在成年早期,哮喘+COPD患者有气流阻塞(低FEV)1/FVC比和低FEV1)及小肺活量(FVC) [38],这可以用几种可能同时发生的致病机制来解释,包括肺生长异常和生命早期损伤[39]。这些研究对象报告说,母亲吸烟和儿童时期呼吸道感染的频率最高,这两个公认的危险因素会导致肺生长减慢和肺功能下降[38,40,41]。哮喘+COPD患者的受教育程度较低[9,29,42],这表明社会经济剥夺可能是另一个不利因素[41]。超过一半的哮喘+COPD患者,哮喘始于儿童时期,这可能导致成年后出现不可逆的气流阻塞[40,43]。B用户界面et al。[20.报道称,7岁时肺功能低下是45岁时同时患有哮喘和慢性阻塞性肺病的一个重要危险因素。
成年生活轨迹
单独COPD的受试者FEV速率最快1和FEV1/FVC下降,他们报告说,50岁以后的体检急剧增加,这可能表明,与其他群体相比,他们的健康状况随着年龄的增长而加速恶化。哮喘+COPD患者FEV下降1和FEV1/FVC介于COPD和其他疾病组之间。总的来说,这些发现可以用单独患有COPD的组中吸入污染物的暴露水平较高来解释。我们观察到,由于控烟政策的成功实施,所有组别的主动吸烟和被动吸烟人数均因年龄而减少[31,44],与其他组相比,单独患有COPD的受试者大约晚了一个生命十年。
哮喘+COPD患者的肺功能下降可以通过长期抗炎治疗得到缓解。该组3人中有2人有过敏致敏史或总IgE高,持续吸入皮质类固醇治疗对特应性哮喘更有效[45,46]。几乎90%的哮喘+COPD患者有AHR病史,我们之前认为AHR与青年期肺功能低下有关,但随后FEV正常1mL·年下降−1[47]。
伴和不伴哮喘的COPD患者肺功能下降
FEV的发现1与大多数文献一致,单纯COPD患者比哮喘+COPD患者下降更快[14- - - - - -20.],但有两种例外情况可能与不同疾病定义的异质性有关(补充表E9) [30.,34]。l安吉等。[30.发现FEV变慢了1与单纯COPD相比,早发性哮喘(年龄<40岁)+COPD患者的下降速度更快,但晚发性哮喘+COPD患者的下降速度更快[30.]。在我们的研究中,90%的哮喘+COPD(慢性阻塞性肺病)患者在40岁之前发病。表1).与我们的研究不同,L安吉等。[30.]在哮喘+COPD的定义中没有考虑吸烟史,而BDR(吸入特布他林后>200 mL)是单独COPD的排除标准。Tkacova等。[34报告了更快的FEV1与无AHR的COPD患者相比,COPD合并AHR患者的死亡率下降。AHR可能与气道结构改变有关,正如作者所承认的,其作为共存哮喘标志的相关性值得争论[34]。
优势与局限
收集记忆信息对临床医生来说是一项挑战[19]。我们研究的一个优势是有详细的过去病史和风险因素暴露的信息,从20年前的个人报告中前瞻性地收集,这似乎减少了回忆偏差。缺乏关于早期生活因素的客观信息是一个局限性,因为这些暴露是在20-44岁时自我报告的(ECRHS I)。我们在ECRHS III的样本来自先前波的自我选择参与者,代表性不足的年轻人,吸烟者和受教育程度较低或基线时肺功能较低的受试者。我们使用自我报告的哮喘而不是更准确的临床诊断来进行疾病分类,尽管与单独的COPD相比,哮喘表型中更高水平的支气管炎症和特应性间接支持了我们定义的有效性。另一个限制是,我们没有血液或痰中嗜酸性粒细胞计数的数据,也没有支气管扩张剂后重复肺活量测定的数据,这些数据可以改善疾病分类[33],我们也没有室外空气污染暴露的数据,这是一个与COPD发病率相关的因素,证据仍然不确定[48,49]。
结论
哮喘和慢性阻塞性肺病的共存似乎是一种起源于生命早期的严重哮喘,而不是单纯的慢性阻塞性肺病,后者与成人接触更多。在我们的研究中,哮喘+慢性阻塞性肺病患者的呼吸道感染、母亲吸烟和儿童哮喘的患病率更高,年龄更小时肺功能受损。这些发现表明,预防这种在老年人中很常见的疾病应该从童年开始,甚至可能更早。50]。在劝阻产妇吸烟、促进儿童免疫接种和防止患有哮喘的年轻人吸烟方面的公共卫生干预措施可能是最有效的。相比之下,不伴有哮喘特征的慢性阻塞性肺病似乎主要与成年期有毒吸入物暴露有关。避免接触(如。通过戒烟和减少职业环境中的污染暴露)可能特别有利于防止“纯COPD”表型的发展,尽管它也可能减少从哮喘到哮喘+COPD的转变。在我们的研究中,单独COPD似乎比哮喘+COPD进展更快。尽管如此,哮喘+COPD患者发生呼吸功能障碍的风险也增加,因为他们的肺功能在早期和进行性损害明显。
补充材料
可共享的PDF
致谢
该研究的负责人是黛博拉·贾维斯。这项研究是在Judith Garcia-Aymerich领导的ALEC工作包4下进行的。原始研究的主要研究者和团队成员报告于附录E2。
脚注
本文的补充资料来自www.qdcxjkg.com
作者贡献:A. Marcon和S. Accordini构思并设计了这项研究。A.马孔起草了分析计划和初稿。F. Locatelli和A. Marcon进行了统计分析。所有作者都参与了分析计划的讨论和结果的解释,并对第一稿草稿进行了评论。所有作者都严格审查并批准了手稿的最终版本。
利益冲突:A.马克龙没有什么可透露的。
利益冲突:F. Locatelli没有什么可透露的。
利益冲突:S.C.损害公司没有什么可透露的。
利益冲突:C. Svanes没有什么可透露的。
利益冲突:J.海因里希没有什么可透露的。
利益冲突:B. Leynaert没有什么可透露的。
利益冲突:P. Burney没有什么可透露的。
利益冲突:A.可口可乐没有什么可透露的。
利益冲突:G.卡利斯坎没有什么可透露的。
利益冲突:卡尔卡诺没有什么可透露的。
利益冲突:吉斯拉森没有什么可透露的。
利益冲突:C.詹森没有什么可透露的。
利益冲突:贾维斯没有什么可透露的。
利益冲突:R. Jõgi获得了爱沙尼亚研究委员会的资助(个人研究补助金第562号),并获得了葛兰素史克、勃林格和诺华的咨询和讲座费用,以及葛兰素史克和勃林格的旅行/住宿/会议费用。
利益冲突:T. Lytras没有什么可透露的。
利益冲突:A. Malinovschi没有什么可透露的。
利益冲突:N. Probst-Hensch没有什么可透露的。
利益冲突:K. Toren没有什么可透露的。
利益冲突:L. Casas没有什么可透露的。
利益冲突:G. Verlato没有什么可透露的。
利益冲突:加西亚-艾默里奇没有什么可透露的。
利益冲突:S. Accordini没有什么可透露的。
支持声明:ALEC研究由欧盟地平线2020研究与创新计划资助,资助协议号为633212。ISGlobal是加泰罗尼亚政府CERCA项目的成员之一。在原始研究中支持数据收集的国家资助者列在附录E2。资助者在研究的设计、数据的收集、分析和解释、手稿的撰写或提交发表的决定中没有任何作用。通讯作者拥有对所有数据的完全访问权,并对是否投稿发表的决定负有最终责任。本文的资助信息已存入交叉基金注册处。
- 收到了2020年12月30日。
- 接受2021年4月6日。
- 版权所有©作者2021。
本版本在知识共享署名非商业许可4.0条款下发布。获取商业转载的权利和许可联系权限在}{ersnet.org