摘要
之前没有蛋白质组学研究集中在肺动脉高压(PAH)的右心室(RV)。本研究研究了PAH患者与右心不适应表型(RHMP)相关的循环蛋白质组学谱。
采用多重免疫分析对121例(发现队列)和76例(验证队列)PAH患者进行了血浆蛋白质组分析。采用偏最小二乘法回归评估蛋白组标记与RHMP之间的关联,该关联由Mayo右心评分(结合右心室品系、纽约心脏协会(NYHA)分类和n端脑利钠肽前体(NT-proBNP))和Stanford评分(右心室收缩末期重塑指数、NYHA分类和NT-proBNP)定义。在肺动脉高压患者和对照组的右心室样本以及肺动脉带带(PAB)小鼠中检测生物标志物的表达。
在两个队列中,高水平的肝细胞生长因子(HGF)、干细胞生长因子-β、神经生长因子和基质衍生因子-1与较差的Mayo和Stanford评分相关,这与肺阻力或压力无关(验证队列有更严重的疾病特征:心脏指数较低和NT-proBNP较高)。在两个队列中,HGF增加了REVEAL评分在预测3年死亡、移植或住院方面的价值。HGF及其受体c-Met的RV表达水平在晚期PAH患者中高于对照组,在PAB小鼠中高于sham。
高血浆HGF水平与RHMP相关,并可预测3年临床恶化。在PAH中,HGF和c-Met RV表达水平均升高。评估血浆HGF水平可确定有心力衰竭风险的患者,这些患者需要更密切的随访和强化治疗。
摘要
高血浆HGF水平与PAH患者的右心适应不良表型和预后相关。HGF和c-Met RV表达均增加。评估血浆HGF水平可确定需要更密切随访和强化治疗的患者。https://bit.ly/3djiy9O
介绍
肺动脉高压(PAH)的特征是进行性闭塞性血管重塑,导致右心后负荷增加。最初,右心室(RV)通过增加其壁厚(适应性表型)进行适应,但PAH的进展通常导致右心室扩大和衰竭(适应性表型)随后死亡或肺移植[1.].这种从适应到不适应RV的转变背后的病理生理学还没有很好地阐明,部分原因是很少有PAH研究工作集中于建立右心适应不良表型(RHMP)的标记。此前对PAH的蛋白质组学研究已经发现了与肺血管疾病严重程度和预后相关的血液谱,包括我们自己的工作,利用非监督机器学习识别具有不同炎症谱的PAH表型,对临床风险进行分层[2.,3.].新出现的证据表明,PAH患者和实验疾病模型中的炎症和RV衰竭之间存在联系[4.,5.,但目前尚无针对右心脏的蛋白质组学筛查研究。
最近的影像学研究已经显著改善了肺动脉高压右心适应性表型,将右心室游离壁纵向应变(RVLS)和收缩末尺寸(如右心室收缩末重塑指数(RVESRI))作为右心室适应性的强超声心动图标志物[6.,7.]这些标记物分别与纽约心脏协会(NYHA)功能分类和N-末端脑钠肽原(NT-proBNP)相结合,以定义RHMP评分:梅奥临床模型(基于RVLS、NYHA分类和NT-proBNP)[6.]和斯坦福模型(RVESRI、NYHA类和NT proBNP)[7.].这些以RV为中心的简单模型的预后价值相当于显示评分[7.],这是一种广泛采用的PAH风险分层工具,需要更广泛的临床数据和有创血流动力学测量。
在这些右心评分的基础上,我们的主要目标是确定PAH中与RHMP相关的新循环蛋白质组学生物标记物。我们假设PAH患者可能表达与RHMP相关的特定血液蛋白质组学特征,与肺部疾病的严重程度无关。此外,我们旨在研究最后,我们试图评估终末期PAH患者和RV压力超负荷实验小鼠模型RV样本中RHMP标记物的组织水平表达,以验证循环水平增加反映RV过度表达的假设,并验证肺动脉条带(PAB)未来机械研究的模型。
材料和方法
研究人群
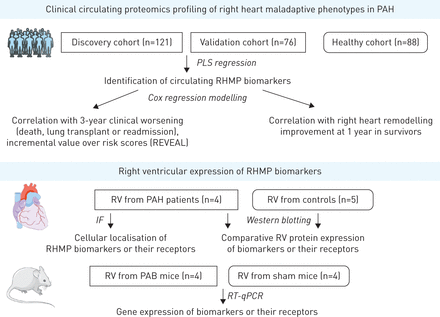
这项前瞻性研究包括2008年至2014年间进入斯坦福大学肺动脉高压生物库(Stanford University Pulmonary Hypertension Biobank, CA, USA)的1组PAH患者,他们在常规超声心动图2周内收集血浆用于蛋白质组分析(图1和补充材料).PAH诊断需要平均肺动脉压(mPAP)≥25 毫米汞柱,肺动脉楔压≤15 毫米汞柱和肺血管阻力(PVR)>240 dyn·s·cm−5..排除标准为慢性感染(7例),原发性免疫缺陷(1例),近期非心衰的急性疾病(1个月内)(8例),先天性系统肺分流(10例),恶性肿瘤(4例),2周内超声心动图缺失(68例)或超声心动图数据欠佳(6例)。研究基线为采血日期。患者被分为发现队列(n=121, 2008-2011)和验证队列(n=76, 2012-2014)。此外,从健康对照组(n=88)中获得血浆,他们经过严格筛选以确定健康。斯坦福大学机构审查委员会(IRB)批准了这项研究(IRB #14083和#20942);所有受试者均提供书面知情同意。
研究设计。肺动脉高压;偏最小二乘;RHMP:右心不适应表型;房车:右心室;如果:免疫荧光;PAB:肺动脉带;RT-qPCR:逆转录酶定量PCR。
血液蛋白质组分析
空腹血样从肘前静脉采集,加工成血浆并按照协议(补充材料).由48种细胞因子、趋化因子和生长因子组成的靶向蛋白质组(表1和补充表E1)采用Bio-Plex多重免疫分析(BioRad, Hercules, CA, USA),这是一种基于Luminex xMAP技术(Austin, TX, USA)的流式细胞仪平台,根据制造商说明(补充材料).每个样品都是一式两份。Luminex 200平板读卡器可以量化每个蛋白质的中位荧光强度(MFI)。所有分析都使用MFI而不是标准曲线推导的绝对浓度,因为MFI不需要检测限截尾,且具有更好的下游统计能力[8.].基于跨试验的内部控制,所有测定的分析物的分析间变异系数<15%。
临床数据收集
使用飞利浦IE 33超声系统(荷兰阿姆斯特丹)进行经胸超声心动图研究。在RV聚焦心尖四腔视图上测量RV尺寸和功能指标,平均三个周期,包括RVESRI(由侧壁与间隔高度比定义)和RVLS,如前所述(补充材料) [7.]这些测量用于计算两个右心适应性表型评分,梅奥临床评分整合RVLS、NYHA等级和NT proBNP,斯坦福评分整合RVSRI、NYHA等级和NT proBNP(补充表E2).幸存者1小时后可获得后续超声心动图 使用相同的方法解释年份。如前所述,治疗后的右心重塑通过基线检查时RVESRI的变化来定义(相对变化<10%时改善,变化>10%时恶化,否则稳定)[7.].
在基线1个月内收集NYHA分级、6分钟步行距离、肺对一氧化碳的扩散能力、肾病患者饮食改良法估计的肾小球滤过率和NT-proBNP水平。纳入后3个月内行右心导管置管,获得血流动力学数据(右心房压、mPAP、肺动脉楔压、PVR和心脏指数)。数据用于计算REVEAL风险评分(补充表E3) [9].
前瞻性随访患者以评估临床恶化的主要终点(即。死亡、肺移植或急性右心衰竭住院)和次要终点(死亡或肺移植)。
人RV样本的病理分析
4例PAH患者的移植心脏的冷冻和石蜡包埋活检(补充表E4在Marie Lannelongue医院接受心肺移植的患者(IRB #18.06.06;Le Plessis-Robinson法国)。为了进行比较,我们从5名没有移植器官(没有石蜡包埋活检)的心脏供体(没有心血管疾病或肺动脉高压(PH))中获得右心室冷冻活检。移植心脏购自INSERM URMS 1148生物样本库(BRIF BB-0033-00029, BBMRI-EU/infrastructure),经法国国家伦理委员会批准(PFS17-002),并在法国研究部宣布(DC-2018-3141)。
在确定临床队列中的RHMP循环生物标记物后,我们1)通过将冷冻RV样品与一级特异性抗体(英国剑桥Abcam)孵育并进行Western blot,比较PAH和对照组中这些蛋白质及其受体的组织水平表达;2)通过免疫荧光染色和共焦显微镜在PAH患者RV组织中定位RHMP生物标记物(蔡司LSM 800显微镜和ZEN软件;卡尔蔡司显微镜,White Plains,NY,USA)(补充材料).
PAB小鼠模型RV分析
所有动物实验均按照国家研究委员会的指导方针进行[10]并经地方当局批准(斯坦福大学实验动物护理管理委员会,方案#27626)。如先前公布的,在10-14周龄的雄性C57BL/6小鼠中诱发慢性RV压力超负荷[11]并在补充材料.麻醉动物进行开胸手术;用6-0线缝合肺动脉(PA);术后1周,超声心动图(GE Vivid 7;General Electric Healthcare, Chicago, IL, USA)。对照组年龄匹配的同窝鼠进行了假手术(PA隔离,不缝合)。5周后用超声心动图测量mPAP、心率和肺动脉瓣速度时间积分,以记录心输出量的减少,并收集右心室样本并快速冷冻。从均质RV样本中分离RNA后,我们应用定量逆转录酶PCR (applied Biosystems, Foster City, CA, USA)测量感兴趣的RHMP蛋白组标记对应的mRNA转录本的表达水平。
统计分析
使用t检验或Mann–Whitney–Wilcoxon检验对连续数据进行比较,使用卡方检验对分类数据进行比较。蛋白质组数据预处理涉及背景荧光减法、平板/批次调整(经验Bayes方法)[12],稳健的分位数归一化,重复平均和年龄、性别和体重指数调整。为了识别RHMP标记,使用“SIMPLS”算法拟合偏最小二乘(PLS)回归模型(补充材料).RHMP标记的选择通过评估1)预测得分的变量重要性和2)回归β系数(使用基于折刀重采样方差估计的系数t检验)。PLS模型适合将蛋白与Mayo和Stanford分数、每个分数的单独成分和肺血流动力学联系起来。在两个队列中,RHMP生物标志物被确定为与RHMP相关的共同生物标志物。研究人员检测了低、中、高危RV表型中的RHMP生物标志物水平(基于Mayo和Stanford评分),将每个风险组与对照组(Kruskal-Wallis和Kruskal-Wallis)进行比较事后Dunn试验)并确认有序PAH组的趋势(Cuzick试验).为了将生物标志物与结果联系起来,通过对数秩统计对四分位数的移植和无住院生存率的Kaplan–Meier估计值进行比较,并拟合Cox比例风险回归模型。循环生物标志物作为连续变量添加。根据每个变量的时间绘制比例Schoenfeld残差图ble,以确保符合比例风险假设。将风险比标准化为预测变量的标准偏差。为了确定每个生物标记物是否增加了用于预测3年结果的既定风险得分的增量值,比较卡方值。使用二元逻辑回归模型确定无论是生物标志物还是右心指标都可以预测1小时的RVESRI改善(相对变化<10%) 2014年纳入的<3岁的患者 使用SPSS(版本19;SPSS,芝加哥,伊利诺伊州,美国)和R(版本3.5.1;R Core Team,维也纳,奥地利)软件程序进行统计分析。
结果
PAH患者RHMP的蛋白质组学分析
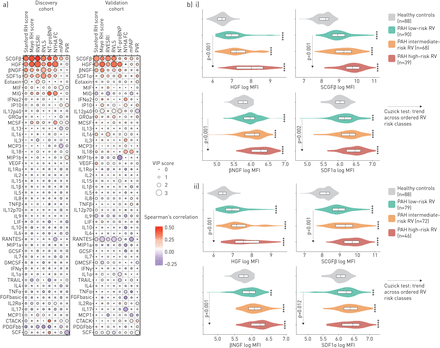
表2总结发现队列的基线特征。高水平的肝细胞生长因子(HGF)、干细胞生长因子(SCGFβ或CLEC11A)、神经生长因子(NGF)和基质细胞衍生因子1(SDF1或CXCL12)与较高风险的梅奥和斯坦福评分、RV功能障碍(RVLS)、RV不良重塑密切相关(RVESRI),与肺部疾病严重程度相比,NT-proBNP更高,NYHA功能分级更差(图2一个;补充表E5和图E1).
a)在两个队列中,每个细胞因子与右心评分和指标的预测变量重要性(VIP)评分和相关性;b)在肺动脉高压(PAH)患者和对照组中,根据右心(RH)适应不良表型的水平,四种标志物的水平。a)使用偏最小二乘回归,我们评估了血浆蛋白质组标记物(使用多重免疫分析)和右心适应不良表型标记物(基于右心室(RV)收缩期末重构指数(RVESRI)的斯坦福RH评分)之间的相关性。纽约心脏协会功能分类(NYHA FC)和n端脑利钠肽前体(NT-proBNP)水平;基于右心室自由壁纵向应变(RVLS)、NYHA FC和NT-proBNP水平的Mayo RH评分;RVESRI;RVLS;中位数水平以上病人;NYHA FC;在121例(发现队列,从2008年到2011年)和76例(验证队列,从2012年到2014年)PAH患者中,平均肺动脉压(mPAP)和肺血管阻力(PVR))。正相关用红色表示,负相关用蓝色表示。 RVLS is presented in absolute value (lowest values indicate worst RV dysfunction). b) Analyte levels of the four strongest biomarkers associated with right heart maladaptive phenotype according to tertiles of the i) Mayo RH score or ii) Stanford RH score in patients with PAH and in the 88 healthy controls. Comparison between each right heart risk category to controls was performed using Dunn's and Kruskal–Wallis test (across-groups among patients with PAH) with事后针对多重测试调整成对比较(Benjamini–Hochberg)。**:p<0.01;***:p<0.001;**:p<0.0001。Cuzick试验的p值用于确认细胞因子水平在有序类别(从低到中到高)中的增加趋势。干细胞生长因子;肝细胞生长因子;神经生长因子;基质细胞衍生因子;巨噬细胞移动抑制因子;干扰素:干扰素;白细胞介素;巨噬细胞集落刺激因子;血管内皮生长因子;肿瘤坏死因子;白血病抑制因子;粒细胞集落刺激因子;GMCSF:粒-巨噬细胞集落刺激因子;TRAIL:肿瘤坏死因子相关凋亡诱导配体;成纤维细胞生长因子;血小板衍生生长因子;干细胞因子。
与发现队列相比,验证队列有更严重的肺部疾病特征,接受背景治疗的患者更少,事件病例发生率更高(表2).结果显示,两个队列中的梅奥和斯坦福风险评分分布相似。高水平的HGF、SCGFβ、NGF和SDF1与较高的梅奥和斯坦福评分、RV功能障碍、较高的NT-proBNP和较差的NYHA功能分级相关(图2一个).在两个队列中,没有发现测量到的细胞因子与有利的右心指标呈正相关。
图2b比较两组低、中、高危RV患者亚组和88名健康对照组(中位年龄58岁,四分位间距(IQR)44-64岁;52.3%为女性)中的四种候选RHMP标记物水平。在患者或对照组中,四种标记物的循环水平并没有因性别而不同(补充图E2).HGF和NGF水平在PAH患者的种族和种族之间没有显著差异(补充图E2),而非西班牙裔白人患者SCGFβ水平低于西班牙裔患者(p<0.01),而SDF1α水平低于西班牙裔和亚洲患者(p=0.04)。
HGF的预后价值
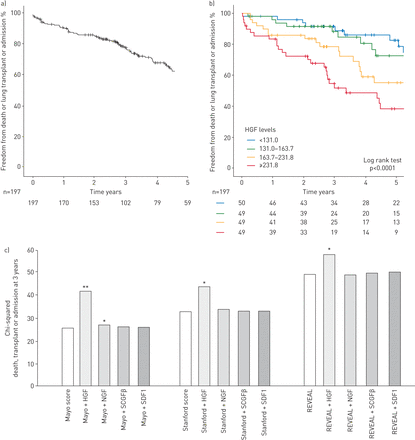
在3.14(2.16-5.44)年的中位随访中,76例患者达到了主要终点(58例住院,10例移植,41例死亡)。无事件生存率(±东南方)主要终点为91±2% 第3年,78±3% 5岁时为62±34% 年头(图3一).49例患者达到了死亡或移植的次要终点。
肝细胞生长因子(HGF)的预后价值及其在预后预测中的风险评分增量值。a)总肺动脉高压(PAH)队列(n=197)的主要联合终点死亡、肺移植或急性右心衰住院的5年Kaplan-Meier生存曲线;b)根据基线时HGF水平的四分之一。c)使用Cox回归方法预测3年肺动脉PAH队列(n=197)主要终点(死亡、移植或右心衰入院)的评分和HGF、神经生长因子(NGF)、干细胞生长因子(SCGF)β和基质细胞来源因子(SDF)1的卡方。使用进入模式将变量输入到模型中。Mayo右心评分是基于纽约心脏协会(NYHA)功能分类、n端脑利钠前肽(NT-proBNP)和右心室纵向张力(RVLS)。斯坦福右心评分基于NYHA分级、NT-proBNP和右心室收缩末重塑指数(RVESRI)。REVEAL评分基于评估早期和长期PAH疾病管理(REVEAL)注册组:低、平均、中等高、高和非常高。*: p < 0.05;* *: p < 0.01。
单变量分析显示,HGF和SCGFβ与主要终点相关(风险比(HR) 1.54, 95% CI 1.24-1.91;P <0.0001, 1.26, 1.12-1.59;p=0.02),而NGF (p=0.83)和SDF1α (p=0.89)则没有。根据HGF (p<0.001)和SCGFβ四分位(p=0.002),主要终点的Kaplan-Meier生存曲线如图所示图3 b和补充图E3.HGF为Mayo、Stanford和REVEAL评分在预测3年主要终点方面增加了显著的增量值(p<0.05;图3 c和补充表E6)HGF和SCGFβ也与死亡或移植的次要终点相关(分别为HR 1.71,95%可信区间1.38-2.12;p<0.0001和1.26,1.01-1.59;p=0.02)。
缺乏心脏纵向重构的生物标志物
在总人口中,174名患者(93.0%的1年幸存者)在1岁时接受了随访超声心动图检查 年(随访研究的中位(IQR)时间为1.03(0.85–1.35)年)。在基线检查和随访期间,37名患者开始使用肠外前列腺素类药物,而55名患者的PH特异性治疗没有改变。无论在基线检查和后续超声心动图检查之间开始何种治疗,基线检查时的四种RHMP生物标记物(使用二元回归分析作为连续变量输入)均未发现与右心重构变化显著相关。同样,基线检查时的斯坦福评分(p=0.50)、梅奥评分(p=0.99)和NT-proBNP(OR 1.85,95%可信区间0.98–3.49;p=0.06)与随访时的右心重塑变化无关。
RHMP生物标记物在人RV组织水平的表达
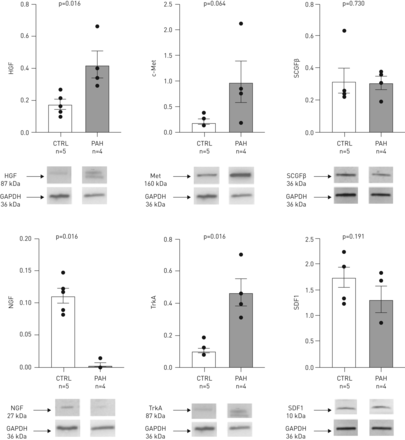
多环芳烃患者RV标本中HGF及其受体c-Met的蛋白水平高于对照组(图4)与对照组相比,PAH患者的NGF水平降低,其受体原肌球蛋白相关受体激酶A(TrkA)增加。在PAH患者中,通过picro-sirius红染色面积百分比评估的RV纤维化水平为11.5%(8.8–15.7%),与PAH病因相似(补充图E4和补充材料).图5和补充图E5显示特发性PAH患者RV样本中四种生物标志物和受体的定位。两例PAH患者(特发性和骨形态发生蛋白受体(BMPR)2突变)表现出定性相似的RV蛋白表达。受体c-Met与心肌细胞、平滑肌细胞、内皮细胞和成纤维细胞标记物共定位点,并在较小程度上与巨噬细胞(图5).HGF呈囊泡状表达,在心肌细胞、平滑肌细胞中表达丰富,在巨噬细胞和成纤维细胞中表达较少。TrkA和NGF均与心肌细胞、平滑肌细胞和巨噬细胞共定位,而TrkA与成纤维细胞共定位,NGF与内皮细胞共定位(补充图E5)SCGFβ存在于心肌细胞、平滑肌细胞和成纤维细胞中,SDF1存在于心肌细胞、平滑肌细胞、内皮细胞和巨噬细胞中。
免疫印迹蛋白质表达的肝细胞生长因子(HGF),其受体c-Met,神经生长因子(神经生长因子)及其受体TrkA,干细胞生长因子(SCGF)β和基质细胞衍生因子(SDF) 1患者的右心室肺动脉高血压(多环芳烃)和控制(CTRL)和量化的信号。每个柱代表平均值±扫描电镜来自四名接受心肺移植的PAH患者和五名对照患者(心脏供体)右心室样本的Western blot裂解物的信号强度,使用t检验进行比较。GAPDH:甘油醛-3-磷酸脱氢酶。
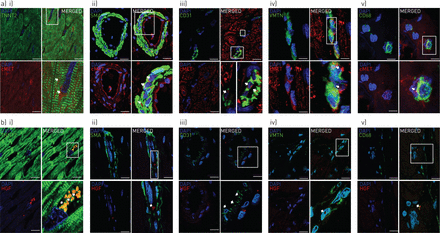
a) c-Met(红色)和b)其配体肝细胞生长因子(HGF;绿色双标记:TNNT2肌钙蛋白(心肌细胞),α-平滑肌肌动蛋白(SMA), CD31(内皮细胞),vimentin (VMTN)(成纤维细胞)或CD68(巨噬细胞)。用二抗培养的细胞无免疫反应,一抗无免疫反应。规模酒吧= 10μm。DAPI: 4 ', 6 ' -diamidino-2-phenylindole。
生长因子右心室表达改变Hgf,c-Met,神经生长因子和Scgfβ在PAB小鼠中
5. 在PAB或假手术后的数周内Hgf,c-Met和神经生长因子显著升高(均p<0.01),而Scgfβ与假药相比,PAB的RV匀浆显著降低(p<0.001),如补充图E6.
讨论
这项靶向蛋白质组学研究确定了与RHMP相关的四种循环细胞因子,它们独立于肺血流动力学的严重程度。HGF作为3年临床恶化的一个强有力的预测因子,增加到REVEAL评分。肺动脉高压患者心肺移植后外植rv中心肌细胞、平滑肌细胞和内皮细胞中c-Met和HGF的蛋白表达增加。PAB小鼠模型进一步证实了RV基因表达增加Hgf和c-Met,这表明PAB是一个有效的模型,可进一步从机理上研究该途径在RV随时间对PH的适应中的作用,并回答HGF表达增加是否代表有益或有害反应的问题;从治疗角度来看,该信息可能有用。该研究的独创性在于其设计(从有监督的床边组学筛查到靶器官和台架分析),这是一种治疗压力超负荷右心的新方法。这种方法使我们能够将血液作为PAH右心衰的窗口,从而确定HGF/c-Met是一种潜在的信号通路。
HGF是一种间充质来源的多效性细胞因子,与酪氨酸激酶受体c-Met结合[13]在实验性心肌梗死和左心肌病模型中,HGF/c-Met信号通路促进血管生成和心肌细胞存活,抑制纤维化[14,15]抑制血管通透性和炎症[16,17].尽管HGF对左心有心脏保护作用,但一些研究矛盾地报告了高循环HGF水平与几种压力超负荷心脏病(高血压和主动脉狭窄)的左心室重构、功能障碍或不良后果之间的关系,还是晚期缺血性左心衰竭[18–20].
关于HGF/c-Met在右心中的分子作用的证据很少。在硬皮病相关性心脏病患者的小队列中有高水平HGF的报道[21]或HGF与mPAP相关的特发性肺动脉高压[22]在另一项针对特发性、家族性或相关PAH患者的研究中,HGF水平与疾病严重程度的任何临床标志物均无相关性[23].我们的研究进一步证明了高血浆HGF水平与肺疾病严重程度以外的RHMP的相关性。包括两个在人口统计学、流行/发病率再分配和功能严重程度方面不同的队列加强了结果,表明识别的生物标志物与跨PAH病因学的RV适应相关。在我们的队列中,高HGF水平与预后密切相关,增加了REVEAL风险评分的增量值,提示HGF/c-Met轴在右心的及时作用。四种RHMP生物标志物中没有一种与1年时右心评分或NT-proBNP水平(已证实的预后标志物)相关,无论开始治疗与否,说明预后标志物和预测治疗反应的标志物之间的区别。未来的研究应该调查生物标志物水平从基线到1年的变化是否与右心重塑的变化相关。
PAH中HGF血浆水平升高的来源仍有待完全阐明,可能是由于HGF的产生增加和/或其系统清除的改变。此前有报道称,在缺氧条件下从人PAH肺中获得的初级内皮细胞表达HGF、SDF1α和其他骨髓激活因子增加[23].在心肌受损的情况下,不能排除心脏对循环高HGF水平的贡献。在本研究中,我们报道了HGF和c-Met蛋白表达增加的肺动脉高压患者终末期右心衰需要心肺移植,跨越肺动脉高压的病因。另一项原始发现是这些标志物在肺动脉高压患者右心室的定位,提示HGF/c-Met的多效作用,正如之前在左心室中证明的[13]与对照组相比,其他标记物在多环芳烃患者RV样本中的表达没有增加,尽管受可用样本数量的限制,这需要进一步研究。
动物模型为循环HGF水平的潜在来源提供了一些见解 据报道,野百合碱诱导的PH值大鼠出现了数周,与肺组织RV mRNA表达增加有关Hgf和c-Met四点钟 周,但不在肝脏,提示血浆HGF来源于心脏而非肝脏[24].我们的PAB模式[11]进一步证明了基因表达的增加Hgf和c-Met在PAB和sham的RV匀浆中(增加了我们人类样本中蛋白表达增加的证据),表明外周血和PAH患者RV中HGF循环水平的增加可能反映了RV中HGF生产的增加。然而,这些数据不能得出以下结论:RV中HGF的增加是否反映了RV适应增加的后负荷的补偿性尝试,或者是否只是一种有害的适应不良反应,进一步使用PAB模型进行研究,对于阐明压力超载的RV中HGF-Met通路的时机和作用具有较高的价值。
HGF作为PAH治疗的潜在有益作用已经被讨论过[25].HGF增加BMPR2的表达[26],一种在PAH家族形式中突变的途径,在非遗传形式中下调,并与PH小动物模型中RV肥大和收缩能力受损相关[27,28].BMPR2的激活有利于PAH和相关的右心室衰竭[29,因此HGF对BMPR2的作用可能构成一种潜在的针对肺动脉高压右心的治疗方法。几种动物模型(例如野百合碱诱导PH的大鼠、分流诱导PH的家兔均显示外源性HGF或Hgf基因转染减少了PH的发展,与SHAM相比,PH与不明显的右心肥大和较低的炎症反应有关[30–33].然而,右心HGF-c-Met轴激活的及时和直接作用尚不清楚。在此,PAB模型可能在探索血浆和组织HGF表达随时间的动态变化和去条带的潜在可逆性方面具有特殊价值[11].
NGF促进心肌细胞存活,是增加心脏交感神经活性的主要神经营养因子[34,35].据报道,PH继发于COPD的患者的肺动脉中NGF的分泌和内皮表达高于无PH的对照组[36]然而,在本研究中,特发性PAH患者的NGF分泌或肺表达没有显著增加。NGF进一步显示在大鼠和人离体肺动脉中诱导对血管收缩剂的高反应性,人肺动脉平滑肌细胞和内皮细胞的增殖和迁移,以及促炎细胞因子IL-1β和TNF-α的分泌[36].抗NGF阻断抗体逆转PH动物模型中的PH,减少肺血管重塑、高反应性和炎症[36]另一项对野百合碱诱导的PH继发RV肥大大鼠的研究报告,NGF的上调与神经元细胞功能的恶化有关[37]在人类中,NGF在终末期左心衰患者中被显示为下调[38,39],这与我们的免疫印迹结果一致,表明心力衰竭中该因子具有时间变异性。
与无PAH的硬皮病患者相比,特发性和硬皮病相关PAH患者的SCGFβ血浆浓度更高[40].据报道,扩张型心肌病和恰加斯病患者循环SCGFβ水平高,与预后无关[41].最后,血浆中SDF1α水平升高,参与肺动脉肌化[42]与健康对照组相比,61例特发性肺动脉高压患者的SDF1α水平与NT-proBNP和RV功能相关[4.].
研究的局限性
本研究的第一个局限性来自于它的单中心设计。事实上,两个队列是在两个不同的时间点收集和分析的,在蛋白质组学分析中排除了批效应的风险,这有助于提高结果的可信度。第二个限制来自于生物标志物分析的横断面性质,这只在基线时可用。还需要进一步的研究来研究循环生物标志物的纵向变化是否可以作为PAH患者治疗反应的预后或预测。第三个限制来自于没有对照的RV石蜡包埋活检,这使我们无法评估PAH中HGF蛋白表达的增加是在所有细胞类型中都存在还是针对一种细胞类型。
总之,高血浆HGF水平与PAH患者的右心适应不良表型相关,并增加了预后预测的显示分数。由于多环芳烃中RV HGF–cMet蛋白和基因表达均增加,该途径值得进一步探索,作为RV特异性治疗靶点。评估血浆HGF水平可以确定PAH患者是否有右心衰风险,以及是否需要进一步随访和加强PAH治疗。
补充材料
可共享PDF
致谢
作者要感谢Andrew Hsi(斯坦福大学,加利福尼亚州斯坦福市)负责斯坦福数据库管理,Lilia Lamrani(玛丽·兰内隆格医院-巴黎南部巴黎萨克莱大学,法国巴黎)帮助收集临床数据,以及Jean-Baptiste Michel(巴黎第七大学,法国巴黎)为了促进控制心脏活检的采购。作者想特别向已故的凯瑟琳·鲁克·马丁(来自巴黎南部巴黎萨克雷大学玛丽·兰内隆格医院)提出一个想法世卫组织为免疫荧光实验和研究设计做出了贡献。作者要感谢斯坦福大学肺动脉高压Vera Moulton Wall中心和斯坦福心血管研究所的资助。
脚注
这篇文章有一篇社论评论:https://doi.org/10.1183/13993003.04506-2020
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:M. Amsallem已获得斯坦福大学Vera Moulton Wall中心2016年青年研究员种子基金、斯坦福大学2019-2020年妇幼健康研究所研究种子基金、Actelion-Janssen研究基金和拜耳演讲费。
利益冲突:a·j·斯韦特没什么可透露的。
利益冲突:J.Arthur Ataam无需披露任何信息。
利益冲突:J.Guihaire没有什么要披露的。
利益冲突:F.Lecerf无需披露任何信息。
利益冲突:兰伯特先生没有什么可披露的。
利益冲突:吉尼亚没有什么可披露的。
利益冲突:M.K.阿里无需披露任何信息。
利益冲突:毛先生没有什么要披露的。
利益冲突:E.Fadel无需披露任何信息。
利益冲突:拉宾诺维奇先生没有什么可透露的。
利益冲突:V.de Jesus Perez没有什么要披露的。
利益冲突:E.Spiekerkoetter由斯坦福心血管研究所、国家心肺血液研究所(NHLBI)和国家卫生研究所(NIH)拨款R01 HL128734和国防部拨款PR161256资助。
利益冲突:O.Mercier得到了法国国家研究机构监督的公共拨款的支持,作为第二个Avenir投资计划(ANR-15-RHUS-0002)的一部分。
利益冲突:F.Haddad获得了Actelion Janssen和飞利浦的研究资助。
利益冲突:扎马尼安没有什么可透露的。
支持声明:这项工作得到了斯坦福妇幼健康研究所(2019-2020种子基金)、国家卫生研究院-国家心脏、肺和血液研究所(职业发展奖,1K23HL15182)、国家研究机构(ANR-15-RHUS-0002基金)的支持以及斯坦福大学Vera Moulton Wall中心(年轻研究员种子基金)。手稿内容完全由作者负责,不一定代表这些资金来源的官方观点。本文的资金信息已存放在交叉参考基金登记处.
- 收到2020年6月20日。
- 认可的2020年10月6日。
- 版权所有©ERS 2021
本文是开放获取的,并根据知识共享188滚球软件署名非商业许可4.0的条款分发。