抽象的
过去几十年儿童哮喘和肥胖的平行流行病刺激了肥胖的研究,作为哮喘的危险因素。然而,关于哮喘在肥胖发病率的作用很少。我们检查了早发哮喘和相关表型是否与发展肥胖的风险有关。
本研究包括从1990年到2008年出生的21个130名儿童在丹麦,法国,德国,希腊,意大利,荷兰,西班牙,瑞典和英国。我们遵循非肥胖的儿童,在3-4岁的情况下进行事件肥胖,长达8岁。医生诊断的哮喘,喘息和过敏性鼻炎可评估高达3-4岁。
具有医师诊断的哮喘的儿童发生的事件肥胖风险高于没有哮喘的患者(调整后危险比(AHR)1.66,95%CI 1.18-2.33)。有活跃的哮喘的儿童(过去12个月的喘息和医师诊断的哮喘)表现出肥胖症的风险更高(AHR 1.98,95%CI 1.31-3.00),而不是没有喘息和哮喘的风险。与从未喘息的人(AHR 1.51,95%CI 1.08-2.09)相比,持续喘息与事件肥胖的风险增加有关。
早发哮喘和喘息可能会增加儿童后期患肥胖症的风险。
抽象的
儿童早期有哮喘或喘息的儿童可能有更高的风险发展为肥胖http://our.ly/hfkw30lhf3x.
介绍
哮喘和肥胖是最重要的儿童慢性疾病之一,近几十年来,这两种疾病在世界范围内的发病率均有平行增长[1.].这些条件的伴随着升高刺激了他们潜在的关系的研究,但哮喘和肥胖发展之间的暂时性尚未确定。这两个障碍都被认为是早期生命中的起源,进一步复杂化这些条件之间对因果关系的评估[2.].虽然有令人信服的证据表明,儿童肥胖会增加哮喘或哮喘样症状的风险[3.–6.,关于早期哮喘是否会引发肥胖发作的证据有限。
两项美国纵向研究考察了哮喘对学龄儿童肥胖发展的潜在影响。第一个研究对象是2171名非肥胖幼儿园和一年级儿童,共10名 多年的随访表明,与那些没有哮喘的儿童相比,被诊断为哮喘的儿童患肥胖症的风险增加了51%[7.].另一方检测了哮喘和肥胖之间的双向关联,在6452名儿童中幼儿园到中学的样本中,观察到哮喘与随后肥胖发病的风险增加有关;然而,肥胖或超重无关与随后的哮喘发作相关[8.]. 一项针对8个欧洲出生队列的汇总研究发现,体重指数(BMI)快速增长的儿童在前2个月出生 年龄在6岁之前发生哮喘的风险较高 年头[6.]但没有欧洲研究已经检查了早期哮喘对事故肥胖的影响。
如果大多数儿童肥胖病例的起源是在学龄前,那么可以合理推测哮喘与肥胖之间的关联也可能在这个关键的时间窗中建立;然而,迄今为止,没有研究评估早期哮喘对儿童肥胖风险的影响。重要的是,以前的研究结果需要在不同的、基于人群的纵向研究中得到重复,不仅检查哮喘,而且检查相关的表型。在这项研究中,我们试图利用来自16个欧洲出生队列的关于早期哮喘和哮喘相关共病的丰富数据,对早期哮喘和相关表型以及随后的肥胖风险之间的潜在关联进行汇总分析。
方法
研究人群
16个欧洲同期出生的发展机制的过敏(MeDALL)联盟和欧洲儿童队列研究策略(chico) FP7协作之下研究资助了哮喘和相关的表型数据在3 - 4岁或更年轻和人体测量信息在3 - 4岁,在任何时候8岁。参与队列包括:ABCD [9],Bamse [10.],DARC [11.],伊甸园[12.],生成r [13.],GINIplus [14., INMA Menorca和Valencia [15.],考拉[16.],LISAplus [14.], MAS [17.], PIAMA [18.],rhea [19.博洛尼亚和罗马[20.]和sws [21.].这些队列的招募期从1990年到2008年。考虑到robic Bologna组和robic Roma组的样本量小和数据收集的相似性,我们将这两个组的数据合并在一起。所有队列都获得了父母或法定监护人的知情同意和当地授权机构审查委员会的道德批准。每项研究都签署一份数据传输协议文件,并将匿名数据集转移到克里特岛大学进行分析。有27117名儿童了解我们的暴露情况和结果。我们排除了5420名儿童,因为在至少2次随访中,他们没有至少一种哮喘或与哮喘相关的表型信息和BMI信息。另外567名儿童被排除在外,因为他们在基线时肥胖,我们的分析剩下2130名儿童。有关参与队列的详细信息见表格1.我们还提供了比较由于数据缺失那些包含在我们的研究中,从我们的分析排除了孩子的母亲和孩子特征的信息(补充表E1).
哮喘及相关表型
参与队列中有关哮喘、哮喘和变应性鼻炎的信息是从国际儿童哮喘和过敏研究(ISAAC)的问卷中获得的,该问卷适用于儿童哮喘和过敏国际研究(ISAAC),并发放给父母[22.].关于哮喘和相关表型数据收集的群体特定信息补充表E2.基线(是/否)在基线(是/否)的存在通过报告在大达3-4岁的任何一定程度的哮喘的医生诊断。基线的喘息(是/否)是基于在3 - 4岁时在胸前的报告喘息或吹口哨。早期喘息(是/否)基于报告过去12个月在婴儿期(0-22岁)的任何时间评估的胸部喘息或吹口哨。基线的过敏性鼻炎(是/否)基于过去12个月在3-4岁时在过去12个月内报告鼻炎(打喷嚏或流鼻涕或鼻子而不是感冒或流感)。哮喘史是基于对基线哮喘和喘息问题的反应,并分类为:1)具有基线哮喘和基线喘息(活性哮喘);2)有基线哮喘,但没有基线喘息;3)没有基线哮喘,但有基线喘息;4)没有基线哮喘,没有基线喘息(参考类别)。基于以前的研究,我们定义了整个童年的明显喘息表型[23.,24.].使用对基线喘息和早期喘息题的响应构建喘息的历史,并分类为:1)具有早期喘息和基线喘息(持续喘息);2)没有早期喘息,但有基线喘息(晚期喘息);3)早熟,但没有基线喘息(短暂的喘息);4)没有早期喘息,没有基线喘息(从不喘息;参考类别)。由于我们缺乏有关IGE致敏的信息,我们基于对基线哮喘和过敏性鼻炎问题的反应创造了一种哮喘和过敏性鼻炎合并症的衡量标准,并分类为:1)具有基线哮喘和过敏性鼻炎;2)具有基线哮喘和过敏性鼻炎;3)没有基线哮喘,没有过敏性鼻炎。我们还创造了哮喘和药物的关节影响的组合衡量标准,分类为:1)是哮喘/是药物使用;2)是哮喘/无药物使用; 3) no asthma/yes medication use; and 4) no asthma/no medication use (reference category).
肥胖
队列根据临床检查,健康记录或父母报告的问卷在3-4岁的情况下提供权重和高度信息,至少在5 - 8岁之间的其他时间点。BMI计算为重量(kg)除以高度(m)平方。由于我们的主要结果是事件肥胖,因此我们将分析视为正常体重或基线超重儿童。肥胖状态是根据2012年美国科尔国际肥胖工作队年龄和性别特定削减[25.].我们还在敏感性分析中使用了2007年世界卫生组织的肥胖临界值[26.,27.].
协变量评估
潜在的协变量在群组中定义如此类似。通过访谈或自我管理的问卷收集有关怀孕期间孕产妇吸烟(是/否),出生(G)和儿童性(男性或女性)的信息,特别的测量,出生记录或医疗登记。我nformation on maternal education (cohort-specific definitions of low, medium or high), any breastfeeding (months), parity (primiparous or multiparous), any dampness or mold in the home at 0–4 years (yes/no), passive smoke (childhood exposure to smoking by others in the household at 0–4 years, yes/no), medication for asthma or breathing problems in the last 12 months at 3–4 years of age (yes/no), parental history of asthma and pets in the home during infancy (0–2 years, yes/no) was obtained通过访谈或自我调查问卷。出生体重随后分为低(<2500 g)、正常(2500 - 3999 g)或高(4000+ g),母乳喂养分为<3个月和≥3个月[28.,29.].体育活动只有16个队列中的三个,因此我们无法将其作为潜在的协变量。有关药物类型的更详细信息,可用于四个队列(BAMSE,DARC,PIAMA和ROBBIC),并定义为3-4岁的吸入皮质类固醇(ICS)的使用(是/否)。
统计分析
我们的主要分析是汇集分析,其中我们将数据与16种不同的队列组合联系起来。为了考虑队列之间的潜在差异,我们为“队列”或“固定效应”介绍了“对队列的固定效果”(即。指示器变量)。因为我们观察到从随机效应得出的估计和固定效应模型之间没有差异,从固定效应模型,我们目前的结果,因为它们更可能提供大样品中的无偏估计[30.].在随访期间,我们使用具有性别特异性基线风险的Cox比例风险模型估算了基线儿童哮喘和相关表型与肥胖发生率之间的调整风险比(aHRs)和95% CIs。我们使用年龄研究访问的时间尺度分析,出现肥胖定义为当孩子第一次成为肥胖在随访中发生(在随访期间的中点之间的访问时不肥胖和随后的访问时评估肥胖)。在随访期间没有变胖的儿童在研究随访结束或失去随访时被删除。调整混杂因素的选择基于有向无环图(dag),由以前的知识提供,并使用DAGitty版本3.0 (补充图E1)[31.].最终模型中包括的混杂因素包括基线年龄、怀孕期间吸烟、被动吸烟、胎次、母亲教育、父母哮喘、母乳喂养和出生体重。除了MAS组和INMA Menorca组的产妇教育和怀孕期间吸烟信息外,所有组都有这些混杂因素的信息。缺失协变量信息的儿童被纳入使用缺失指标法的分析,缺失值作为分类变量的一个额外组。虽然根据我们的DAG,婴儿时期家中的潮湿或霉菌以及家中的宠物是潜在的混杂因素,但对这些协变量的进一步调整并没有显著改变效果估计,因此这些变量没有被纳入最终模型。由于药物使用可能是哮喘和肥胖关系的潜在中介因素,我们通过以下几个分析进一步探讨其作用:1)在不调整哮喘状态的情况下,我们检验了药物使用对肥胖发生率的影响;2)在同一模型中,我们评估了哮喘和药物使用对肥胖发生率的影响;3)我们采用哮喘和药物使用的联合测量方法,模拟了哮喘和药物使用对肥胖发生率的联合影响。我们使用Schoenfeld残差确认了比例危害假设是符合的。
我们进行了几种敏感性分析。首先,我们调整了基线的超重,以确定我们的结果是否受到这一类别的儿童受到不成比例的影响。其次,我们将样本限制为基线正常重量的样品,并进行单独分析检查超重或肥胖的发病,以及肥胖,以进一步评估超重在基线的影响。第三,我们调整了基线BMI作为一种连续变量来评估初始BMI状态是否会影响我们的结果。第四,我们排除了在随访期间开发哮喘的儿童,以评估我们的结果是否受到新的哮喘案件的影响。第五,我们评估了影响是否根据因素(性,出生,父母哮喘,母体教育,哮喘药物和母乳喂养(从未,<6个月,6个月))各种各样变化,这可能使某些团体通过进行分层分析和引入来更加脆弱互动条款[32.].六,我们使用世界卫生组织(WHO)削减肥胖的削减来重复我们的分析,以使用肥胖的替代定义来比较我们的结果。第七,我们评估了在随访结束时对高度的调整是否改变了我们的结果,以取消重量的变化主要推动该协会。八分之一,我们限制了对肥胖的儿童的定义,至少有两次访问。最后,我们探讨了完全分析的估计是否有所不同。
此外,我们对个体参与者进行了荟萃分析,作为补充分析,以评估我们的结果是否与我们的汇总分析一致。我们使用Cox比例风险模型与性别特异性基线风险和上述混杂因素来评估随访期间基线哮喘和其他相关表型与肥胖发生率之间的队列特异性ahr和95% CIs。我们使用随机效应荟萃分析结合了特定队列的估计,其中分配给每个研究的权重是基于研究内和研究间的变异性。我们用I检验了队列特异性估计之间的异质性2.统计和X2.我们还通过重复荟萃分析和每次排除一个队列来测试结果的稳健性。最后,我们基于联合国的分类(南欧、西欧和北欧),通过meta回归分析探讨了参与队列的区域潜在异质性。所有分析均使用Stata 14.2软件(StataCorp LLC, College Station, TX, USA)进行。
结果
分析包括21个130名儿童在群组中,平均年龄为4.1±0.6岁(表格1).与那些由于缺失数据而被排除在我们研究之外的人群相比,我们研究的总人群的母亲和儿童特征显示在补充表E1.总的来说,除了产妇受教育程度低的比例略高(60.2%)外,我们没有观察到这些群体在特征上的任何实质性差异与55.0%)和母乳喂养时间较短(63.1%)与排除在外的儿童为67.7%。总体而言,医生诊断的哮喘在基线检查时的患病率为6.0%,而基线检查时喘息和早期喘息的患病率分别为12.5%和18.1%(表2.).约13.7%的儿童患有过敏性鼻炎。哮喘患病率和相关表型的每个队列基线显示补充表E3.随访次数和随访结束时的年龄因队列而异,总平均年龄为7.1±1.2岁,平均随访3.2次(表格1). 在随访期间,483名儿童(2.3%)患肥胖症。基线肥胖和偶发肥胖的队列特异性患病率如表1所示补充表E4,而按队列划分的基线母婴特征见补充表E5.
A.ssociation of early-onset asthma and asthma-related phenotypes with incident obesity up to age 8 years in a pooled sample of 21 130 children from 16 European birth cohorts
在基线和随访时,哮喘和相关表型之间关联的汇总分析结果显示在后续行动中表2..被医生诊断为哮喘的儿童发生肥胖的风险比未被诊断为哮喘的儿童高66% (aHR 1.66, 95% CI 1.18-2.33;表2.).基线时喘息的儿童比无基线喘息的儿童有更高的肥胖风险(aHR 1.29, 95% CI 1.00-1.67)。活动性哮喘儿童表现出更大的肥胖风险(aHR 1.98, 95% CI 1.31-3.00)比那些没有哮喘和喘息的儿童。婴儿期喘息对肥胖发生率的影响与基线喘息相似(aHR 1.22, 95% CI 0.99-1.52)。然而,对于有喘息史的儿童,与从未喘息过的儿童相比,持续性喘息(aHR 1.51, 95% CI 1.08-2.09)比晚发性喘息(aHR 1.12, 95% CI 0.77-1.63)或短暂性喘息(aHR 1.06, 95% CI 0.81-1.39)的儿童肥胖风险更大。变应性鼻炎与肥胖发病呈正相关(aHR 1.29, 95% CI 0.98-1.68)。有哮喘且没有变应性鼻炎的儿童比没有哮喘的儿童发生肥胖的风险更高(aHR 2.04, 95% CI 1.32-3.13)。
显示哮喘和药物肥胖症的联合关联的结果表3.用于哮喘或呼吸困难的药物用途增加了事故肥胖的风险(AHR 1.37,95%CI 1.04-1.80)。在调整哮喘状态时,略微衰减药物对肥胖症的影响,不再有统计学意义(AHR 1.23,95%CI 0.91-1.66)。相比之下,用于药物用途的调整没有改变哮喘和事件肥胖之间的显着阳性关联(AHR 1.57,95%CI 1.04-2.37)。在评估哮喘和药物用途的组合影响时,我们发现与哮喘无哮喘和没有药物使用的儿童相比,发生药物的哮喘儿童具有更高的事件肥胖风险(AHR 1.91,95%CI 1.25-2.92)比哮喘儿童更高不服用药物(AHR 1.65,95%CI 0.73-3.73)和非发育儿童服药(AHR 1.24,95%CI 0.90-1.69)。ICS使用与哮喘调节(AHR 1.42,95%CI 0.82-26)和没有(AHR 1.45,95%CI 0.97-2.18)的调整,与事件肥胖有关。
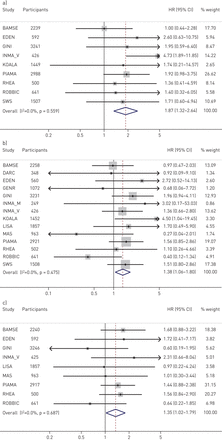
介绍了哮喘和相关表型之间的随机效应元分析的群体特异性估计和组合估计和事件肥胖症图1.INMA Menorca和LISA对医生诊断的哮喘和DARC对变应性鼻炎的队列特异性估计是不可估计的,因为在各自的队列中没有暴露的肥胖病例。综合效应估计值与我们的综合分析结果一致,尽管强度更大。没有证据表明队列之间存在显著的异质性(I2.=0, p-值>0.48)或按地理区域分组。当一次忽略一个队列时,结果仍然相似(补充表E6).
个体参与者的meta分析结果表明,早发哮喘和哮喘相关表型与8岁前的肥胖发生率之间的关联。a)基线哮喘和肥胖事件之间的关联。b) 3-4岁时过去12个月基线喘息与肥胖事件之间的关系。c)过去12个月基线变应性鼻炎与肥胖事件之间的关系。风险比率(人力资源;采用Cox比例风险模型对基线年龄、怀孕期间吸烟、被动吸烟、胎次、母亲教育、父母哮喘、母乳喂养和出生体重进行校正,并结合特定性别的基线风险得出。使用随机效应荟萃分析获得联合估计。方格代表每个研究的估计点,方格大小与分配给每个队列的权重成正比,该权重基于研究内和研究间的变异性。水平线表示95% ci,菱形表示总体估计。某些CIs上的箭头表示置信区间的上限或下限超过了x轴上显示的值的范围。
在我们的汇总分析中,当调整基线超重时,我们观察到的相关性略有减弱,但仍然显著(补充表E7).在将我们的样品限制为正常体重之后,观察到的关联衰减,不再有统计学意义,但仍然指示事件肥胖的积极协会(补充表E8).在调整基线BMI后,我们观察到的相关性同样减弱且不显著,但仍与肥胖发生率呈正相关(补充表E9).当在随访中排除新的哮喘病例(n=448)时,哮喘和肥胖发生率之间的相关性没有变化(aHR 1.65, 95% CI 1.17-2.32)。在哮喘与性别、出生体重、父母哮喘、母亲教育、哮喘药物治疗和母乳喂养之间的分层分析中,没有相互作用或差异的证据。在随访结束时对儿童身高的调整没有改变哮喘和肥胖发病率之间的关系(aHR 1.64, 95% CI 1.17-2.31)。当我们使用世界卫生组织对肥胖的定义时,我们观察到类似的结果,而当我们将肥胖定义为至少两次就诊时仍处于肥胖状态时,结果略有减弱(数据未显示)。我们的结果在完全病例分析中没有观察到差异(数据未显示)。
讨论
我们发现早发性哮喘和喘息与儿童肥胖的高发病率相关。过敏性鼻炎的证据不那么有力,但仍然表明肥胖的风险更高。这是迄今为止唯一一项纵向、多中心研究,研究了早发哮喘对儿童肥胖发展的影响。包括来自许多欧洲国家的出生队列,以及我们的队列特异性效应估计之间缺乏异质性,支持了我们结果的稳健性和普遍性。
虽然许多研究已经评估了儿童肥胖对哮喘发展的影响,但这些情况之间的时间顺序仍然不清楚,这主要是因为缺乏研究来检验哮喘是否会影响肥胖的发病。我们能够评估早期哮喘诊断对随后儿童肥胖风险的影响。我们的研究证实了之前美国两项纵向研究的发现,即患有哮喘的学龄儿童肥胖的风险增加[7.,8.].儿童哮喘的诊断是困难的,医生可能会犹豫在早期作出诊断。因此,儿童时期的喘息通常被用作未来哮喘发展的指标。虽然这种方法缺乏特异性,但我们的发现是,患有持续性哮鸣的儿童肥胖风险最高,这很重要,因为持续性哮鸣的儿童比短暂性或迟发性哮鸣的儿童更有可能患早发性哮喘[24.,33.].此外,我们对活动性哮喘的研究结果表明,目前正经历喘息症状的哮喘儿童的风险最高。此前唯一一项评估了活动性哮喘对肥胖发展影响的研究发现了类似的结果[7.].
最近的研究表明,至少有两种不同的哮喘表型与肥胖有关,一种是伴有肥胖的早发型哮喘,另一种是由于肥胖引起的晚发型哮喘。早发型哮喘的特点是变应性疾病和t辅助细胞2型(Th2)炎症的患病率较高,而晚发型哮喘的变应性疾病患病率较低,与Th2炎症的相关性较小[34.].在患有严重过敏性哮喘表型的儿童中,哮喘本身可能导致肥胖,尽管该假设在迄今为止的研究中尚未探索[2.,35.].然而,在我们的研究中,我们发现哮喘效果更强,没有过敏性鼻炎的哮喘症比鼻炎。虽然过敏性鼻炎的存在与过敏性哮喘强烈相关,但这些结果是不确定的,因为它们不是基于特性措施(即。特定的IgE措施)。在这一方向上,还需要进一步的研究来区分ige致敏和不致敏个体以及过敏性哮喘和非过敏性哮喘患者的儿童肥胖风险。
哮喘和肥胖之间的联系也可以用共同的生物学途径来解释,这些生物学途径促进了这些疾病在生命早期的发展。最近的一项小鼠研究发现几丁质酶3样蛋白1 (Chi3l1)在白色脂肪组织积累和肺部Th2炎症中起关键作用。高脂肪饮食和空气过敏原刺激增加了白色脂肪组织和肺部Chi3l1的表达,提示高脂肪饮食通过刺激Chi3l1途径促进了内脏脂肪增多和哮喘,而哮喘本身可以增加肥胖[36.].哮喘和肥胖的其他假设途径包括全身性炎症,己酮呼吸困难和共同的遗传学或表观遗传变化,以及肠道微生物组;但是,这些途径的证据是有限的[34.,37.].
与哮喘和肥胖相关的常见生活方式因素可能部分解释了它们之间的关联。例如,研究表明哮喘儿童的体力活动水平较低,睡眠较差,这也是肥胖的危险因素[38.].我们缺乏关于孩子身体活动和睡眠的信息,因此我们无法在研究中验证这一假设。此外,鉴于这些疾病的早期起源,分享子宫内暴露也可以解释我们观察到的关系。例如,产前饮食,产妇肥胖和早期婴儿生长已与两混乱[风险的增加有关37.,39.].
由于哮喘药物治疗导致的体重增加也被认为是哮喘和肥胖之间的潜在联系。两项前瞻性研究发现,与服用低剂量ICS的哮喘儿童相比,服用高剂量ICS的儿童BMI增加幅度更大[40,41.].药物使用本身可能增加肥胖风险,也可能是患有更严重哮喘的儿童,他们也使用更高剂量的类固醇,活动水平降低或其他因素使他们容易肥胖。在我们的研究中,我们缺乏药物剂量和哮喘严重程度的详细信息。然而,我们观察到,与未服药或未服药的哮喘相比,服药的哮喘肥胖风险最大。当我们相互调整哮喘和药物时,药物使用和肥胖发生率之间的正相关性减弱,但哮喘和肥胖之间的相关性没有显著变化。对于四个有可用数据的队列,吸入类固醇的使用与肥胖呈正相关,即使在哮喘调整后。因此,我们的结果表明,哮喘和药物使用的共同存在对肥胖风险有最大的影响,哮喘和肥胖之间的关联不能完全解释药物使用。此外,我们关于药物使用对肥胖的影响的结果,虽然不是结论性的,但表明它可以增加独立于哮喘状态的肥胖风险。
本研究的优势包括基于人群的纵向设计,以及包括来自几个欧洲出生队列的具有不同背景特征和行为的个体参与者数据。其他优势包括该研究的大样本量、标准化的暴露定义和协调的协变量信息。鉴于文献中关于儿童肥胖定义的差异[42.],我们测试了三种定义,并发现了可比较的结果,表明我们的发现不受不同定义标准的约束,并且代表了肥胖的真实发病。
虽然我们的研究在规模上新颖而庞大,但也存在一些局限性。一些队列没有所有混杂变量的可用数据,并且使用一个额外的类别来遗漏混杂信息可能会引入残余混杂。然而,当我们进行完整的案例分析时,我们观察到可比较的结果。虽然我们对母乳喂养进行了控制,但母亲或孩子早期的饮食模式和能量摄入仍有可能残留混淆[37.].由于母体BMI,我们也可能具有不受控制的混淆,因为研究表明孕前肥胖可能会增加儿童哮喘的风险;但是,我们的研究缺乏对母体肥胖状态调整的数据[43.].当我们排除了基线组的超重儿童时,或者当我们调整为基线BMI时,哮喘和肥胖之间的关联被衰减,但结果朝着相同的方向,可能是由于我们的几年后的几年和低肥胖发病率学习。因此,根据我们的结果,我们不能排除反向因果关系的可能性;然而,在我们调整基线超重的分析中,我们仍观察到显着升高的效果估计。我们承认哮喘患病率和受国家喘息的普遍性有很大的变化,因为哮喘可能更容易被诊断出在某些国家并在其他国家下诊断[44.].此外,肥胖患病率因国家而异,部分原因是饮食、体育活动和久坐行为的差异[45.,46.].然而,在研究特定估计中没有异质性表明,任何潜在的暴露错误分类都不是偏见的主要来源。由于缺失数据而被排除在我们的研究中的儿童更有可能具有较低的社会经济地位(SES)和更短的母乳喂养持续时间,这两者都认为是哮喘和肥胖的危险因素。由于两种因素与我们的曝光和结果正相关,因此由其排除产生的选择偏差可能会对我们的结果产生负面偏见。鉴于我们观察到的哮喘和事故肥胖之间的关联的大小,这一潜在的偏见来源不太可能是对我们研究有效性的重大威胁。通过父母报告评估哮喘和相关的合并症,这可能会引入错误分类,但根据ISAAC研究,调查问卷是良好的验证[22.].我们在我们的分析中也有较少的力量,其中我们组合多种哮喘和哮喘相关条件的存在,因为并非所有儿童都有关于这些条件的完整数据。由于人类测量措施基于父母报告和临床评估信息的组合,因此有可能在我们的研究中错误分类。但是,我们不期望通过哮喘状况通知报告的重量信息的任何错误分类,因此由此产生的偏差将朝向零点。
这项大型、多中心纵向研究表明,早发哮喘和喘息可能导致儿童后期肥胖发生率的增加。我们的发现支持了进一步调查导致哮喘儿童肥胖风险增加的因素的必要性,以更好地量身定做未来的肥胖预防工作。
补充材料
致谢
BAMSE:我们感谢所有参与BAMSE队列的儿童及其家长以及在BAMSE项目中工作的护士和其他工作人员。伊甸园:我们承认伊甸园母子队列研究小组的承诺:I。安妮西·梅萨诺,J.Y.伯纳德,J。波顿,M.A.查尔斯,P。达金特·莫利纳,B。德劳松·吉兰,P。杜西梅蒂埃,M。德阿戈斯蒂尼,B。福利盖,A。福汉,X。煎饼,A。杰玛,V。古阿,R。汉卡,B。黑德,M。卡明斯基,B。拉罗克†, N.勒隆,J. Lepeule, G. Magnin, L. Marchand, C. Nabet, F. Pierre, R. Slama, M.J. saurelle - cubizolles, M. Schweitzer, O. Thiebaugeorges。罗比克当前位置我们感谢所有现场工作人员和他们的家庭为研究做出的贡献。SWS.:我们感谢南安普敦妇女调查研究小组的成员和SWS的许多参与者对研究的贡献。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:Z.A.Contreras,T。鲁梅利奥塔基和L。Chatzi完全可以访问研究中的所有数据,并对数据的完整性和数据分析的准确性负责。研究概念与设计:L。查齐;数据采集:所有作者;统计分析:Z.A.Contreras和T。鲁梅利奥塔基;资料解释:所有作者;手稿起草:Z.A.孔特雷拉斯和L。查齐;对重要学术内容的手稿进行批判性修订:所有作者;学习督导:L。查齐。
利益冲突:L. Duijts报告赠款欧盟展望2020联合资助计划ERA-网的生物标志物的营养与健康(ERA HDHL)(字母项目(编号696295,2017年)和ZonMW荷兰(编号529051014; 2017年))和来自欧盟的展望2020方案(生命周期项目,赠款协议号733206补助金; 2016),该研究进行期间。
利益冲突:B.格哈德研究进行期间报告的赠款来自欧盟FP7。
利益冲突:H. inskip报告来自英国医学研究委员会的赠款(薪水),英国心脏基金会的赠款,英国食品标准机构,英国肺基金会,关节炎研究英国,NIHR南安普顿生物医学研究中心和欧洲联盟的第七框架计划(FP7 / 2007-2013,在该研究的行为期间,在拨款协议编号为289346的项目早期);H. Inskip的团队成员已获得Nestec,Abbott Nutrition和Danone Nutricia的资金,为她所关联的各种项目,但她没有接受过Inself的直接资金。
利益冲突:S. Lau报告来自Symbiopharm和Allergopharma,个人费用(酬金)和非财政支持(咨询委员会工作)的资助和个人费用(酬金),来自ALK的个人费用和非财务支持(咨询)董事会工作)来自Boehringer和Merck,在提交的工作之外。
利益冲突:D. Maier在研究期间报告了来自欧盟委员会的拨款(FP7 MeDALL, 261357)。
支持声明:这项工作部分得到了南加州环境健康科学中心(批准# P30ES007048)的支持,该中心由国家环境健康科学研究所(PI F. Gilliland)资助。Z.A. Contreras得到了NIH的资助(T32 ES013678)。MeDALL和CHICOS项目:导致这些结果的研究已经收到了欧盟第七框架计划(健康-F2赠款协议261357和241604)资助。ABCD队列:阿姆斯特丹出生的儿童及其开发队列的数据与荷兰卫生研发组织的资金有关(Zonmw 40-00812-98-11010)的资金部分支持。该研究赞助商在研究设计,数据分析,数据的解释或本报告中没有作用。BAMSE:我们感谢所有的资金来源(瑞典研究理事会、瑞典心肺基金会、瑞典工作生活和社会福利研究理事会、瑞典哮喘和过敏协会研究基金会、瑞典研究理事会Formas、斯德哥尔摩郡议会和欧洲委员会的第七框架计划奖章,授予协议编号261357)。伊甸园:我们承认伊甸园研究的所有资金来源(医学研究(FRM),国家研究所(ANR),国家公共卫生研究所(IRESP:TGIR COHORTESanté2008计划),法国人卫生部(DGS),法国研究部,内部骨骼和联合疾病国家研究(PRO-A)和人类营养国家研究计划,巴黎 - 苏丹大学,雀巢,法国国家人口健康监测研究所(INV),法国国家健康教育研究所(INPES),欧盟FP7计划(FP7 / 2007-2013,螺旋,逃脱,RERIECO和MEDALL项目),糖尿病国家研究计划(通过与法国糖尿病协会协会合作患者(AFD)),法国环境保健机构(现在ANSES),MutuelleGénéraledeL'教育国家是一个互补的健康保险(MGEN),法国国家粮食安全机构和法语演讲协会糖尿病和新陈代谢(Alfediam))。生成研究:在代R研究由来自Erasmus医学中心,鹿特丹,鹿特丹Erasmus大学,荷兰组织健康研究与发展(ZonMw)的资金支持成为可能,荷兰科学研究组织(NWO),卫生部,福利和体育和青年和家庭部。,欧洲研究委员会(ERC-2014-COG-648916),并从共同资助ERA-Net的关于生物标志物的;该项目得到了欧盟的展望2020研究和创新计划(2016生命周期项目,赠款协议号733206)资助营养与健康(ERA HDHL),展望2020(赠款协议号696295; 2017年),ZonMW荷兰(编号529051014,2017年),爱尔兰科学基金会(无SFI / 16 / ERA-HDHL / 3360)和欧洲联盟(简称ALPHABET项目)。研究人员独立于出资方。该研究赞助商在研究设计,数据分析,数据的解释或本报告中没有作用。INMA:本研究的数据由Inma-Environment和Closshial Broject提供(www.proyectoinma.org.).这项研究由西班牙卡洛斯三世研究所(Red INMA G03/176和CB06/02/0041)、西班牙卫生部(fi - pio41436、PI06/0867、PI081151和fi - feder 03/1615、04/1112、04/1931、05/1079、05/1052、06/1213、07/0314和09/02647)、加泰罗尼亚共和国公共卫生总局1999SGR00241、巴伦西亚纳总医院、巴斯克政府卫生部(2005111093和2009111069)和吉普斯科阿省政府(DFG06/004和DFG08/001)。考拉:本分析中使用的KOALA出生队列研究的数据收集得到了Friesland Foods(现为FrieslandCampina)、荷兰哮喘基金会(批准号为3.2.07.022和3.2.03.48)、荷兰心脏基金会(批准号为2014 T037)、荷兰卫生研究和发展组织(第1.210-00-090号ZonMw预防方案)、Triodos基金会、凤凰基金会、Raphaël基金会、Iona基金会和促进Heilpedagogie基金会,所有这些都在荷兰。马斯: MAS出生队列由德国联邦教育和研究部(BMBF;参考编号07015633,07 ALE 27, 01ee9405 / 5,01ee9406)和德国研究基金会(DFG;参考编号KE 1462/2-1)。皮亚马:该研究由荷兰卫生研究与发展组织、荷兰科学研究组织、荷兰哮喘基金、荷兰空间规划、住房和环境部以及荷兰卫生、福利和体育部资助。rh:瑞典项目由欧洲项目经济(欧盟FP6-003-FOOD-3-NEWGENERIS,合约编号16320;欧盟FP6 Strep HIWWATE,合同号36224;欧盟FP7 ENV.2007.1.2.2.2,项目编号211250逃生;欧盟FP7-2008-ENV-1.2.1.4环境常规标志物,合同编号226756;欧盟FP7-Health-2009-单阶段芝麻,合同号241604;欧盟FP7 Env.2008.1.2.1.6,提案号码226285 EnrieCo; Eu-FP7,提案号码264357 Medall;欧盟-FP7-Health-2012,提案号308333螺旋)和希腊卫生部(预防肥胖和神经发育疾病的幼儿园儿童,Heraklion区,希腊,希腊:2011-2014;“raea加“:预防生殖健康环境风险因素,儿童健康:2012 - 2015年)。罗比克罗马群组的数据部分得到了意大利卫生部资金的支持(方案特别方案)。12,逗号2,字母b) del D. Lgs. 502/92, 2001, 2003)。SWS.:南安普敦妇女调查得到了医学研究委员会,英国心脏基金会,食品标准机构,英国肺基金会,关节炎研究中心,NIHR南安普敦生物医学研究中心,南安普敦大学南安普敦南安普敦南安普敦基金会信托和欧盟第七框架计划(FP7 / 2007-2013,在拨款协议编号为289346下的项目早期)。本文的资金信息已存入Crossref资助者注册表.
- 已收到2018年3月13日。
- 认可的2018年7月30日。
- 版权所有©ers 2018