摘要
由于个体放射学和生理上的差异,特发性肺纤维化预后的准确评估仍不明确。我们假设短期放射学变化可以预测生存率。
我们探索了CALIPER(计算机辅助肺信息病理评估和评级)的使用,这是由梅奥诊所罗彻斯特(Rochester, MN, USA)生物医学成像资源实验室开发的一种新型软件工具,用于在高分辨率计算机断层扫描上分析和量化肺实质异常。我们评估了55例特发性肺纤维化患者的基线和随访(分别为时间点1和2)高分辨率计算机断层扫描,并将caliper量化测量结果与专家放射科医生的评估和临床结果相关联。
经CALIPER量化的网状密度体积(危险比1.91,p=0.006)、间质异常总体积(危险比1.70,p=0.003)和间质异常总百分比(危险比1.52,p=0.017)的间隔变化(平均289天)的发现可预测中位随访2.4年后的生存。放射科医生对肺间质性疾病短期整体进展的解释,而不是特定的放射学特征,也可预测死亡率。
这些数据证明了在高分辨率计算机断层扫描上量化间隔短期变化的可行性,以及它们可能用作特发性肺纤维化生存的独立预测指标。
摘要
短期定量CT改变可预测IPF的生存http://ow.ly/qmbjd
简介
疾病严重程度的基线测量已用于预测特发性肺纤维化(IPF)的生存,包括临床特征、肺功能测量、计算机断层扫描(CT)表现和综合评分指标[1- - - - - -4]。虽然这些措施已在多项研究中得到验证,但它们似乎不如疾病进展的动态替代指标,如生理指标的纵向变化,即。肺活量和肺对一氧化碳的扩散能力下降(DLCO)超过6-12个月[2,5,6]。然而,这种纵向生理指标在个体患者管理中的应用仍然受到个体内部差异的显著限制,可能还存在共存疾病的混杂,如肺气肿或肺动脉高压[7,8]。
CALIPER(病理评估和分级计算机辅助肺信息学)是由罗彻斯特梅奥诊所(Rochester, MN, USA)的生物医学成像资源实验室开发的一种图像分析工具,用于高分辨率计算机断层扫描(HRCT)上肺实质发现的特征描述和量化。CALIPER对肺实质的检测和定量是基于直方图特征映射技术,该技术是通过肺组织研究联盟(LTRC)获得的病理确认训练集的放射科专家共识评估训练出来的[9]。我们假设,这种分析胸部HRCT肺实质特征的新型计算机辅助方法将提供可重复和准确的疾病评估,这可能与放射科医生的半定量评估相关。我们进一步假设,CALIPER或放射科医生检测到的实质特征的总体程度或短期变化可能与IPF患者的生存相关,并独立预测其生存。
材料与方法
患者与CT选择
选取2000年1月至2010年12月在梅奥诊所进行评估的患者,根据最新的国际共识指南诊断IPF [10](包括或不包括手术肺活检),其中至少两次连续hrct在3 - 15个月内获得,分别代表时间点1和2。在急性发作、感染、液体过载或血栓栓塞性疾病时获得的hrct被排除在研究之外。此外,HRCT必须满足CALIPER的技术要求,包括高分辨率图像(≤2mm切片厚度)。本研究中的扫描是使用LightSpeed Ultra (BONE内核;GE医疗保健,克利夫兰,OH,美国)和Model Sensation 64 (B46内核;西门子,慕尼黑,德国)扫描仪。
收集的人口学资料包括年龄、性别、吸烟史和包年数。诊断时间定义为与临床护理提供者接触的第一天,该临床护理提供者根据临床表现评估、HRCT扫描和/或活检做出或怀疑诊断IPF。随访患者至死亡终点或梅奥诊所医疗记录中记录的最后已知就诊日期。对接受肺移植的患者进行随访,直到移植日期并进行检查,在此之前的HRCT间隔变化也包括在分析中。
该研究方案得到了梅奥诊所机构审查委员会(IRB编号10-000320)的批准。所有受试者均提供知情同意。
肺功能研究
所有入选患者均在所选扫描后30天内获得相应的肺功能测试(PFT)数据。根据美国胸科学会/欧洲呼吸学会指南制定的标准,使用基于清教班尼特文艺复兴(Mallinckrodt,圣路易斯,密苏里州,美国)的流量肺活量仪进行肺活量测量[188bet官网地址11]。流量用M的参考方程表示为预测的%伊勒河et al。[12]。
放射科医生对CT的半定量评估
为了比较放射科医生对HRCT结果的半定量评估与CALIPER定量,两名亚专科胸科放射科医生(T.E. Hartman和B.J. Bartholmai)独立审查了每位患者对时间点1和2不盲化的HRCT扫描,并在对临床数据和CALIPER结果不盲化的情况下,以标准化方式对其进行评分。评分系统包括对实质受累百分比的视觉估计,最接近5%,在特定区域的四种放射学异常:肺气肿,磨玻璃样影,网状混浊和蜂窝状。在12个区域内分别对异常分布进行评分:右上叶、右中叶、右下叶、左上叶、舌叶和左下叶的中央和外围区。复查放射科医生还记录了他们对每个受试者两次扫描之间的间隔稳定性、整体CT异常进展或改善的评估。每个异常的区域受累百分比和每个放射学参数(肺气肿、磨玻璃、网状和蜂窝状)的总受累百分比用于统计分析。
井径仪分析
数据处理
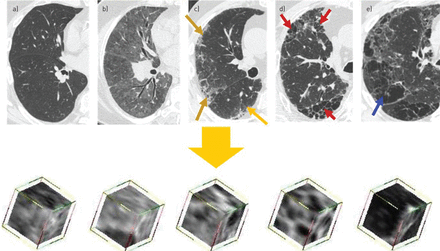
数据处理步骤包括肺提取和分割,识别和提取中央气道和中央血管结构,手动分割解剖叶,并对剩余肺实质进行分类。肺的分割是使用自适应密度形态学方法实现的[13]。气道采用迭代三维区域生长和连接成分分析进行分割。使用优化的多尺度管状结构增强过滤器提取肺血管[14]。胸科放射科医生(B.J. Bartholmai)通过手动示踪技术对解剖叶进行额外的亚分割,并通过三维体积侵蚀技术完成中央/外周区域的确定,使得外周区占每个肺总体积的~ 50%。通过气管树分析,半自动化地确定肺门,并从肺门点两侧包涵一个5厘米的球形区域,将肺门周围区域单独包涵到每个肺叶的中心区域。实质组织类型的检测和定量(正常、肺气肿、磨玻璃、网状和蜂窝状)(图1)使用滑动窗口监督分类方案进行。
计算机断层扫描图像显示a)弥漫性肺部疾病的正常外观和各种视觉表现:b)磨玻璃,c)网状改变(箭头),d)蜂窝状(箭头)和e)肺气肿(箭头)。在训练数据集中,四名胸科放射科医生的共识被用于识别多个感兴趣的15×15×15像素,对应于正常、磨玻璃密度、网状异常、蜂窝状和肺气肿。
在预处理监督训练阶段,4名亚专业胸科放射科医生通过独立分析,从14名经病理诊断为弥漫性肺疾病(肺气肿间质性肺疾病(ILD))或无ILD的已知对照受试者的HRCT扫描中选择了多个(n=976) 15×15×15-pixel感兴趣的卷。所有四名放射科医生对异常类别达成一致的候选样本被用于使用自动聚类亲和技术确定每种视觉异常类别的典型直方图特征,每种视觉类别的特征被用于测试对象的HRCT数据的体积分类(图2).
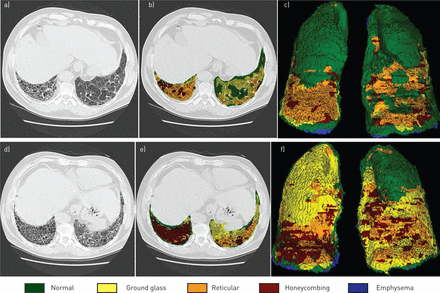
CALIPER定量分析的代表性结果。这两行(a-c)和(d-f)分别对应其中一位患者的两个时间点。原始切片(a和d)中肺区域的个体体素被分类并用颜色编码为可见异常(b和e)的一类。c和f)三维最大特征投影。CALIPER定量和放射科医师回顾均表明毛玻璃样混浊、网状异常和蜂巢状的整体增加。
组织量化
CALIPER分析包括五种放射实质特征的算法识别和容量量化:正常肺、肺气肿、磨玻璃密度、网状异常和蜂窝,以整个肺的总升为单位测量。总ILD定义为毛玻璃总密度、网状异常和蜂窝状的体积总和。Percentage ILD定义为总ILD之和除以CALIPER分割的肺实质总容积的比值。
统计分析
使用Spearmans相关系数评估CALIPER测量、pft和放射科医生估计的受累百分比之间的相关性。计算每位受试者两次CT扫描之间CALIPER测量值的变化,包括正常肺总体积、磨玻璃密度、网状异常、蜂蜂窝、总肺体积、总ILD和ILD百分比。使用Cox比例风险回归评估CALIPER测量的变化和放射科医生对局部半定量结果的评估的变化以及疾病进展、回归或稳定性的总体印象与生存的关系。从第二次CT开始进行里程碑式生存分析,我们选择这种方法是为了避免生存到第二次CT的生存偏差。单变量和多变量分析包括性别、包年、基线覆盖度% pred、基线DLCO% pred和ct之间的时间。在所有病例中,双侧p值<0.05被认为有统计学意义。
结果
患者与HRCT特征
55例纳入分析,均数±sd年龄72.4±6.9岁,男性占51% (n=28) (表1).55例患者中有31例(56%)进行了肺活检,以证实通常的间质性肺炎病理,其余患者的诊断依据是HRCT上典型的通常间质性肺炎模式,临床排除了已知的肺纤维化原因。从第二次HRCT时间点开始,中位无移植生存期为2.1年(范围1.1-3.4年)。对于18名未知死亡的受试者,中位随访时间为2.4年(范围0.1-8.5年)。均值±sd连续HRCT间隔时间为289.2±109天。虽然该研究没有根据两次扫描的扫描仪品牌或型号的差异排除受试者,但75%的受试者在两个时间点都使用了同一品牌的扫描仪(西门子和GE医疗)。
击球
两个CT扫描时间点对应的PFT值(绝对值和% pred值)表示在表2以及区间内% pred的差异。
井径仪分析
CALIPER在时间点1和2对每个特定放射参数的平均容积定量(单位为升)载于表3以及时间间隔上的差异。由于CALIPER量化了不同IPF严重程度阶段患者中磨玻璃、网状和蜂蜂窝的总体积比例,因此在生存分析中使用的是随时间变化的总平均值和百分比,而不是单个时间点体积。放射科医生对时间点1和2的放射学结果的解释载于表4.平均百分比表示每个区域得分最接近5%,并在12个区域平均整个肺的放射学发现的百分比。单变量分析的结果调整性别,包年,基线覆盖度% pred和基线DLCO% pred表示在表5.的变化与生存有统计学意义的相关性DLCO% pred(危险比(HR) 2.14, 95% CI 1.27-3.60;p=0.004)和总肺活量(HR 4.17, 95% CI 1.42-12;P =0.009)肺功能检测分析。CALIPER测量的ILD百分比随时间变化的调整分析(HR 1.52, 95% CI 1.08-2.15;p=0.017), ILD总容积(HR 1.70, 95% CI 1.19-2.43;p=0.003)和总网状体积(HR 1.91, 95% CI 1.21-3.0;P <0.006)与生存率相关(表4).
CALIPER测量的总肺容积与PFT测量的总肺活量之间的相关性非常好(分别在时间点1和2上r=0.77 (p<0.001)和r=0.87 (p<0.001))。
放射科医师与CALIPER和生存率的相关性
在线补充表S3和S4中报告了两名放射科专家和CALIPER之间的观察员协议。总体而言,两名放射科医生在所有区域的ILD评分(磨玻璃样影、网状样影和蜂窝状样影)之间的相关性为中等至显著(范围为0.33,p<0.001至0.73,时间点1为p<0.001,时间点2为0.33,p<0.001至0.77,p<0.001)。在所有叶瓣中,磨玻璃样影和网状样影的总体相关性最好,而蜂窝状样影的相关性最差。放射医师1和CALIPER之间的ILD评分相关性为轻度至中度(范围为0.29,p=0.001至0.63,时间点1和0.24 p<0.005, p<0.001至0.64,时间点2 p<0.001),相关性为轻度至中度(范围为0.29,p<0.001至0.48,时间点1和0.28 p<0.001至0.64,时间点2 p<0.001)。调整后的吸烟史(包年),性别,FVC和DLCO根据放射科医生的评估,% pred和HRCT扫描之间的时间,个体ILD实质变化不能预测生存(表5).放射科医生对ILD进展方面的整体变化的解释可预测生存率。
讨论
CALIPER是一种自动体积量化工具,用于评估HRCT上特定的实质放射学特征。在我们对IPF患者的研究中,CALIPER测量了短期(3-15个月)的网状改变,以及ILD改变的百分比和总数可以预测生存。对于磨砂玻璃和网状发现,放射科医生之间的相关性为中度至显著性,估计为最接近的5%,对于同样的ILD发现,放射科医生和CALIPER之间的相关性为轻度至中度。虽然在我们的研究中,放射科医生对疾病进展或改变的整体评估是可预测的,但根据放射科医生的评估,ILD的具体实质估计不能预测生存。
由于缺乏一种金标准来验证病理标本中特定区域CALIPER容量测量的准确性,因此我们试图将放射学纤维化定量估计的纵向变化与患者结局,特别是死亡率联系起来。由于CALIPER对纤维化的定量评估不受诸如肺气肿或肺动脉高压等可能影响肺功能测量的混合条件的影响,我们认为放射学特征可能更直接地反映纤维化过程的进展,并可能是评估和管理IPF患者的一种新颖而有前途的工具。
在间质性肺疾病中,CALIPER测量值与两名放射科专家估计的纤维化程度之间的轻度到中度相关性令人欣慰,这表明CALIPER确实可以进行准确和可重复的评估,尽管当连续扫描之间难以识别细微变化时,CALIPER对特定实质间质纤维化特征的半定量测量可能更有优势。在我们的研究中,使用最接近5%的评分系统进行估计,允许两位有经验的放射科医生之间存在中度至重度相关性,但与CALIPER仅存在轻度至中度相关性。我们注意到,虽然CALIPER的算法定量分析可以检测到放射科医生可能检测不到的细微异常,但对密度相似但形态不同的异常(如蜂巢状)的错误分类与肺气肿)可能发生在CALIPER或与放射科医生的评估略有不同(磨玻璃与网状异常),解释了相关性的差异。
有趣的是,在我们的研究中,放射科医生对短期ILD进展的整体评估也可以预测生存。我们知道,一般来说,放射科医生的定量评估和诊断解释往往彼此不一致,尽管我们的放射科医生相关性较高。也许这可以解释为,我们的审查放射科医生是同一机构的胸科放射学亚专家,他们都审查和标准化了病例和术语,作为其他ILD研究的培训。对时间点1和2的非盲化可能增加了放射科医生对间隔扫描和疾病进展的偏倚解释之间预期变化的警惕性。尽管如此,这一结论是令人满意的,因为经验丰富的放射科医生在较短的时间间隔内检测进展,从统计学上预测生存,尽管检测这种微妙的变化可能无法在所有实践和机构中重现或一致。CALIPER等定量方法可以提供这种一致性,特别是在较短时间间隔内检测细微进展可能对估计生存期有价值,并可能在未来的临床试验中用作治疗反应的标记。我们感到鼓舞的是,我们对疾病的可重复定量评估与结果的相关性是显著的,独立于放射科医生对疾病特征的主观描述。
由于缺乏有效的疾病进展替代标记物和不可预测的自然史,IPF的预测仍然具有挑战性。使用生理数据作为替代标记有很大的局限性。首先是生理指标,如植被覆盖度和DLCO,具有显著的个体内差异。事实上,植被覆盖度下降10%的阈值低于最近指南所建议的正常个体内变异的程度[15]。其次,生理测量只能间接估计纤维化的进展,并可能受到常与IPF相关的肺气肿和/或肺动脉高压的影响[7,8]。最后,PFTs可能不够敏感,无法检测亚临床进展的纤维化:在IPF临床试验中,由当前阈值定义的FVC下降是相对罕见的事件,这导致一些作者认为FVC的边际下降可能更敏感,尽管不太特异性[16]。
其他一些研究表明,HRCT半定量评估的纤维化程度是IPF预后的一个强有力的预测因子[1,4,17]。通过自动分析定量估计肺纤维化与死亡率的相关性一直是少数报道的对象[1,18,19]。这方面的研究由于缺乏验证方法和难以获得高质量的HRCT来对肺实质进行容量评估而受到阻碍。现有的肺纤维化定量分析数据大多集中在基线HRCT异常的预测能力上。
使用HRCT确定的肺纤维化纵向定量指标可能是一种有吸引力的生理测量方法。在HRCT上监测纤维化进展的准确和可重复的方法将是一种有价值的疾病替代标志物。不幸的是,专家放射科医生对纤维化体积的评估一直受到观察者内部和观察者之间的巨大变性的阻碍,而使用分形分析和基于全局直方图的方法的定量CT指数迄今尚未得到验证或在临床实践中被发现有帮助[1,4,19- - - - - -24]。CALIPER基于纹理敏感的体积分析,允许根据感兴趣的HRCT体积数据库自动分类肺实质,放射科医生使用LTRC数据验证[9]。大多数现有的专家系统和相关的定量工具依赖于严格控制的图像采集协议,以提供一致的结果。我们认为,精心选择训练集的CALIPER使分类更具可重复性,其基于灰度局部直方图的算法受图像噪声、重建核和其他扫描参数的影响较小。
虽然我们的初步结果很有希望,但我们认识到我们研究的局限性。首先,CALIPER技术是基于LTRC数据库中使用的标准化CT分析和采集协议得出的“肺模式特征”开发的[9]。这项回顾性研究中用于CT的扫描参数与LTRC数据库中使用的扫描参数不同,并且在两个时间点的扫描并不总是相同。尽管某些数据集的采集参数存在差异,但放射科医师半定量评估与CALIPER分析之间的轻度到中度相关性支持了我们结果的有效性。我们假设,与其他基于纹理或像素计数技术相比,我们基于直方图签名的方法可能更鲁棒,对特定切片厚度或图像重建参数不太敏感。其次,仅为随访目的而获得两组HRCT的要求导致我们排除了因共存疾病(心力衰竭、感染和急性加重)而获得HRCT的患者和仅获得一组HRCT的患者。这种排除标准可以说限制了我们研究的外部有效性,因为纳入的患者更有可能代表逐渐下降的IPF患者的子集,而不是稳定的(不太可能重复HRCT)或不稳定的患者(更有可能失去随访,死亡或经历急性加重)。然而,纳入患者的中位生存期与IPF患者的典型生存期相似,这一点令人欣慰。最后,由于严格的资格标准,纳入的患者数量很少。虽然这些数字很小,但与先前评估生理测量纵向趋势价值的研究中使用的数字相当。我们认识到这些局限性,并认为有必要进一步验证我们的初步结果,包括具有等效时间间隔的标准化HRCT的前瞻性分析,IPF异常与其他ILD的比较,以及应用CALIPER发现的短期变化来预测急性加重或相关并发症(如肺动脉高压)的存在。
总之,我们已经证明,HRCT上肺实质的CALIPER表征和定量与放射科专家的视觉评估相关,并且连续HRCT上定量的短期容量纵向变化与IPF死亡率相关。我们认为,CALIPER在HRCT上测定ILD的定量特征可能是IPF的准确和可重复的生物标志物,值得进一步的验证研究和应用。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明:本研究由布鲁尔特发性肺纤维化和其他间质性肺疾病研究奖资助。本出版物得到了NIH/NCRR CTSA拨款号UL1 RR024150的支持。其内容仅为作者的责任,并不代表NIH的官方观点。
利益冲突:可以在本文的在线版本中找到信息披露www.www.qdcxjkg.com
- 收到了2012年5月5日。
- 接受2013年2月19日。
- ©2014人队