抽象
本研究的目的是量化体重指数(BMI;以及中年男性和女性的哮喘,并评估作为哮喘危险因素的BMI变化。
哮喘发病率是根据2004-2007年期间从挪威全国处方数据库中检索到的抗哮喘药物赎回处方的数据估计的。BMI是在1994年至1999年对出生在1952年至1959年间的10万人进行健康调查时测量的。BMI的变化是基于自我报告。使用泊松回归估计相对风险。
在对混杂因素进行调整后,与BMI增加3个单位相关的相对风险范围为:当前吸烟者的1.14(95%置信区间为1.10-1.18)到从不吸烟者的1.27(1.22-1.32)。在对混杂因素(包括性别、吸烟和BMI)进行调整后,BMI增加3个单位的相对风险为1.21(1.16-1.26)。
以抗哮喘药物使用为指标,哮喘发生率与体重指数和体重指数变化呈正相关。就体重指数而言,不吸烟者比已戒烟者和现在吸烟者的关联更强。
许多研究表明,肥胖是哮喘的危险因素1,2尤其是女性3.,4。这些发现在青少年和成年人中是一致的5。一项研究还报告了臀腰比与哮喘发病率之间的正相关关系6另一项研究发现,身高与哮喘发病率呈负相关7。此外,一项研究发现,体重指数(BMI)与哮喘的关系仅存在于非特应性疾病中6。最近一项前瞻性研究的荟萃分析得出结论,超重/肥胖个体的哮喘发病率增加了50%8。研究还得出结论,性行为与肥胖和哮喘之间存在剂量-反应关系,而且性行为对肥胖和哮喘之间的关系并没有特别大的影响8。
Fewer studies have investigated the relationship between change in BMI (ΔBMI) and subsequent asthma, but, in a prospective study of 85,911 female nurses, weight gain after the age of 18 yrs was strongly associated with an increased risk of adult-onset asthma9。Romieuet al。10研究发现,在法国中年女性人群中,体重的下降和增加都与哮喘风险的增加有关。然而,其他研究表明,减轻体重似乎可以减轻哮喘患者的症状11,12。
评估人群中的哮喘患病率是一项挑战,因为没有一个单一的工具可以用来确定哮喘。使用自我报告的哮喘或哮喘症状作为衡量哮喘的一种方法受到了几项研究的质疑13,14。上抗哮喘药物的处方使用数据提供了一种替代方法15。大量的处方医疗数据库已经证明了使用这类数据来识别哮喘患者的可行性16- - - - - -18。一项来自荷兰普通医学处方数据库的研究发现,一种或多种抗哮喘药物的处方可以确定95%的成年人患有哮喘19。在本研究中,因此,哮喘发病率估计数据对来自全国挪威处方数据库(NorPD)检索到的抗哮喘药物处方赎回的基础上。
本研究的目的是量化BMI和哮喘之间的关系在中年男性和女性,并评估ΔBMI作为哮喘的危险因素。
材料和方法
研究人群
从1994 - 1999年期间,由挪威政府进行的健康调查数据有联系的信息从NorPD,其中包括自2004年以来,挪威在药店分配所有处方药20.。健康调查进行问卷的方式(部分进行如。有关吸烟、运动习惯、受教育程度及哮喘、心脏梗塞、心绞痛、中风及糖尿病史的资料,以及部分身体测量资料(如。身高和体重)。问卷在家填写,并在检查时发放。
共有107,001名男性及102,911名女性获邀参与健康调查。总共有159,331人(分别为70人和82%的受邀男性和女性)参加了会议,132,924人回答了关于哮喘病史的问题(“你有或曾经有过哮喘吗?”)”(yes / no))。8,638名回答“是”的被排除在外,还有4,325名因为其他原因被排除在外(图1)⇓),余下118,723名(男性55,940名及女性62,783名)作分析。BMI的计算方法是体重(公斤)除以身高(米)的平方。
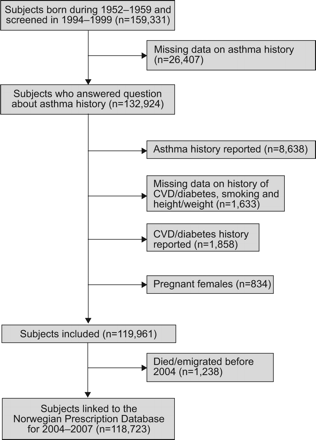
流程图显示了研究人群。1994 - 1999年期间,挪威健康调查结果链接到挪威全国处方数据库2004 - 2007年。CVD:心血管疾病。
共有114577个科目也报告了最低(W最小值)和最大重量(w马克斯)在筛选前的5年内。女性被要求在怀孕期间不要报告体重。ΔBMI计算测量高度和报道w最小值和w马克斯ΔBMI = (w马克斯- 含最小值)·高度−2。计算相对ΔBMIΔBMI / BMI×100%, BMI的测量体重指数。
此外,健康调查的下列变数包括:吸烟(从不、以前和现在)、体育活动(低、中、高)、教育(五级)、出生年份、城乡居住和领取残疾养恤金(是/否)。
体力活动是通过询问花在光(无汗或沉重的呼吸)和硬活动的时间解决。The alternatives in both categories were 0, <1, 1–2 and ≥3 h·week−1的平均值。将这两个问题加入到一个新变量中,该变量分为三个等级:1)< 1h(轻度活动)和0 h(重度活动),2)< 3h(重度活动)和3)≥3h(重度活动)。
教育水平的五个类别:1)小学(一个16岁的时代),2)技术学院或类似(1 - 2岁),3)继续教育/高中或类似(3岁),4)大学/学院< 4岁,5)≥4年大学/学院。
居住在50,000 >居民的城市的受试者被划分为城市受试者,其他受试者被划分为农村受试者。然而,挪威最大的两个城市在1994-1999年期间没有进行普查。
测量哮喘发病率
哮喘发病率(筛查至2007年期间发生的哮喘新病例)是根据2004-2007年期间从NorPD检索的吸入性抗哮喘药物赎回处方数据估算的。自2004年1月1日起,挪威所有的药店都被法律强制要求向挪威公共卫生研究所(Norwegian Institute of Public Health)发送所有处方的电子数据20.。NorPD包含所有在药房领取处方药的个人信息。所有的处方,无论是否报销,都存储在数据库中。根据解剖治疗化学(ATC)分类系统对药物进行分类21。所收集的资料包括病人的唯一识别号码(加密)、性别和年龄、配药日期、药物的详细资料(品牌名称、包装尺寸、包装数量、管制代码、规定的每日剂量和价格)和有关的报销代码。
至少使用了两种可报销的吸入性抗哮喘药物,其中最后一种药物在第一种药物后≥6个月才开出,即。药物与ATC代码R03AC(选择性β2激动剂),R03BA(糖皮质激素)和/或R03AK(长效β2-激动剂/糖皮质激素联合吸入器)。挪威的一般报销制度基本上是一种阳性清单制度,其基础是可报销药物治疗的疾病或条件清单。只有在病人患有慢性疾病(如。哮喘) for which long-term medication (>3 months) is necessary22。
使用糖皮质激素也表明持续性哮喘比使用β2受体激动剂。还进行了一项分析,其中,终点定义为至少两个已报销的糖皮质激素(ATC代码R03BA或R03AK)的处方,最后一个处方在第一个处方后≥6个月分发。
药物处方数据与健康调查数据相关联,使用的是每个挪威公民在出生或移民时分配的唯一个人身份证号(加密)。挪威数据监察局(挪威奥斯陆)和医学研究伦理区域委员会批准了这种联系。
统计方法
泊松回归是用来估计协会(表示为相对风险(RRs))之间的影响变量(BMI和ΔBMI)和结果变量(事件哮喘)对于不吸烟者,过度吸烟者和吸烟者分开23。估计是使用在统计软件包R中的GLM(一般线性模型)函数24。效果变量分为类别变量和连续变量。RR估计值是根据年龄(出生年份;连续变量)和性别、体育活动、受教育程度、城乡居民和残疾抚恤金(分类变量)。在分析与ΔBMI效应变量中,BMI(连续变量)也进行调整。
性之间的相互作用和影响变量(BMI和ΔBMI),和吸烟影响变量,是由包括相关检测模型中交互方面除了性之外,吸烟类别和上面列出的潜在的混杂因素。效果变量输入为连续变量。
在基线时,使用线性回归对连续变量进行检验,使用逻辑回归对是/否变量进行检验,并输入BMI作为连续变量,以检验潜在混杂因素作为BMI函数的趋势。BMI <20 kg·m的个体−2没有包括在趋势测试中。
结果
基线时男性的平均BMI较高(26.2 kg·m−2) than in females (24.7 kg·m−2),但重度肥胖(BMI≥35 kg·m−2)在女性中比在男性中更常见(表1⇓和2⇓)。女性也报道了更大的ΔBMI多于男性,无论是绝对还是相对而言。Smoking habits and education were comparable for males and females, but more males were physically active and more females received disability pension (tables 1⇓和2⇓)。超重在基线与受教育水平低、低体力活动,农村住宅,盛行的残疾退休金,低流行率的吸烟,后来出生年份和大型ΔBMI(表1所示⇓和2⇓)。突发哮喘通常与超重的基线特征相关,除了吸烟和高体力活动(男性)在筛查突发哮喘病例时比其他病例更常见(表1)⇓和2⇓)。哮喘病例的出生和筛查也比其他病例稍早。
BMI与哮喘发病率
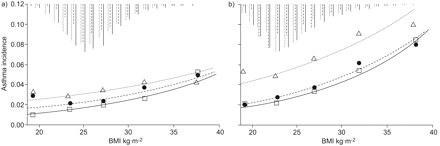
总的哮喘发病率为3.4%。Incidence was highest in current smokers and lowest in never-smokers, higher in females than in males (table 3⇓;图。 2⇓) and positively related to BMI (table 3⇓;图。 2⇓)。There was no significant interaction between BMI and sex (p = 0.25), but the BMI–asthma relationship was significantly weaker in current smokers than in never-smokers (p<0.001 for interaction). As measured by the risk difference, the three smoking groups were more similar (fig. 2⇓;平行曲线将指示等于风险差)。处方率高三倍以上为非常肥胖(≥35的BMI)从不吸烟者比正常体重(20≤BMI<25)从不吸烟者。Treating BMI as a continuous variable, the RR associated with an increase of 3 kg·m−2在BMI调整混杂因素时,从当前吸烟者1.14到从不吸烟者1.27不等。The RRs obtained by adjusting for sex and age alone were very similar to those shown in table 3⇓。
哮喘发病(数的新哮喘例中的风险的受试者数量除以)身体质量指数的(BMI)在一个函数:1)雄性;和b)女性(▵·····:现在吸烟者;•; -------:戒烟者;□; ----:不吸烟者)。The mean BMI for each category (<20, 20–24.9, 25–29.9, 30–34.9 and ≥35 kg·m−2)作为×坐标的点。曲线被装配泊松回归曲线从单变量模型与BMI作为连续变量。直方图代表BMI的相对分布。
使用糖皮质激素定义的持续性哮喘的总发病率为2.7%,与BMI的相关性在偶发的持续性哮喘中通常略高于偶发哮喘(见网上补充资料第1节)。
ΔBMI和哮喘发病率
ΔBMI的方向是未知的,但是,如果体重增加受试者的测量体重在筛选接近报道w马克斯比所报告的w ^最小值,而在其他受试者体重减轻的情况下,改变的方向影响较小(表S2.1在线补充材料)。因此它似乎是合理的使用绝对(direction-free)ΔBMI变量产生影响。之间没有显著的交互自述ΔBMI之前在过去5年筛查和性(p = 0.97)或者吸烟(p > 0.47)。与事件哮喘ΔBMI呈正相关。3公斤·米−2增加ΔBMI在前5年筛查与哮喘发病的风险增加了35%在调整了性别、年龄和吸烟类别(表4所示⇓)。在对包括BMI在内的所有混杂因素进行调整后,RR(95%置信区间(CI))仍然高达1.21(1.16-1.26)。
在每个类别的BMI,范围在20≤BMI < 35岁的RR规定抗哮喘药物高个人报道相对ΔBMI≥10%的筛查体重指数比那些小ΔBMI(表S2.2在线补充材料)。这适用于所有的吸烟类别。
讨论
在中年以后患哮喘,通过使用吸入报销抗哮喘药物作为估计的风险,增加而增加体重。的关系最强在不吸烟者和最弱在当前吸烟者,如由RR测量的。事件发生哮喘的非常肥胖的风险(≥35的BMI)从不吸烟者比正常体重的3.5倍(20≤BMI<25)不吸烟者,调整混杂因素后。The risk of incident asthma in individuals with a self reported ΔBMI of ≥10 kg·m−2在过去的5年筛查之前两倍的那些ΔBMI≤2.5公斤·m−2,然后根据BMI和其他混杂因素进行调整。
优势和局限性
目前研究的主要优势是,它是基于信息测量体重指数和几个重要的混杂因素> 100000健康个体在一个狭窄的年龄范围,以及之间的所有处方吸入抗哮喘药物分配1月1日,2004年和2008年1月1日为同一个人。这种方法消除了关于哮喘事件的回忆偏差问题,并减弱了哮喘季节性变化的任何影响,这些影响可能影响基于具有自我报告的哮喘症状和/或医生诊断的哮喘的横断面调查的患病率估计。
本研究的主要局限是(请参阅下面的讨论)假阴性的可能性(未被发现的轻微哮喘病例)和假阳性(哮喘药物可能已经规定了慢性阻塞性肺病,尤其是吸烟者,或其他疾病)和使用自我报告的数据来计算ΔBMI。另外,被邀请参加健康调查的人中有25%没有参加。如果BMI和哮喘之间的联系在不注意和注意者之间有所不同,那么效果评估就会有偏差,但我们认为,参与率比效果评估更有可能影响患病率评估。此外,患者自我报告哮喘历史被排除在外,和自我报告可能是受到回忆偏倚,但再一次,效果估计只是偏见之间的关系的哮喘和BMI正确那些回忆他们的哮喘之间不同历史和那些没有。
处方药使用气喘代理
假阳性
在挪威,医生在确认病人的症状与哮喘相似后,才会开出抗哮喘药物。我们认为,至少使用两个间隔≥6个月的此类处方作为哮喘病的代理,应该能将误报的数量最小化。正式的验证这种方法没有被执行,但来自荷兰的一项研究发现,在年龄49岁,哮喘病人从处方数据库能够识别一般实践(阳性预测值为0.79当使用至少两个抗哮喘药物在12个月定义标准)19。本研究人群年龄较大(2007年为48-56岁),可能包括接受抗哮喘治疗的非哮喘患者。最相关的例子是与吸烟密切相关的慢性阻塞性肺病(COPD)患者。一项针对挪威成年研究人群的研究发现,与从不吸烟的人相比,目前吸烟者和已戒烟者的调整优势比分别为9.6 (95% CI 3.6-25.2)和5.0 (95% CI 1.8-13.8)25。因此,我们认为目前不吸烟的人群(2007年为48-56岁)中COPD患者的数量较少,但在已戒烟和正在戒烟的人群中,这一数字可能更高。然而,在一项对485名年龄在40-75岁之间的无COPD基线的男性的研究中,13.1%的BMI≤24.3 kg·m−2(tertile 1)在10年期间出现慢性阻塞性肺病,而BMI为26.6 kg·m的人群中,这一比例仅为4.6%−2(tertile 3)26,27。这表明,在目前人群中,肥胖人群中COPD患者的比例可能也低于正常体重人群中的比例,如果有可能消除COPD患者,那么哮喘与BMI之间的关系将比观察到的关系更强。
假阴性
间隔≥6个月的两方定义标准可能导致部分轻度哮喘病例的丢失。在2004-2007年期间,其中一些可能未被诊断,也没有开任何抗哮喘药物。如果一个人因为任何原因去看医生,那么他被诊断出患有轻度哮喘的几率就会增加,而一般的药物流行率也会随着BMI的增加而增加。2004年至2007年间,在正常体重组中有86%的男性接受过至少一次药物处方,在≥35公斤·米组中有96%的男性接受过至少一次药物处方−2组。对女性而言,相应的比例分别为94和98的男性只有12%,而女性的5%,2004 - 2007年期间,没有收到任何处方,并且它们的比例比较高需要有以未被发现哮喘显著影响本研究的结果。
有些人在2004 - 2007年曾收到可能的哮喘的诊断在2004年之前,无需任何抗哮喘药物。在那些谁报的哮喘病史的健康调查,并排除在这项研究中,只有44%的人会被定义为使用本标准哮喘患者。For those who were aged >20 yrs at the first asthma incidence (self-reported age), the percentage was 52, and relatively independent of BMI at screening. This indicates that not all of the subjects who developed asthma before screening were in need of anti-asthmatic drugs during 2004–2007. Thus it is also possible that some subjects may have developed asthma after the screening without any need for anti-asthmatic drugs during 2004–2007. Among the subjects without an asthma history at screening who redeemed anti-asthmatic drugs and got the first prescription in 2004, 12% did not receive any prescription during 2006 and 2007, the proportion being approximately the same in the various BMI groups. In conclusion, there might have been some cases of incident asthma that were not identified in the present study, but, as the probability of not being identified seems to be relatively independent of BMI, the observed relationship between BMI and adult-onset asthma should remain valid.
使用自我报告ΔBMI最大重量为依据
从自我wΔBMI计算最小值和w马克斯在筛查前的最后5年,因此其准确性低于BMI的测量本身。众所周知,自我报告的体重和身高往往分别过低和过高,因此相应的BMI过低28,29。是否有系统性低估或随BMI是不知道,但事实证明,相对ΔBMI随BMI可能表明ΔBMI的随BMI过度报告增加ΔBMI的过度报告。然而,ΔBMI和哮喘之间的相关性仍然存在调整BMI后显著。
ΔBMI的方向是未知的,但是,如果体重增加受试者的测量体重在筛选接近报道w马克斯比所报告的w ^最小值其他科目,减肥,ΔBMI了轻微影响的方向(表S2.1在线补充材料)。因此,虽然定义体重减轻和体重增加的方法并不精确,但它们都与哮喘发病率增加有关,这与Romieu的结果一致et al。10。相反,基于行为变化和肥胖治疗研究的减肥研究显示,许多体重减轻的肥胖哮喘患者的临床状态有了显著改善11,12。
身体质量指数与腰臀比和腰围
腰围和腰围与臀围的比例已被建议为更好的筛选工具比BMI心血管危险因素三十。在71424名研究对象的子样本中,腰围和臀围的测量数据是可用的,腰臀比和腰围与哮喘的关系与BMI大致相同。在对包括BMI在内的混杂因素进行调整后,两者均与哮喘发作显著相关(参见在线补充资料S3部分)。
肥胖和哮喘:可能的机制
许多作者发现了肥胖和哮喘发病率之间的联系,但尚不清楚这种联系是否是因果关系,或者这两种情况是否具有相同的环境、行为或遗传影响。虽然肥胖与哮喘发病之间的确切机制尚不清楚,但一些可能的解释已被提出31。这些措施包括肥胖对肺力学,全身炎症和合并症的影响32。伴随症状包括血脂异常、2型糖尿病、胃食管反流病和高血压。不包括2004-2007年期间配发抗高血压药物(ATC组C02)、脂质改进剂(C10)、胃食管反流疾病药物(A02B)或糖尿病药物(A10)的23141名个体,其RR值为3-kg·m−2BMI增加见表3⇑通过<0.02在所有吸烟类别改变。这表明,这些合并症不解释BMI与哮喘之间的关系在本研究中发现。
促炎细胞因子的增强和雌激素的作用也被提及33。然而,文学是模糊的。巴尔et al。34发现绝经后使用激素与新诊断的哮喘发病率增加有关。相反,卡尔森et al。35研究发现,使用激素替代疗法的绝经后女性在1秒内用力呼气量更高,这也被认为能降低患哮喘的风险。在老鼠哮喘模型中,Matsubaraet al。36描述雌激素如何抑制气道高反应性。在目前的人口中,使用雌激素的比例随着BMI的增加而下降,但排除2004-2007年期间使用雌激素的7000名女性(ATC组G03C), BMI -哮喘的相关性并没有改变,见表3⇑。然而,不能排除的可能性是,一些女性在从筛查到NorPD开始的间隔期间使用雌激素。在评估激素的潜在影响时,使用的时间和持续时间以及剂量似乎都是非常重要的。这一点在妇女健康倡议研究中得到了明确的证明,该研究关注的是对冠心病的影响37。
感兴趣的语句
没有宣布。
脚注
这篇文章有补充材料可从www.www.qdcxjkg.com
- 收到了2008年12月19日。
- 接受2009年11月27日。
- ©人队