文摘
闭塞性细支气管炎综合征(BOS)是一个主要的并发症肺移植与贫穷有关的生存。国际社会对心脏和肺移植,美国胸腔学会和欧洲呼吸学会召开的一个国际专家委员会来描述和/或提供建议1)BOS的定义,2)风险因素发展BOS, 3)的诊断BOS, 4) BOS的管理和预防。188bet官网地址
务实的证据合成进行了识别所有独特的BOS相关引用从1980年到3月出版,2013年。专家委员会讨论的可用性研究证据更新BOS的定义,识别风险因素和建议。委员会随后年级(分级的推荐、评估、开发和评估)方法来开发特定的临床建议。
BOS应该使用这个词来形容延迟的同种异体移植物功能障碍与持久用力呼气量下降1 s,不是由其他已知和潜在可逆的移植后肺功能丧失的原因。委员会制定具体建议关于系统性皮质类固醇的使用,环孢霉素,他克莫司、阿奇霉素和疑似和确诊患者BOS的筛选标准。
BOS的诊断需要注意排除其他移植后并发症会导致延迟移植肺功能障碍,和几个危险因素已确定有显著联系BOS的发作。目前可用的治疗方法还没有被证明导致重大BOS的预防或治疗中获益。充分设计和执行随机对照试验,正确衡量和报告所有patient-important结果需要确定最优治疗建立BOS和有效的防治策略。
文摘
BOS需要仔细的诊断排除其他并发症会导致延迟移植肺功能障碍http://ow.ly/AZmbr
执行概要
许多肺移植受者开发延迟同种异体移植物功能障碍,传统上称为闭塞性细支气管炎综合征(BOS),这被认为是由炎症引起的,破坏和纤维化肺小航空公司的同种异体移植物导致闭塞的毛细支气管炎(OB)。因为确诊OB很难使没有外科肺活检,减少1 s (FEV的用力呼气量1)已经被用来作为替代指标来确定开发一个综合症患者的肺移植的重要和持久的损失函数出现三个或更多个月后移植。然而,现在认识到,许多因素除了OB会导致延迟性,肺功能明显下降,这些原因的延迟性移植功能障碍时,必须仔细地排除诊断的BOS。一般来说,BOS的治疗反应不佳但可能稳定,和一些患者可能FEV的显著改善1与某些疗法。
全面审查关于肺移植的文献和BOS允许委员会得出的结论,给出了表1。此外,委员会成员用系统化的方法制定一些具体的循证建议BOS的预防和管理,给出了表2。证据表在网上提供的补充材料。我们希望这条指导原则将促进当前的理解方法的评价和管理肺移植受者开发延迟同种异体移植物功能障碍,以及刺激进一步的研究提供高质量的证据可能基于未来的指导方针。
范围和目的
本文档的目的是修改BOS的定义,讨论了风险因素BOS的发展,并提供指导疑似或确诊患者BOS的管理。这些指导方针的目标受众是呼吸内科专家管理成人和儿童接受肺移植。其他呼吸医学专家也可能受益于这些指导方针。
介绍
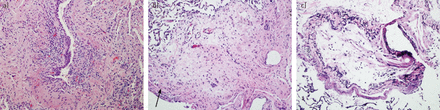
OB,于1984年首次描述的心肺移植受者(1),被认为是肺移植后肺同种异体移植物功能障碍的主要原因(2- - - - - -5]。移植后OB的特点是逐步消灭小航空公司(图1),通常是伴随着肺活量的肺功能指标的持续下降,通常是阻塞性肺量测定的模式,本质上是清晰的胸片(4]。然而,OB很难检测到通过transbronchial肺活检,不能自信地诊断通过非侵入性测试(6- - - - - -10]。因此,以前公布的共识声明指定FEV持续下降1移植后FEV≤80%的基线1存在至少3周(没有混杂的条件)的替代标记可能OB, FEV1被称为BOS[下降4,5]。
)闭塞性细支气管炎在部分外科肺活检术腔的妥协伴随着轻微的慢性炎症在墙上和焦黏膜溃疡。b)闭塞性细支气管炎与完整transbronchial活检腔的消亡。缺乏细支气管肌(箭头所指)有助于识别伤痕累累结构残余气道(苏木精和伊红染色)。c)的弹性组织染色稍微更深的部分相同的细支气管(b)所示突显出剩余弹力。在右边的伴随动脉相比,只有一个弹性薄板在细支气管壁。原来放大:100×。
BOS分类方案,采用1993年(4),提供分期系统,基于移植后肺功能衰退的严重性,已经用于临床决策和研究目的。这个分期系统是最近2002年的修改(表3)[5]。FEV基线值1和用力呼气流量用力肺活量(FEF的25 - 75%25 - 75%)被定义为每个测量的两个最高的值的平均值,得到至少3周移植后没有一个支气管扩张剂的政府。来帮助区分BOS和急性或亚急性肺移植的并发症,并考虑建立一个基线FEV所需的时间1FEV的下降1确定两个FEV1测量执行3周,根据定义,三个或更多个月是需要经过移植的时间为了BOS的诊断是(4,5]。此外,它变得明显,肺功能下降符合BOS可以稳定在某些病人的诊断,而不是导致持续、渐进的同种异体移植物功能恶化和贪污损失。因为担心设置FEV的截止值1在80%最好的移植后价值可能对早期的同种异体移植物功能下降由于早期OB, BOS年级0-p(≥10%,但< FEV下降20%1和/或FEF下降≥25%25 - 75%)添加到暂存系统中表示“潜在BOS”(5]。
BOS影响50%或更多的受者生存超过5年,占相当比例的情况下移植肺失功和接受者超出3个月移植后死亡。它是死亡的主要原因为受者存活超过1年移植后(2,3],普遍认为免疫相关的生理代孕现象由于许多观察,包括其发生急性细胞排斥反应协会(11),受者的趋势发展BOS有更大程度的人类白细胞抗原(HLA)不匹配12),和积累的证据自身免疫途径的参与13]。此外,OB有惊人的相似之处,也可能发生在同种异体骨髓或干细胞移植受者以及结缔组织疾病,患者也视为同种免疫的或自身免疫性疾病,分别。因此,BOS经常等同于术语慢性排斥反应。然而,各种干预措施,包括强化免疫抑制,可能很少或根本没有影响患者的同种异体移植物功能BOS的逐步丧失。此外,许多多发地机制也被牵连或建议在BOS发病机制中发挥作用。这些包括气道损伤由于原发性移植物功能障碍(PGD) gastro-oesophageal回流(工资),各种感染和气道局部贫血由于破坏支气管循环14- - - - - -16]。这些“无免疫力”因素可能促进组织损伤和炎症,反过来加剧进行同种免疫的接受者的反应。建立OB炎症的证据显示变量,同种免疫的反应,自身免疫,fibroproliferation气道闭塞导致同种异体移植物的气道重塑和损失函数(14- - - - - -16]。OB可能代表最后一个共同的端点为各种形式的同种异体移植物损伤。
因为BOS临床定义为是一个持续的肺功能下降,FEV移植后下降1可能会错误地认为只由于OB。它已经越来越认识到其他同种异体移植物疾病可以发生在慢性移植后设置(表4)。这些实体的一些可能导致同种异体移植物功能障碍可能不可逆,但满足肺活量的BOS的诊断标准,尽可能多的这些实体也可能导致FEV持续减少1。可以进一步复杂化,同时存在其他病理生理实体(感染、各种形式的排斥和弥漫性肺泡损伤)当OB也出现在同种异体移植物。
这个国际社会对心脏和肺移植(ISHLT) /美国胸科学会(ATS) /欧洲呼吸学会(ERS)临床实践指南提供了一个全面的,概念上的平衡和以证据为基础的角度,探讨了概念有关的诊断和管理BOS以来出现在医学文188bet官网地址献第一次描述这种综合症。它的目的是提供指导管理只要有可能,和识别差距在知识和需要解决的问题通过额外的基础和临床研究。应该承认,绝大多数患者发表文献中描述已经成人,和一些建议可能没有公司当应用于儿科基础肺移植受者。
如何使用这些指导方针
ISHLT / at /人的管理指导方针BOS不是为了征收标准的护理。他们提供理性决策的基础管理的疑似或确诊患者BOS。临床医生、患者、第三方支付者,机构审查委员会、其他利益相关者或法院不应该认为这些建议是规定。没有指导方针和建议可以考虑所有的经常引人注目,独特的个人临床环境。因此,没有人负责评估临床医生的行动应该试图应用这些指导方针的建议死记硬背或毯子的方式。
语句的基本价值观和偏好以及附带的资格评论每个推荐组成部分和服务促进更准确的解释。引用时不应忽略或者从这些指南翻译的建议。
方法
一个ISHLT, ATS和赞助的人特别的委员会举行预备会议在2008年4月和5月开始的过程识别和优先主题覆盖着这条指导原则。椅子被批准的三个社会。小组成员被确定为领导人在肺移植领域,选择从建立移植中心在世界范围内,椅子,审查现有的文献和回答根据公布的证据或临床问题,当这样的证据是缺乏,基于观察的临床实践提供指导。委员会的所有成员披露潜在的利益冲突,这是审查根据ISHLT的政策,ATS和人。每个委员会的成员参与开发本文档提供的结论和建议。
一个全面的文献检索是由一个医学图书馆员。PubMed接口是用来搜索MEDLINE相关出版物(原创文章和系统评价)从1980年到2009年英语。搜索更新两次,2012年3月,2013年。搜索条件包括“肺移植”、“闭塞性细支气管炎综合征”和术语特定管理选项在临床考虑的问题。总共031手稿被确定使用电子搜索。相关的出版物被委员会成员使用预先确定的入选标准,选择和选择文章的参考文献综述了确定额外的文章。务实的证据合成主要是定性的而不是定量的(即。一些数据可能汇集通过荟萃分析)。这条指导原则的方法总结表5。
委员会的成员提供整个编译文件的收集和解决特定主题小组委员会成立。每个小组委员会审查、评价和总结相关的证据。年级(分级的推荐、评估、开发和评估)方法用于评价的证据的质量相互支持的建议。临床治疗相关的问题与没有治疗,一个治疗与人口替代治疗,或治疗建议,回答了在制定和使用等级分级方法(表6)[17]。有分歧的讨论和解决的共识。最后建议和成绩被整个委员会审查和批准9月,2013年。与其他系统的开发建议,委员会的结论是基于文献评价和委员会审议。
强烈建议是如果委员会感到自信之间的平衡的和不受欢迎的后果。有条件的建议是如果委员会感到信心不足的理想之间的平衡和不受欢迎的后果。建议的影响强度的因素,包括估计的效果理想和不良结果的兴趣,信心这些估计的影响,估计价值和偏好和资源使用。在任何情况下适当的行动取决于临床上下文。委员会的判断的基本价值观和偏好消息灵通的患者根据委员会成员的临床经验。证据表总结每个推荐的相关文献在网上提供的补充材料。
委员会发现很少有实验研究BOS的管理。数据是非常有限的由于小数量的科目。因此,大多数的建议是基于观察性研究有或没有一个对照组和委员会成员的临床经验(即。从他们的临床实践)无组织的临床观察。
术语用于BOS
几个潜在的混杂状况可逆的同种异体移植物功能(可能导致延迟下降表4)。当这样的实体被排除在外,FEV大幅下降1符合标准BOS, BOS可能的诊断。然而,BOS阻塞性生理可能是最近描述实体的区分限制性的同种异体移植物综合症,限制性的生理学特征的同种异体移植物实质纤维化的证据(18]。因此,它应该认识到,不是所有的病人谁FEV的下降1和/或气流阻塞发展一定弄错。此外,神秘OB可能不显示在同种异体FEV的重要模式1减少会议目前公认的诊断标准BOS [19,20.]。
术语慢性肺部同种异体移植物功能障碍(复合)已经被用于参考BOS和慢性排斥反应,和这三个术语交替使用出版的手稿。然而,复合是一个术语,需要有一个严格的和被广泛接受的定义。不加选择的,可以互换使用这些术语可能被视为表明FEV的下降1总是显示OB的存在由于慢性排斥反应,但FEV1下降可能会由于各种原因如上所述。
BOS表型
病人组与特定属性或模式的识别疾病可能允许的特定风险因素的识别,发病的疾病机制,和/或治疗和预防策略,属于一个可识别的子集(表现型)BOS患者。患者早期FEV下降的模式1符合BOS标准可能代表一个BOS表型有更严重的和侵略性的OB,它的特点是快速进展和预后不良(19,21- - - - - -23]。然而,一些患者肺功能迅速下降可能稳定,尽管最初的迅速出现和肺功能损失(24]。最近文献中另一个潜在的BOS表型建议由接受者重要支气管肺泡灌洗(BAL)嗜中性应对阿奇霉素治疗(25,26];FEV1可以改善这样接收者不再满足BOS肺活量的标准。这些患者出现可逆,BOS-like综合症与BAL嗜中性,最近出版的,随机的前瞻性临床试验由V操作系统等。(27)建议预防性管理阿奇霉素发起移植后不久可以抑制这种综合症的发展。患者符合BOS标准但不应对阿奇霉素可能代表一个表型fibroproliferative OB (25]。尽管如此,不同的表型的BOS基于特定风险因素(表7)或其他参数尚未完全建立。
风险因素与BOS的发展
Non-minimal (≥A2级)急性细胞排斥反应和淋巴细胞性细支气管炎
A2级或以上急性细胞排斥反应肺活检(28BOS)与后续发展(6,29日- - - - - -36]。晚期急性细胞排斥反应(30.,31日,33越来越频繁和严重的急性细胞排斥反应(6,30.,33被发现是BOS的危险因素。大多数调查发现,急性细胞排斥反应是一个主要的风险因素BOS即使其他临床事件所占时间Cox回归模型和多元分析。乙级拒绝(淋巴细胞性细支气管炎(磅))也被视为一个风险因素发展的BOS [30.,33,34,37,38]。
我们的文献检索发现没有研究比较了增强免疫抑制和增强免疫抑制患者non-minimal (≥A2级)急性细胞排斥反应或磅。这些研究将不会执行,因为non-minimal增强免疫抑制急性细胞排斥反应或磅是如此被广泛接受,对照组是可能的(不太可能即。患者不太可能接受的机会被放置到没有增强免疫抑制组)。然而,我们确定了两个相关的研究支持这一概念,增强免疫抑制可能降低BOS的风险患者non-minimal急性细胞排斥反应或磅(33,39]。
第一项研究是一个病例对照研究发现患者BOS更有可能有不足维护免疫抑制(环孢霉素、咪唑硫嘌呤和强的松,环孢霉素水平< 200 ng·毫升−1)比没有BOS的患者(p < 0.0001) (33]。第二项研究是一系列案例显示,增强免疫抑制与改善或消除细胞排斥在年级A2急性细胞排斥反应患者的54%,48%,A3级急性细胞排斥反应,83%品位A4急性细胞排斥反应,患者和43%的磅;患者急性细胞排斥反应或磅改善和解决通常保持稳定(9]。急性细胞排斥反应和磅标记(即。代理措施BOS)的风险。系列没有衡量发达BOS许多病人,也没有指定哪个方案(s)被用来增加免疫抑制(在线补充表S2a)。
在决定是否增强免疫抑制是必要的,防止BOS上面描述的可能性必须平衡的伤害增加免疫抑制。这种平衡会有所不同取决于所选择的方案;然而,短疗程的全身性类固醇是最常见的方案选择(40]。最好的证据有关的潜在不利影响的短期课程系统性类固醇是间接的,从随机试验进行了推断患者有慢性阻塞性肺疾病(COPD)的恶化。这些试验发现,短期课程的系统性类固醇增加不良反应的发生率,尤其是高血糖症和体重增加(在线补充表S2a)。
我们对报告的准确性的信心的影响增强患者的免疫抑制的发展BOS non-minimal急性细胞排斥反应或磅(即。证据的质量很低。这是因为估计源于一项观察性研究和案例系列,由偏见的风险有限,小样本大小,模棱两可的人口(包括所有移植后患者而不是专门non-minimal患者急性细胞排斥反应或磅(33]),模棱两可的结果(急性细胞排斥反应的变化或磅,而不是BOS的发展(39])。我们对报告的准确性的信心全身性类固醇的副作用是moderate-to-high因为估计来自随机试验,其中一些被小样本量有限(在线补充表开通)。
委员会建议增强免疫抑制患者non-minimal急性细胞排斥反应或磅为了防止BOS。这是根据我们的评估,最常见的潜在好处方案用于增强免疫抑制(短疗程的系统性类固醇)大于风险的重要性(即。防止危及生命的并发症与高血糖症和体重增加)和持续时间(即。潜在的好处是长期的,而风险是只有短期和可逆在停药治疗)。此外,短疗程的全身性类固醇并不过分昂贵的繁琐和委员会的集体临床观察表明,从这些疗法有有益的影响在这个病人的人口。
建议是有条件的,因为非常低质量的证据提供了确定性,增强免疫抑制的理想效果超过了不良的后果。虽然最初的方法增加免疫抑制全球在此设置通常受雇于移植中心静脉注射给予大剂量糖皮质激素(如。甲基强的松龙在1000毫克每日3天),可能需要其他疗法(如。排斥lymphodepletion-inducing代理)。各种变化维护免疫抑制药物疗法也可能是适当的(参见推荐4)。
建议1
对肺移植受者non-minimal急性细胞排斥反应(≥A2级)或淋巴细胞性细支气管炎transbronchial肺活检标本,我们建议增强免疫抑制过程的系统性类固醇来防止BOS的发展(有条件的推荐,非常低质量证据)。
价值观和偏好
这个建议高度重视防止危及生命的并发症肺移植和低价值避免短期的负面影响。
讲话
典型课程系统性糖皮质激素用于增强免疫抑制的成人接受静脉注射甲基强的松龙1000毫克每日3天(许多中心使用10 - 15 mg·公斤−1每天为较小的患者)。
最小(A1级)急性细胞排斥反应
最小的急性细胞排斥反应的重要性(A1级)是有争议的。Hopkinset al。(41)报道,A1级急性细胞排斥反应仍然是相对普遍的监视transbronchial活检移植后2年。可用的研究表明,患者的多个集A1级拒绝BOS早期发作,和一个集A1拒绝被发现与进展相关独立BOS (42]。
我们搜索确定了两个观察性研究表明增强免疫抑制最小(A1级)急性细胞排斥反应可能会降低患BOS的风险(41,43]。在一项研究中,静脉注射类固醇,后跟一个圆锥形的口服类固醇并不与发展BOS相关(p = 0.48),而缺乏系统性治疗类固醇与发展BOS相关(p = 0.01)43]。在其他研究中,课程的口服类固醇减少发展到更高等级的急性细胞排斥反应和磅(BOS)标记的风险16.7%和15.6%,分别为(41]。无论是研究报告的副反应的全身性类固醇(在线补充表S3a)。
在决定是否增强免疫抑制是必要的,防止BOS上面描述的可能性必须平衡的伤害增加免疫抑制。最好的证据关于短期课程系统性类固醇的副作用是间接的,从随机试验进行了推断患者有慢性阻塞性肺病的恶化。这些试验发现,短期课程的系统性类固醇增加不良事件的频率,尤其是高血糖症和体重增加(在线补充表S3b)。
我们对报告的准确性的信心的影响增强患者的免疫抑制的发展BOS最小急性细胞排斥反应(即。证据)的质量很低,因为估计来自于观察性研究的风险是有限的偏见,模棱两可的结果(测量发展为更高等级的急性细胞排斥反应和磅而不是发展BOS [41])或使用一种间接比较器(看着协会分别在治疗和治疗病人,而不是直接比较治疗不治疗(43])。我们对报告的准确性的信心全身性类固醇的副作用moderate-to-high是因为因为估计来自随机试验,其中一些被小样本量有限(在线补充表S3b)。
委员会表明,临床意义上的最小的急性细胞排斥反应患者全身性类固醇的治疗。这反映了委员会的判断可能的好处(即。防止BOS)治疗超过风险(即。高血糖症和体重),这样患者的成本和负担。基本原理与全身性类固醇治疗最小的急性细胞排斥反应类似于提供早期治疗non-minimal急性细胞排斥反应和全身性类固醇磅。建议有条件的,因为理想的平衡与不良后果的不确定性是由于非常低质量的证据,以及不确定性是强化了委员会的临床经验。相比之下,为临床稳定的A1级患者急性细胞排斥反应监测活检,决定是否立即治疗患者免疫抑制或增强观察和重复活检之前决定增加免疫抑制应视情况而定。
建议2
肺移植受者的临床重要的最小的急性细胞排斥反应(A1级)transbronchial肺活检标本,我们建议增强免疫抑制过程的系统性类固醇来防止BOS的发展(有条件的推荐,非常低质量证据)。
价值观和偏好
这个建议高度重视防止危及生命的并发症肺移植和低价值避免短期副作用。
讲话
我们认为A1级急性细胞排斥反应是临床上重要的如果它与临床表现相关联,如症状(如。呼吸困难、疲劳或最近诊断为咳嗽)或目标测量(如。FEV下降1与移动或oxyhaemoglobin稀释),表明同种异体移植物功能障碍的存在。典型的全身性类固醇增加免疫抑制用于成人接受静脉注射甲基强的松龙1000毫克每日3天(许多中心使用10 - 15 mg·公斤−1每天为较小的患者)。
其他风险因素
其他风险因素的发展BOS讨论了在线补充材料,包括anti-HLA抗体的存在(44- - - - - -48],PGD [49- - - - - -52)和重要程度(异常)气油比的存在(53- - - - - -55]。附加相关的风险因素包括病毒感染(29日,31日,32,56- - - - - -64年),细菌感染(65年- - - - - -68年)和真菌感染(69年- - - - - -71年]。巨细胞病毒感染先天和适应性免疫成分,导致upregulation HLA类的我在上皮细胞和类II抗原(72年,73年),刺激和增加同种异体免疫反应的生成和促炎细胞因子(72年,74年]。瞬态气道细菌殖民化可显著提高BAL中性粒细胞和其他肺部炎症指标(75年]。Botha等。(53连续]检查155肺移植和报道新创同种异体移植物殖民与铜绿假单胞菌显著相关,BOS移植后2年内发展。V操作系统等。(54)报道,持续假单胞菌BOS殖民是一个更大的风险新创殖民。此外,克ottlieb等。(55)发现持久的同种异体移植物殖民假单胞菌在接受者与囊性纤维化BOS的患病率显著增加。V的爱人等。(69年)确定真菌肺炎或肺炎作为一个独立的预测随后的BOS,和Weigt等。(70年)报道,曲霉属真菌殖民化是独立BOS相关的后续发展。
一个前瞻性研究,监测外周血单核细胞反应54肺移植受者在7年时间内显示一个强大的协会胶原蛋白V-specific反应与发病率(风险比为5.4(人力资源)BOS BOS 2级1级和9.8人力资源)和严重性BOS [13),诱导胶原蛋白V反应与异常有关气油比和BOS的发展(76年]。此外,年代爱伲人等。(77年)发现一个强大的协会之间的外观供体特异性anti-HLA抗体和抗体的检测针对自体抗原(胶原蛋白V和K-α1微管蛋白)的回顾性分析42例肺移植受者BOS。
众多研究显示中性粒细胞招募的证据和激活落下帷幕在接受者急性排斥反应时,感染和/或BOS [78年- - - - - -81年]。Neurohret al。(82年)发现,BAL嗜中性是后续BOS的预测。年代chloma等。(83年)也报道,增加BAL中性粒细胞与早发性BOS相关,和随后的调查由Gottlieb等。(26)和V操作系统等。(25BOS)也与BAL嗜中性。
建议减少风险因素BOS超出这条指导原则的范围,但可以解决在未来指导方针。
BOS的诊断
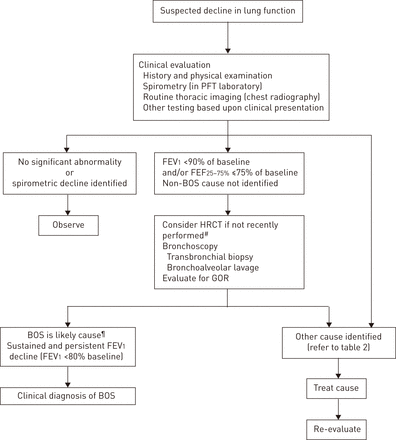
一个FEV1衰退将引发担忧,移植物功能障碍和可能BOS演变,从进化和相当大的同种异体移植物损伤BOS FEV可能已经发生的时间1从其基线值下降了20%。当稳定的患者出现临床症状(如。呼吸困难、咳嗽、疲劳或发烧)和/或(FEV下降迹象1在家里呼吸量测定法或诊所访问后续评估)可能表明同种异体移植物功能障碍,综合评价确定原因通常是启动(图2)。这通常包括一个常规评估在诊所,紧随其后的是特定的测试(成像,证实肺量测定法和支气管镜检查显示)来识别一个特定的肺功能下降的原因或原因。如果BOS似乎是肺功能下降的原因,在下一节中讨论的治疗方法可以考虑。
临床评估算法疑似闭塞性细支气管炎综合征(BOS)。这个算法是一个集体的描述临床实践委员会的成员。它不是基于循证诊断系统的开发建议。击球:肺功能测试;FEV1:在1 s用力呼气量;FEF25 - 75%:用力呼气流量在25 - 75%的用力肺活量;HRCT:高分辨率计算机断层扫描;气油比:gastro-oesophageal反胃。#:获得吸气和呼气的观点来评估空气滞留;¶:闭塞性细支气管炎的存在病变在肺活检(如果获得)被认为是诊断和HRCT的发现与毛细支气管炎一致(如。困气)支持,严格的同种异体移植物综合症是一种诊断考虑如果找到限制模式在肺功能测试。
lama等。(84年)发现的概率测试阳性BOS FEV 0-p年级1标准是71%,发病前2年BOS和FEV的特异性1在单肺移植受者标准是93%。Hachemet al。(85年]报道的阳性预测值为79%,阴性预测值为82%阶段0-p FEV1标准203年成人双边肺移植受者,但FEF25 - 75%0-p标准有可怜的预测价值。BOS的患病率研究41 - 63%取决于所使用的标准来定义BOS。相比之下,N收听等。(86年)发现了FEF的敏感性80%,特异性82.6%25 - 75%0-p标准在一群43单肺移植受者。这些研究之间的差异可能与不同的统计技术,样本大小和随访时间。
高分辨率计算机断层扫描(HRCT)可能检测诊断有用pleuroparenchymal变化和/或空气滞留常规胸片是麻木不仁87年- - - - - -94年]。支气管镜肺活检(TBLB) transbronchial落下帷幕是有用的和检测感染或其他实体可能会造成功能下降。虽然变化和OB可能取得一致通过TBLB,非手术肺活检是不敏感,缺乏变化的OB TBLB可怜的预测价值。虽然许多的潜在生物标志物BOS已报告在文献中,没有被确认为有足够的敏感性和特异性。
评估和/或筛查儿童肺功能的变化是特别具有挑战性的,而且4岁以下的儿童可能无法进行肺量测定法,需要专门的方法(95年,96年]。儿科中心可能会使用替代肺功能测量或成像模式,如通气/灌注扫描和吸气呼气HRCT扫描,提高检测存在的气流阻塞的能力。因为TBLB很难执行在婴儿和小孩,很多儿科中心使用外科肺活检证实诊断为疑似OB (97年]。
诊断建议BOS超出这条指导原则的范围,但可以解决未来的指南。
BOS的治疗和预防
加强药物免疫抑制没有BOS没有混杂因素的影响如急性细胞排斥反应,抗体介入拒绝或缺乏BAL嗜中性。
长期大剂量糖皮质激素
持续治疗高剂量皮质类固醇(≥30毫克·天−1强的松或一个等价的)没有显示改善BOS,和这样的治疗与众多,经常严重副作用(98年]。搜索确定一系列案例10患者肺功能下降符合BOS [99年]。所有10个病人表现出进步的肺功能下降,尽管接受大剂量甲基强的松龙。不利影响的持续大剂量甲基强的松龙没有报道系列;然而,有间接的证据从慢性肺部疾病患者,持续的高剂量皮质类固醇对患者有害。具体来说,持续的高剂量皮质类固醇增加骨质疏松性骨折的发生率,白内障和消化不良。发现,持续的高剂量皮质类固醇诱导肺功能上没有任何有益的效果,但引起许多严重的不利影响,是由委员会成员的集体临床观察(在线补充表S4a)。
我们对报告的准确性的信心持续高剂量皮质类固醇的影响患者的肺功能FEV的下降1与BOS一致(即。证据)的质量很低,因为估计来自于一个小案例系列。我们对报告的准确性的信心全身性类固醇的副作用从低到高不同取决于结果,因为估计来自于观察性研究的一个结果(骨质疏松性骨折)升级有剂量反应梯度和影响被认为即使混杂因素倾向于低估(在线补充表S4b)的影响。
我们建议不使用大剂量持续系统性糖皮质激素的患者FEV的下降1符合BOS由于缺乏效益和潜在的严重副作用。建议有条件的,因为证据提供了非常低的信心持续高剂量全身糖皮质激素的影响。
建议3
对肺移植受者开发FEV的下降1符合BOS的发病,我们建议临床医生不要使用长期、大剂量糖皮质激素(有条件的推荐,非常低质量证据)。
价值观和偏好
这个建议高度重视避免有害影响由于无效的治疗方法。
讲话
我们将持续高剂量皮质类固醇管理定义为≥30毫克·天−1强的松或一个等价的配方。
环孢霉素转化为他克莫司
如果病人正在接受环孢霉素本文免疫抑制,从环孢霉素A他克莫司一直缓慢,据报道,肺功能损失在很多情况下系列99年- - - - - -108年]。然而,没有进行随机试验来支持这个开关。
我们的搜索找到10个病例分析,描述转换的影响环孢霉素在BOS肺移植患者他克莫司。六个系列的报道缓解转换后的肺功能下降,而剩下的四大系列报道后改善肺功能转换。大多数情况下系列没有提及负面影响;然而,那些评估肾毒性或高血糖症报道频繁上升血清肌酐和葡萄糖水平。没有描述的病例分析感染或恶性肿瘤(在线补充表S5a)。
有间接的证据从随机试验的病人在接受肾移植表明他克莫司不增加感染的风险,恶性肿瘤,肾毒性或高血糖症与环孢霉素(相比109年]。我们没有理由相信他克莫司和环孢霉素是不同的不利影响肺移植患者与肾移植患者相比。
我们对报告的准确性的信心将环孢霉素转换为他克莫司对肺功能的影响,肾毒性和高血糖症(即。证据)的质量很低,因为估计来自小案例系列(在线补充表S5b)。
在肺移植受者开发BOS接收维护免疫抑制方案,包括环孢霉素,我们表明,环孢霉素是转换为他克莫司。这反映了委员会的意见,可能减轻或逆转肺功能下降的好处大于风险的增加血清肌酐和/或血糖水平。可取的建议是有条件的,因为平衡和不受欢迎的后果是非常不确定的,由于非常低质量的证据。
推荐4
肺移植受者发展BOS而接受慢性免疫抑制方案,包括环孢霉素,我们建议换他克莫司的环孢霉素(有条件的推荐,非常低质量证据)。
价值观和偏好
这个建议的地方更看重缓解肺功能下降和低价值避免肾毒性和高血糖症。
讲话
环孢霉素的转换他克莫司通常是由停止环孢霉素和启动他克莫司虽然是暂时性的增加维护皮质类固醇剂量,直到他克莫司血水平确定达到期望的目标区间。他克莫司的目标治疗血槽水平通常被认为ng范围从5到15毫升−1为患者≥18岁一旦达到一个稳定的状态。
阿奇霉素
有利影响已报告大约为35 - 40%的肺移植受者用阿奇霉素治疗(25,26,110年- - - - - -116年]。完成逆转FEV1下降可能发生在一些病人,BAL患者嗜中性似乎代表一个子集的患者,尤其可能对阿奇霉素治疗(25,26,114年]。
我们的文献检索发现了10个研究(一个观察性研究和9例系列),描述了阿奇霉素的影响和BOS肺移植患者的肺功能。研究发现,30 - 83%的患者改善肺功能(定义为FEV的增加1≥10%)收到阿奇霉素后,即使意味着FEV1没有增加在一些研究中因为nonresponders继续有肺功能下降。此外,两个观察性研究发现,描述了阿奇霉素对死亡率的影响肺移植患者BOS。这两项研究发现,早期治疗,降低死亡率在一些病人。在一项研究中,肺移植患者BOS第一阶段接受阿奇霉素死亡率要低于那些没有收到阿奇霉素(HR 0.29, 95% CI 0.11 - -0.82)。患者死亡率下降并不是出现在BOS第二阶段(116年]。在其他的研究中,40%的患者对阿奇霉素和患者死亡率的减少(HR 0.96, 95% CI 0.95 - -0.98)。反应者倾向于接受阿奇霉素post-transplantation早些时候(25]。大部分的研究没有提到的不利影响;然而,报告最常见的不良反应是恶心、腹泻、消化不良和结肠炎,发生在不到5%的患者(在线补充表S6a)。
有间接证据从其他条件的随机试验,可能更好的估计从阿奇霉素不良反应的发生率。12个随机试验的荟萃分析1406例接受阿奇霉素治疗急性下呼吸道感染244年发现的1363名患者(17.9%)开发了一个不良事件(117年]。大多数的不良事件是轻微的恶心和腹泻。研究被我们的系统回顾和荟萃分析的阿奇霉素对下呼吸道感染,报道致命的心律失常。然而,有其他的证据表明,阿奇霉素与致命的心律失常。在一项观察性研究,研究了超过一百万个实例服用阿奇霉素,病人服用阿奇霉素更有可能遭受致命的心律失常比那些没有采取一种抗生素(风险比为2.85,95%可信区间1.13 - -7.24)(118年]。绝对致命的心律失常的风险在阿奇霉素治疗小(1.1例每1000人每年)的风险并没有增加与患者服用另一种抗生素(危险比为0.93,95%可信区间0.56 - -1.55)(118年]。这些发现支持了阿奇霉素(制造商进行的另一项研究119年]。还有来自一个随机试验的证据,COPD患者治疗慢性阿奇霉素治疗更有可能经历一个衰减在听力和殖民azithromycin-resistant生物(120年]。
我们对报告的准确性的信心阿奇霉素的审判对肺功能的影响,生存,肠胃不适和过敏反应很低,因为估计主要来自案例系列和一些小的观察性研究(在线补充表S6b)。同样,我们对报告的准确性的信心阿奇霉素的审判对致命的心律失常的影响很低,因为它来自于观察性研究在不同的患者人群。报道致命的心律失常的相关性肺移植患者是不确定的,因为肺移植受者统一筛选排除存在显著的冠状动脉疾病或心脏功能障碍之前被列出的移植。最后,我们对报告的准确性的信心影响审判的阿奇霉素对听力损失和殖民的收购azithromycin-resistant生物体是温和的,因为它来自一个随机试验用不同的患者人群。
我们建议阿奇霉素的审判肺移植受者BOS发展。这反映了委员会的判断,改善肺功能和降低死亡率的重要性超过轻微肠胃不适的风险,听力下降,殖民azithromycin-resistant生物体,罕见的致命的心律失常和罕见过敏反应。建议是有条件的,因为我们非常低的信心报告影响提供了有限的好处(改善肺功能和降低死亡率)超过潜在不良事件(恶心、腹泻、致命的心律失常,听力下降,殖民azithromycin-resistant生物和过敏反应)。
建议5
对肺移植受者开发FEV的下降1符合BOS的发病,我们建议的审判阿奇霉素(有条件的推荐,非常低质量证据)。
价值观和偏好
这个建议高度重视预防肺功能恶化,并可能减少死亡率,避免不利影响和较低的价值。
讲话
阿奇霉素通常每天口服250毫克的5天,然后每周3次250毫克。我们定义了一个审判的阿奇霉素与阿奇霉素治疗持续至少3个月。另外,目前尚不清楚1)阿奇霉素是否应该继续长期有益的反应是观察,或2)是否应该停止期间如果肺功能不显示改善后续的临床评价。
抗反流手术
异常气油比(通过食管pH值识别探针在大多数研究)是非常普遍的在晚期肺病患者和肺移植受者(65年,66年,68年,121年- - - - - -126年),它已经涉及BOS[作为一个风险因素65年,66年,68年,127年,128年]。出于这个原因,委员会成员经常测试新发病患者BOS气油比。近端研究胃肠道蠕动和pH /阻抗测试可以用来诊断运动性异常和异常酸和/或non-acid气油比(129年]。此外,检查标记落下帷幕的愿望(如。油红O染色和决心的脂质指数,落下帷幕落下帷幕流体液体胃蛋白酶和胆汁酸)的检测报告为有用的microaspiration回流gastro-oesophageal材料(66年,130年,131年]。然而,额外的气油比和BOS落下帷幕的标记关联的研究愿望需要促进接受者的选择和BOS可能受益于腹腔镜fundoplication等干预措施。
抗反流手术(如。Nissen fundoplication和Toupet fundoplication)可以安全地进行肺移植候选人与晚期肺病或肺移植受者记录异常气油比(123年,124年,127年- - - - - -129年,132年- - - - - -138年胃分泌物的),从而防止回流,愿望和相关的后遗症。
我们的文献检索发现三个观察性研究和5例系列报道的抗反流手术对肺功能的影响和死亡率在肺移植受者。七个八个研究发现,FEV1改善抗反流手术后(包括这两项研究,特别考察了肺移植受者BOS)和长期生存所描述的两个研究报告改善生存的抗反流手术后(在线补充表S7a)。
关于安全的抗反流手术,一个观察性研究和三个案例系列报道集中时的并发症率不到5%。同样,一个观察性研究和6例系列报道的围手术期死亡率低于1%时集中。三个案例系列报道,6 - 14%的患者出现术后吞咽困难(在线补充表S7a)。也有间接证据的抗反流手术的安全性,可以推断从nontransplant倾心于患者。考虑下面的例子。在一个系统的回顾,三个随机试验的荟萃分析111 nontransplant患者接受Nissen fundoplication发现术中并发症(如。胃出血,肝脾胶囊流泪,穿孔)发生在18%的病人和吞咽困难了14%139年]。无围手术期死亡。在一个类似的系统回顾,与388年五个随机试验的荟萃分析nontransplant倾心于发现患者围手术期的发病率在14%的病人发生和吞咽困难发达在17%的病人140年]。无围手术期死亡。
有冲突的数据关于肺移植患者接受抗反流手术是否有非致命的围手术期并发症发生率高于nontransplant患者接受抗反流手术。一个回顾性队列研究的52名患者没有发现差异估计失血,手术时间、住院时间、并发症或重新接纳率(135年]。相比之下,另一个28个病人的回顾性队列研究发现术后住院时间更长(2.9和0.7天)和30天重新接纳率较高(25%与比nontransplant患者(3.2%)在肺移植患者23]。
我们对报告的准确性的信心的抗反流手术对肺功能的影响,死亡率和并发症peri-operative很低,因为他们来自观察性研究和病例系列模棱两可的人口限制(大多数研究观察了肺移植患者气油比一般来说,而不是肺移植患者气油比和可能的BOS)和不精确的报道影响由于一些观察到的事件(在线补充表S7b)。
我们建议肺移植患者倾心于那些开发FEV的下降1一致的BOS被称为潜在fundoplication gastro-oesophageal结。这是基于委员会的观察,fundoplication可以改善肺功能,减少死亡率较低的围手术期并发症的风险。我们的建议是有条件的,因为非常低质量的现有证据提供了理想的小肯定大于不良的后果。
推荐6
对肺移植受者开发FEV的下降1一致的BOS和证实气油比,我们建议安排一名有经验的外科医生评估的潜在fundoplication gastro-oesophageal结(有条件的推荐,非常低质量证据)。
价值观和偏好
这个建议高度重视降低肺功能恶化甚至死亡的风险,避免手术并发症和较低的价值。
讲话
Nissen fundoplication更广泛研究比Toupet fundoplication;然而,我们没有理由相信,一个是优于其他和感觉的选择在外科医生的手术技术应该保持谨慎。
筛选标准
只有观察性研究和病例分析评估结果的筛选标准(141年- - - - - -147年]。存活率有明显改善在现代145年,146年后,结果患者精心挑选BOS筛选标准(走动的病人选择通过相同的过程用于首次移植)可能接近第一次肺移植如果由经验丰富的中心(142年,148年]。
我们的文献检索识别四个观察性研究和三个案例系列报道筛选标准在肺功能和生存的影响141年- - - - - -147年]。对肺功能、自由BOS筛选标准手术后的BOS报道是85 - 90%在1年,70 - 77%在2 - 3年,50 - 77%在4 - 5年。病人筛选标准由于BOS BOS复发的风险有一个高于病人筛选标准为其他原因,但这是不确定他们是否也有更高的风险比病人首次肺移植BOS,因为结果是相互矛盾的。生存后,据报道BOS筛选标准为60 - 78%,1年,2年53 - 64%和44 - 61%在5年。生存在病人接受了BOS筛选标准高于在病人筛选标准为其他原因,但这是低于接受主肺移植的患者(在线补充表S8a)。
筛选标准的安全性还没有得到充分的研究。我们确认没有研究围手术期的发病率和只有一个观察研究报道,报道围手术期死亡率。在那项研究[147年),有39人(10%)死亡在180天内389名病人中筛选标准。死亡原因是感染、呼吸衰竭和多器官系统衰竭。接受筛选标准的患者术后死亡风险增加相比,病人主要移植(在线补充表S8a)。我们的信心从BOS的报道自由,生存和围手术期死亡率(即。质量的证据)很低,因为估计来自于观察性研究和案例研究的局限性,通常模棱两可的人口(在线补充表S8b)。
我们建议他的病人发展耐火材料终末期BOS的移植外科医生评估筛选标准有两个原因。首先,筛选标准通常是唯一的生存希望因为这些病人已经没有选择干预措施。其次,筛选标准可能改善生存。生存没有筛选标准已经3年据报道51%所有BOS阶段(32)和肯定是低得多的BOS严重到需要筛选标准(病人通常归类为第三阶段当筛选标准),观察到所显示两到三倍的死亡风险增加发展的BOS更高年级每个年级(如。阶段1到2,然后阶段2 - 3)23,32]。值得注意的是最近报道不同早期生存与晚期发病与死亡风险在逐步减少BOS BOS发作发生后(如。< 1年,1 - 2年、2 - 3年或>移植后3年)与早些时候开始(149年与早发性BOS),这表明收件人一个贫穷的生存风险特别高的结果。我们的建议是有条件的,因为非常低质量的现有证据提供了小的理想的后果(即。潜在的死亡率降低)大于不良后果(即。BOS复发的风险增加,围手术期死亡率和资源利用率);因此,适当的行动可能取决于临床上下文。
建议7
终末期肺移植受者发展BOS耐火材料与其他疗法,我们建议转诊的移植外科医生评估筛选标准(有条件的推荐,非常低质量证据)。
价值观和偏好
这个建议高度重视避免手术并发症(如。死亡率),复发BOS和资源利用率。
讲话
筛选标准的选择过程是一样的,用于初次肺移植。
主要悬而未决的问题和具体的研究需求
列出关键的悬而未决的问题和研究的需要表8。尽管众多风险因素的识别与BOS的发病相关的具体机制BOS肺同种异体移植物的启动仍未知,和关键调解人的气道损伤可以通过具体的有针对性的治疗方法需要被识别。此外,肺功能下降为特征的BOS FEV1标准可能是由于许多不同的机制。还需要更多的研究来理解和描述复杂的组织病理学变化,可能出现不正常的肺移植和识别和描述BOS表型可以区分的基础上,临床、组织病理学和/或致病机制。治疗可用,可能对BOS,治疗效果可靠的早期疾病的生物标记物需要确定优化治疗干预的影响。指导解决如何检测异常气油比、选择抗反流手术的患者,选择适当的类型的抗反流手术预防或治疗BOS尚未建立。此外,最佳的同种异体移植物监测方法(如。支气管镜检查的作用与transbronchial活检临床肺移植受者稳定,筛查新创anti-HLA抗体和体液排斥的存在)尚未确定。
许多复杂的问题需要通过更多的研究来解决。其中包括如何处理分类和管理接受者的肺量测定法价值大幅波动随着时间的推移,符合诊断标准的患者分类BOS但随后经历了显著的改善,以应对治疗(如。阿奇霉素或fundoplication)导致临床和功能(FEV1BOS)改进的标准不再是满足,FEV的问题1下降时,满足BOS标准存在同种异体移植物感染的证据。事实上,感染(如。慢性细菌感染)和OB可能共存,诊断为BOS可能只经过一段时间之后变得明显(如。3 - 6个月),当感染清除了或被充分抑制和同种异体移植物功能仍然没有显著改善。此外,吸入抗生素的作用,用于防止或抑制细菌感染的预防和管理BOS需要确定。
进步在理解同种异体移植物细胞衰老的影响(加速老化)对同种异体移植物功能需要和BOS风险,和更好的理解interleukin-17的作用150年- - - - - -156年),自身免疫途径、监管淋巴细胞的数量(157年- - - - - -163年)和中性粒细胞反应,以及机制的假设epithelial-mesenchymal过渡现象(这还是假说,并没有被验证在人类)(164年- - - - - -167年导致气道纤维化,可能导致新的治疗方法预防和治疗BOS。需要改善动物模型的OB和可能是有用的在改善我们的理解这些和其他角色的现象开始,进展,OB肺移植后的预防和治疗。
同种异体移植物调节的新方法,如体外肺灌注(EVLP) [168年- - - - - -172年)可能导致改善早期同种异体移植物功能障碍,减少PGD的风险,并减少BOS的发病率和严重程度,但数据来确定EVLP BOS风险的影响尚未公布。强化免疫抑制,总淋巴辐照(TLI) [173年,174年]或体外光(ECPP) [175年,176年]表明,这些干预措施可能有重大的,有益的影响由于BOS肺功能下降,但这些干预措施可以有显著的负面影响,可能会造成重大的经济问题,和额外的临床研究需要建立这些干预措施的有效性。只有其它研究表明,免疫抑制疗法,如西罗莫司(177年),阿仑单抗(178年,179年)或anti-thymocyte球蛋白(180年),可能在BOS的预防和管理中发挥作用,但需要更多的研究来评估的效用,TLI ECPP或其他的变化通过使用替代免疫抑制剂长期维护免疫抑制(如。mTOR抑制剂,everolimus)来预防或管理BOS。最后,多中心临床试验中需要更好的建立免疫抑制的感应和维护的最优方案,既能充分防止急性和慢性同种异体移植物功能障碍但不产生过度的风险感染或其他有害的后果,和肺移植中心之间的协作提供了充分有力的临床试验将极大地促进特定风险因素的识别和干预治疗和预防BOS。
结论
这条指导原则的目的是增强了解BOS的诊断和管理移植医生和其他医生,并帮助他们在适当的临床决策评估患者被诊断为BOS怀疑。这条指导原则的建议被告知通过出版文献和临床观察肺移植的该领域的专家。因此,他们可以使用世界范围内的BOS帮助标准化管理。希望这条指导原则将会引发和促进未来的临床研究肺移植受者开发延迟同种异体移植物功能丧失。
确认
ISHLT / at /人BOS专责小组委员会成员如下。
椅子:基思·c·迈耶(医学与公共卫生学院大学麦迪逊分校麦迪逊,WI,美国)。
主席:Ganesh拉(西雅图华盛顿大学医学院,佤邦,美国);基尔特•m . Verleden(比利时鲁汶鲁汶大学);Paul a . Corris(弗里曼医院、纽卡斯尔、英国);阿兰·r·格兰维尔(肺移植单位,圣Vincents医院,悉尼,澳大利亚);保罗·奥罗拉(英国伦敦大奥蒙德街儿童医院,);吉姆·j·j·伊根(板牙Misericordiae大学医院,都柏林,爱尔兰)。
委员会成员:斯莱姆Arcasoy(哥伦比亚大学,纽约,纽约,美国;罗伯特·阿里斯(北卡罗莱纳大学教堂山分校、数控、美国);罗宾·k·艾弗里(美国马里兰州巴尔的摩约翰斯·霍普金斯大学);约翰Belperio(洛杉矶加州大学洛杉矶分校的CA,美国);于尔根·贝赫(鲁尔大学波鸿,德国波鸿,);Sangeeta Bhorade(美国西北大学、芝加哥、IL);安妮特Boehler(瑞士苏黎世大学、苏黎世);塞西莉亚查(多伦多大学,多伦多,加拿大);杰森·d·克里斯蒂(美国宾夕法尼亚州费城宾夕法尼亚大学);列文j·杜邦(Katholieke项目鲁汶,鲁汶,比利时); Marc Estenne (Hospital Erasme, Brussels, Belgium); Andrew J. Fisher (University of Newcastle, Newcastle, UK); Edward R. Garrity, Jr (University of Chicago, Chicago, IL, USA); Denis Hadjiliadis (University of Pennsylvania, Philadelphia, PA, USA); Marshall I. Hertz (University of Minnesota, Minneapolis, MN, USA); Shahid Husain (University of Toronto, Toronto, ON, Canada); Martin Iversen (Rigshospitalet, Copenhagen, Denmark); Shaf Keshavjee (University of Toronto, Toronto, ON, Canada); Vibha N. Lama (University of Michigan, Ann Arbor, MI, USA); Deborah J. Levine (University of Texas San Antonio, San Antonio, TX, USA); Stephanie M. Levine (University of Texas San Antonio, San Antonio, TX, USA); James C. Lee (University of Pennsylvania, Philadelphia, PA, USA); Gilbert Massard (University of Strasbourg, Strasbourg, France); Atul C. Mehta (Cleveland Clinic, Cleveland, OH, USA); Steven D. Nathan (Inova Fairfax Hospital, Falls Church, VA, USA); Jonathan B. Orens (Johns Hopkins University, Baltimore, MD, USA); Scott M. Palmer (Duke University, Durham, NC, USA); Greg I. Snell (Alfred Hospital, Melbourne, Australia); Marc Stern (Hôpital Foch Suresnes, Paris, France); Sean M. Studer (New York University, Woodhull Medical Center, New York, NY, USA); Stuart C. Sweet (Washington University, St. Louis, MO, USA); Henry D. Tazelaar (Mayo Clinic, Scottsdale, AZ, USA); Timothy P. Whelan (Medical University of South Carolina, Charleston, SC, USA); David S. Wilkes (Indiana University School of Medicine, Indianapolis, IN, USA); Trevor J. Williams (University of Melbourne, Melbourne, Australia); Martin R. Zamora (University of Colorado, Denver, CO, USA).
方法学家:Jan Brozek(加拿大麦克马斯特大学,汉密尔顿)和凯文·c·威尔逊(美国波士顿大学医学中心,波士顿,MA)。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:披露可以找到与本文的在线版本www.qdcxjkg.com
- 收到了2014年6月12日。
- 接受2014年8月26日。
- ©2014人队