许多病人报告持续症状急性COVID-19决议后,无论SARS-CoV-2变体,即使最初的疾病是温和的1,2]。众多的症状描述了这个术语“长COVID”,或称为“post-COVID综合症”或“所有的后遗症SARS-CoV-2 (PASC) ';为简单起见,我们将使用术语COVID长。不同,但症状包括呼吸困难、疲劳和大脑雾,据报道,影响高达69%的情况下(3]。长COVID可以衰弱,45.2%的病人需要减少工作安排(4]。世卫组织估计,有1700万人在欧洲经历了前两年的大流行期间长COVID [5]。SARS-CoV-2变体继续流通和急性并发症的风险仍然;病人56 003英国最近的一项研究发现,即使ο感染,4.5%遭受持续的症状6]。因此可能长COVID将提供大量医疗经济负担在可预见的未来。目前迫切需要了解疾病的机制和发展基于这种理解的有效的治疗方法。
鉴于临床表现的异质性似乎不同长COVID表型是由不同的机制,然而,很少有研究关注精心挑选病人所定义的机制和影响器官(图1)[7,8]。在这个问题上,斯科特等,研究了75例住院急性COVID-19与142年恢复期的病人,随访63至246天出院后(ref)。在急性COVID-19作者描述severity-related单核细胞特征,发现不同的炎症在恢复期的患者的症状。这些概要文件之间的不同疲劳症状的患者相比,那些有呼吸困难,与最初的疾病的严重程度无关。这项工作提供了一个重要一步了解长COVID症状的复杂性。
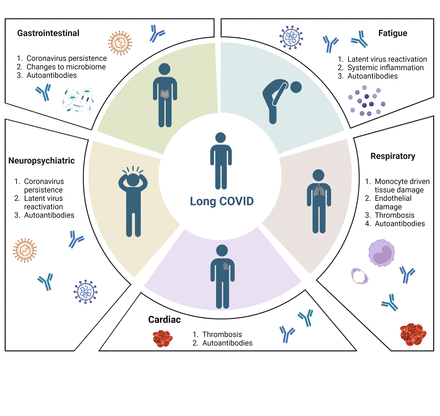
常见的症状与长COVID和可能潜在的病理生理学。
来自一个协作的团队与专业知识在单核细胞生物学,斯科特et al。演示增强单核细胞趋化因子受体的表达CXCR6和粘附分子PSGL1 post-COVID患者呼吸困难。既能促进迁移到肺组织(9,10),在那些与放射学异常变化最为明显。作者认为monocyte-driven COVID-19后肺损伤可能会导致呼吸困难。重要的是,斯科特et al。包括post-RSV /流感群5住院后10仍然扣人心弦但没有显示COVID-19后单核细胞表型的改变。另外,他们发现PSGL1表达式没有进步fibrosing间质性肺病患者升高,再次支持这些发现的特异性post-COVID肺损伤。这些发现提供了一个激动人心的洞察post-COVID症状的潜在原因。
关于长COVID综合症的多样性,斯科特et al。区分患者出现疲劳和那些患有呼吸困难。他们发现,疲劳的人表现出持续低单核COX2的表达和CXCR2 COVID-19后9个月。cox - 2是一个prostaglandin-producing酶参与类二十烷酸途径被认为是重要的在维护组织的完整性,血小板功能和对病原体的先天免疫反应11,12]。因此,斯科特et al。提出充分理由局部肺损伤在post-COVID呼吸困难,同时更全面涉及单核细胞和组织巨噬细胞炎症可能驾驶疲劳。
然而,一些重要的问题仍然存在:什么导致了持续的炎症在这些患者中,为什么有些人发展异常免疫档案和延迟复苏?描述了血栓事件,甚至几个月后急性COVID-19 [13),导致缺血和坏死组织可以解释斯科特描述的单核细胞衍生肺部炎症et al。(14]。事实上,作者提出的证据表明,一些患者呼吸困难之后COVD-19可能极其细微变化只有明显的肺使用先进的成像技术,如超极化氙MRI [15]。在这个研究中,患者呼吸困难在扩散能力的局限性,这是符合血栓栓塞疾病。为了解决这个问题,斯科特et al。(ref)用定量肺密度分析确定肺部炎症患者正常的传统成像。使用这种方法,他们发现,37.5%的患者呼吸困难但正常传统成像微妙的肺损伤的迹象。它将用于未来的研究来检查这些患者团体专门确定那些症状有无异常传统成像表现出不同的病理。几个抗凝血剂临床试验正在进行,小心这些试验的病人选择将积分成功(8]。
病毒已被建议作为一个潜在的持久性机制持续免疫扰动在许多post-viral综合症,并演示了埃博拉病毒感染后(16]。一个87人的研究发现持续进化的B细胞反应SARS-CoV-2感染后6个月时44%持续症状(17]。在这项研究中病毒抗原检测在肠活检在感染后4个月,提供证据表明,持续的病毒可能刺激COVID-19后慢性免疫干扰。有鉴于此,有趣的是,斯科特et al。发现增强单核细胞表达gut-homing整合素β7患者急性严重COVID-19,突出一个肠道coronaviral水库的可能性可能会推动持续的炎症(ref)。持续的病毒也被发现在肺SARS-CoV-2感染后300天,这或许可以解释持续的肺部炎症所描述的斯科特et al。(18]。另外,潜伏期EBV(或巨细胞病毒)感染就可能导致炎症反应在某些患者中,所显示的两项研究的患者持续疲劳和/或神经系统症状,如脑雾(19,20.]。未来的研究证实或反驳病毒持久性或重新激活潜在的原因可能是变革,抗病毒药物的试验应显示清除病毒和解决持续的症状。
最后,anti-IFN与严重急性COVID-19相关自身抗体,导致许多质疑长COVID有时可能会有自身免疫发病机理(21]。在最近的一项研究的220名患者没有发现长COVID之间的关联和自身抗体(22),与胃肠道和呼吸道症状长期COVID表型相关自身抗体(23]。斯科特的结果et al。支持不同的生物机制支撑不同的建议长COVID亚型。
斯科特et al。更改用于肺功能测试(击球)证实了他们的发现,炎症损伤肺组织构成持续的呼吸困难。同时击球是有用的在临床实践中他们必须认真解释对理解的生理疾病。斯科特et al。报告一个减少FEV1患者呼吸困难但差异小,而平均预测百分比值高于80%的预期结果(阈24]。如果是真诚的,减少气流阻塞的原因尚不清楚。Monocyte-driven alveolar-capillary膜损伤可能会影响气体传输(DLCO)而不是气流,在他们的研究中未见。然而,作者承认这项研究没有动力去寻找肺功能可以微妙的变化在疾病的早期阶段和研究问题仍然开放的生理学基础在这些患者呼吸困难。至关重要的是,未来的工作将继续整合临床和免疫数据,但是大的和精心设计的研究将被要求检测细微变化的生理参数,并提供清晰的上下文中如何解释击球长COVID。
这项工作提供了一个重要的贡献增长文学长COVID是一种繁杂的疾病与多元化的原因。鉴于越来越多的证据表明,不同模式的症状可能是由不同的病理生理途径(图1),至关重要的是,严谨和以证据为基础的疾病分类是用来设计试验的具体干预措施基于这方面的知识。许多临床试验正在进行中,以识别潜在的治疗(8这些试验),但有可能会显示没有好处如果患者不同的致病通路不分化。通过检查不同长COVID亚型的根本原因,研究等,斯科特et al。最终可能导致治疗对齐到特定患者表型基于深入了解疾病的途径。
消息这样的研究也是希望为那些遭受多年的神秘和难以管理的条件称为各种post-viral疲劳、纤维肌痛、自主的不稳定和其他条件可能禁用,但没有明显的根本原因或治疗。如果COVID流行最终导致更好地了解是什么原因导致这种疾病和如何对待他们,许多人会有理由庆祝。
确认
FL由MRC支持临床培训奖学金奖/ W000970/1先生。特首是由NIHR[格兰特P91258-4]。支持PJMO NIHR高级研究员奖[奖201385]。
脚注
利益冲突:PJMO报告来自欧盟的资助创新药物倡议(IMI) 2合营企业在提交工作;授予来自英国医学研究理事会,葛兰素史克,威康信托基金会EU-IMI,英国国家健康研究所和英国研究和Innovation-Department业务,能源和工业策略;从辉瑞公司和个人费用,詹森,Seqirus,外提交的工作。FL、CE和PJMO PHOSP-COVID财团的成员,英国广泛研究与COVID-19住院后长期的健康结果。
- 版权©2023年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org















