摘要
COVID-19的代谢组学变化预测了患者的急性结局,并提示了生物能量危机的作用。因此,COVID-19的代谢组学变化可以作为一种生物标志物,为了解致病机制和药物靶点提供参考。https://bit.ly/2XkJeU8
2019年12月,当2019冠状病毒病(COVID-19)大流行首次出现时,这种疾病的病理生理学基础在很大程度上尚不清楚。来自世界各地的科学家、医生和政府机构采取了“全员出动”的方法,希望找到治疗这种疾病的潜在疗法,并了解这种疾病的病理生理学。1]。目前,超过4800项临床试验在clinicaltrials.gov已在世界各地进行或提出,许多受试者来自截然不同的民族和种族背景,以及不同的标准护理策略[2]。尽管做出了这些努力,但除了单克隆抗体之外,很少出现有效治疗COVID-19的疗法;疫苗仍然是控制和减轻大流行的最佳方法[3.]。
尽管缺乏治疗上的成功,但我们对这种疾病的进展有了前所未有的了解。4]。在大流行期间发表的大量临床和生物学数据中,一些最一致和最令人兴奋的结果来自患者血清样本的代谢组学分析[5]。代谢组学是一个迅速发展的研究领域,在该领域中,组织或液体中的代谢物被全面分析,加深了我们对多种疾病的病理生物学的理解,确定了可预测的生物标志物,并突出了潜在的新型治疗策略。在整个2020年和2021年,已经发表了几篇专注于COVID-19的代谢组学论文。最早的报告发现,重症COVID-19患者处理脂质、氨基酸和碳水化合物的代谢途径发生了变化。最近的研究已经开始将代谢组学变化与代表特定器官系统衰竭的症状联系起来,例如,神经系统的急性谵妄和康复后的精神健康问题以及消化系统的破坏[6,7]。犬尿氨酸通路失调一直是众多独立研究报告中最一致的发现之一[5]。潜在的重要意义是,COVID-19中的许多代谢组学异常与败血症和急性呼吸衰竭中发现的代谢组学异常相似,这表明导致急性生物能量危机的共同机制[8,9]。
根据这些思路,Jia等。[10]报道了对确诊的COVID-19患者进行深入、精心设计的代谢组学分析。发现的患者(n=63)被细分为轻度、重度和恢复期组,并在另一个队列中独立验证,其中有90名患者和41名未感染对照组。研究人员同时使用了广谱半定量质谱分析和靶向质谱分析。作者发现葡萄糖代谢的持续中断和TCA和尿素循环的失调被确定为治疗干预的潜在靶点(图1一个)。这些代谢组学变化与其他背景下的代谢组学研究一致,并指出潜在的生物能量危机是COVID-19的关键致病特征[5]。
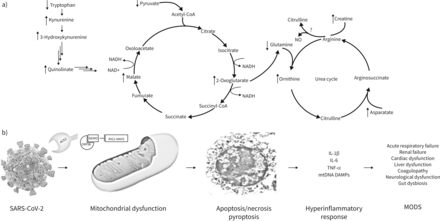
由sars - cov -2引起的代谢组学变化是患者急性和长期预后的预测指标,并反映可能由病毒劫持线粒体引起的生物能量危机。a)由SARS-CoV-2感染引起的代谢组学变化通常导致犬尿氨酸途径、TCA循环和尿素循环中断。精氨酸是否转化为瓜氨酸和NO尚不清楚;但由于鸟氨酸和肌酸的增加,Jia等。[10]推测尿素循环代谢精氨酸而不是NO生成途径。b) SARS-CoV-2被内化进入细胞通过血管紧张素转换酶2 (ACE2)受体许多病毒蛋白,包括ORF7a和ORF9b位于线粒体内。这些蛋白可以抑制维甲酸诱导基因i -线粒体抗病毒信号蛋白(RIG1-MAVS)依赖的干扰素信号,增强病毒复制并破坏线粒体功能。这最终会导致细胞死亡通过细胞凋亡、坏死或焦亡、促炎细胞因子的释放以及线粒体DAMPs(损伤相关分子模式),最终导致多器官功能障碍综合征(MODS)。Jia等。[10]也证明了许多因SARS-CoV-2而改变的预测代谢物与促炎细胞因子密切相关。TNF:肿瘤坏死因子;核因子κB必需调制器。
此外,作者能够将白细胞介素(IL)-1β、肿瘤坏死因子(TNF)-α和IL-6的变化与代谢组学特征联系起来。毫不奇怪,这三种细胞因子都随着疾病的严重程度而增加。尽管在康复期间血清水平有所下降,但相对于未感染的对照组患者,血清水平持续升高。重要的是,细胞因子水平与TCA周期相关代谢产物呈正相关,包括天冬氨酸、肌酐、苹果酸和2-氧戊二酸。精氨酸是尿酸循环的关键成分,它可以转化为鸟氨酸或一氧化氮和瓜氨酸。作者认为精氨酸的减少和鸟氨酸的增加表明精氨酸被代谢了通过精氨酸酶和尿素循环而不是一氧化氮循环。尽管如此,由于一氧化氮可以通过影响刺突蛋白及其主要靶标血管紧张素转换酶2 (ACE2)来减少病毒RNA的产生,目前正在对COVID-19进行治疗气体的临床试验[11]。
代谢组学研究ia等。[10],与败血症和急性呼吸衰竭(ARF)的类似研究一样[9,12- - - - - -15],指出线粒体功能障碍是COVID-19结果的关键驱动因素[16]。在这种情况下,大量线粒体DNA损伤相关分子模式(mtDNA DAMPs),一类已知能促进免疫和非免疫细胞产生细胞因子的DAMP [17,18],是COVID-19患者ICU入院、需要插管和死亡率的早期预测指标[19]。实验研究已经确定了SARS-CoV-2引发线粒体功能障碍的多种途径,从而导致COVID-19的病理生理效应(图1 b)。例如,SARS-CoV-2会损害COVID-19患者的外周血单个核细胞的氧化代谢,并促进其向糖酵解表型的转变[20.]。这种效应可能是由ACE2介导的,ACE2被广泛称为介导SARS-CoV-2进入细胞的受体,据信它直接改变线粒体功能,导致ATP生成减少和NADPH氧化酶(NOX)的激活4 [21,22]。与NOX4激活相关的活性氧生成增加可能会产生多种有害事件,包括破坏线粒体基因组,导致其断裂为促炎mtDNA DAMPs [23,24],以及激活PARP1导致NAD+耗散,伴随干扰素产生减少,病毒复制增强和线粒体自噬减少[25]。与ACE2一样,SARS-CoV-2编码的蛋白质也可能扰乱线粒体功能。在这里,对SARS的开放阅读框架ORF-9b和ORF-7a的研究表明,这些蛋白质定位于线粒体。ORF9b通过破坏k63连接的核因子κB基本调节剂(NEMO)的多泛素化,使维甲酸诱导基因i -线粒体抗病毒信号蛋白(RIG1-MAVS)依赖的干扰素信号通路失活[26]。在SARS中,ORF-7a和ORF-8a促进病毒复制,而ORF-8a可激活caspase-3介导的细胞凋亡[22,27]。与SARS不同,SARS- cov -2基因组包含ORF-8,已知ORF-8通过下调主要组织相容性复合体(MHC)类Ι在免疫逃避中发挥作用,以蛋白质为目标进行溶酶体降解通过beclin-1自噬起始途径[28]。虽然ORF-8的全部功能尚未阐明,但基于其促进MHC I类降解的能力需要与beclin 1密切相互作用这一事实,人们很容易推测它可能对线粒体产生不利影响,而后者已知与心磷脂相互作用并介导线粒体自噬[29]。病毒以及促炎细胞因子和mtDNA DAMPs的释放诱导高度炎症反应[22,24,27,30.,31]。确定这些生物能量代谢组学变化与线粒体功能障碍之间的关系,可以预测出旨在使代谢组学特征恢复到稳态的新疗法。
更令人惊讶的发现之一是,对照组和COVID-19患者之间代谢组学差异最大的是康复组,240种代谢物中有98种存在显著差异。这一发现可能对所谓的“长COVID”特别重要,它与其他形式的严重疾病幸存者中注意到的生活质量长期下降有某些相似之处[32,33]。据估计,50%入住ICU需要机械通气的患者会继续发展为重症监护后综合征,高达80%的危重症幸存者在首次发病后2年内重新入住养老院、康复中心或ICU。一半的幸存者患有长期的认知能力下降。在ICU每多住一天,即使在2年随访后,肌肉质量也会减少11%。由于这些患者中的许多人再也没有重返工作岗位,医疗保健系统和社会将在大流行减弱多年后处理这些问题。了解代谢组学变化与生活质量结果的关系,可能会确定改善COVID-19幸存者长期生活质量的治疗策略。
这项研究的最终优势在于,许多确定的代谢物可以预测患者的预后,在独立队列中得到验证,并且与其他研究有很强的重叠。在发现队列和验证队列之间进行预测建模的大型荟萃分析,可以提供有价值的生物标志物,不仅可以预测SARS-CoV-2感染,还可以确定败血症和ARF的急性和慢性结局是否显示与COVID-19相同的通路。
这份报告仍有一些局限性。正如作者所指出的,他们的队列年龄不匹配,因为严重病例主要在老年人中观察到。更大的队列将为这些结果提供更大的信心。
考虑到多项研究中发现的一致代谢紊乱,以及败血症和ARF中代谢组学变化的大量重叠,这些结果表明,应定期监测代谢生物标志物,以确定COVID-19进化过程中的时间依赖性变化。未来的治疗可能会考虑有针对性的营养干预如何使代谢组学曲线回到稳态[34]。例如,Jia等。[10]建议进一步研究I型干扰素是否调节感染上皮细胞的尿素循环,以及COVID-19感染是否通过减少一氧化氮的产生将葡萄糖代谢的代谢途径切换到尿素循环,从而保护病毒复制。其他靶向犬尿氨酸通路和NAD+/NADH比值的疗法可能会减轻生物能量危机和NADH调节的免疫反应[8,25]。最后,抑制线粒体氧化应激或修复氧化性mtDNA损伤的策略也有可能成为靶向代谢组学监测指导下的治疗策略[23,35,36]。
可共享的PDF
确认
正如Milad Zandi博士的信件所指出的,发表在本期的欧洲呼吸杂志(https://doi.org/10.1183/13993003.02818-2021),该手稿的早期观点发表表明,ORF-8a存在于SARS-CoV-2基因组中。这一推论已从最终发表的手稿中删除,并明确了ORF-8在SARS-CoV-2中的功能。我们感谢赞迪博士指出了SARS和SARS- cov -2基因组之间的重要区别。
脚注
作者贡献:所有作者都参与了本稿件的撰写和编辑,并通过了最终稿件。
利益冲突:所有作者声明国家卫生研究院对本手稿的支持,没有进一步的披露。
支持声明:由美国国立卫生研究院提供支持:5KL2TR003097, NR01933801A1, UL1TR003096, R01HL11361406A1, R01GM127823。本文的资助信息已存入交叉参考基金注册。
- 收到了2021年9月5日。
- 接受2021年10月9日。
- 版权所有©作者2022。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org