摘要
入院时抗膜联蛋白A2抗体水平强烈预测住院COVID-19患者的死亡率。考虑到膜联蛋白A2在肺中的重要保护功能,其拮抗作用可能在COVID-19的病理生理学中发挥重要作用。https://bit.ly/2UMPr9w
致编辑:
2019年严重冠状病毒病(COVID-19)的病理生理学在很大程度上被归因于高炎症反应,但没有明确的潜在机制[1].呼吸窘迫的出现有一个典型的延迟,大约在症状出现6至12天后才出现,这在其他严重的病毒性呼吸道感染中有些不典型[2].对于这种延迟已经提出了几种理论,如惰性感染或病毒持久性。然而,来自严重急性呼吸综合征冠状病毒2型(SARS-CoV-2)病毒培养的数据(非PCR)表明,在患病第9天之后缺乏阳性培养[3.].
COVID-19导致呼吸窘迫的时间与体液免疫反应的发生时间明显一致,有证据表明住院的COVID-19患者中存在自身抗体,包括抗干扰素和抗磷脂抗体[4,5].这些自身抗体的致病性尚不清楚。然而,一项关键的研究表明,在COVID-19的严重病例中,胞外B细胞激活水平很高[6].这种类型的免疫反应是几种自身免疫疾病的特征,这提出了一个问题,即严重的COVID-19是否是发生在感染SARS-CoV-2病毒的患者子集中的灾难性自身免疫反应的结果[7].
本研究调查了COVID-19患者对肺和其他器官表达的保护蛋白膜联蛋白A2具有自身免疫抗体的可能性。由于这种磷脂结合蛋白对纤维蛋白溶解、肺弹性、细胞膜修复和肺血管系统完整性至关重要,因此膜联蛋白A2的拮抗可能解释COVID-19重症病例的许多标志性临床特征[8].
为了评估这种可能性,我们分析了纽约大学朗格尼健康中心86名因COVID-19住院并经PCR证实为阳性的患者在住院第0或第1天的血浆。ELISA法检测抗膜联蛋白A2 IgG抗体。作为比较,我们还研究了针对膜联蛋白A5的IgG抗体,这是血栓前抗磷脂抗体的另一个靶点,但不知道在维持肺血管的完整性方面有直接作用[9].抗体水平以相对单位(RU)计算,使用先前确定为IgG自身抗体高应答者的血浆样本。如果患者住院但未插管,则分为1)非危重患者;如果患者住院并插管,则分为2)危重患者;或3)在住院期间死于COVID-19。
在对研究人群进行描述性分析后,我们使用方差分析对疾病严重程度分层的抗膜联蛋白A2和A5抗体水平进行分析。为了进行初步分析,我们使用多变量logistic回归检验抗体水平与死亡之间的关系,并调整年龄、性别、种族、高血压、糖尿病和肥胖史(体重指数>30 kg·m)−2).p值为0.025用于解释多次比较。我们使用边界分析以图形方式显示在一系列抗体水平下的死亡风险。对异常值进行了分析,以确保抗体水平不存在对结果有不当影响的极端值。此外,通过敏感性分析评估了抗体水平和死亡之间关联的稳健性,其中包括这些COVID-19患者住院期间的最大实验室值。这些常用的检测包括白细胞计数(WBC)、天冬氨酸转氨酶(AST)、丙氨酸转氨酶(ALT)、肌酸激酶(CK)、乳酸脱氢酶(LDH)、c反应蛋白(CRP)、铁蛋白和d -二聚体。
所有统计分析均在Stata 16.2中进行。患者同意通过纽约大学机构审查委员会批准的中央生物库和方案将其生物标本用于COVID-19研究。更详细的方法描述可在本研究的预印本中查阅[10].
在我们研究的86例患者中,28例非危重症,36例危重症,22例死亡。与存活的患者相比,死亡的患者患高血压(p=0.04)和肥胖症(p=0.05)的比例更高。在分析这些住院COVID-19患者的WBC、AST、ALT、CK、LDH、CRP、铁蛋白和d -二聚体值时,最大值随着疾病严重程度的增加而增加(p<0.01)。我们发现,与非危重患者(0.80 RU, 95% CI 0.66-0.94)和危重患者(0.89 RU, 95% CI 0.77-1.01)相比,住院死亡的COVID-19患者抗annexin A2 IgG抗体的平均水平(1.16 RU, 95% CI 0.95-1.37)更高。相比之下,按疾病严重程度分层时,抗膜联蛋白A5 IgG抗体平均水平无统计学差异(p=0.32)。
在我们对86例住院COVID-19患者死亡率的初步分析中,我们发现,在调整年龄、性别、种族和共病后,抗膜联蛋白A2抗体水平强烈预测死亡,优势比为9.3 / RU (95% CI 1.9-44.6;p = 0.005)。相比之下,抗膜联蛋白A5抗体水平与较高的死亡率无关(95% CI 0.5-15.2;p = 0.22)。使用边界分析,我们以图形方式描述了抗膜联蛋白A2抗体的一系列水平的预测死亡率(图1).在我们的敏感性分析中,我们添加了对WBC、AST、ALT、CK、LDH、CRP、铁蛋白和d -二聚体水平的最大调整。该多变量回归显示,抗annexin A2抗体水平强烈预测死亡率,优势比为12.9 / RU(95%可信区间1.5-108.7;p=0.019),即使在对这些COVID-19患者住院期间的最大实验室异常进行调整后。
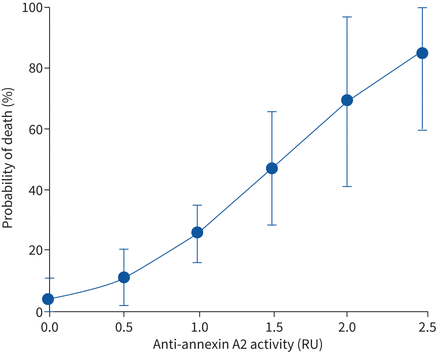
基于抗膜联蛋白A2抗体水平的死亡率预测基于逻辑回归结果的边际分析描述了在相对单位(RU)中抗膜联蛋白A2抗体水平范围内的预测死亡率。误差条描述了95%置信区间。
我们的研究发现,在死亡的COVID-19患者中,针对膜联蛋白A2的IgG抗体水平较高。更重要的是,在控制了患者风险因素和与严重COVID-19相关的关键实验室标志物的最高水平后,抗膜联蛋白A2抗体水平强烈预测死亡率。
尸检证据表明,COVID-19重症病例有广泛的血栓性疾病、弥漫性肺泡损伤和内皮破坏,导致肺水肿和纤维蛋白沉积[11].这些发现与严重COVID-19的临床表现相关,包括弥漫性凝血、急性呼吸窘迫综合征(ARDS)、非心源性肺水肿和一般无细菌重复感染的肺纤维性渗出[1].尽管我们的研究没有提供任何直接证据证明这些自身抗体的致病性,但膜联蛋白A2的拮抗作用可以解释许多COVID-19重症患者的临床表现。
Annexin A2作为一种辅助受体,激活内源性组织纤溶酶原激活物,溶解血栓,促进纤维蛋白清除,对肺中的纤维蛋白溶解至关重要[8].最近,人们发现膜联蛋白A2可以维持肺微血管内皮细胞连接,防止肺水肿,尤其是在缺氧时[12].最后,膜联蛋白A2促进肺弹性,也参与细胞膜稳定和肺上皮细胞修复,从而防止细胞凋亡[13].它的抑制可能也解释了COVID-19严重病例中出现的弥漫性肺泡损伤、ARDS和肺纤维化。
值得注意的是,先前对SARS- cov -1的研究发现了对肺上皮和内皮细胞具有细胞毒性的自身抗体,也专门针对住院SARS患者中的膜联蛋白A2 [14].在一部分患者中丧失免疫耐受和灾难性的自身免疫损伤可以解释为什么某些患者出现COVID-19的严重症状[15].其他没有这种自身免疫反应的患者可能有较轻的症状,与其他只导致无症状或轻微疾病的冠状病毒感染一致。
虽然这些自身抗体可能是肺损伤的非特异性标记物,但探索这些抗膜联蛋白A2抗体的致病性至关重要,因为它们可以解释严重COVID-19的潜在病理生理学。进一步的研究应评估这些COVID-19自身抗体的特异性,方法是调查它们是否也发生在其他呼吸道疾病中,如流感或其他类型的ARDS。此外,我们认为应该研究这些抗膜联蛋白A2抗体的持久性,特别是在具有持续呼吸道症状的后急性COVID-19综合征(“长COVID”)患者中。
可共享的PDF
确认
我们要特别感谢纽约大学医学院生物标本研究与发展中心、Brian Fallon对生物信息学的支持,以及所有帮助获取和处理本研究和其他与COVID-19有关的研究所用样本的志愿者。
脚注
作者贡献:A. Rodriguez和D.C. Lee设计了这项研究。M. Zuniga和C. Gomez进行了实验。A. Rodriguez和P. Cotiza在纽约大学朗格尼健康中心收集数据并确定患者样本。D.C. Lee起草了手稿并进行了统计分析。所有作者都解释了数据,并为手稿提供了关键的输入。
利益冲突:祖尼加先生没有什么可透露的。
利益冲突:C.戈麦斯没有什么可透露的。
利益冲突,s。e。卡森斯没什么可透露的。
利益冲突,本德医生没什么可透露的。
利益冲突:P. Cotiza没有什么可透露的。
利益冲突:苗祺荣没有什么可透露的。
利益冲突:华盛顿·李没什么可透露的。
利益冲突:A.罗德里格斯没有什么可透露的。
支持声明:本研究得到了纽约大学朗格尼2019冠状病毒病特别基金的内部拨款支持。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2021年1月15日。
- 接受2021年6月24日。
- 版权所有©作者2021。
本版本按照创作共用署名非商业性许可4.0的条款发布。商业复制权利及许可请联系权限在}{ersnet.org















