特发性肺纤维化(IPF)是一种独特的临床实体,通常影响60岁以上的人群,确诊后的中位生存期为3 - 5年。IPF的自然病程是众所周知的:大多数IPF患者肺功能稳定下降,一些患者长时间保持稳定,一组患者迅速下降,一组患者在死亡前出现IPF急性加重[1].而在IPF的发病机制中,已经确定了几个被认为是“损伤”之后的关键细胞和分子事件[2],IPF的最终原因和伤害肺部的触发因子仍然难以捉摸,目前无用的药理学药物均未表现出IPF患者的改善的结果和生存。
IPF的发病率和患病率与高龄高度相关,据估计,75岁或以上男性的发病率和患病率为每年每10万人71和271人,女性为每年每10万人67和266人与以广泛的诊断标准计算,每年每10万人中有16.3人和42.7人的总体发病率和流行率[3.].有趣的是,许多观察表明,衰老的肺更容易受到各种刺激引起的损伤和纤维化,这种易感性可能与年龄相关的基因表达变化或基因多态性有关,如年龄相关的端粒酶功能障碍[4- - - - - -7].
老年还伴随着食道和胃动力下降,食管上括约肌压力下降,食道酸暴露增加[8].Heral Hernias出现在推进年龄,已被发现高达60%以上超过60岁的人[9].食管裂孔疝的形成与食管下括约肌功能障碍有关(食管下括约肌基底压降低,食道酸暴露增加,糜漫性食管炎的可能性增加),随着年龄的增长,食管裂孔疝的大小往往增加。9].食道裂孔疝和/或胃食管反流(GER)与肺纤维化的相关性已被充分证实[10- - - - - -12].老年人GER相关症状(胃灼热、上腹部不适和反胃)的严重程度和频率趋于降低[13],因此有助于“沉默/神秘的GER和微吸气”的概念。当人们考虑到GER、GER疾病、裂孔疝和IPF与高龄密切相关时,必须认真考虑GER和微吸入与IPF发病机制和/或IPF急性加重发作相关的可能性。
在健康受试者睡眠期间记录了近端GER[14,休息时食管上括约肌的压力在睡眠时也大幅下降[15].事实上,G利森等.[14]发现,近一半的健康成年人,他们在睡眠期间评估了他们在睡眠期间吸出少量的口咽分泌物,表明“沉默”的微散,是成人中的常见现象。微量痉挛已被假定为IPF发病机制中的一种安全性因素,这是基于异常的,“沉默”酸GER在〜90%的IPF患者中观察到基于24-H食管pH监测[16,17].然而,由于在通常的间质性肺炎(UIP)区域缺乏“微观和/或宏观吸入”的组织学特征,对接受GER和微观吸入在IPF发病机制中的作用提出了适当的犹豫。尽管如此,在过去几年里积累的越来越多的证据支持这一概念,即隐性反流胃液微抽吸可能在IPF发病机制中发挥重要作用。有趣的是,这些研究表明,IPF患者中典型的GER症状(胃灼热和反流)是较差的GER预测指标。
尽管越来越多的研究,但在IPF患者中记录了GER的高度普及[16- - - - - -20.], GER和IPF之间的因果关系尚未确定。尽管如此,值得注意的是,一些病例系列表明GER抑制和临床稳定之间存在联系。这导致临床评价“抗反流”疗法作为异常GER患者IPF的唯一治疗方法。RAghu.et al。[21]描述了4例明确的IPF患者,他们的临床病程在4年时间内通过使用抗反流疗法(通过质子泵抑制剂(PPIs)抑制酸性GER和/或抗反流手术)的唯一干预得到了稳定或改善通过对所有四名患者进行24小时食管pH监测英登et al。[22]报道了一系列14名患者,发现接受Nissen胃底折叠术的患者的需氧量趋于稳定。最近,我eeet al。[23]报道,在一组204例IPF患者中,使用抑制GER的药物与高分辨率ct放射学纤维化评分较低相关,是延长生存时间的独立预测因素。回顾性观察IPF患者据称服用抑制胃分泌物酸度的药物后生存率提高[23提示PPIs和/或H2受体拮抗剂治疗可减少远端肺实质上皮屏障的“损伤”和/或防止后续复发性“损伤”的后果,这种损伤可能是由胃液酸组分间歇性吸入引起的。
检测反流和相关微吸出的一种新方法是检测呼吸分泌物中的吸出生物标志物,如胃蛋白酶。已定量测定痰液和支气管肺泡灌洗液中的胆汁酸和胃蛋白酶,作为微量吸入的标志[24- - - - - -27].年代tarostaet al。[28]据报道,24小时pH监测检测到的近端反流事件数量与BAL液中胃蛋白酶水平相关。尽管BAL胃蛋白酶或胆盐检测是吸入回流胃液的直接标志物,但需要进一步研究测量BAL液中胃蛋白酶和胆盐与IPF患者疾病严重程度、进展风险和/或急性加重的发展相关。
在这一期的欧洲呼吸杂志,两组独立的研究人员进一步探讨了IPF中微抽吸的概念[29,30.].使用IPF的患者使用多探测器计算机断层摄影成像我et al。[29)证实了先前已知的IPF患者食管裂孔疝的患病率增加,表明IPF患者食管裂孔疝有比患者更大的生理损伤肺功能测试没有食管裂孔疝,,在一个小的子集IPF患者进行24小时pH监测(n = 14),显示酸性GER异常与裂孔疝的存在有关。在74例有使用抗反流药物数据的患者中,接受治疗组的肺一氧化碳扩散能力和综合生理指数评分明显更好。
leeet al。[30.]首次检测到IPF患者的Bal流体中的微痉挛的生物标志物Pepsin。他们的大量患者患有IPF的急性加剧的临床证据,并且对IPF急性加剧的群体的差异BAL细胞计数的BAL PEPSIN和中性粒细胞百分比显着增加与稳定患者。BAL胃蛋白酶水平与稳定组相比增加一个标准差,其优势比为1.46(95%可信区间1.03–2.09;p=0.04)然而,经放射学鉴定的食管裂孔疝的患病率或大小与恶化状态无关。此外,BAL胃蛋白酶水平不能预测生存率,胃蛋白酶水平的升高是由一个亚组(33%的病例)驱动的BAL中胃蛋白酶水平显著升高eeet al。[30.]是有趣的,因为在IPF发作急性加重开始时,BAL液中检测胃蛋白酶是直接证据,胃液内容物可以到达下呼吸道,而没有明显的误吸事件。这些发现支持了长期存在的假设,即微误吸在IPF发病机制中发挥了作用,而引起肺损伤的未知“触发因素”和/或病原可能是回流胃液转移到肺实质的远端区域(图1).
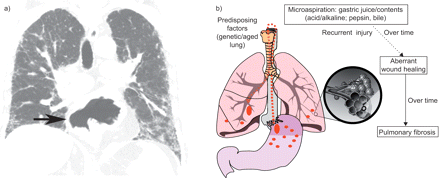
a)特发性肺纤维化(IPF)患者的胸部高分辨率ct (HRCT)图像;根据所述标准确定的诊断[1]),显示同时存在裂孔疝(箭头)。b)胃食管反流(GER)和微吸入在IPF发病机制和IPF急性加重中的概念。注意图示食管裂孔疝(小),胃液回流物进入远端肺实质通过GER和微吸入(从食管远端到食管近端并吸入肺(箭头)的小点所示),可造成肺损伤。由间歇性微通气引起的复发性损伤导致异常的伤口愈合和随后的肺纤维化(在肺组织病理学和IPF临床诊断中表现为通常的间质性肺炎模式),特别是在遗传易感性的人(如。端粒酶缺乏或MUC5B表达增加)和更容易发生IPF的老年人(因为肺老化和食管上下括约肌功能障碍)。
吸入事件的临床后果取决于性质(酸度、胃蛋白酶、胆汁酸和胃液其他成分的存在)、吸入量、吸入频率以及受试者从肺部中和和清除吸入物质从而防止/限制粘膜损伤的能力,炎症和随后的肺纤维化。观察到的食管裂孔疝和异常酸性GER的相关性,以及从远端肺实质取回的BAL中检测到胃蛋白酶,支持了一个长期存在的假说,即微呼吸是IPF的致病因素,可能触发IPF急性加重。这两份报告进一步加深了我们对GER和微呼吸在IPF发病机制中的认识,并支持了GER和微呼吸与没有IPF急性加重的患者更严重的肺损伤相关,GER和隐匿性吸入可能引发急性呼吸衰竭的概念失代偿。胃液微呼吸作为急性加重的触发因素是一个很有吸引力的假设,特别是当我们考虑到IPF急性加重的主要组织病理学损害是弥漫性肺泡损伤的观察结果时,这是在将酸或胃液注入实验动物的肺中时观察到的,IPF急性加重的原因尚不清楚。虽然已知酸可导致肺上皮损伤,但胃液中的非酸成分,如胃蛋白酶,可在远端气道中发现,尤其是在IPF急性加重期,这一观察结果不容忽视,并对治疗干预具有指导意义。事实上,BAL液中的胃蛋白酶可被视为微呼吸的生物标志物,可用于评估抗反流疗法的疗效。可以监测BAL液中的胃蛋白酶或胆汁盐,以确定抗反流手术干预(如胃底折叠术)的疗效,这在肺移植受者的肺移植功能障碍中已有报道[31].
我们推测,高龄的碰撞及其相关的肺损伤易感性变化(这可能与端粒酶突变和MUC5B表达等基因表达变化有关[32),发生GER、食管裂孔疝和胃液及其成分微吸出的风险增加,包括发生幽门螺杆菌,可能导致易感个体肺上皮损伤、异常修复反应和纤维化(图1).此外,胃液微吸入的发作可能导致持续的损伤和纤维化反应,纤维化反应导致肺功能加速丧失,纤维化反应是IPF中UIP组织病理学的特征。最后,大剂量胃液到达肺的发作可能引发IPF急性发作。
迄今为止,对IPF患者生存和生活质量有重大影响的唯一干预措施是肺移植,但只有少数IPF患者可以接受这种干预[33].没有在临床试验中评估的药理治疗干预症已经表现出对IPF患者的生存益处,并且非常需要稳定疾病和改善存活的新方法。n的观察我et al。[29]还有我eeet al。[30.]显然需要进一步调查,并对包括保守措施(包括保守措施(避免+膳食大小有限,避免某些食物,避免酒精或含咖啡因饮料)的抗反照等),以降低GER和/或腹腔镜抗反流手术(如。这可能是重要的治疗干预措施,而不仅仅是通过使用PPIs和H2受体拮抗剂等酸抑制剂来抑制胃反流分泌物的酸度。
应进一步研究GER和微滴吸在IPF发病机制中的作用,以获得进一步的见解,从而更好地理解发病机制,并确定抗反流治疗在稳定IPF和预防急性加重中的作用。尽管抑制酸度的药物制剂的使用与疾病稳定和提高生存率有关,但必须强调的是,GER和吸入性本身不受PPI抑制,并且仍然可能发生与碱性胃液的抽吸。需要建立使用阻抗pH监测和检测微吸收的生物标志物的策略,以便允许可靠的筛选和监测显着的GER和微吸收,并将这些结果与IPF患者的疾病课程相关联。希望防止GER的治疗策略将保护已经受伤的肺部免受进一步的侮辱,并保留肺的气体交换单元的微环境,从而导致IPF患者的改善结果。
脚注
兴趣表
没有宣布。
- ©ERS 2012